Депрессия у кардиологических больных, или как разорвать порочный круг

Проблема связи депрессивных расстройств и заболеваний сердечно-сосудистой системы длительное время остается предметом активных дискуссий. Полученные в последние годы результаты исследований в области психосоматических заболеваний достаточно противоречивы. Часть из них свидетельствует о необходимости выявления и лечения депрессивных расстройств у пациентов с сердечно-сосудистой патологией, поскольку это позволяет улучшить прогноз и выживаемость таких больных, а также повысить их приверженность к терапии. В то же время авторы других работ утверждают, что данная стратегия не является обязательной, поскольку требует дополнительных затрат (как времени, так и материальных ресурсов), при этом не оказывая существенного влияния на результаты терапии больных сердечно-сосудистыми заболеваниями. В настоящей работе мы попытаемся обобщить результаты последних клинических исследований.
Распространенность депрессии у больных с сердечно'сосудистой патологией
О существовании тесной взаимосвязи депрессии и заболеваний сердечно-сосудистой системы известно давно. Проведенный более 20 лет назад метаанализ исследований, опубликованных в период с 1945 по 1985 год, показал, что депрессия является основным психосоциальным фактором риска развития кардиоваскулярных заболеваний (D.L. Musselman et al., 1998). Среди пациентов с ишемической болезнью сердца (ИБС) депрессия встречается в 3 раза чаще, чем в общей популяции (B.D. Thombs et al., 2006).
По данным Американской ассоциации сердца (АНА, 2001), каждый пятый пациент с ИБС страдает большой депрессией. Распространенность тревожно-депрессивных расстройств у больных артери- альной гипертензией (АГ) достигает 40% (А.Б. Смулевич, 2005).
Высокая распространенность депрессивных расстройств у соматических больных признана одной из причин увеличения кардиоваскулярной смертности за период с 1990 по 2003 год (Е.И. Чазов, 2004). Сегодня можно с полной уверенностью утверждать, что депрессия является независимым фактором риска таких сердечно-сосудистых заболеваний (ССЗ), как ИБС, инфаркт миокарда (ИМ), хроническая сердечная недостаточность и АГ (F. Dobbels et al., 2000). Кроме того, у больных с сердечно-сосудистой патологией депрессия может развиться вторично – как реакция пациента на тяжелое соматическое заболевание. При этом возникновение тревожных расстройств у больных ССЗ усугубляет течение последних, служит фактором риска преждевременной смерти, ухудшения прогноза и снижения качества жизни таких пациентов.
Доказано, что лица с депрессивными нарушениями находятся в группе высокого риска развития ССЗ, и наоборот, у больных с сердечно-сосудистой патологией повышен риск развития расстройств аффективного спектра. Следовательно, можно говорить о существовании порочного круга: ССЗ → появление депрессии → ухудшение течения ССЗ и повышение риска развития другой патологии сердечно-сосудистой системы.
Эту закономерность подтверждают результаты современных исследований. Например, при опросе пациентов, обратившихся к врачам общей практики, было показано наличие психических расстройств почти у 30%, в том числе большой депрессии у 8,4% и малой депрессии у 10,4% (J.L. Jackson et al., 2007). По данным случайной выборки 5% пожилых больных, госпитализированных в США в течение года с обострением хронической сердечной недостаточности, коморбидные психические расстройства были выявлены у 15,8% пациентов, у 8,4% из них была обнаружена депрессия (S.L. Sayers et al., 2007). Коморбидное течение заболеваний сердечно-сосудистой системы и депрессивных расстройств приобретает особое значение в связи c их широкой распространенностью как среди пациентов медицинских учреждений, так и среди населения в целом.
- Депрессивные расстройства повышают риск развития различных ССЗ, ухудшают их течение, а также снижают качество жизни и трудоспособность пациентов.
Известно, что сочетание депрессии и ИБС в 2 раза ухудшает социальное функционирование пациентов по сравнению с каждым из этих заболеваний в отдельности. У пациентов со стабильной стенокардией и коморбидной депрессией почти в 3 раза повышается риск таких сердечно-сосудистых событий, как ИМ, остановка сердца, кардиальная смерть и реваскуляризация (N. Frasure-Smith et al., 2008; J. Denollet et al., 2010). Кроме того, при наличии депрессии у больных CCЗ доля повторных сердечно-сосудистых катастроф или вмешательств на сердце увеличивается более чем на 7% в год (I. Shiotani et al., 2002).
В прошлом году были представлены результаты проспективного когортного исследования HeSSup (Health and Social Support study), в котором приняли участие более 23 тыс. жителей Финляндии (H. Nabi, 2010). Было показано, что при наличии легких или умеренных симптомов депрессии риск ИБС повышается более чем в 1,5 раза, в случае тяжелой депрессии этот риск увеличивался в 2 раза.
- Психические расстройства ассоциируются с повышением общей и кардио- васкулярной смертности.
Результаты многочисленных исследований свидетельствуют о том, что депрессию следует рассматривать как независимый фактор риска смерти по причине ССЗ. Так, наблюдение за 35 715 амбулаторными пациентами показало, что при наличии депрессии смертность повышается на 17% (L.S. Kinder et al., 2008), при этом смертность по причине ИБС увеличивается в 1,5-2,7 раза (P.G. Surtees et al., 2008; W. Whang et al., 2009). В большом проспективном исследовании EPIC- Norfolk United Kingdom Prospective Cohort Study у пациентов с большой де- прессией риск смерти от ИБС был повышен в 2,7 раза в течение 4 лет наблюдения (P.G. Surtees et al., 2008).
F. Lasperance (2000) выделяет депрессию в качестве самостоятельного фактора риска повышения смертности после перенесенного ИМ. Выявление депрессии у больных, перенесших ИМ, связано с повышением летальности в 2,3 раза (в течение 8 лет) и риска развития стенокардии почти в 2 раза (C. Dickens et al., 2008). Важно отметить, что риск смерти от CCЗ у пациентов с депрессивными расстройствами существенно зависит от возраста. Так, риск смерти от ИБС у таких больных в возрасте 18-49 лет повышен в 3,2 раза, 50-75 лет – в 1,9 раза, старше 75 лет – лишь в 1,05 раза (D.D. Osborn et al., 2007). A. Sherwood и соавт. (2011) также соглашаются с тем, что депрессия является независимым фактором риска госпитализации, кардиоваскулярной и общей смертности.
Следует отметить, что депрессия увеличивает риск кардиоваскулярной смерти не только у пациентов с диагностированными заболеваниями сердца. В проведенном B. Penninx и соавт. (2001) дол- госрочном клиническом исследовании было отмечено, что наличие депрессии увеличивает относительный риск смерти от ССЗ независимо от наличия у пациентов заболеваний сердца, а на фоне тяжелой депрессии риск смерти от ССЗ достоверно повышается и составляет при легкой и умеренной депрессии – 1,6 у больных ССЗ и 1,5 – у лиц без ССЗ, при тяжелой депрессии – 3,0 и 3,9 соответственно.
В проведенном в Финляндии популяционном исследовании показано, что депрессия достоверно повышает риск внезапной смерти у пожилых пациентов (ОР 2,74; 95% ДИ 1,37-5,50) даже после коррекции с учетом таких значимых факторов риска, как пол, наличие в анамнезе острого ИМ и СД (H. Luukinen et al., 2003).
Аналогичные данные были получены в исследованиях с участием женщин среднего и пожилого возраста (W. Whang et al., 2010; A. Pan et al., 2011).
- Психические расстройства снижают приверженность пациентов к лечению, следовательно, ухудшая результаты терапии ССЗ.
Исследования свидетельствуют о том, что у больных с депрессивной симптоматикой значительно снижена приверженность к лечению и выполнению врачебных рекомендаций. Такие пациенты не соблюдают режим лечения, реже придер- живаются здорового образа жизни, хуже выполняют врачебные рекомендации относительно диеты, отказа от курения, увеличения физической активности, ограничения приема алкоголя; они редко участвуют в мероприятиях по реабилитации и вторичной профилактике (M.J. Zellweger et al., 2004).
Как известно, комплайенс оказывает существенное влияние на результаты лечения: в частности, четкое выполнение рекомендаций врача позволяет снизить смертность на 44% (S.S. Simpson et al., 2008). В Европейских рекомендациях по профилактике ССЗ депрессия и тревога рассматриваются как значимые препятствия к модификации образа жизни пациентов в желаемом направлении. В подобных случаях важная роль отводится психотропному лечению. Например, в исследовании H.R. Bogner и соавт. (2008) было показано, что терапия антидепрессантами у больных АГ связана со значительно лучшей приверженностью к антигипертензивному лечению – 78 против 31%.
- У пациентов с CCЗ наличие коморбидных психических расстройств значительно увеличивает затраты на лечение.
По данным зарубежных исследований, отсутствие коррекции депрессивных расстройств связано со значительным (в 2-3 раза) повышением стоимости терапии соматических заболеваний. Американские ученые подсчитали, что у госпитализированных пациентов с сердечной недостаточностью наличие депрессивного расстройства увеличивает продолжительность госпитализации на 0,6-1,4 дня и затраты на лечение на 7763 доллара (S.L. Sayers et al., 2007; N.M. Albert et al., 2009). На первый взгляд, увеличение продолжительности госпитализации кажется незначительным, однако с учетом большого количества больных с сердечной недостаточностью это приводит к существенным материальным затратам.
- Психологическая и фармакологическая поддержка больных ССЗ, страдающих депрессией, может улучшить результаты их лечения.
Согласно результатам ряда исследований, терапия депрессивных расстройств может уменьшить их негативное влияние на течение ССЗ (J.H. O’Keefe et al., 2009; J.C. Huffman et al., 2011). Проведенное еще в 1997 г. исследование показало, что хорошая социальная поддержка, способствующая снижению выраженности депрессивной симптоматики, уменьшает неблагоприятное влияние депрессии на смертность больных после ИМ (N. Frasure-Smith et al.).
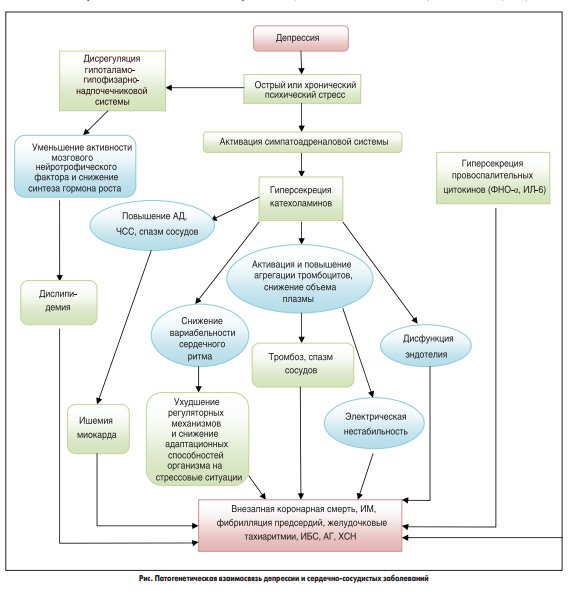
Патогенетическая взаимосвязь депрессии и ССЗ
Ученые утверждают, что некоторые нейрохимические и нейроэндокринные изменения при депрессивных расстройствах могут служить патофизиологическими механизмами, обусловливающими повышенную уязвимость больных депрессией в отношении ССЗ. В осуществлении взаимосвязи между депрессией и CCЗ важна роль гипоталамо-гипофизарно-надпочечниковой (ГГНС) и симпатоадреналовой (САС) систем.
Известно, что стресс сопровождается рядом физиологических реакций, таких как повышение уровня адреналина и нор- адреналина, частоты сердечных сокращений и артериального давления, а также активации тромбоцитов. На фоне этого может повышаться риск развития атеросклероза, ИМ, гипертрофии миокарда, нарушений ритма сердца и внезапной смерти (рис.).
На сегодняшний день рассматривают нескольких возможных механизмов влияния депрессии и расстройств депрессивного спектра на развитие и прогрессирование ССЗ (L. Pozuelo et al., 2009). Наиболее важными из них являются такие:
• изменение вариабельности сердечного ритма и дисбаланс автономной нервной системы;
• нарушение функционального состояния тромбоцитов, повышение вязкости крови и дисфункция эндотелия;
• повышение уровня воспалительного ответа;
• генетическая предрасположенность.
Влияние депрессии на сердечный ритм
Известно, что вариабельность сердечного ритма (ВСР) – надежный неивазивный маркер активности вегетативной нервной системы. Снижение ВСР рассматривается в качестве прогностического маркера заболеваемости и смертности от ССЗ как среди относительно здоровых лиц, так и среди пациентов, перенесших острое коронарное событие.
Еще в 1995 г. результаты исследования Kawachi и соавт. с участием 581 человека в возрасте от 47 до 86 лет показали, что у пациентов, страдающих депрессивными расстройствами, существенно снижается ВСР. Это, в свою очередь, свидетельствует об ухудшении регуляторных механизмов и адаптационных возможностей организма в стрессовых ситуациях, что сопровождается повышением риска внезапной сердечной смерти. Исследование Heart and Soul Study показало, что сниженная ВСР является фактором риска желудочковых аритмий и внезапной сердечной смерти у пациентов с CCЗ (A. Gehi et al., 2005).
R. Krittayaphong и соавт. также подтвердили существование четкой взаимосвязи между тяжестью депрессии и снижением ВСР у пациентов с ИБС. Аналогичные данные были получены в ходе анализа результатов исследования NESDA (The Netherlands Study of Depression and Anxiety), в котором приняли участие более 2 тыс. пациентов (C.M. Licht et al., 2009). По мнению авторов исследования, снижение ВСР было обусловлено применением пациентами с депрессивными нарушениями антидепрессантов различных групп, в том числе трициклических антидепрессантов (ТЦА), селективных ингибиторов обратного захвата серотонина (СИОЗС) и др. Всегда ли депрессия приводит к снижению ВСР или это результат терапии антидепрессантами? В настоящее время этот вопрос остается открытым.
Влияние депрессии на функциональную активность тромбоцитов и дисфункцию эндотелия
Неблагоприятное влияние депрессии на течение CCЗ может также опосредоваться через тромбоцитарные механизмы. Тромбоциты играют важную роль в поддержании гемостаза, могут влиять на развитие атеросклероза, тромбоза и острого коронарного синдрома путем взаимодействия с субэндотелиальными компонентами пораженных сосудов и факторами свертывания. Как известно, тромбоциты имеют рецепторы для катехоламинов и серотонина (5-НТ-рецепторы). Увеличение уровня катехоламинов у пациентов с депрессией приводит к активации тромбоцитов, повышению их агрегации. Вследствие активации тромбоцитов высвобождаются гранулы, содержащие хемотаксические и митогенные факторы. Патогенетическая связь между депрессией и ССЗ также объясняется повышением вязкости крови (G. Lowe et al., 1997).
Увеличение активности тромбоцитов является типичным для пациентов с депрессией. Результаты исследований подтверждают, что у лиц с депрессивной симптоматикой повышены внутриклеточный уровень свободного кальция, плотность рецепторов, связывающих 5-НТ2, и агрегация тромбоцитов (C.V. Serrano et al., 2011). Также отмечено повышение плазменных уровней тромбо- цитарного фактора IV и β-тромбоглобулина (маркеры активации тромбоцитов) у пациентов с ИБС и депрессивными расстройствами (F. Laghrissi-Thode et al., 1997). В подисследовании SADHART (Sertraline AntiDepressant Heart Attack Randomized Trial Platelet Substudy) было показано, что лечение СИОЗС сертралином больных с депрессивными расстройствами, перенесших ИМ, существенно снижает уровень биомаркеров активации тромбоцитов (V.L. Serebruany et al., 2003). Эндотелиальная дисфункция, определяемая по изменению потокзависимой дилатации плечевой артерии, также оказалась характерным признаком наличия депрессии у пациентов, у которых традиционные факторы риска атеросклероза отсутствовали (А. Sherwood et al., 2005).
Повышение уровня воспалительного и иммунного ответа
Депрессивные состояния связаны также с иммунными и воспалительными нарушениями. Были получены клинические и экспериментальные данные, свидетельствующие о роли иммунитета, в первую очередь гиперсекреции провоспалительных цитокинов (TNFα, IL-6 и др.), в манифестации и течении депрессии (W. Jiang et al., 2001; М. Macs et al., 2002). Наличие депрессивных расстройств может сопровождаться повышением чувствительности миокарда к кардиотоксическому действию TNFα (J. Pasic et al., 2003). Социальная изоляция пациентов с депрессией также повышает уровни маркера воспаления IL-6 и, как следствие, риск сердечно-сосудистых заболеваний (E. Loucks et al., 2005).
Для пациентов с депрессией характе- рен более высокий уровень С-реактивного белка и воспалительных цитокинов, которые играют важную роль в атерогенезе (J.P. Empana et al., 2005). Недавние исследования также показывают существование прямой зависимости степени выраженности депрессии от концентрации С-реактивного белка у пациентов, перенесших ИМ (N. Frasure-Smith et al., 2007). В связи c этим приобретают интерес результаты исследования ATTICA, в котором изучалась взаимосвязь между депрессией и повышенным риском развития ССЗ у 953 относительно здоровых пациентов (D.В. Panagiotakos еt al., 2004).
Выяснили, что депрессия при учете других факторов риска, таких как возраст, пол, приверженность к курению, наличие сахарного диабета, низкий уровень физической активности, ассоциируется с достоверным повышением уровней С-реактивного белка, лейкоцитов и фибриногена.
В исследовании Y. Young-Xu и соавт. (2003) было показано снижение риска развития депрессии и тревожного расстройства у больных ИБС на фоне применения статинов.
Генетическая предрасположенность к развитию депрессии и ССЗ
Ученые обнаружили общие генетические механизмы, предопределяющие развитие депрессии и ССЗ. Оказывается, что депрессия, АГ и ИБС развиваются в результате неблагоприятного воздействия не только факторов внешней среды, но и общих генетических факторов. Следовательно, развитие депрессии и основных ССЗ отчасти может быть детерминировано одними и теми же генетическими факторами (J.F. Scherrer et аl., 2003).
Следует также напомнить данные исследований, подтвердивших генетичес- кую предрасположенность к депрессии у пациентов с S-аллелем инсерционно-делеционного полиморфизма (5-HTTLPR) в промоторном регионе гена переносчика серотонина (5-HTT). Известно, что серотонинергическая нейромедиаторная система мозга участвует в регуляции настроения, а ее дисфункция может приводить к развитию депрессии. Переносчик серотонина 5-HTT играет важную роль в трансмиссии серотонина в головном мозге. Впервые «ген депрессии» под названием 5-HTTLPR попал в поле зрения ученых еще в 2003 г. Оказалось, что у носителей короткого варианта этого гена нарушается ответ нервной системы на стрессовые ситуации, что в конечном итоге ведет к развитию депрессии (J.A. Schinka et al., 2004; S.A.G. Willis- Owen et al., 2005). С тех пор было проведено большое количество исследований, посвященных стрессу, депрессии и генетическим особенностям. В частности,было доказано, что у пациентов с ИМ, имеющих один или оба аллеля этого короткого гена, чаще развивается депрессия и повышен риск возникновения кардиоваскулярных событий (D. Nakatani et al., 2005).
Совсем недавно американские ученые смогли подтвердить роль генетических факторов в развитии депрессии. Научные сотрудники Мичиганского университета (K. Karg et al., 2011) проанализировали 54 исследования, проводившиеся с 2001 по 2010 год, в которых приняли участие более 41 тыс. человек, и доказали наличие четкой взаимосвязи между коротким вариантом гена 5-HTTLPR и развитием депрессии.
В свете изложенных данных становится понятным, почему полиморфизм гена ангиотензинпревращающего фермента, являющегося одним из важных звеньев формирования кардиоваскулярной патологии, ассоциируется не только с активностью этого фермента, но и с гиперкортизолемией (нейроэндокринной составляющей депрессии) и, как следствие, с развитием собственно депрессии (T.C. Baghai et al., 2006).
Таким образом, полученные на сегодняшний день данные могут отчасти объяснить механизмы коморбидности депрессии и ССЗ. В то же время отсутствуют убедительные подтверждения возможности значимых изменений структуры миокарда и сосудов, причиной которых являются депрессивные расстройства.
Общие принципы лечения депрессивных расстройств у больных ССЗ
Несмотря на большое число рекомендаций по диагностике и лечению депрессивных расстройств в соматической практике за рубежом, такие важные руководства практически отсутствуют в Украине. В то же время врачи общей клинической практики и кардиологи, прошедшие специальную подготовку, могут достаточно эффективно лечить нетяжелые депрессивные расстройства. Это представляется особенно актуальным, принимая во внимание тот факт, что специализированная психиатрическая и психотерапевтическая помощь доступна не во всех медицинских учреждениях нашей страны.
Нельзя также игнорировать существующее предубеждение многих пациентов относительно лечения у психиатра и психотерапевта. Не случайно, по данным международного исследования ВОЗ 17 стран, лишь каждый 5-й человек, страдающий выраженным психическим расстройством, получает соответствующее лечение (P.S. Wang et al., 2009). По-этому разработка национальных рекомендаций по ведению психических расстройств врачами-интернистами является насущной потребностью отечественной системы здравоохранения.
К основным методам лечения депрессивных состояний относят медикаментозную терапию и немедикаментозные вмешательства (различные методы психотерапии, в том числе когнитивно-поведенческую психотерапию, а также релаксационные методики, такие как аутогенная тренировка, дыхательно-релаксационный тренинг, прогрессивная мышечная релаксация, релаксационная методика с использованием биологической обратной связи) (Т.А. Айвазян, 2002). Немаловажными также являются устранение стрессогенного фактора, нормализация режима труда и отдыха, увеличение физической активности.
В 2008 г. были опубликованы рекомендации Комитета клинической кардиологии, Комитета эпидемиологии и профилактики, Междисциплинарного совета АНА по повышению качества медицинской помощи при лечении депрессии у пациентов с ИБС. Вышеуказанные международные сообщества для лечения депрессии у больных CCЗ рекомендуют назначать фармакотерапию антидепрессантами, когнитивно-поведенческую терапию, сердечную реабилитацию, а также мероприятия по увеличению физической активности. Авторы руководства заявляют, что когнитивно-поведенческая терапия может с успехом применяться у больных ИБС и быть альтернативой для пациентов, которым противопоказаны антидепрессанты. Частоту и продолжительность такой терапии следует подбирать индивидуально для каждого пациента. Кроме того, снизить депрессивный статус у больных CCЗ могут физические упражнения и сердечная реабилитация, при этом программа физических нагрузок должна быть разработана индивидуально для каждого пациента с учетом уровня его физического и психического здоровья.
В условиях малой доступности квалифицированной психотерапии для большинства пациентов общемедицинской сети здравоохранения основным методом лечения депрессивных расстройств на сегодняшний день остается фармакотерапия. Наиболее изученными группами антидепрессантов у кардиологических больных являются ТЦА и СИОЗС. Данные об эффективности и безопасности антидепрессантов других групп у кардио- логических больных ограничены.
ТЦА оказывают выраженный антидепрессивный эффект и по эффективности при тяжелой депрессии превосходят некоторые более новые группы лекарственных средств, в частности СИОЗС. Однако ТЦА значительно уступают антидепрессантам последующих поколений по безопасности и переносимости. В последние годы появляется все больше данных о том, что у пациентов с ИБС ТЦА могут повышать риск смерти, более чем в 2 раза повышать риск развития ИМ. Способность ТЦА в отличие от СИОЗС повышать риск кардиоваскулярных заболеваний была доказана в крупном европейском исследовании (M. Hamer et al., 2010).
ТЦА характеризуются рядом недостатков:
• могут замедлять внутрижелудочковую проводимость, удлинять интервал QT и повышать риск развития желудочковой аритмии по типу «пируэт»;
• могут накапливаться в миокарде, значительно изменяя проводимость и сократимость;
• способны вызывать атриовентрикулярную блокаду I и II степени, асистолию и внезапную сердечную смерть, риск которой увеличивается при применении высоких доз препаратов;
• могут приводить к синусовой тахикардии вследствие увеличения концентраций норадреналина в сыворотке крови;
• в 20% случаев связаны с развитием ортостатической гипотензии, обусловленной сочетанием центрального и периферического антиадренергического действия и непосредственного угнетающего влияния на миокард;
• опасны для пациентов пожилого возраста, у которых на фоне персистирующей рефлекторной тахикардии могут вызывать ишемию миокарда;
• сопровождаются неблагоприятными побочными эффектами (сонливостью, ухудшением памяти, снижением концентрации внимания, нарушением координации движений); у пациентов пожилого возраста побочные эффекты ТЦА могут проявляться в парадоксальной форме, имитируя симптомы делирия и деменции;
• обладают высоким потенциалом лекарственного взаимодействия, например с клонидином, антиаритмическими препаратами, варфарином и ацетилсалициловой кислотой;
• могут вызывать увеличение массы тела;
• снижают ВСР;
• имеют узкий терапевтический индекс, характеризуются высоким риском летальности в случае передозировки и требуют титрации дозы.
С учетом высокого риска развития по- бочных эффектов при приеме ТЦА и наличия более безопасных альтернативных препаратов в настоящее время рекомендуют применять ТЦА только для терапии тяжелых, рефрактерных и резистентных случаев депрессии, лечением которых должны заниматься исключительно врачи-психиатры.
Вторая группа препаратов – СИОЗС – обладает широким спектром фармакологической активности, оказывая выраженный антидепрессивный, анксиолитический и анальгетический эффекты. СИОЗС имеют более низкий риск кардиотоксичности по сравнению с таковым ТЦА.
Благоприятное соотношение эффективность/безопасность, подтвержденное в многочисленных клинических исследованиях, позволяет рассматривать СИОЗС в качестве препаратов первого ряда в общесоматической практике, в том числе у кардиологических больных. В качестве одного из возможных механизмов благоприятного эффекта СИОЗС рассматривают их антитромбоцитарное действие.
Доказано, что СИОЗС угнетают захват серотонина тромбоцитами, истощают в них запасы серотонина, блокируют внутриклеточную мобилизацию кальция. Антитромбоцитарное действие СИОЗС может обусловливать и их профилактический эффект в отношении ИМ.
В рандомизированных клинических исследованиях у кардиологических больных наиболее хорошо изучены три препарата из группы СИОЗС – пароксетин, флуоксетин и сертралин. По результатам этих исследований можно предположить наличие у этих препаратов кардиопро- текторного эффекта. К преимуществам СИОЗС также относятся возможность проведения лечения фиксированными дозами или минимальная потребность в титрации, а также высокая безопасность при передозировке.
Рандомизированные исследования показали, что СИОЗС безопасны для пациентов с ИБС и эффективны при умеренных, сильных и периодических депрессиях. Применение СИОЗС после перенесенного ИМ также является безопасным, относительно недорогим и может быть эффективным при постинфарктных депрессиях. Более того, в исследовании W.H. Sauer и соавт. (2001) было продемонстрировано снижение риска развития острого ИМ у лиц, принимавших препараты данной группы. В данном исследовании с участием более 3500 пациентов применение пароксетина, флуоксетина и сертралина ассоциировалось со значительным снижением риска ИМ по сравнению с приемом других антидепрессантов или отсутствием лечения. Эти результаты были подтверждены в одном из последних исследований, в котором продолжительный прием СИОЗС ассоциировался со снижением риска ИМ у пациентов, страдающих депрессией (S.E. Kimmel et al., 2011).
Таким образом, при лечении депрессии у больных ССЗ следует отдавать предпочтение антидепрессантам нового поколения с благоприятным профилем безопасности и не превышать рекомендуемые дозы препаратов. ТЦА и ингибиторы моноаминоксидазы противопоказаны к применению у пациентов с ССЗ вследствие их кардиотоксичности.
Согласно рекомендациям Комитета по профилактике АНА антидепрессантами первого выбора для пациентов с ИБС являются сертралин и циталопрам. В начале лечения антидепрессантами пациенты должны находиться под наблюдением в течение первых 2 мес для контроля суицидального риска и риска медикаментозных осложнений.
Врачи должны помнить и проинформировать больного о том, что клинический эффект большинства антидепрессантов проявляется в среднем через 2 нед терапии. Важно также соблюдать определенную длительность курсового лечения антидепрессантами, которая должна быть не менее 1,5 мес, а при выраженных, рекуррентных, а также затяжных депрессивных состояниях – 2-6 мес в зависимости от состояния пациента. Отмена антидепрессантов нового поколения может проводиться одномоментно, без предварительного снижения дозы, поскольку для этих препаратов не характерны привыкание, а также синдром отмены. Однако назначать сразу несколько различных психотропных препаратов не рекомендуется ввиду возможного и непредсказуемого лекарственного взаимодействия.
Лечить или не лечить?
На сегодняшний день ни в одном крупном рандомизированном исследовании убедительно не доказано положительное влияние антидепрессантов и психотерапии на отдаленный прогноз пациентов с CCЗ. Несмотря на то что психотерапия и психотропные средства снижают выраженность тревоги и депрессии, как оказалось, они незначительно влияют на прогноз соматического заболевания.
В частности, один из последних метаанализов 11 исследований подтвердил, что лечение депрессии у пациентов с заболеваниями сердца не повышает эффективность терапии ССЗ (B.D. Thombs et al., 2008).
На основании полученных данных авторы анализа заявляют, что скрининг депрессии у больных ССЗ не спо- собствует повышению эффективности терапии кардиоваскулярной патологии. Кроме того, существующие анкеты и опросники для выявления депрессии не исключают риск ложноположительных результатов и, следовательно, назначение лечения при отсутствии показаний. Также следует учитывать, что в течение первого месяца терапии около 25-35% соматических пациентов, а в течение 3 мес каждый второй больной прекращают прием антидепрессантов.
В многоцентровом рандомизированном контролируемом исследовании MIND-IT (The Myocardial INfarction and Depression-Intervention Trial) с участием более 2 тыс. пациентов было показано, что терапия антидепрессантами существенно не улучшает прогноз больных ССЗ (J.P. van Melle et al., 2007). Результаты рандомизированного двойного слепого плацебо контролируемого исследования сертралина SADHART-CHF (Sertraline Against Depression and Heart Disease in Chronic Heart Failure trial) свидетельствуют о том, что назначение СИОЗС пациентам с сердечной недостаточностью не снижает смертность и риск сердечно-сосудистых событий (C.M. O’Connor, 2010).
Хотя в настоящее время не существует прямых доказательств того, что скрининговые исследования на наличие депрессии и последующее ее лечение приводят к улучшению состояния пациентов с ССЗ, доказано, что это расстройство связано с увеличением смертности и заболеваемости, ухудшением прогноза пациентов, перенесших кардиоваскулярные события, и ухудшением качества их жизни. Важной представляется оценка влияния лечения антидепрессантами на выживаемость пациентов с ССЗ, их трудоспособность и восстановление после ИМ, для чего необходимо проведение дополнительных масштабных клинических исследований.
Список литературы находится в редакции.
Подготовила Ольга Татаренко
СТАТТІ ЗА ТЕМОЮ
Проблема когнітивних розладів є однією з найважливіших у сучасній клінічній медицині. Це зумовлено не тільки збільшенням частки людей старшого віку серед населення, а й посиленням ролі стресу та інших патогенетичних чинників. У березні відбувся семінар «Академія сімейного лікаря. Біль в грудній клітині. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста», у якому прийняли участь провідні вітчизняні науковці і фахівці різних галузей. У рамках заходу професор кафедри військової терапії Української військово-медичної академії Міністерства оборони України, кандидат медичних наук Мар’яна Миколаївна Селюк представила доповідь «Війна та когнітивні порушення. Причина чи наслідок? Як вирішити проблему?». Подаємо огляд цієї доповіді у форматі «запитання – відповідь»....
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...