Тактика лечения дислипидемий при метаболическом синдроме: статины или фибраты?
Метаболический синдром (МС) представляет собой совокупность метаболических факторов риска развития сердечно-сосудистых заболеваний (ССЗ) атеросклеротического генеза, ассоциированных с абдоминальным ожирением и инсулинорезистентностью (ИР). В настоящее время МС в экономически развитых странах встречается у 10-25% населения. Наличие МС в 2-4 раза увеличивает частоту внезапной смерти и развития ССЗ, а риск формирования сахарного диабета 2 типа (СД 2) у пациентов с повышенным индексом массы тела (ИМТ), по данным различных авторов, увеличивается в 5-9 раз. Среди подростков и молодежи частота встречаемости МС за последние 60 лет возросла в 1,5 раза, а ИМТ у детей в экономически развитых странах регистрируется в 12-14% случаев. Распространенность МС приобретает эпидемические масштабы, что требует интеграции различных медицинских специальностей с целью адекватной диагностики и эффективного лечения этой патологии.
Роль дислипидемии в патогенезе метаболического синдрома
Особенностью нарушения липидного спектра крови при МС является сочетание «традиционных» маркеров высокого риска развития ишемической болезни сердца (ИБС), таких как повышенные уровни холестерина (ХС) липопротеидов низкой плотности (ЛПНП), снижение уровня липопротеидов высокой плотности (ЛПВП), с «нетрадиционными» – высокими концентрациями триглицеридов (ТГ) и модифицированных (малых, плотных) частиц ЛПНП, низким уровнем ЛПВП. По мере увеличения числа «нетрадиционных» маркеров риска вероятность развития ИБС повышается в 20 раз, в то время как при комбинации из трех «традиционных» маркеров риска – только в 4,5 раза.
Основными факторами МС являются: повышение концентраций ТГ, модифицированных частиц ЛПНП, снижение уровня ЛПВП, нарушение гомеостаза глюкоза/инсулин, активация протромботического/провоспалительного состояния, эндотелиальная дисфункция, сопровождающиеся развитием артериальной гипертензии.
В Фрамингемском исследовании в 1986 г. впервые показано, что повышение уровня ТГ увеличивает риск развития коронарных событий. Это было подтверждено Стокгольмским, Хельсинкским и Парижским исследованиями: «ТГ являются независимым фактором риска ИБС». Еще в 1966 г. J.E. Hokanson и М.А. Austin, проанализировав результаты многих проспективных исследований, установили, что без точного учета уровней ЛПВП повышение концентрации ТГ на каждый 1 ммоль/л увеличивает риск развития ИБС у женщин на 76, а у мужчин – на 32%. И, наоборот, при учете уровней ЛПВП аналогичный рост концентрации ТГ увеличивает риск развития ИБС у женщин только на 37%, а у мужчин – на 14%. Результаты этих исследований позволили авторам сделать следующий вывод: «...ТГ могут быть более вероятными предикторами ишемических эпизодов, чем уровень общего ХС».
Многие исследователи показали, что уровни ТГ являются предикторами степени протяженности поражения коронарных артерий – даже при стенозах менее 50% от диаметра просвета коронарных сосудов. Также установлено, что повышение уровня ТГ ассоциируется с нарастанием толщины комплекса интима-медиа общей сонной артерии.
Связь ТГ с толщиной сосудистой стенки, тяжестью атеросклеротического поражения сосудов и риском развития острого коронарного синдрома можно объяснить несколькими причинами:
- Липопротеиды, богатые ТГ, являются хорошими посредниками кислородных свободно-радикальных реакций, которые могут способствовать дестабилизации и разрыву бляшки.
- ТГ имеют тесную связь с уровнем инсулина сыворотки крови, который способствует гиперплазии гладкомышечных клеток и утолщению мышечного слоя сосудов (ремоделированию).
При анализе результатов исследования MARS (Monitored Aterosclerosis Regression Study) и CLAS (Cholesterol-Lowering Aterosclerosis Study) показано, что не только уровень ТГ плазмы является независимым фактором риска ИБС, но и уровни модифицированных липопротеидов, богатых ТГ, коррелируют с тяжестью ИБС. Этот факт был подтвержден и другими исследователями. Более того, высокие концентрации липопротеидов, богатых ТГ (липопротеидов очень низкой плотности – ЛПОНП, ЛПНП), могут предопределять темп прогрессирования ИБС. Возможно, это связано с тем, что липопротеиды, богатые ТГ, являются хорошими посредниками кислородных свободно-радикальных реакций (перекисного окисления липидов), способствующих формированию и дестабилизации атеросклеротических бляшек – их разрыву.
В настоящее время доказано, что увеличение уровней ТГ, модифицированных (мелких с высокой плотностью) ЛПНП, и снижение уровня ЛПВП являются независимыми факторами риска ИБС.
G.R. Thompson (1998) в обзорной статье, посвященной анализу 12 проспективных исследований, отметил, что липопротеиды, богатые ТГ, играют важную роль в прогрессировании ИБС и являются контрольными точками, отражающими эффект гиполипидемической терапии, особенно уровень Апо С-ІІІ, который является маркером метаболизма, липопротеидов, богатых ТГ.
Большой интерес представляет тот факт, что не только тощаковые, но и постпрандиальные уровни ТГ имеют тесную связь с прогрессированием ИБС. Причем данная связь не зависит от уровней ЛПВП и является более сильной, чем таковая с ЛПВП. Это обусловлено тем, что постпрандиальная гипертриглицеридемия уменьшает протективный эффект ЛПВП и индуцирует захват окисленных ЛПОНП (гипертриглицеридных) стромальными клетками медии и адвентиции сосудистой стенки и накопление их в макрофагах.
Нарушения метаболизма липидов тесно связано с эндотелиальной дисфункцией, которая проявляется нарушением эндотелийзависимой вазодилатации и повышением адгезивных (тромботических) свойств эндотелиальной выстилки сосудов. Доказано, что окисленные ЛПНП обладают высокой токсичностью, снижают способность сосудистого эндотелия продуцировать оксид азота (NО) – эндотелийзависимый фактор релаксации (ЭЗФР), что сопровождается относительно избыточной продукцией вазоконстрикторных факторов (эндотелина-1, ангиотензина), активацией апоптоза сосудистых клеток. В настоящее время «стартовая» роль дисфункции эндотелия сосудов признана в патогенезе ИБС и инфаркта миокарда (ИМ).
В многочисленных исследованиях установлена прямая тесная корреляционная связь между изменениями функционального состояния коронарного русла (коронарный резерв) и реакцией периферических сосудов на ЭЗФР (вазодилатационный резерв), т. е. выраженность нарушений ЭЗФР плечевой артерии отражает степень атеросклеротического поражения коронарных и сонных артерий. В связи с этим определение ЭЗФР плечевой артерии можно рассматривать как адекватный метод исследования функционального состояния эндотелия коронарных сосудов.
Установлено, что наиболее уязвимыми являются эндотелиоциты в области деления магистральных сосудов (бифуркации), где за счет гидродинамических эффектов происходят усиленная пролиферация, апоптоз и гибель клеток. Доказано, что вынужденно регенерирующие эндотелиальные клетки отчасти утрачивают способность в полной мере высвобождать NО (ЭЗФР), особенно в ответ на агрегационную активность тромбоцитов. Дисфункция эндотелия является стартовым моментом, инициирующим атерогенез, способствует прогрессированию атеросклероза, что в конечном итоге приводит к дестабилизации атеросклеротической бляшки, ее разрыву, развитию острого коронарного синдрома и ИМ.
Гиполипидемические лекарственные средства
С учетом конкретной клинической ситуации и типа дислипидемии в настоящее время применяют пять следующих категорий гиполипидемических лекарственных средств (различия в их эффектах на липидный спектр хорошо известны):
- ингибиторы ГМГ-КоА-(3-гидрокси-3-метил-глутарил-коэнзима А)-редуктазы – статины;
- фибраты;
- секвестранты желчных кислот;
- никотиновая кислота и ее производные (ниацин);
- ингибиторы желудочно-кишечной липазы (орлистат).
Имеется много доказательств, полученных в тщательно проведенных рандомизированных клинических исследованиях и обосновывающих назначение статинов в качестве основной терапии ССЗ. В соответствии с данными метаанализа независимых исследований (4S, HPS, ASC0T-LLA, CARDS, 4D), опубликованного в 2005 г., снижение риска ИБС на фоне приема статинов в среднем составило 23% (от 11 до 51%) . Тем не менее статины не устраняют риск, связанный с низким уровнем ЛПВП или другими проявлениями МС, также не было достоверно установлено значимое снижение остаточного риска у пациентов с СД 2. Таким образом, проведенный метаанализ обозначил актуальность проблемы и основное направление дальнейших исследований.
На протяжении последних 10-15 лет проведен ряд крупных проспективных исследований (HHS, BIP, VA-HIT), среди которых ведущим является исследование FIELD (The Fenofibrate Intervenention and Event Lowering in Diabetes Trial) с участием 9795 пациентов с нарушениями углеводного обмена. Эти исследования были посвящены сравнительному изучению влияния гиполипидемической терапии (статинами или фибратами) на уровни сердечно-сосудистой заболеваемости и смертности. Оказалось, что фибраты особенно эффективны у пациентов с СД 2 и/или признаками МС и достоверно снижают высокий риск сердечно-сосудистых осложнений. В исследованиях, включенных в программу FIELD, показано плейотропное действие фибратов (фенофибрата), которые подавляют миграцию эндотелиальных клеток сосудов, оказывают противовоспалительное действие, подавляют активность окислительного стресса. При применении фенофибрата документировано статистически значимое снижение уровня провоспалительных цитокинов, таких как фактор некроза опухоли a (ФНО-a), интерлейкин-6 (ИЛ-6),
ИЛ-1b, снижение уровней активности супероксиддисмутазы плазмы и малондиальдегида – липидного гидропероксида, образующегося при окислительном стрессе. Подобные различия клинических результатов гиполипидемического эффекта статинов и фибратов среди пациентов с МС, вероятно, обусловлены специфическими особенностями их биотрансформации и механизмами воздействия на различные уровни липидного обмена.
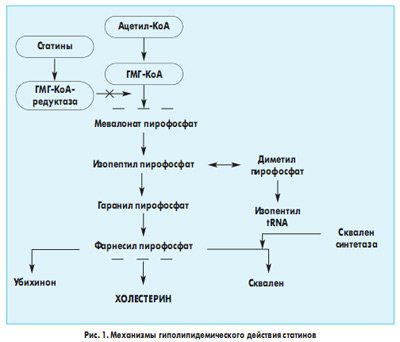 Статины являются ингибиторами ГМГ-КоА-редуктазы и образуют группу препаратов с гипохолестеринемическим действием, основанным на их способности конкурентно ингибировать активность ГМГ-КоА-редуктазы, превращение которой в мевалоновую кислоту является ключевым этапом синтеза эндогенного ХС (рис. 1). Это приводит к компенсаторной экспрессии гепатоцитами повышенного числа рецепторов ЛПНП, что увеличивает клиренс ЛПНП из плазмы. Статины, подавляя синтез ЛПОНП (предшественников ЛПНП) в печени, способствуют уменьшению уровня последних, что в итоге снижает атерогенное действие дислипидемии.
Статины являются ингибиторами ГМГ-КоА-редуктазы и образуют группу препаратов с гипохолестеринемическим действием, основанным на их способности конкурентно ингибировать активность ГМГ-КоА-редуктазы, превращение которой в мевалоновую кислоту является ключевым этапом синтеза эндогенного ХС (рис. 1). Это приводит к компенсаторной экспрессии гепатоцитами повышенного числа рецепторов ЛПНП, что увеличивает клиренс ЛПНП из плазмы. Статины, подавляя синтез ЛПОНП (предшественников ЛПНП) в печени, способствуют уменьшению уровня последних, что в итоге снижает атерогенное действие дислипидемии.
Убедительно доказанная прогностическая польза длительного приема ингибиторов ГМГ-КоА-редуктазы при атеросклерозе и СД уверенно вывела эту группу препаратов на ведущее место в рекомендациях по современной медикаментозной терапии и профилактике ССЗ. Клинические результаты, полученные при лечении статинами, объясняются наличием у них не только антихолестеринемического, но и множества других положительных эффектов. Полезные свойства статинов, не зависящие от их влияния на липиды плазмы, получили название плейотропных. Они проявляются в первые 3-4 месяца лечения и обеспечивают положительное влияние на функцию эндотелия, оказывают антиишемический, антитромботический, антиаритмический, антиатерогенный и другие эффекты. Благодаря этому спектр показаний к назначению статинов при лечении ССЗ расширяется.
По данным экспериментальных работ и клинических исследований, подтверждающих плейотропные свойства статинов (симвастатина, аторвастатина, правастатина, розувастатина и др.), выявлены эффекты, оказывающие влияние на патогенез и течение МС: противовоспалительный, иммуномодулирующий (посредством снижения в плазме уровней ИЛ-6 и ФНО-a), увеличение секреции мозгового натрийуретического гормона, а также секреции NО эндотелием сосудов. Одним из нежелательных эффектов статинов в процессе ингибирования синтеза ХС является снижение биосинтеза убихинона (коэнзима Q10) – основного клеточного антиоксиданта, защищающего от перекисного окисления свободными радикалами фосфолипидный слой клеточной мембраны.
 Фибраты (дериваты фиброевой кислоты) используются для лечения нарушений липидного обмена с конца 1950-х гг. При этом их традиционно назначают пациентам с гипертриглицеридемией и СД, а также для лечения больных ИБС. Утрата интереса к фибратам произошла после получения результатов исследования HPS (Heart Protection Study), основанного на 5,5-летнем наблюдении за 20 536 пациентами с высоким риском ИБС, леченных симвастатином в дозе 40 мг/сут. В этом исследовании (при использовании статинов в схеме лечения пациентов с высоким риском ССЗ) достижение конечных точек показало значительное снижение частоты ИМ, инсультов, внезапной сердечной смерти.
Фибраты (дериваты фиброевой кислоты) используются для лечения нарушений липидного обмена с конца 1950-х гг. При этом их традиционно назначают пациентам с гипертриглицеридемией и СД, а также для лечения больных ИБС. Утрата интереса к фибратам произошла после получения результатов исследования HPS (Heart Protection Study), основанного на 5,5-летнем наблюдении за 20 536 пациентами с высоким риском ИБС, леченных симвастатином в дозе 40 мг/сут. В этом исследовании (при использовании статинов в схеме лечения пациентов с высоким риском ССЗ) достижение конечных точек показало значительное снижение частоты ИМ, инсультов, внезапной сердечной смерти.
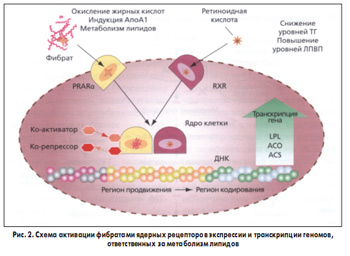
Механизм гиполипидемического действия фенофибратов опосредован через активацию внутриклеточного ядерного рецептора, пролифератора пероксисом – PPAR-a (peroxisome-proliferator-activated receptor). Этот рецептор играет доминирующую роль во внутриклеточной регуляции экспрессии (переноса) и транскрипции (переписывания) геномов ДНК, ответственных за уровни липидного метаболизма и воспалительных цитокинов. Фенофибраты являются агонистами рецепторов, активируемых PPAR-a. Активация рецепторов PPAR-a в результате связывания с фенофибратом приводит к образованию гетеродимерных комплексов PPAR-a и ретиноидного рецептора – RXR (рис. 2). Далее они связываются с чувствительными элементами («элементами ответа пролифератора пероксисом») рецептора PPAR-a (PPRE – response elements) и стимулируют экспрессию с последующей транскрипцией генов, ответственных за функциональное состояние системы липазных ферментов. Активация липазной ферментной системы сопровождается уменьшением образования частиц, богатых ТГ, с благоприятной модификацией размеров частиц ЛПНП от мелких, плотных и атерогенных к более крупным, плавучим и менее атерогенным частицам, повышением уровня ЛПВП, что в итоге приводит к уменьшению атерогенности липидного спектра крови.
Установлено, что некоторые виды терапии оказывают отчетливое влияние на функциональное состояние эндотелия. При кратковременном приеме ингибиторов ангиотензинпревращающего фермента, антиоксидантов, эстрогенов, L-аргинина, блокаторов кальциевых каналов проявляется кратковременное положительное действие на функциональное состояние эндотелия. Тем не менее при длительной терапии МС лучший эффект на его функциональное состояние оказывают гиполипидемические препараты. Эти клинические наблюдения открывают более широкие возможности для внедрения эффективных медикаментозных воздействий на метаболические нарушения, связанные с ИР, что дает возможность улучшить прогноз и снизить риск сердечно-сосудистых осложнений уже на ранних этапах, когда заболевание еще не сформировалось как диагноз.
Материал и методы
С целью сравнительной оценки гиполипидемического эффекта статинов и фибратов нами проведен анализ историй болезни 66 пациентов, имеющих следующие признаки МС:
– абдоминальное ожирение (объем талии/объем бедер >1,0);
– ИМТ >25 кг/м2;
– артериальную гипертензию I-III степени (артериальное давление >145/95 мм рт. ст.);
– уровень глюкозы крови натощак >5,2 ммоль/л;
– атерогенную дислипидемию – индекс атерогенности (ИА) >2,2. Индекс ИР (ИИР) рассчитан как произведение показателя уровня глюкозы плазмы натощак (ммоль/л) на концентрацию иммунореактивного инсулина плазмы натощак (ИРИ, мкМЕ/мл), деленное на 22,5 (по D.R. Matthews, 1985).
В зависимости от назначенной гиполипидемической терапии больные, включенные в программу исследования, были распределены на две группы: в группу А вошли 27 пациентов, которым в состав комплексной терапии МС (Физиотенс® – моксонидин, метформин, a-липоевая кислота) был включен микронизированный фенофибрат (Трайкор 145 мг) в дозе 145 мг 1-2 раза в сутки; группу Б составили 39 пациентов с МС, у которых на фоне комплексного лечения гиполипидемическая терапия осуществлялась статинами – аторвастатином в дозе 80 мг/сут. Длительность лечения в среднем по группам составила 8,5±0,6 недели.
Результаты и обсуждение
Результаты обследования до и после лечения представлены в таблице, из которой видно, что исходные антропометрические, клинические и лабораторные показатели гликемического и липидного спектров крови по группам статистически не различались.
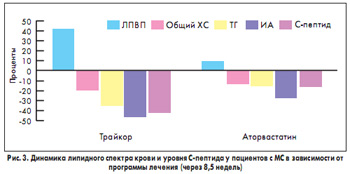 После проведенного лечения отмечена более выраженная положительная динамика со стороны липидного профиля среди пациентов с МС, в комплексную программу лечения которых был включен Трайкор 145 мг (рис. 3). В этой группе ИА снизился на 45,4%, т. е. практически вдвое (с 4,05±0,20 до 2,5±0,3; р<0,001), уровень ТГ уменьшился на 34,3% (с 2,10±0,25 до 1,3±0,20 ммоль/л; р<0,01), общий ХС – на 18,4% (с 5,9±0,3 до 4,8±0,3 ммодь/л; р<0,05), уровень ЛПВП повысился на 41,2% (с 0,85±0,07 до 1,20±0,08 ммоль/л; р<0,01). В группе Б ИА снизился только на 27,5% (с 4,0±0,3 до 2,90±0,15; р<0,01), уровень ТГ – на 15,4% (с 1,95+0,30 до 1,65+0,20 ммоль/л; р<0,01), общий ХС – на 14% (с 5,70+0,35 до 4,9±0,2 ммоль/л; р <0,05), концентрация ЛПВП увеличилась на 10,5% (с 0,95+0,04 до 1,05±0,05 ммоль/л; р<0,05). Также в группе А отмечено более выраженное снижение уровня С-пептида на 42,4% (с 5,9±0,4 до 3,4±0,3 нг/мл; р<0,01), а в группе Б аналогичный параметр снизился только на 16,3% (с 5,14+0,35 до 4,3±0,3 нг/мл; р<0,05).
После проведенного лечения отмечена более выраженная положительная динамика со стороны липидного профиля среди пациентов с МС, в комплексную программу лечения которых был включен Трайкор 145 мг (рис. 3). В этой группе ИА снизился на 45,4%, т. е. практически вдвое (с 4,05±0,20 до 2,5±0,3; р<0,001), уровень ТГ уменьшился на 34,3% (с 2,10±0,25 до 1,3±0,20 ммоль/л; р<0,01), общий ХС – на 18,4% (с 5,9±0,3 до 4,8±0,3 ммодь/л; р<0,05), уровень ЛПВП повысился на 41,2% (с 0,85±0,07 до 1,20±0,08 ммоль/л; р<0,01). В группе Б ИА снизился только на 27,5% (с 4,0±0,3 до 2,90±0,15; р<0,01), уровень ТГ – на 15,4% (с 1,95+0,30 до 1,65+0,20 ммоль/л; р<0,01), общий ХС – на 14% (с 5,70+0,35 до 4,9±0,2 ммоль/л; р <0,05), концентрация ЛПВП увеличилась на 10,5% (с 0,95+0,04 до 1,05±0,05 ммоль/л; р<0,05). Также в группе А отмечено более выраженное снижение уровня С-пептида на 42,4% (с 5,9±0,4 до 3,4±0,3 нг/мл; р<0,01), а в группе Б аналогичный параметр снизился только на 16,3% (с 5,14+0,35 до 4,3±0,3 нг/мл; р<0,05).
Динамика в липидном спектре плазмы крови, содержании С-пептида произошла на фоне снижения ИР (ИИР в группах А и Б уменьшился соответственно на 63,8 и 55,4%; р<0,001), о чем свидетельствовало снижение показателей ИРИ и глюкозы крови натощак в группе А на 51,4 и 24,1% соответственно (р<0,01), а в группе Б – на 45,7 и 18,5% соответственно (р<0,01). Нормализация гликемического профиля способствовала снижению показателя гликозилированного гемоглобина (НbA1c) по группам соответственно на 8,2 (А) и 7% (Б), что в целом по обеим группам составило – 7,1% (от 7,1±0,4 до 6,6+0,2%; р<0,05).
Подобный суммарный эффект со стороны липидного спектра и гликемического профиля крови не может быть объяснен влиянием сопутствующих препаратов (Физиотенс®, метформин), в равной степени использованных в обеих группах. Более выраженная положительная динамика липидного спектра и гликемического профиля крови у пациентов с МС в группе А, видимо, является следствием специфического биологического воздействия фибрата на метаболизм липидов и углеводов через ядерные рецепторы клеток исполнительных органов (печени, поджелудочной железы).
Биотрансформация ЛС осуществляется в печени под действием цитохромов Р450 (CYP450). У человека выделено более 30 энзимов системы CYP450, которые в максимальном количестве находятся в печени, где метаболизируется самая многочисленная группа субстратов, таких как ЛС, эндогенные вещества (статины, стероиды, жирные кислоты, простагландины). Статины (аторвастатин, ловастатин, симвастатин) метаболизируются до неактивных метаболитов под действием изофермента CYPЗА4. Трайкор 145 мг не взаимодействует со статинами ни на уровне цитохрома CYPЗА4, ни на уровне глюкоронирования, в его метаболизме участвуют другие подтипы CYP450 и UGT (уридиндифосфат-глюкоронозилтрансферазы), не участвующие в метаболизме статинов. Благодаря уникальному микросомальному метаболизму в печени Трайкор 145 мг безопасен при лечении пациентов с ожирением и ИР в комбинации со статинами.
Микронизированные фенофибраты обладают большей биодоступностью, способствуют снижению уровней ТГ, ЛПНП, увеличивают размеры частиц ЛПНП, повышают уровень ЛПВП и обратный транспорт ХС за счет стимуляции a-рецептора клеточного ядра, активируемого РРАR-a, более эффективно снижают уровень мочевой кислоты. Терапия микронизированными фенофибратами улучшает показатели липидного спектра крови, перекисного окисления липидов (снижаются уровни супероксиддисмутазы и малондиальдегида, образующихся при окислительном стрессе). Кроме того, улучшается состояние эндотелия у больных ИБС, что выражается в достоверной положительной динамике показателя ЭЗФР плечевой артерии, отсутствии вазоконстрикторных реакций при проведении пробы с реактивной гиперемией и снижении уровня фактора Виллебранда.
Улучшение функционального состояния эндотелия при лечении микронизированными фенофибратами носит комплексный характер: увеличивается активированное частичное тромбопластиновое время, возрастает фибринолитическая активность крови (время ХIIа-зависимого фибринолиза снижается на 47%, содержание фибринмономерных комплексов – в 4,7 раза), уменьшается уровень ингибитора активатора плазминогена-1.
Микронизированный фенофибрат снижает экспрессию адгезивных молекул и провоспалительных цитокинов, в частности ИЛ-6, ФНО-a и интерферона g, уровень С-реактивного белка.
Положительные клинические эффекты фенофибрата при лечении пациентов с признаками МС и СД 2 представлены в исследованиях FIELD и DAIS (Diabetes Atherosclerosis Intervention Study). В совокупности эти наблюдения свидетельствуют о благоприятном эффекте фенофибрата на макро- и микроциркуляторное русло, что клинически проявляется снижением уровня ТГ на 40-55%, повышением уровня ЛПВП на 15%, уменьшением риска осложнений ИБС на 25% (кардиопротекция), прогрессирования коронарного атеросклероза – на 42%, прогрессирования альбуминурии – на 14% (нефропротекция), частоты лазерного лечения диабетической ретинопатии – на 31% (офтальмопротекция).
Заключение
Таким образом, не претендуя на роль универсальных гиполипидемических средств, фибраты занимают свою нишу в лечении пациентов с дислипидемией и ИР. Они рекомендованы к применению у лиц с низким уровнем ЛПВП, высоким уровнем ТГ и нормальным/умеренно повышенным уровнем ЛПНП. Такой липидный профиль характерен для больных СД 2, лиц с ИР, абдоминальным ожирением и другими проявлениями МС. Не следует рассматривать фибраты как гиполипидемические агенты в «чистом» виде. Эта группа препаратов имеет широкий спектр благоприятных нелипидных эффектов, среди которых особый интерес представляют противовоспалительные, антиоксидантные, антикоагулянтные эффекты, влияние на функциональное состояние эндотелия сосудистого русла. Возможно, что, как и в случае со статинами, именно эти свойства фибратов играют ключевую роль в снижении риска сердечно-сосудистых осложнений.
Статья напечатана в сокращении.
«Фарматека», № 6, 2009 г.
СТАТТІ ЗА ТЕМОЮ
Проблема когнітивних розладів є однією з найважливіших у сучасній клінічній медицині. Це зумовлено не тільки збільшенням частки людей старшого віку серед населення, а й посиленням ролі стресу та інших патогенетичних чинників. У березні відбувся семінар «Академія сімейного лікаря. Біль в грудній клітині. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста», у якому прийняли участь провідні вітчизняні науковці і фахівці різних галузей. У рамках заходу професор кафедри військової терапії Української військово-медичної академії Міністерства оборони України, кандидат медичних наук Мар’яна Миколаївна Селюк представила доповідь «Війна та когнітивні порушення. Причина чи наслідок? Як вирішити проблему?». Подаємо огляд цієї доповіді у форматі «запитання – відповідь»....
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...




