Національний консенсус щодо ведення пацієнтів із гіперпролактинемією

М. Д. Тронько, д.мед.н., професор, академік НАМН України, член-кор. НАН України, директор ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України»
Ю. Г. Антипкін, д.мед.н., академік НАМН України, директор ДУ «Інститут педіатрії, акушерства і гінекології НАМН України», президент Асоціації педіатрів України
В. В. Камінський, д.мед.н., професор, член-кор. НАМН України, завідувач кафедри акушерства, гінекології та репродуктології НМАПО ім. П. Л. Шупика, головний позаштатний спеціаліст з акушерства та гінекології МОЗ України, виконавчий директор Асоціації акушерів-гінекологів України
Т. Ф. Татарчук, д.мед.н., професор, член-кор. НАМН України, заступник директора з наукової роботи, завідувач відділення ендокринної гінекології ДУ «Інститут педіатрії, акушерства та гінекології НАМН України», головний позаштатний спеціаліст із дитячої гінекології МОЗ України та інші (с. 11)
Протягом останніх років накопичено багато нових доказових даних про роль гіперпролактинемії в патогенезі дисгормональних порушень, раку молочної залози, розладів з боку кісткової системи в жінок, а також при пролактиномах гіпофіза. Це привело до перегляду діагностичних підходів і схем лікування цієї патології.
У документі представлено огляд існуючих методів діагностики та лікування гіперпролактинемії, запропоновано алгоритми ведення пацієнток цієї категорії в Україні.
Термінологія
Гіперпролактинемія – стійке підвищення рівня пролактину в сироватці крові. Синдром гіперпролактинемії – це симптомокомплекс, що виникає на фоні підвищеного рівня пролактину, найбільш характерним проявом якого є порушення функції репродуктивної системи, а в тяжких випадках, при існуванні пролактинсекретуючих пухлин гіпофіза – до неврологічних і нейроофтальмологічних порушень.
Епідеміологія
Офіційні дані про поширеність гіперпролактинемії в Україні та у світі відсутні. М. Kars et al. [7] в 2009 р. опублікували дослідження, за результатами якого поширеність гіперпролактинемії становила приблизно 10/100 000 у чоловіків і 30/100 000 у жінок, її пік спостерігався серед осіб віком 24-35 років. Гіперпролактинемія – найбільш розповсюджений гіпофізарний гормональний розлад, який зустрічається в клінічній практиці [6], що є причиною порушень менструальної та генеративної функцій у більш ніж 25-30 % випадків, а також багатьох доброякісних захворювань молочних залоз і матки, що в цілому негативно впливає на якість життя жінок.
Етіологія
Гіперпролактинемія може бути фізіологічною, патологічною та фармакологічною (табл. 1) [8, 13]. Встановлюючи її причину, необхідно виключити передусім найбільш поширені фізіологічні стани, такі як вагітність і годування грудьми [8].
Стресові умови, в т.ч. легкий стрес від венепункції, можуть викликати транзиторне підвищення рівня пролактину в сироватці крові, що слід враховувати при діагностиці [6]. Інші фізіологічні стани, що пов’язані з підвищеною концентрацією пролактину, включають фізичні вправи, сон і коїтус [9]. Патологічні причини – це специфічні стани передньої долі гіпофіза, порушення гіпоталамо-гіпофізарної системи і системні розлади, які впливають на підвищення сироваткового рівня пролактину.
Пролактиноми є найбільш поширеними (приблизно 40 %) пухлинами гіпофіза [10]. Зазвичай вони є доброякісними та мають моноклональне походження, залежно від розміру вони класифікуються на мікроаденоми з діаметром < 10 мм та макроаденоми з діаметром ≥ 10 мм (синоніми: мікро- та макропролактинома) [11]. Пролактиноми становлять близько 40 % від субклінічних аденом гіпофіза, виявлених при понад 10,4 % розтинів [12]. У той же час клінічні ознаки пролактиноми варіюються в діапазоні від 6-10 до 50/100 000 досліджених випадків, переважають в жінок і рідко зустрічаються у дітей [13, 14]. Важливо визначити наявність симптомів, пов’язаних з акромегалією, адже змішані аденоми, що секретують гормон росту і пролактин, були добре задокументовані [16].
Травми турецького сідла та параселярні травми, в т.ч. пухлини гіпофіза і негіпофізарні, наприклад гранулематозні захворювання (саркоїдоз, гістіоцитоз), а також черепно-мозкові травми можуть призвести до вторинної гіперпролактинемії зі збільшенням виділення гіпоталамусом дофаміну або з транспортуванням нейромедіатора до гіпофіза внаслідок ущільнення гіпофізарного стовбура [18].
Концентрації пролактину також можуть бути підвищені в пацієнтів із хронічною нирковою недостатністю, як правило, через зниження кліренсу гормона. Діаліз не підвищує рівень пролактину в сироватці крові, але він може бути нормалізований тільки після трансплантації нирки [19-21].
Первинний гіпотиреоз і його неадекватне лікування в анамнезі можуть викликати легку і помірну гіперпролактинемію шляхом підвищення синтезу гіпоталамічного тиреотропного гормона, який здатний стимулювати лактотрофи і викликати гіперплазію гіпофіза, імітуючи аденому [22, 23].
Така гіперпролактинемія може бути компенсована призначенням левотироксину як замісної терапії при гіпотиреозі [23, 24].
Синдром полікістозних яєчників часто асоціюється з гіперпролактинемією, ймовірно, за рахунок підвищеної ароматизації андрогенів в естрогени і стимуляції секреції пролактину зазвичай без гіпофізарних порушень. Однак цей синдром і пролактинома можуть співіснувати й потребують окремого лікування [25].
Іншою досить поширеною причиною непухлинного походження є стрес-індукована гіперпролактинемія. Рівень пролактину підвищується при психосоціальному стресі, однак зі значними індивідуальними відмінностями у величині відповіді. Характер реакції пролактину не відрізняється в осіб чоловічої і жіночої статі. Проте є певні свідчення, що в жінок спостерігається більш значне підвищення рівня пролактину, ніж у чоловіків, і це, можливо, залежить від рівня естрадіолу [75].
Гіперпролактинемія без встановленої причини визначається як ідіопатична [18]. Це стосується невеликих аденом гіпофіза, які не ідентифікуються методами візуалізації (МРТ головного мозку), але можуть спричиняти невелике підвищення рівня гормона. Відомо, що у 10 % випадків врешті-решт виявляється мікроаденома, прогресія якої
в макроаденому спостерігається рідко. Спонтанна нормалізація концентрації пролактину відбувається у 30 % пацієнтів з ідіопатичною гіперпролактинемією [18, 29].
Однією з найбільш частих причин гіперпролактинемії непухлинного походження є застосування лікарських засобів [6]. Нейролептики/антипсихотичні препарати можуть викликати гіперпролактинемію у 40-90 % хворих у зв’язку з антагоністичним ефектом дофаміну на такий тип ліків [26]. Терапія верапамілом спричиняє гіперпролактинемію у 8,5 % пацієнтів. У жінок, які приймають комбіновані оральні контрацептиви, у 12-30 % випадків можуть діагностуватися злегка підвищені рівні сироваткового пролактину [27, 28].
Клінічні ознаки
З огляду на те, що пролактин стимулює вироблення молока молочними залозами і що підвищена продукція гормона може змінювати синтез гонадами статевих стероїдів шляхом порушення пульсуючої секреції гонадотропін-рилізинг гормона і гонадотропінів, галакторея та дисфункція в репродуктивній сфері є клінічними маркерами патологічної і фармакологічної гіперпролактинемії. Однак у деяких пацієнтів гіперпролактинемія може мати безсимптомний перебіг [2, 6].
При макроаденомі гіпофіза, що продукує пролактин, окрім проявів, пов’язаних із гормональною гіперсекрецією, можуть з’являтися неврологічні та нейроофтальмологічні симптоми як наслідок локального компресійного синдрому (табл. 2) [10, 18]. Існують дані про участь пролактину в патогенезі пухлинних процесів. Відомо, що пролактин знижує синтез глобуліну, що зв’язує статеві гормони, збільшує утворення андрогенів в наднирниках.
Рецептори до пролактину виявлено як в молочних залозах, так і в міометрії та тканинах лейоміоми матки. Цей гормон має мітотичну активність щодо гладеньком’язових клітин лейоміоми матки, пригнічує апоптоз, стимулює синтез інсуліноподібного фактору росту 1 [56]. Матка є другим після гіпофіза органом за кількістю синтезованого пролактину. До 80 % жінок у перименопаузі на фоні підвищеного рівня пролактину можуть страждати від галактореї. Гіперпролактинемія може мати місце у 30 % пацієнток із вторинною аменореєю та у 75 % із синдромом аменореї -галактореї [6].
У жінок зі збереженою менструальною функцією гіперпролактинемія призводить до недостатності лютеїнової фази і, як наслідок, до безпліддя [10, 62]. Крім того, поширеним проявом гіперпролактинемії є передменструальний синдром із проявами мастодинії [58, 59] та розвиток із часом морфологічних змін у молочних залозах (фіброзно-кістозна мастопатія) [71].
У жінок у постменопаузальному періоді в результаті фізіологічного зниження рівня естрогенів класичні симптоми гіперпролактинемії відсутні, і захворювання визначається тільки за наявності компресійного синдрому в осіб із макроаденомами гіпофіза [28].
У чоловіків у результаті гіпогонадизму виявляється зниження статевого потягу, еректильна дисфункція, безпліддя і гінекомастія. Галакторея в чоловіків має місце у виняткових випадках при дуже високих концентраціях пролактину [10, 31]. Індукований гіперпролактинемією гіпогонадизм може призвести до зниження мінеральної щільності кісткової тканини та остеопорозу в осіб обох статей з переважною втратою хребетної трабекулярної кісткової тканини і підвищеним ризиком переломів, здебільшого в жінок із пролактиномами за відсутності лікування [18, 32]. Тривало існуюча гіперпролактинемія у пацієнток молодого віку призводить до втрати мінеральної щільності кісткової тканини та порушень формування піку кісткової маси. Доведено безпосередній корелятивний зв’язок між тривалістю аменореї і порушеннями мінеральної щільності кісток [10, 45]. Нормалізація менструального циклу не компенсує втрату піку кісткової маси, яка так і не повертається до норми [13]. Таким чином, стосовно молодих жінок необхідний обов’язковий контроль і корекція рівня пролактину для запобігання незворотній втраті піку кісткової маси.
Якщо гіперпролактинемія зумовлена макроаденомою гіпофіза, в залежності від розмірів пухлини можуть виявлятися компресійні симптоми. Проявами макроаденоми є сильний біль в лобній частині голови і порушення полів зору, які варіюються у широкому діапазоні від квадрантанопсії (випадіння верхніх або нижніх квадрантів поля зору) до класичної гетеронімної бітемпоральної геміанопсії (випадіння обох зовнішніх половин поля зору) [8]. За наявності великих пухлин ефект компресії інших клітин гіпофіза або стиснення гіпоталамо-гіпофізарної ніжки може викликати
гіпопітуїтаризм [28]. Атипові прояви, такі як параліч черепних нервів, частіше зустрічаються при злоякісних пухлинах гіпофіза [18].
У дітей симптоматика гіперпролактинемії є стертою і включає затримку статевого дозрівання в обох статей з первинною аменореєю та галактореєю в дівчаток і гінекомастією у хлопчиків. Через високу поширеність макроаденом гіпофіза в цій віковій групі пролактиноми часто супроводжуються неврологічними симптомами [28, 31].
Діагностика
Лабораторна діагностика
Для діагностики гіперпролактинемії достатньо одноразового аналізу на рівень пролактину в сироватці крові (> 25 нг мл у жінок і > 20 нг/мл у чоловіків) [13] за умови виключення стресу при венепункції. Якщо є сумнів щодо постановки діагнозу, пропонується повторне визначення концентрації пролактину в інший день шляхом двох вимірів з інтервалом у 15-20 хв для уникнення похибок, викликаних пульсуючою секрецією цього гормона [28].
Аналізи в динаміці для визначення рівня пролактину не є більш доказовими, ніж один вимір, тому використання таких тестів не рекомендується застосовувати при діагностиці гіперпролактинемії [13, 18]. Слід пам’ятати, що в фолікулярній фазі менструального циклу концентрація пролактину є нижчою, ніж у лютеїновій (але знаходиться в межах референтних значень) [13].
Помірне підвищення рівня пролактину або коливання його на верхній межі норми є більш характерним для стрес-індукованої гіперпролактинемії. Тому лабораторні показники повинні аналізуватись в комплексі з клінічною картиною та даними додаткових методів дослідження (оцінка стресу, УЗД молочних залоз та/або мамографія, визначення рівня гонадотропінів, естрадіолу та прогестерону).
Можуть мати місце дві конфліктні ситуації між клінічним і біохімічним діагнозом. Насамперед безсимптомна гіперпролактинемія може бути пов’язана з наявністю високих концентрацій димерів і полімерів пролактину (big пролактин та big-big пролактин), які мають більш низьку біологічну активність (макропролактинемія). Макропролактин слід вимірювати методом осадження імунних комплексів за допомогою полі етиленгліколю. Циркулюючий пролактин представлений у вигляді мономера із молекулярною масою 23,5 кДа (основна біологічно активна форма), ковалентно зв’язаного димера big пролактину з молекулярною масою 50 кДа та полімерної форми – макропролактину, або bigbig
пролактину. Макропролактин – ізоформа молекули пролактину з великою молекулярною масою (> 100 кДа) та більш низькою біологічною активністю. Істотне підвищення вмісту пролактину в сироватці крові за рахунок переважання макропролактину в циркулюючій крові (так званий феномен макропролактинемії) не призводить до симптомів гіперпролактинемічного гіпогонадизму, оскільки в такому випадку вміст низькомолекулярного біологічно активного пролактину залишається в фізіологічних межах. Саме тому при відсутності типових симптомів гіперпролактинемії можна запідозрити макропролактинемію (переважання big-big пролактину або наявність антипролактинових антитіл).
Ретроспективний аналіз [13] показав, що приблизно в 40 % випадків гіперпролактинемії має місце макропролактинемія, яка у 20 % пацієнток супроводжується галактореєю, у 45 % – оліго-/аменореєю; аденому гіпофіза діагностують у 20 % випадків [13]. Рекомендується вимірювання рівня макропролактину у хворих із безсимптомною гіперпролактинемією,
адже його можуть мати до 40 % пацієнтів, однак досліджень щодо відмінності між мономерним пролактином та макропролактином здебільшого не проводять [40, 41].
У пацієнтів із гіперпролактинемією без клінічних проявів слід виключити феномен макропролактинемії [13]. При макропролактинемії в крові переважають не мономерні біологічно активні фракції пролактину, а полімерні димери або комплекси молекули пролактину з імуноглобуліном класу G, що мають значну молекулярну масу і характеризуються відсутністю біологічних ефектів. Також можуть спостерігатися значні розбіжності між розміром пухлини гіпофіза і концентрацією пролактину, вторинна дисоціація пов’язана з hook-ефектом. Це артефакт лабораторії, який спостерігається в присутності високих концентрацій пролактину, здатних наситити антитіла при проведенні імунного аналізу, даючи помилково дуже низькі результати [35-39]. Крім того, за наявності великих пухлин із легкою гіперпролактинемією рекомендується повторити вимір рівня пролактину після розведення 1:100, адже цей крок допоможе диференціювати макропролактиноми і нефункціонуючі аденоми та виключити потенційний hook-ефект [13]. Hook-ефект – це
артефакт в методиці визначення рівня пролактину, при якому виміряний вміст гормона може бути незначно підвищеним або навіть нормальним при дуже високих справжніх значеннях. Тому в таких ситуаціях рекомендовано вимірювати рівень пролактину в пробах із розведенням, що дає можливість отримати справжні відомості про вміст гормона [13].
У разі невідповідності великих розмірів аденоми гіпофіза і помірного підвищення рівня пролактину рекомендується послідовне розведення сироватки крові для запобігання отриманню хибних результатів [13].
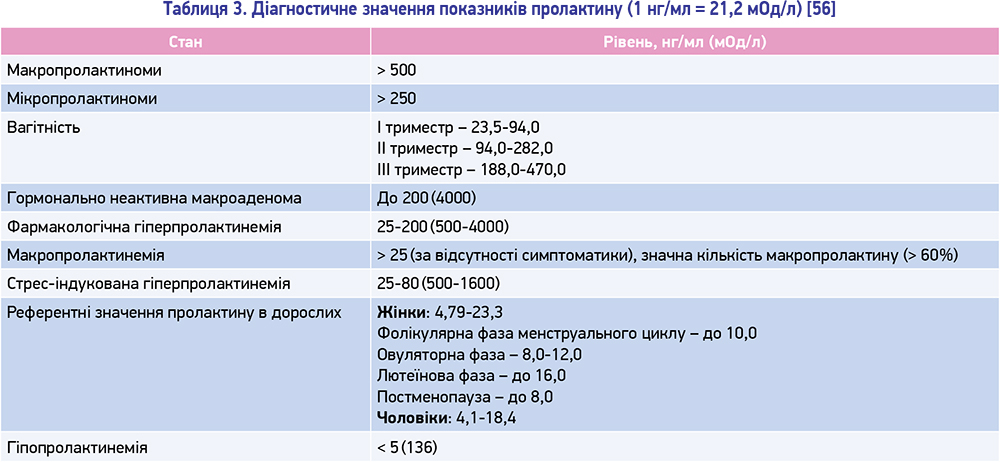
Прийнято вважати, що при рівні пролактину до ~ 200 нг/мл має місце фармакологічна гіперпролактинемія, > 250 нг/мл – мікропролактинома, ≥ 500 нг/мл – макропролактинома (табл. 3). Подібний розподіл є дуже умовним, оскільки мікропролактиноми можуть призводити як до мінімального, так і до дуже значного підвищення рівня пролактину [13, 74].
Візуалізаційні методи
МРТ з гадолінієм та з акцентом на селярній ділянці дає змогу дослідити анатомічні структури найбільш точно, а також виміряти розмір пухлини та її зв’язок зі зоровою хіазмою і кавернозним синусом, тому в даний час є методом вибору для діагностичної візуалізації [36].
Нейровізуальні дослідження показані пацієнтам із гіперпролактинемією будь-якого ступеня, щоб виключити наявність патології в гіпоталамо-гіпофізарній зоні [36].
Підозра на фармакологічну гіперпролактинемію
Рекомендується повторне визначення рівня пролактину через 72 год після відміни препарату, якщо це не призведе до погіршення стану пацієнта.
Механізм гіперпролактинемії при застосуванні визначених лікарських засобів (табл. 1) полягає в їхній антидофаміновій дії. Рівень пролактину при пероральному прийомі препаратів підвищується поступово, і для його нормалізації достатньо 3-денної перерви в терапії. Незважаючи на те що фармакологічна гіперпролактинемія часто має
безсимптомний перебіг, в деяких жінок можуть спостерігатися галакторея та аменорея, у чоловіків – зниження лібідо й еректильна дисфункція.
Інші методи обстеження при гіперпролактинемії
При встановленні діагнозу гіперпролактинемії рекомендується виключити вторинні причини, такі як вагітність, ниркова або печінкова недостатність, гіпотиреоз та наявність параселярних пухлин [18].
У жінок репродуктивного віку з аменореєю рекомендовано аналіз на β-хоріонічний гонадотропін людини або УЗД для виключення вагітності. Щоб виключити наявність гіпотиреозу при виявленні гіперпролактинемії, важливим є визначення концентрацій тиреотропного гормона і вільного тироксину.
При діагностуванні макропролактиноми або гормонально неактивної аденоми гіпофіза з супраселярним ростом показані консультації нейрохірурга, а також офтальмолога з оцінкою гостроти зору, стану зорового нерва і комп’ютерною периметрією (з метою визначення полів зору).
При тривалому анамнезі гіперпролактинемічного гіпогонадизму для оцінки мінеральної щільності кісткової тканини і діагностики остеопорозу доцільно виконати рентгенівську остеоденситометрію.
Лікування
Медикаментозне лікування гіперпролактинемії
Лікування гіперпролактинемії ґрунтується на її першопричині. За наявності фізіологічної гіперпролактинемії у пацієнтів з безсимптомною її формою і макропролактинемією медикаментозне лікування не показане [13, 73, 74]. У випадках патологічної гіперпролактинемії терапія призначається ендокринологом або акушером-гінекологом, при виявленні макропролактином обов’язковими є консультації окуліста і нейрохірурга, при фармакологічній гіперпролактинемії – психіатра та інших профільних спеціалістів за показаннями.
Поєднання гіперпролактинемії із гіпотиреозом у жінок має назву синдрому Ван Віка – Росса – Хеннеса [74]. Частота гіперпролактинемії при маніфестному гіпотиреозі становить 21-35 %, при субклінічному – 8-22 %. На фоні призначення
адекватних доз тиреоїдних гормонів (левотироксину) відзначається досягнення не тільки еутиреозу, але і нормопролактинемії. Тому при підтвердженні гіпотиреозу питання про подальше лікування гіперпролактинемії необхідно вирішувати тільки після нормалізації рівня тиреотропного гормона [22-24]. Однак терапія тиреоїдними гормонами не завжди приводить до зниження рівня пролактину, відновлення менструальної функції та овуляції, зникнення галактореї, тому в таких пацієнток слід розглянути питання про доцільність паралельного призначення агоністів дофаміну [74].
Мета лікування гіперпролактинемії полягає у нормалізації рівня біологічно активного пролактину для відновлення функції статевих залоз та припинення галактореї, а в разі, коли етіологічним фактором є пролактинома, – у зменшенні маси пухлини та ефектів локальної компресії.
У групі пацієнтів із безсимптомним перебігом гіперпролактинемії буде достатньо періодичного клінічного контролю [6, 36]. Фармацевтичні засоби, що застосовуються при лікуванні гіперпролактинемії і пролактином, представлені двома групами [72, 74]:
- похідні алкалоїдів ріжків (ерголінові агоністи дофаміну):
– препарати 2-бромо-α-ергокриптину (бромокриптин – I генерація);
– препарати 2-бромо-α-ергокриптину і 2-бромо-β-ергокриптину мезилату;
– препарати каберголіну (III генерація);
- похідні трициклічних бензогуанолінів (неерголінові агоністи дофаміну):
– препарати хінаголіду (II генерація).
Лікування, як правило, включає призначення агоністів дофаміну, таких як каберголін або бромокриптин, чи рослинних препаратів дофамінергічної дії на основі стандартизованих екстрактів прутняка звичайного, початкові і терапевтичні дози та побічні ефекти яких представлені в таблиці 4.
Каберголін є препаратом першої лінії як найбільш ефективний щодо нормалізації рівня пролактину та зменшення розмірів пухлини гіпофіза. Доза може бути підвищена в залежності від переносимості препарату. Концентрацію пролактину слід контролювати кожні 4 тиж при прийомі бромокриптину та кожні 8 тиж – каберголіну з титруванням препаратів для досягнення мінімальної ефективної дози.
Побічні ефекти спостерігаються при застосуванні всіх агоністів дофаміну, але вони є менш поширеними при використанні каберголіну та можуть бути зведені до мінімуму, якщо терапію розпочато з прийому дуже низької дози з їжею ввечері. Бромокриптин можна призначати в розділених щоденних дозах, а каберголін у розділених щотижневих дозах за потребою для поліпшення переносимості [10, 40]. Доза агоністів дофаміну зазвичай не перевищує 10 мг бромокриптину на добу та 3 мг каберголіну на тиждень [10].
Зниження дози препарату або його відміна рекомендовані не раніше ніж через 2 роки безперервного лікування агоністами дофаміну за умови тривалої нормалізації рівня пролактину та значного зменшення розмірів або відсутності пухлини за даними МРТ головного мозку.
Незважаючи на можливість відміни терапії при позитивній динаміці, до цього питання потрібно ставитися індивідуально. Небажано відміняти агоністи дофаміну при пролактиномах, що межують зі зоровим перехрещенням або кавернозним синусом. Основні критерії для відміни медикаментозної терапії такі [73]:
- тривалість лікування понад 2 роки;
- нормалізація рівня пролактину;
- відсутність аденоми за результатами МРТ;
- значне зменшення розмірів пухлини: на > 50 % від вихідного розміру; зменшення розміру макроаденоми < 10 мм;
- вагітність;
- постменопауза;
- можливість подальшого медичного спостереження.
Лікування фармакологічної гіперпролактинемії
Фармакологічна гіперпролактинемія виникає внаслідок застосування ряду медикаментозних засобів, що можуть підвищувати рівень пролактину (табл. 1). Гіперпролактинемія є вторинною по відношенню до дофамінергічних блокаторів, як правило, в діапазоні від 25 до 100 нг/мл, за винятком метоклопраміду та рисперидону, які можуть спричинити підвищення рівня пролактину навіть > 200 нг/мл [6, 44]. У більшості пацієнтів симптоми гіперпролактинемії відсутні, проте в чоловіків може спостерігатися зниження статевого потягу, а в жінок – галакторея та аменорея. До того ж існують дані про підвищений ризик втрати кісткової маси у жінок із гіперпролактинемією на фоні застосування нейролептиків як вторинний наслідок гіпогонадизму [45].
Концентрація пролактину повільно підвищується після перорального прийому визначених медикаментів (табл. 1) і нормалізується приблизно через 3 дні після його припинення [13, 46]. При відсутності симптомів у пацієнтів із підозрою на фармакологічну гіперпролактинемію рекомендується за можливості припинити лікування або замінити лікарський засіб на альтернативний, а пізніше провести повторне дослідження сироваткового рівня пролактину [13].
В осіб із симптомами гіперпролактинемії, початок якої не збігається з ініціюванням лікування, за неможливості відміни препарату показане проведення МРТ головного мозку для виключення об’ємних новоутворень гіпоталамуса або гіпофіза, які можуть бути тригерами гіперпролактинемії [13].
Необхідно оцінити можливість заміни одного психотропного препарату на інший, що не викликає гіперпролактинемії; таку терапію слід завжди проводити під контролем психіатра. Заміна препаратів не рекомендується для лікування хворих із безсимптомною фармакологічною гіперпролактинемією [13]. За необхідності агоністи дофаміну в поєднанні з психотропними засобами можна використовувати з особливою обережністю в пацієнтів із клінічними проявами гіперпролактинемії, в яких лікування не може бути відкладено або змінено через ризик загострення психозу або іншої
патології [13, 45, 47]. Деякі автори припускають можливість використання комбінованих оральних контрацептивів у жінок із вторинним гіпогонадизмом, зумовленим фармакологічною гіперпролактинемією [6, 13].
Лікування стрес-індукованої гіперпролактинемії
Помірне надпорогове підвищення рівня пролактину (табл. 3) під впливом перманентних стресів низької та середньої інтенсивності є стрес-індукованою гіперпролактинемією. Характерною ознакою цього розладу є відсутність постійного підвищення рівня пролактину в сироватці крові, також відзначаються його значні коливання протягом доби в залежності від стресових ситуацій.
Основними проявами стрес-індукованої гіперпролактинемії є розвиток передменструального синдрому, дисгормональних захворювань молочних залоз (мастопатія з мастодинією), клінічні ознаки недостатності лютеїнової фази, зниження рівня гонадотропінів і стан відносного естрогенного домінування. При обстеженні таких хворих після виключення аденоми гіпофіза потрібно провести комплексне гормональне обстеження для визначення рівня пролактину, естрадіолу, прогестерону та гонадотропінів. Крім цього, потрібно звернути увагу на частоту та рівень стресових навантажень та їхню тривалість.
При лікуванні розладів, асоційованих зі стрес-індукованою гіперпролактинемією, необхідно проводити терапію, спрямовану як на боротьбу зі стресом (модифікація способу життя, прийом заспокійливих та антидепресивних засобів, вітамінів групи В, зокрема піридоксину [вітаміну В6]), так і на корекцію безпосередньо гіперпролактинемії. Для цього найбільш раціонально застосовувати рослинні лікарські засоби, що містять стандартизовані за вмістом циклічних дитерпенів екстракти плодів вітекса священного (Vitex agnus castus).
Рекомендації щодо використання екстракту Vitex agnus castus ґрунтуються на результатах декількох рандомізованих подвійних сліпих плацебо-контрольованих досліджень, які продемонстрували його ефективність як щодо зниження рівня пролактину [57, 58], так і нормалізації естроген-прогестеронової рівноваги та відновлення ритмічної секреції гонадотропінів [61, 63].
Відновлення гормонального фону супроводжувалось ліквідацією мастодинії [58, 59, 65, 67], нормалізацією овуляторного менструального циклу та зниженням рівня стресової напруги [61, 63, 64]. Вітекс священний рекомендований Комісією Е в Німеччині (German Commission E)* до використання при передменструальному синдромі та мастодинії, асоційованими зі стрес-індукованою гіперпролактинемією.
Лікування пролактином
Основні цілі лікування хворих із пролактиномами включають [28, 36]:
- зниження секреції пролактину з нормалізацією його сироваткового рівня і купірування клінічних проявів гіперпролактинемії з особливим акцентом на відновлення функції статевих залоз;
- зменшення розміру пухлини з нівелюванням неврологічних симптомів;
- збереження функції гіпофіза та відновлення гормонального дефіциту;
- профілактику прогресування або рецидиву пухлини.
При мікропролактиномах основним маркером результативності лікування є зміна клінічних симптомів гіперпролактинемії, а в разі макропролактином контроль за зменшенням розміру пухлини також стає важливим [28]. Рекомендується тривале використання агоністів дофаміну для всіх пацієнтів із макроаденомами і мікропролактиномами за наявності клінічних проявів [13, 28].
Усі агоністи дофаміну є ефективними, препарати швидко нормалізують концентрацію пролактину, відновлюють репродуктивну функцію, усувають галакторею та зменшують розмір пухлини у більшості хворих, однак переважно використовуються бромокриптин і каберголін [10, 28].
Кілька досліджень продемонстрували перевагу каберголіну з погляду профілю переносимості, нормалізації концентрації пролактину, відновлення функції статевих залоз і зменшення розміру пухлини [46, 47], що, ймовірно, пояснюється більшою спорідненістю цього препарату до рецепторів дофаміну. Каберголін є ефективним у більшості пацієнтів, у т.ч. тих, хто не реагує на попереднє лікування бромокриптином [48]. У зв’язку з цим деякі автори рекомендують використовувати в першу чергу каберголін в порівнянні з іншими агоністами дофаміну [13, 28].
За даними дослідження R. Krysiak та B. Okopien (2014), призначення каберголіну є більш пріоритетним, ніж бромокриптину, у пацієнток із гіпер пролактинемією і супутньою дисліпідемією, кардіоваскулярними факторами ризику та інсулінорезистентністю. Як зазначає I. Shimon et al. (2014), лікування каберголіном жінок із пролактиномою покращує параметри метаболічного гомеостазу, такі як інсулінорезистентність, ліпідний профіль, товщина комплексу інтима-медіа, незалежно від зниження рівня пролактину.
Деякі автори припускають, що в пацієнток із аменореєю, зумовленою мікроаденомою гіпофіза, які не мають репродуктивних планів, лікування може включати використання комбінованих оральних контрацептивів або агоністів дофамінових рецепторів [13].
Встановлено, що гіперпролактинемія в жінок у постменопаузі значно підвищує частоту переломів хребців у порівнянні з контрольною групою.
Оскільки концентрації пролактину відповідають змінам розміру пухлини, слід щороку оцінювати рівень пролактину і проводити МРТ гіпофіза протягом перших 3 років лікування, а потім кожні 2 роки, якщо стан пацієнта є стабільним [10].
Необхідна тривалість терапії агоністами дофаміну все ще залишається невизначеною. У дослідженні А. Colao et al. [49] брали участь 200 пацієнтів з гіперпролактинемією, які отримували лікування каберголіном для досягнення нормалізації концентрації пролактину та зменшення розміру пухлини на > 50 % за наявності пролактиноми.
Учені повідомили про подальше рецидивування при відміні препарату в 24 % хворих із непухлинною гіперпролактинемією, у 31 % – з мікропролактиномою, у 36 % – з макропролактиномою. Більш висока частота ремісії спостерігалася в осіб, які не мали ніяких видимих залишків пухлини за результатами МРТ головного мозку на момент відміни лікування.
Рекомендується припинення терапії агоністами дофаміну у пацієнтів, які отримували її понад 2 роки та мають нормальну концентрацію пролактину без видимих залишків пухлини за даними МРТ головного мозку [13]. Медичне спостереження повинно здійснюватися з моніторингом концентрацій пролактину щоквартально протягом першого року після відміни препарату, а потім щорічно з проведенням МРТ у разі підвищення концентрації цього гормона [13].
Незважаючи на те що відповідь на агоністи дофаміну є позитивною в більшості пацієнтів, приблизно 5-10 % хворих резистентні до одного з цих препаратів [8]. Резистентними до агоністів дофаміну пацієнтами з пролактиномами вважаються ті, у кого рівень пролактину не може повернутися до норми зі зменшенням розміру пухлини на 30-50 % при використанні максимально переносимої дози препарату [53]. Резистентність найчастіше відзначалася у хворих чоловічої статі [73] та в пацієнтів із інвазивними аденомами в кавернозному синусі або супраселярній ділянці [51].
Резистентність до агоністів дофаміну – складне явище, пов’язане з декількома порушеннями: зменшенням афінності та кількості D2-рецепторів, зміною співвідношення ізоформ D2-рецепторів у вигляді зниження співвідношення D2S/D2L < 1, відсутністю продукції фактора росту нервів, що забезпечує аутокринну регуляцію проліферації і диференціювання лактотрофів гіпофіза [40, 56]. Пацієнти можуть мати різні реакції на терапію агоністами дофаміну, що проявляються нормалізацією концентрації пролактину без зменшення розміру пухлини або навпаки, інші ж можуть мати часткову стійкість до цих препаратів та вимагати більш високих їхніх доз, які зазвичай використовуються для досягнення клінічної відповіді [6]. У пацієнтів із клінічною симптоматикою гіперпролактинемії, в яких не знижується рівень пролактину та не зменшуються розміри пухлини гіпофіза при застосуванні стандартних доз агоністів дофаміну, рекомендується підвищити їхню дозу до максимально допустимої, перш ніж запропонувати оперативне втручання [13, 30]. Хворих, резистентних до бромокриптину, слід перевести на каберголін, адже у 80 % осіб у такий спосіб може бути досягнута нормалізація рівня пролактину [13].
Ехокардіографію для виявлення аномалій клапанів серця доцільно виконувати в пацієнтів, які отримують високі початкові дози агоністів дофаміну (наприклад каберголін > 2 мг/тиж) або їх стандартні дози при тривалості терапії понад 5 років [73].
Хірургічне лікування
З огляду на високу ефективність медикаментозного лікування тільки невелика частина пацієнтів з пролактиномами вимагає хірургічного втручання. Показання до проведення хірургічного втручання включають [73]:
- збільшення розмірів пухлини, незважаючи на оптимальну схему лікування;
- апоплексію гіпофіза;
- непереносимість медикаментозної терапії;
- наявність макропролактином, резистентних до лікування агоністами дофаміну;
- діагностування мікроаденом, резистентних до лікування агоністами дофаміну, в жінок, які планують вагітність;
- компресію зорового перехрестя, що зберігається на фоні медикаментозного лікування;
- наявність пролактиноми з кістозним компонентом, резистентної до лікування;
- появу ліквореї на фоні прийому агоністів дофаміну;
- виявлення макроаденоми в пацієнтів із психічними захворюваннями за наявності протипоказань до призначення агоністів дофаміну.
Проведення трансфеноїдальної операції рекомендується пацієнтам із непереносимістю високих доз каберголіну та резистентністю до інших препаратів цієї групи.
Виконання операції трансфеноїдальним доступом переважає над трансчерепним, проте ефективність лікування залежить від досвіду нейрохірурга і ступеня пухлинного поширення та може становити 80-90 % для мікроаденом, але < 50 % для макроаденом [10].
Променеве лікування
Променеву терапію слід застосовувати в разі необхідності впливу на залишкову тканину пухлини за неможливості проведення радикальної операції, у випадках непереносимості або резистентності до лікування агоністами дофаміну, при агресивних пролактиномах або карциномах [13].
Нормальної концентрації пролактину можна досягнути у третини пацієнтів, які пройшли курс променевої терапії, але потрібен тривалий проміжок часу, щоб отримати максимальний ефект [53].
Пролактинома і вагітність
Під час вагітності може спостерігатися збільшення розмірів пролактиноми у < 3 % пацієнток із мікропролактиномами, але у до 30 % жінок із макроаденомами [13]. З іншого боку, під час вагітності відбувається фізіологічне підвищення секреції пролактину (табл. 3), тому немає ніякої кореляції між концентраціями пролактину і збільшенням розміру пухлини. Найбільш сприятливим фоном для зачаття є повна нормалізація рівня пролактину та зменшення розмірів пухлини менше за 10 мм [13]. Крім того, препарати, що використовуються для лікування гіперпролактинемії, проникають через плацентарний бар’єр, тому повинні бути розглянуті потенційні несприятливі наслідки для плода [30].
Агоністи дофаміну не схвалюються для використання під час вагітності, тож як тільки вагітність підтверджена, рекомендується припинити лікування [10, 13].
Водночас існують повідомлення про 15 випадків використання каберголіну під час вагітності (Glezer A., Bronstein M., 2014). Усі вагітності пройшли без порушень розвитку плода, що розширило доказову базу безпечності застосування каберголіну у вагітних.
Для пацієнток із макроаденомами, особливо якщо пухлина є інвазивною або розташована дуже близько до зорової хіазми, пропонується продовжити дофамінергічну терапію під час вагітності [13].
Хоча каберголін не є тератогенним й не пов’язаний зі збільшенням кількості випадків ускладнень під час гестації, у вагітних із симптомним збільшенням пролактиноми пропонується застосовувати саме бромокриптин через наявність більшої кількості опублікованих досліджень щодо безпечності цього препарату [10, 30].
Не рекомендується вимірювати сироватковий рівень пролактину під час вагітності [13], в цей період проводиться динамічний клінічний моніторинг із особливим акцентом на неврологічні та нейроофтальмологічні симптоми, такі як головний біль або зміни полів зору. За наявності пролактином консультації ендокринолога та окуліста з проведенням комп’ютерної периметрії слід проводити 1 раз у кожному триместрі вагітності, а консультації нейрохірурга – за показаннями [73].
Проведення МРТ гіпофіза без гадолінію рекомендується під час вагітності тільки у хворих із клінічними ознаками росту пухлини [10, 13]. Пацієнткам, у яких незважаючи на лікування агоністами дофаміну відмічається поступове зменшення полів зору, виконується трансфеноїдальна хірургічна операція [55]. Трансфеноїдальну аденомектомію при
відсутності відповіді на медикаментозне лікування та при прогресивному погіршенні зору доцільно проводити у ІІ триместрі вагітності.
Пацієнткам із гіперпролактинемією пухлинного походження необхідно обмежити період годування грудьми до 6-12 міс, а в деяких випадках (наприклад при швидкому збільшенні розмірів макропролактиноми) взагалі варто відмовитися від нього [73].
В окремих випадках після вагітності спостерігається спонтанна ремісія захворювання. Поновлення лікування такі пацієнтки не потребують, однак подальше спостереження слід проводити впродовж щонайменше 5 років.
Лікування пролактином у постменопаузі
Тактика лікування пролактином у постменопаузі не відрізняється від такої у пацієнток інших вікових груп.
У хворих із мікропролактиномами можлива відміна терапії з подальшим динамічним контролем протягом 5 років.
*Репродуктивна ендокринологія, 2016, № 4 (30).
*Наукова консультативна рада Bundesinstitut fur Arzneimittel und Medizinprodukte – німецький аналог Управління з контролю за харчовими продуктами та лікарськими засобами США (Food and Drug Administration, FDA), створена 1978 р.
Інші автори:
О. О. Колеснік, д.мед.н., професор, директор Національного інституту раку МОЗ України
І. І. Смоланка, д.мед.н., професор, зав. науково-дослідним відділенням пухлин грудної залози та її реконструктивної хірургії Національного інституту раку МОЗ України, головний позаштатний спеціаліст
з онкохірургії МОЗ України
О. В. Грищенко, д.мед.н., професор, зав. кафедрою перинатології, акушерства та гінекології Харківської медичної академії післядипломної освіти
О. В. Булавенко, д.мед.н., професор, зав. кафедрою акушерства та гінекології № 2 Вінницького медичного університету ім. М. І. Пирогова
Ю. О. Дубоссарська, д.мед.н., професор, зав. кафедрою акушерства, гінекології та перинатології
ФПО ДЗ «Дніпропетровська медична академія МОЗ України»
З. М. Дубоссарська, д.мед.н., професор кафедри акушерства, гінекології та перинатології ФПО ДЗ
«Дніпропетровська медична академія МОЗ України»
О. С. Чабан, д.мед.н., професор, зав. відділом психіатрії та психосоматичної медицини Українського
НДІ соціальної і судової психіатрії та наркології
О. В. Бурлака, д.мед.н., ст. наук. співробітник відділення ендокринної гінекології ДУ «Інститут педіатрії, акушерства і гінекології НАМН України»
М. О. Гук, д.мед.н., лікар-нейрохірург відділення транссфеноїдальної хірургії аденоми гіпофіза
ДУ «Інститут нейрохірургії ім. А. П. Ромоданова НАМН України»
В. Л. Орленко, к.мед.н., ст. наук. співробітник ДУ «Інститут ендокринології та обміну речовин
ім. В. П. Комісаренка НАМН України»
О. О. Єфименко, к.мед.н., ст. наук. співробітник відділення ендокринної гінекології ДУ «Інститут
педіатрії, акушерства і гінекології НАМН України»
Список використаної літератури знаходиться в редакції
Журнал «Медичні аспекти здоров'я жінки» № 1 (106) ‘ 2017