Практичний посібник з лікування екзокринної недостатності підшлункової залози: руйнуючи міфи

Екзокринна недостатність підшлункової залози (ЕНПЗ) визначається як дефіцит екзокринних панкреатичних ферментів (ЕПФ), що призводить до нездатності організму забезпечити нормальне травлення. Порушення перетравлення нутрієнтів (і, зокрема, мальабсорбція жирів) спостерігається при зниженні інтрадуоденального рівня ЕПФ на 5-10% і спричиняє виникнення панкреатичної стеатореї, зменшення маси тіла, потенційне зниження якості життя.
ЕНПЗ, викликана муковісцидозом або хронічним панкреатитом (ХП), полягає в зниженні синтезу бікарбонатів і зменшенні інтестинального рН, що асоціюється з преципітацією жовчних кислот і порушенням формування міцел жиру. Мальабсорбція жирів посилюється зниженням панкреатичної секреції ліпази, коліпази і подальшим порушенням гідролізу внутрішньопросвітного жиру.
Розроблено безліч тестів для діагностики ЕНПЗ, проте вибір оптимального є складним, як і розуміння причини отримання хибнопозитивних результатів дослідження. Існує значна плутанина в дозуванні і схемі прийому ферментних препаратів (ФП). Метою цієї публікації є руйнування існуючих міфів і усунення наявної плутанини; стаття може бути використана як практичний посібник з діагностики та лікування ЕНПЗ.
Обговорення
Міф: ЕНПЗ розвивається тільки при зниженні екзокринної функції підшлункової залози (ПЗ) на ≥90%.
Думка експерта: ЕНПЗ являє поетапний процес і не є раптовим припиненням функціонування ПЗ, тому пацієнти можуть отримати деякі вигоди від ранньої діагностики захворювання.
Основною причиною ЕНПЗ є ХП. Іншими панкреатичними причинами є гострий розповсюджений некротичний панкреатит в анамнезі, рак ПЗ, перенесене оперативне втручання на ПЗ, муковісцидоз. До непанкреатичних причин відносять целіакію, цукровий діабет (ЦД), хворобу Крона (ХК), перенесене оперативне втручання на шлунку, синдром короткого кишечнику, синдром Золлінгера-Еллісона. Клінічні прояви ЕНПЗ можуть включати стеаторею (глинясті, рідкі, жирні, рясні випорожнення, що погано пахнуть), абдомінальний дискомфорт, здуття живота, зниження маси тіла. Незважаючи на те що характерною ознакою стеатореї вважаються плавучі калові маси, насправді це не так – більш специфічною ознакою є погане змивання фекалій зі стінок унітаза.
ХП
ХП є персистуючим запальним процесом з необоротними морфологічними змінами в ПЗ і прогресуючою втратою панкреатичної паренхіми. Відомо три великі групи мутацій, що сприяють розвитку ХП, – PRSS1, SPINK1, CFTR. Патогенетичні теорії включають оксидативний стрес, токсико-метаболічні розлади, порушення функціонування або обструкцію проток, некроз-фіброз.
При ХП приблизно у 20% пацієнтів розвивається ЕНПЗ, яка в подальшому призводить до прогресуючого зменшення кількості функціонуючих ацинарних клітин. Layer і співавт. довели, що час від появи перших симптомів захворювання до розвитку ЕНПЗ значно більше при ранньому початку ХП (медіана – 19,2 року) в порівнянні з відносно пізнім початком ідіопатичного ХП (медіана – 56,2 року) або алкогольного панкреатиту (медіана – 13,1 року).
Муковісцидоз
Муковісцидоз – аутосомно-рецесивне захворювання, викликане мутацією гена, який відповідає за функціонування каналів-переносників іонів хлору і є регулятором мембранної провідності при муковісцидозі (CFTR). Найбільш високий рівень експресії CFTR спостерігається у протокових епітеліальних клітинах; функція цього гена полягає в забезпеченні транспорту рідини та аніонів у просвіт кишечнику. Дисфункція гена CFTR призводить до зменшення обсягу внутрішньопросвітної рідини і зменшення рН, що спричиняє преципітацію білків у просвіті проток і порушення нормального функціонування ацинарних клітин.
ЕНПЗ найчастіше розвивається при народженні або дещо пізніше внаслідок внутрішньоутробного ушкодження ПЗ. Waters і співавт., проводячи скринінг новонароджених, встановили, що в 63% дітей з муковісцидозом ознаки ЕНПЗ були наявні вже на момент народження, а приблизно в 30% пацієнтів з наявною від самого початку збереженою екзокринною функцією ПЗ симптоми ЕНПЗ з’являлися через 36 міс. У пацієнтів з мутацією IV, V або VI класів (менш значущими мутаціями гена CFTR і відносно збереженою функцією цього гена), як правило, прояви ЕНПЗ виникають у другій половині життя. Corey та співавт. проаналізували дані 1 тис. хворих на муковісцидоз, за якими спостерігали в клініках Бостона і Торонто, і довели, що тривала відсутність медикаментозної корекції ЕНПЗ асоційована з погіршенням довгострокового прогнозу, а стан пацієнтів, які перебували на дієті з великим вмістом жиру (100 г/добу) і отримували високі дози ЕПФ, був кращим, ніж стан хворих, які дотримувалися дієти з низьким вмістом жиру і застосовували малі дози ФП. Близько 85% хворих на муковісцидоз потребують довічної замісної терапії панкреатичними ферментами (ЗТПФ).
Оперативне втручання на ПЗ
До факторів, що провокують виникнення ЕНПЗ після оперативного втручання на ПЗ, відносять зменшення об’єму панкреатичної тканини, широку денервацію після диссекції лімфатичних вузлів, післяопераційні анатомічні зміни. Такі захворювання, як рак ПЗ, внутрішньопротокова папілярно-муцинозна пухлина, передракові муцинозно-кістозні ураження і доброякісні новоутворення ПЗ, можуть створювати умови для появи ЕНПЗ внаслідок обструкції панкреатичної протоки. Ступінь тяжкості ЕНПЗ після оперативного втручання залежить від об’єму тканини ПЗ, що підлягала резекції, і функціональної активності паренхіми ПЗ, що залишилася; після тотальної панкреатектомії розвивається абсолютна ЕНПЗ. Механізм виникнення ЕНПЗ у пацієнтів, які перенесли операцію Уїппла, може бути пов’язаний з асинхронізацією утворення ендогенних панкреатичних ферментів і їх змішування з хімусом.
В одному великому систематичному огляді поширеність ЕНПЗ після дистальної панкреатектомії оцінена в 19-80%; такі значні коливання могли бути зумовленими використанням різних діагностичних методик. Після виконання операції Уїппла ЕНПЗ виникає в 56-98% випадків. Halloran і співавт. спостерігали 40 хворих, які перенесли резекцію пухлини ПЗ, і встановили, що ЕНПЗ є характерною для цієї патології, вона розвивається в післяопераційному періоді, але не супроводжується появою вираженої клінічної симптоматики. У пацієнтів із вперше виниклою ЕНПЗ зафіксована тенденція до погіршення якості життя.
Целіакія
Целіакія є хронічним запальним захворюванням кишечнику, яке розвивається в генетично схильних осіб і провокується прийомом глютену. Поширеність цього захворювання в США і Великобританії становить близько 1%. При целіакії, незважаючи на збереження екзокринної функції ПЗ, знижується рівень секреції холецистокініну, внаслідок цього виникає атрофія ворсинок у дванадцятипалій кишці, порушується скорочувальна функція жовчного міхура і знижується екзокринна секреція ПЗ.
ЦД
Термін «острівково-ацинарна вісь» використовується для опису ендо- та екзокринних взаємозв’язків усередині ПЗ, за допомогою якого відбувається судинна та фізіологічна взаємодія між різними типами клітин залози. Патофізіологічно ЦД може спричинювати виникнення ЕНПЗ, і, навпаки, тривалий час існуюча ЕНПЗ може спровокувати появу ЦД. При ЦД спостерігається кілька різних станів, здатних пояснити розвиток ЕНПЗ: брак трофічного впливу інсуліну (і, можливо, глюкагону та соматостатину) на ацинарні клітини, аутоімунне ураження острівців, що призводить до деструкції ендо- та екзокринної тканини ПЗ, зниження екзокринної панкреатичної секреції внаслідок діабетичної нейропатії. Недостатній синтез інсуліну й аутоімунний характер ураження при ЦД 1 типу пояснюють високу поширеність ЕНПЗ у порівнянні з такою при ЦД 2 типу (60 vs 30% відповідно). У нещодавно опублікованій статті Soave і співавт. доведено, що чим нижчий рівень імунореактивного трипсиногену (що свідчить про виражену внутрішньоутробну ЕНПЗ) у дітей, хворих на муковісцидоз, при народженні, тим раніше в них виникне важка ендокринна патологія (ЦД), пов’язана з муковісцидозом.
Як ми можемо діагностувати ЕНПЗ?
Міф: рутинна діагностика ЕНПЗ у пацієнтів із хронічною діареєю за допомогою визначення фекальної еластази (ФЕ) є ефективним і доцільним діагностичним методом з референтними значеннями 100-200 мкг/г, що відображають легку і середньоважку панкреатичну недостатність, а 100 мкг/г – важку ЕНПЗ.
Думка експерта: рутинна діагностика ЕНПЗ у пацієнтів із хронічною діареєю за допомогою визначення ФЕ не є достовірною при дослідженні несформованих калових мас.
Протягом останніх декількох років розроблено безліч тестів для діагностики ЕНПЗ; вони класифікуються як пряме або непряме визначення екзокринної функції ПЗ. У той же час багато з них мають низьку чутливість або специфічність (наприклад, сироваткова концентрація трипсину, якісне визначення жиру у фекаліях) і/або доступні тільки у великих центрах (13С-змішаний тригліцеридний дихальний тест).
72-годинний збір калу
Раніше золотим стандартом був метод 72-годинного збору калу, коли пацієнт дотримувався дієти з вмістом 100 г жиру на добу. Мальабсорбцію жирів діагностували при визначенні >7 г жиру в 100 г випорожнень протягом доби, виражену стеаторею – при ≥15 г/добу. На жаль, проведення цього дослідження займає багато часу, погано переноситься пацієнтами у зв’язку зі здуттям живота, абдомінальним дискомфортом, метеоризмом і посиленням стеатореї. Крім того, при зборі калових мас та підрахунку спожитого жиру можуть виникати помилки. Захворювання, що впливають на всмоктування жирних кислот (ХК, синдром надлишкового бактеріального росту, синдром короткого кишечнику), можуть стати причиною отримання патологічних результатів дослідження, незважаючи на незмінну екзокринну функцію ПЗ. 72-годинний збір калу використовувався в США для визначення ефективності ЗТПФ при ЕНПЗ.
Визначення ФЕ
ПЗ виробляє панкреатичну еластазу 1, високостабільний фермент, активність якого не змінюється під час кишкового транзиту. Вміст цього протеолітичного ферменту в калових масах визначається за допомогою твердофазного імуноферментного аналізу. У зв’язку з тим що панкреатична еластаза залишається стабільною під час кишкового транзиту, її вміст у фекаліях значно корелює з активністю екзокринної секреції ПЗ. Діагностичні тести, засновані на визначенні ФЕ, мають деякі переваги над іншими дослідженнями, позаяк не потребують тривалого збору калу або дотримання спеціальної дієти; вони мають високе негативне прогностичне значення і високу чутливість у діагностиці середньоважкої і важкої ЕНПЗ за умови дослідження сформованих калових мас. Референтні значення <200 мкг/г можуть застосовуватися в дітей і дорослих для діагностики ЕНПЗ. Деякі вчені вважають, що рівень ФЕ <100 мкг/г відповідає ЕНПЗ, а значення 100-200 мкг/г є невизначеними і складними для інтерпретації.
При легкій і середньоважкій ЕНПЗ визначення ФЕ характеризується меншою чутливістю (до 30%) і специфічністю, що може призвести до недостатньої діагностики захворювання. У дітей оцінка ФЕ є ефективним неінвазивним скринінговим тестом для діагностики ЕНПЗ, що має високе негативне прогностичне значення (99%) стосовно виключення цієї патології. Оскільки рівень ФЕ визначається як концентрація ферменту у фекаліях, вимір його в рідких калових масах завжди демонструватиме низькі результати; цей неінвазивний тест слід використовувати для оцінки функції ПЗ тільки в тих клінічних ситуаціях, коли підозрюється ЕНПЗ і є можливість досліджувати сформовані зразки калових мас. Це дослідження замінило громіздкий 72-годинний збір фекального жиру. Не слід переривати ЗТПФ для визначення ФЕ, оскільки свинячі ферменти не вступають у реакцію з антитілами до людської ФЕ.
Лікування ЕНПЗ
Міф: ЗТПФ слід починати з найменших доступних доз і приймати в будь-який час до вживання їжі і перед сном.
Думка експерта: титрувати дози ЗТПФ до передбачуваного ступеня ЗТПФ і використовувати ЗТПФ перед прийомом першої порції їжі, розглянути можливість додавання додаткових ферментів під час або наприкінці прийому їжі.
Дієтичні рекомендації і модифікація способу життя
Мальабсорбція жиру є основною причиною появи симптомів панкреатичної стеатореї, що призводять до зниження маси тіла і дефіциту жиророзчинних вітамінів А, D, Е, К. Хворим на ХП рекомендується дієта з низьким вмістом жирів з метою мінімізації больового синдрому, а в поєднанні із ЗТПФ – для ефективної терапії стеатореї. Однак у пацієнтів з муковісцидозом дотримання дієти з високим вмістом жирів й одночасним збільшенням дози ФП покращує стан легень, уражених при муковісцидозі; тому при цій патології не рекомендується дотримуватися дієти з низьким вмістом жирів. Слід додатково призначати жиророзчинні вітаміни А, D, Е, К (при наявності показань) і приймати їх під час ЗТПФ. Консультація дієтолога може допомогти оцінити відповідність раціону харчовим потребам. Доведено, що куріння є фактором ризику гострого панкреатиту і ХП, раку ПЗ і асоційоване зі зниженням екзокринної функції ПЗ. Тому при ЕНПЗ, обумовленій ХП, рекомендується відмовитися від куріння і вживання алкоголю.
ЗТПФ
Метою ЗТПФ є елімінація мальабсорбції, зменшення проявів мальдигестії, профілактика захворюваності і смертності, пов’язаних з мальнутрицією. Це твердження найбільш очевидне при муковісцидозі: у період до появи ЗТПФ діти гинули в перший рік життя. До 2010 р. FDA не контролювала випуск ФП, і вони мали різну активність. У 2010 р. FDA схвалила всі лікарські засоби, призначені для ЗТПФ. Слід підкреслити, що проведені клінічні дослідження були порівняно невеликими (число учасників <40), а також заздалегідь було відомо, що відібрані хворі відповідають на ЗТПФ. Усі препарати, що містять ферменти ПЗ, є екстрактом із ПЗ свиней (панкреліпаза), доступні в інкапсульованій формі випуску: мінімікросферах або мікротаблетках, що значно відрізняються за розміром частинок і рН-залежною кінетикою вивільнення. Кишковорозчинна оболонка капсул повинна бути резистентною до дії соляної кислоти і рН-чутливою для захисту ліпази від денатурації кислим вмістом шлунка. На жаль, плутанина виникла в результаті різного дозування ЗТПФ.
Ферменти, вкриті кишковорозчинною оболонкою, найбільш ефективні при рН >6. Разом із тим у хворих на муковісцидоз рН у дванадцятипалій кишці <6. Застосування кислотосупресивних препаратів може збільшити рівень рН у шлунку й теоретично підвищити ефективність ЗТПФ, зменшити вираженість симптомів ЕНПЗ. Результати опублікованих випробувань підтримують доцільність призначення антисекреторних препаратів хворим на муковісцидоз із рефрактерною стеатореєю. Однак нещодавно опубліковане ретроспективне дослідження не довело збільшення коефіцієнта абсорбції жиру (72-годинного збору фекального жиру) при призначенні інгібіторів протонної помпи дітям, хворим на муковісцидоз.
Панкреатичні ферменти, які не мають кишковорозчинної оболонки, як вважають, добре перемішуються з вмістом шлунка і швидко вивільняють велику кількість дуоденальної ліпази, потрібної для розщеплення жирів. Додаткове призначення кислотосупресивного препарату є необхідним для профілактики деградації панкреатичних ферментів, які не мають кишковорозчинної оболонки. Доведено, що такі ферменти зменшують інтенсивність болю в пацієнтів із ХП. Застосування незахищених екзогенних ферментів у поєднанні з ферментами, які мають кишковорозчинну оболонку, є рекомендованим для лікування рефрактерної ЕНПЗ.
Дозування і схема ЗТПФ
Доза і частота прийому ФП є складними питаннями ЗТПФ, оскільки в умовах in vivo різні кишковорозчинні мікросфери мають неоднакову біоеквівалентність; проведено невелику кількість порівняльних клінічних досліджень, у яких вивчали біодоступність ФП in vivo. У дослідженнях in vitro час розчинення (час напіввиведення – 49-71 хв) й оптимальне рН (5,0-5,8) ФП значно варіювали.
Різні країни рекомендували різні дози ЗТПФ. Австралійський панкреатичний клуб, Італійська асоціація з вивчення ПЗ та Іспанський панкреатичний клуб рекомендують дорослим приймати 25 000-50 000 ОД ліпази під час основного прийому їжі. На жаль, доказова база цієї рекомендації відносно слабка, що і підкреслив Австралійський панкреатичний клуб у своєму нещодавньому дослідженні з лікування ЕНПЗ.
У нідерландському дослідженні, проведеному Sikkens і співавт., показано, що 70% (n=161) пацієнтів з ЕНПЗ, викликаною ХП, не отримували належного лікування і мали скарги, обумовлені наявністю стеатореї, незважаючи на проведення ЗТПФ (середня кількість прийнятих ферментів – 6 капсул, 25 000 ОД ліпази/добу). Ці відмінності в рекомендаціях демонструють значну плутанину в питаннях дозування і схемі прийому ФП у практикуючих лікарів.
Немає єдиної думки й стосовно доцільної частоти прийому ФП. У 1977 р. DiMagno і співавт. довели, що прийом ФП під час їди є так само ефективним у зменшенні стеатореї, як і їх щогодинне використання.
Інші рекомендації, сформульовані на підставі різних оглядів, полягають у такому:
- необхідно прийняти 50% дози ЕПФ на початку прийому їжі, решту 50% – під час наступних прийомів їжі;
- ФП слід приймати під час або відразу після їди;
- 25% ферментів необхідно прийняти з першою ложкою їжі, 50% – під час прийому їжі і решту 25% ЕПФ – з останньою ложкою.
У нещодавно опублікованому рандомізованому тристоронньому перехресному дослідженні (n=24), у якому використовувалася доза ФП з розрахунку 40 000 ОД ліпази на один прийом їжі, порівнювалася ефективність трьох різних схем ЗТПФ (до, під час або після прийому їжі) за допомогою 13С-змішаного тригліцеридного дихального тесту для визначення коефіцієнта абсорбції жиру. Кількість пацієнтів, у яких нормалізувався процес перетравлення жирів, становила 50, 54 і 63% відповідно. Незважаючи на те що в дослідженні були зафіксовані статично недостовірні відмінності в ефективності використаних схем, автори цієї роботи рекомендували приймати ЗТПФ під час або після прийому їжі.
У пацієнтів з можливою ЕНПЗ і обтяженим анамнезом щодо патології ПЗ емпірична ЗТПФ може бути призначена без проведення формального обстеження. Адекватна відповідь, з одного боку, підтвердила б ЕНПЗ, з іншого – була необхідним лікуванням. При неадекватній відповіді на ЗТПФ слід врахувати ймовірність наявності поєднаної гастроінтестинальної патології: непереносимості лактози, бактеріальної кишкової інфекції, паразитарного захворювання (особливо лямбліозу), синдрому надлишкового бактеріального росту, патології жовчовивідних шляхів (холестазу), коліту, целіакії, синдрому короткого кишечнику, ХК. З-поміж інших причин неефективності ЗТПФ можуть бути: недостатнє дозування, погана прихильність до терапії, неправильний час прийому ФП, недотримання дієти.
Терапевтичні стратегії при недостатній відповіді на ЗТПФ:
- збільшити дозу;
- перевірити прихильність пацієнта до лікування;
- призначити антисекреторний препарат;
- розглянути доцільність додавання ферментів під час і наприкінці прийому їжі;
- обстежити для виявлення супутньої гастроінтестинальної патології.
 ФП слід приймати з першою ложкою їжі; необхідно розглянути доцільність додаткового призначення ферментів під час або наприкінці прийому їжі. Таким чином, якщо прийом їжі триває <15 хв, усю дозу ФП слід прийняти на початку їди; при прийомі їжі протягом 15-30 хв ми рекомендуємо прийняти половину дози ФП з першою ложкою їжі, другу половину – у середині прийому їжі; якщо прийом їжі триває >30 хв, рекомендуємо прийняти 1/3 дози ФП на початку вживання їжі, 1/3 – у середині і останню третину – наприкінці прийому їжі.
ФП слід приймати з першою ложкою їжі; необхідно розглянути доцільність додаткового призначення ферментів під час або наприкінці прийому їжі. Таким чином, якщо прийом їжі триває <15 хв, усю дозу ФП слід прийняти на початку їди; при прийомі їжі протягом 15-30 хв ми рекомендуємо прийняти половину дози ФП з першою ложкою їжі, другу половину – у середині прийому їжі; якщо прийом їжі триває >30 хв, рекомендуємо прийняти 1/3 дози ФП на початку вживання їжі, 1/3 – у середині і останню третину – наприкінці прийому їжі.
Обґрунтуванням такого способу прийому ФП є імітація фізіологічної активності організму, коли секреція ферментів ПЗ відбувається під час прийому їжі. Слід враховувати, що чим більше кількість з’їденої їжі і/або вміст жирів у раціоні, тим вище рівень продукції ЕПФ; кількість прийнятих капсул ЗТПФ має відповідати даному факту.
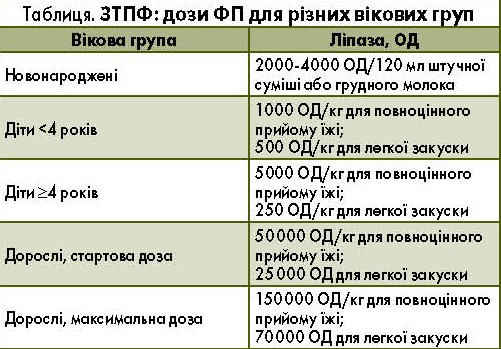
У таблиці представлено огляд режимів ЗТПФ для різних вікових груп.
Висновки
Після того як у 2010 р. FDA схвалила ЗТПФ, в арсеналі клініцистів з’явився надійний метод лікування ЕНПЗ. Цей спосіб терапії зменшує вираженість суб’єктивних і об’єктивних проявів, викликаних ЕНПЖ, таких як стеаторея, абдомінальний дискомфорт, зниження маси тіла, мальнутриція, ймовірно, навіть підвищує якість життя. ЗТПФ значно покращує стан хворих на муковісцидоз (до введення цього методу лікування новонароджені з цією патологією вмирали від мальнутриції протягом першого року життя). Однак серед практикуючих лікарів, як і раніше, залишається багато розбіжностей щодо найкращого способу діагностики ЕНПЗ, дозування і режиму ЗТПФ. Більшість країн розробили настанови із ЗТПФ, закликаючи до створення консенсусу і практичного керівництва з діагностики та лікування ЕНПЗ за допомогою ЕПФ.
Існує дві сфери, які потребують особливої уваги. По-перше, лікарі повинні знати, коли необхідно діагностувати ЕНПЗ, і користуватися відомими методами діагностики. Протягом останнього десятиліття значно змінилися способи виявлення ЕНПЗ: від ненадійного дослідження якісного складу фекалій і громіздкого 72-годинного збору фекального жиру до більш чутливого, але менш специфічного визначення ФЕ, особливо в пацієнтів з легкою/середньоважкою ЕНПЗ. Багато клініцистів не усвідомлюють необхідність дослідження сформованого випорожнення, що може стати проблематичним при хронічній діареї. По-друге, слід оптимізувати існуюче лікування ЕНПЗ. Результати досліджень розрізняються за рекомендованими дозами ЕПФ від 25 000 до 80 000 ОД ліпази на основний прийом їжі; також є невизначеність щодо режиму прийому ФП: до, під час або після прийому їжі.
Мета цих досліджень також істотно відрізняється: від зменшення вираженості панкреатичної стеатореї до елімінації мальдигестії і мальабсорбції, профілактики захворюваності і смертності, зумовлених мальнутрицією. Усе це ускладнюється великою кількістю ФП із широким діапазоном дозування. Тому не дивно, що серед клініцистів виникла плутанина в питаннях стосовно оптимального дозування, режиму прийому і цілей ЗТПФ.
Наші рекомендації щодо проведення ЗТПФ:
- титрувати дозу ФП до допустимої дози ЗТПФ;
- приймати ЗТПФ із першою ложкою їжі, розглянути доцільність додаткового призначення ферментів під час або наприкінці прийому їжі;
- обговорити раціональність використання капсульованих форм; можливе додаткове призначення ФП швидкого вивільнення та/або антисекреторних препаратів;
- коригувати дозу залежно від вмісту жирів у їжі.
Стаття друкується в скороченні.
Struyvenberg M. R. et al. Practical guide to exocrine pancreatic insufficiency – Breaking the myths. BMC Medicine (2017) 15: 29.
Переклала з англ. Тетяна Можина
Медична газета «Здоров’я України 21 сторіччя» № 6 (403), березень 2017 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...




