Інфекції шкіри і м’яких тканин: сучасні погляди і стратегія антибіотикотерапії

Інфекції шкіри і м’яких тканин (ІШМТ), які тепер в іноземній літературі трактують як гострі бактеріальні інфекції шкіри та структур шкіри, є частою патологією в клінічній практиці й у більшості випадків потребують застосування антибіотиків [9]. Мікробний спектр збудників інфекції характеризується зростанням резистентності до існуючих антибактеріальних середників. Водночас лікування хворих з ІШМТ додатково ускладнюється наявністю низки чинників, які призводять до тяжких ускладнень та інтоксикації організму (старечий вік, ожиріння, діабет та інші тяжкі супутні захворювання) [7]. Так, у 2004 році у Франції, Німеччині, Італії, Іспанії, Великій Британії 1,3 млн пацієнтів були госпіталізовані з приводу ІШМТ, у тому числі внаслідок флегмон (52,7%), локальної хірургічної інфекції (15,8%), діабетичної стопи (15,3%), пролежнів (12%). За експертними оцінками, в Україні частота захворювання на ІШМТ становить від 480 до 700 тис. пацієнтів на рік. Щороку в Україні в медичні установи звертаються за допомогою близько 1,5 млн хворих із трофічними виразками, близько 500 тис. хворих із синдромом діабетичної стопи (СДС).
ІШМТ унаслідок мікробної інвазії призводять до запалення епідермісу, дерми і підшкірної тканини з ознаками в різних комбінаціях локальної гіпертермії, почервоніння, набряку і болю. Шкіра – найбільший орган організму і разом із підшкірними м’якими тканинами, які включають шари жирової тканини, фасції і м’язи, становить основну частину тканин в організмі людини. Зазвичай шкіра колонізована ендогенною флорою і представлена різними видами стафілококів, коринебактерій, пропіонібактерій і дріжджами в цифрах, які можуть варіювати від декількох сотень до декількох тисяч на квадратний сантиметр у відповідних ділянках, таких як пахвова, пахвинна і промежина. Ця флора може діяти як конкурентний інгібітор патогенних мікробів. Дефекти шкіри, такі як виразки, опікові, хірургічні рани або рани внаслідок травм, спричиняють колонізацію із ширшим спектром бактерій. У низці випадків наведених дефектів шкіри ці колонізації бактерій не призводять до запалення, але іноді за деяких обставин інфекція може прогресувати й джерелом стають власне колонізації з оточуючих тканин [9]. Інфекція може потрапити в тканини зі шкіри пацієнта у разі неналежного дотримання правил особистої гігієни, а також гігієни постільної білизни, рук медичного персоналу тощо. З клінічної точки зору важливо розрізняти такі колонізації, які не потребують лікування антибіотиками [14, 16, 19].
Особливі труднощі виникають під час лікування хворих з інфекцією шкіри і м’яких тканин (трофічні виразки, пролежні, термічні ураження шкіри, післяопераційні і посттравматичні рани) за наявності алергії, лікарських і мікробних дерматитів, повторного інфікування ран госпітальними високорезистентними штамами (S. аureus, S. pyogenes, Enterococcus spp., P. аeruginosa, Enterobacteriaceae, Bacteroides spp.).
Зазвичай ІШМТ спричиняють кілька мікробів одночасно, проте у більшості випадків збудником є золотистий стафілокок (S. аureus). Особливу небезпеку становить широке поширення штамів, стійких до більшості антимікробних препаратів – бета-лактамних антибіотиків, аміноглікозидів, лінкозамідів, фторхінолонів. Отже, S. аureus посідає провідні позиції в запальному процесі як неускладненої, так і ускладненої ІШМТ. Зростання інфекції, спричиненої резистентними штамами, переважно метицилін-резистентним золотистим стафілококом (MRSA), асоціюється зі значним збільшенням показників захворюваності, летальності, тривалим перебуванням у стаціонарі й чималими витратами на лікування. Крім того, в лікувальних установах широко поширені грамнегативні бактерії сімейства Enterobacteriaceae (Klebsiella spp., Enterobacter spp., E. coli), які зазвичай є резистентними до бета-лактамів. Знання сучасної епідеміології і мікробіологічного спектра при ІШМТ є ключовими моментами для вибору відповідної антибіотикотерапії (АБТ) та оптимізації лікування [11, 15, 16].
Під час вибору засобів антибактеріальної терапії вкрай важливим є підхід, який визначається рівнем ураження м’яких тканин, особливостями перебігу захворювання і наявністю феномена резистентності [7, 9]. В цьому огляді розглянемо останні тенденції у стратегії антимікробної складової лікування ІШМТ.
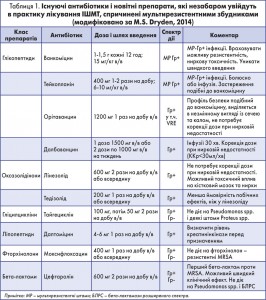
Згідно з аналізом літературних джерел стосовно досліджень АБТ ІШМТ нові антибіотики є вкрай необхідними, оскільки резистентність збудників до антибіотиків становить серйозну небезпеку для національних систем охорони здоров’я. На сучасному етапі вирішення проблеми резистентності бактерій до антибіотиків неможливе без впровадження в практику нових препаратів. Припинення розробки і синтезу нових середників загальмує подальший розвиток медичної науки, і майбутнє лікування хірурічної інфекції може виявитися під загрозою. Мультирезистентні бактерії швидко поширюються внаслідок неконтрольованого застосування антибіотиків і недостатньої профілактики інфекцій, недотримання санітарних норм населення в усьому світі [4, 8, 10]. Причиною надмірного використання антибіотиків є дефекти застосування діагностичних процедур, що призводить до того, що антибіотики призначають пацієнтам, у яких немає інфекції або за наявної інфекції вірусної етіології тощо. В таблиці 1 наведено узагальнений перелік уже існуючих препаратів, а також нових антибіотиків, які незабаром увійдуть в практику лікування.
Основна когорта наявних досліджень стосується порівняльної оцінки ефективності ванкоміцину та інших нових антибіотиків, зокрема лінезоліду [17, 20, 24, 25]. Для оцінки ефективності й безпечності лінезоліду порівняно з ванкоміцином для лікування ІШМТ, спричинених золотистим стафілококом, J. Yue і співавт. (2016) провели метааналіз відповідних рандомізованих контрольованих випробувань. Застосовували базу даних дослідників з усього світу, в тому числі групи фахівців Cochrane Wounds (2015), і ретельний пошук Pubmed, MEDLINE, EMBASE тощо. Аналіз було виконано на базі даних дев’яти рандомізованих клінічних досліджень, які містили результати обстеження 3144 хворих. Лінезолід виявився ефективнішим, ніж ванкоміцин у популяції (співвідношення ризиків, СР 1,05; 95% довірчий інтервал, ДІ 1,01-1,10) за ходом лікування, у тому числі при порівнянні клінічної (СР 1,09; 95% ДІ 1,03-1,16) і мікробіологічної ефективності (СР 1,08; 95% ДІ 1,01-1,16). Лінезолід корелює зі значно кращими результатами лікування пацієнтів із MRSA-інфекцією як за клінічними (СР 1,09; 95% ДІ 1,03-1,17), так і за мікробіологічними показниками (СР 1,17; 95% ДІ 1,04-1,32). Не встановлено суттєвої різниці в показниках смертності при застосуванні лінезоліду й ванкоміцину (СР 1,44; 95% ДІ 0,75-2,80). Водночас лінезолід більше асоціювався з гематологічними (тромбоцитопенія) побічними ефектами (CP 13,06; 95% ДІ 1,72-99,22) і розладами шлунково-кишкового тракту (СР 2,45; 95% ДI 1,52-3,94), а ванкоміцин – з побічними ефектами шкіри, у тому числі синдромом «червоної людини» (СР 0,04; 95% ДІ 0,01-0,29), свербежем (СР 0,36; 95% ДІ 0,17-0,75) і кропивницею (СР 0,27; 95% ДІ 0,12-0,58). На підставі аналізу об’єднаних даних рандомізованих контрольованих досліджень автори встановили, що лінезолід слід вважати кращим вибором для лікування пацієнтів з інфекціями, спричиненими золотистим стафілококом, ніж ванкоміцин, особливо при лікуванні пацієнтів з MRSA-інфекцією [17]. Окрім зазначеного доведено кращі фармакодинамічні показники лінезоліду: проникнення препарату в м’які тканини порівняно з ванкоміцином [22]. Утім, коли прийнято рішення застосовувати лінезолід, слід пам’ятати і брати до уваги ризик виникнення гематологічних і шлунково-кишкових побічних реакцій, які найчастіше спостерігаються у специфічних пацієнтів. Водночас наявність таблетованих форм лінезоліду спрощує процес курації, відтак – зменшує вартість лікування. У схожому за сценарієм дослідженні, в яке залучили 2652 пацієнти (1291/ванкоміцин і 1361/лінезолід) з ІШМТ, спричиненою MRSA, M. Bounthavong і D.I. Hsu (2010) довели, що клінічна й мікробіологічна ефективність виявилася вищою в лінезоліду без суттєвої різниці у показниках смертності між препаратами порівняння, хоча і з ймовірністю ризиків тромбоцитопенії, нудоти та діареї при застосуванні лінезоліду, що може обмежити використання препарату в лікуванні ІШМТ, спричиненої MRSA [5]. Цікаве дослідження провели H.W. Boucher і співавт. (2014), в якому порівняли ефективність далбаванцину в одній групі (525 пацієнтів із внутрішньовенним введенням препарату на 1-шу і 8-му добу лікування) і комбінації ванкоміцину (521 пацієнт, із внутрішньовенним введенням антибіотика впродовж 3 діб) із переходом на таблетовані форми лінезоліду тривалістю 10-14 днів у пацієнтів з ІШМТ – у другій групі. Автори довели, що далбаванцин у дозі 1 раз на тиждень не поступався за ефективністю схемі ванкоміцин-лінезолід. Для пацієнтів, інфікованих золотистим стафілококом, у тому числі штамами, стійкими до метициліну, клінічний успіх був помічений у 90,6% хворих, які отримували далбаванцин, і у 93,8% пацієнтів, які приймали ванкоміцин-лінезолід. У групі далбаванцину побічні ефекти спостерігалися в меншій кількості, ніж у групі ванкоміцин-лінезолід. Найпоширенішими небажаними явищами в обох групах, які пов’язані з лікуванням, були нудота, діарея, свербіж [18].
На сучасному етапі широко застосовують емпіричне лікування, яке часто триває необгрунтовано довго, деескалаційна терапія відбувається рідше. Численні програми зі стратегії АБТ намагаються вирішити ці питання [1, 12, 13]. З першого погляду вирішення цієї проблеми видається простим, однак його складно виконати. Оптимізація і покращення підходів до застосування протибактеріальних середників дасть змогу знизити феномен резистентності. Іще одними моментами у цьому напрямі є постійний контроль за інфекціями, вирішення проблем гігієни, що має на меті зменшення епізодів інфекцій та їх поширення, а відтак – зменшення кількості випадків застосування антибіотиків. Покращення діагностики інфекції (клінічної і мікробіологічної складової) забезпечить меншу необхідність у проведенні емпіричної терапії (табл. 2), а відкриття і впровадження в практику нових антибіотиків означатиме більший вибір для клініцистів у боротьбі із множинною полірезистентною інфекцією.
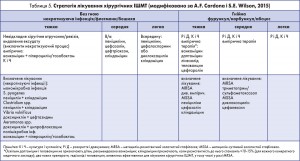
Раціональна АБТ і належне використання цієї групи препаратів є настільки важливими для бактеріальної екології та майбутнього охорони здоров’я, що всі лікарі повинні розглядати в кожному конкретному випадку, чи є клінічні показання до застосування антибіотиків (табл. 3).
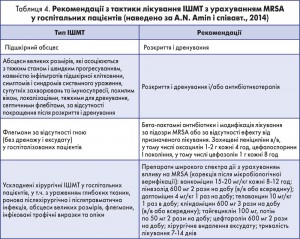
Як зазначено вище, штами MRSA – найпоширеніша причина ІШМТ в усьому світі внаслідок необгрунтованого застосування антибіотиків [4, 8, 10, 22]. Результати досліджень і рекомендації з раціональної АБТ MRSA-інфекції в Європі продемонстрували, що колонізації бактерій шкіри не мають потребувати застосування системних антибіотиків, хоча значна частина практикуючих клініцистів для боротьби з колонізацією MRSA застосовує власне системні антибіотики [5, 14, 15]. Зазвичай у позалікарняних ІШМТ наявні штами MRSA внаслідок попереднього перебування на госпітальному лікуванні. За гострої ситуації лікування часто включає розкриття і дренування вогнища інфекції з або без ад’ювантної терапії антибіотиками (табл. 4). У відділеннях невідкладної допомоги клінічні фармацевти, маючи конкретні дані, інформують чергових лікарів про кращий вибір із наявних антибіотиків для пацієнтів з ІШМТ. З іншого боку, дані відділу, який складає паспорт зі спектра флори кожної лікарні (на основі аналізу антибіотикограм), можуть стати орієнтирами емпіричного вибору антибіотика і допоможуть клініцистам у разі необхідності здійснити оптимальний вибір антибіотика для призначення терапії [8].
Лікування ІШМТ досягається за допомогою комбінації хірургічного методу й антимікробної терапії. Наприклад, для лікування підшкірних абсцесів насамперед застосовують хірургічне лікування (розкриття і дренування) і лише для пацієнтів, які не реагують на проведені початкові втручання, додатково призначають антибактеріальну терапію. Антибіотики призначають у разі поширення захворювання або абсцесів у складних для дренування ділянках, при швидкому прогресуванні інфекції, наявних ознаках системних захворювань, супутніх тяжких патологіях або імуносупресії. Провідна складова емпіричного вибіру антибіотика залежить від клінічних проявів ІШМТ. У більшості випадків, коли вірогідною причиною є грампозитивні інфекції і відсутня підозра на MRSA, застосовують пеніциліни, цефалоспорини, кліндаміцин або котримоксазол.
Там, де інфекція, ймовірно, має полімікробний характер (інфекції в безпосередній близькості від статевих шляхів, прямої кишки, СДС, кусані рани тощо), лікування антибіотиками має охоплювати широкий спектр патогенних мікроорганізмів. За таких умов АБТ може включати бета-лактамні антибіотики, захищені інгібіторами, препарати з підвищеною активністю стосовно грампозитивних штамів, такі як глікопептиди, карбапенеми, оксазолідінони, фторхінолони ІІІ-IV покоління і нові препарати (тайгециклін, цефтаролін тощо), в комплексі з належним доглядом за раною і раннім хірургічним втручанням, яке займає провідне місце у лікуванні ІШМТ [7, 9].
A.F. Cardona і співавт. (2015) довели, що ІШМТ є важливою причиною захворюваності та смертності серед госпіталізованих пацієнтів і стають серйозним викликом для клініцистів. Незважаючи на те що неускладнені форми ІШМТ успішно лікуються в амбулаторних умовах, тяжкі форми інфекції, які поширюються на підшкірну клітковину, фасції або м’язи, потребують складного різновекторного лікування. Рання діагностика, вибір відповідних антимікробних препаратів і своєчасне хірургічне втручання є ключем до успішного лікування [6]. Післяопераційні ранові інфекції – важлива складова ІШМТ і щороку спостерігаються у приблизно півмільйона пацієнтів у Північній Америці. ІШМТ також є потенційним джерелом для загрозливих життю бактеріємій і метастатичних абсцесів. Грампозитивні мікроорганізми, такі як золотистий стафілокок і Streptococcus pyogenes, є домінуючими організмами, які верифікуються на початку інфекційного процесу, тоді як грамнегативні мікроорганізми виявляються в хронічних ранах. Резистентний до метициліну золотистий стафілокок (MRSA) є потенційним джерелом для ймовірної генералізації інфекції, що потребує агресивної антибактеріальної терапії й хірургічного лікування. Останні застереження з приводу зменшення активності ванкоміцину включають наявність гетерорезистентності за наявності MRSA і зростання мінімальних інгібуючих концентрацій (>1 або 2 мкг/мл) препарату. Такі альтернативні засоби, як телаванцин, даптоміцин, лінезолід, цефтаролін, далбаванцин, орітаванцин і тедізолід, уже використовують для лікування тяжких інфекцій, спричинених MRSA. Хоча слід зазначити, що більшість із наведених препаратів відсутні на вітчизняному фармацевтичному ринку.
Для гнійної ІШМТ стратегія лікування за наявності легких форм інфекції полягає у розкритті й дренуванні; для захворювання середньої тяжкості із системними ознаками інфекції, крім вищенаведеного, додають пероральні антибактеріальні середники, для тяжких випадків інфекції, в тому числі неефективності після розкриття і дренування з додаванням пероральних антибіотиків або за наявності системних ознак інфекції (температура >38 °C, тахікардія >90 уд/хв, тахіпное >24/хв, зміни в показниках крові зі зсувом вліво) або імуносупресії, виконують повторні хірургічні втручання і парентеральне введення антибіотиків (табл. 5).
До легких видів негнійної ІШМТ належать типові флегмони/бешиха без гнійних вогнищ; до інфекції середньої тяжкості – типові флегмони/бешиха з наявністю системних ознак інфекції; тяжкої форми – неефективність пероральних антибіотиків, системні ознаки інфекції (див. вище тяжкі гнійні інфекції), імуносупресія або клінічні ознаки ураження глибоких тканин (були, відшарування і некрози шкіри, гіпотензія та ознаки органної дисфункції).
Однією із сучасних проблем лікування ІШМТ в усьому світі залишається СДС. Ця інфекція є найчастішою причиною нетравматичних ампутацій у людей, які страждають на цукровий діабет. У більшості випадків СДС існує потреба у системній терапії антибіотиками, і початковий вибір зазвичай є емпіричним [21]. Незважаючи на великий вибір антибіотиків, і досі маємо невизначеність стосовно того, що вважати кращим для лікування СДС. O.A. Selva і співавт. (2015) здійснили метааналіз 20 досліджень, в які залучили 3791 пацієнта. Випробування характеризувалися гетерогенністю за дизайном дослідження. Автори згрупували шістнадцять різних антибіотиків і розподілили їх на шість категорій: 1) антисиньогнійні пеніциліни (три дослідження); 2) пеніциліни широкого спектра дії (одне випробування); 3) цефалоспорини (два випробування); 4) карбапенеми (чотири випробування); 5) фторхінолони (шість випробувань); 6) інші антибіотики (чотири випробування). Тільки 9 із 20 досліджень були виконані за методикою оцінки результатів «сліпим конвертом». За підсумками лише третини досліджень було отримано достатньо інформації, на підставі якої можна зробити висновок, чи адекватно було виконано рандомізацію. Вісімнадцять із 20 досліджень отримали фінансування від фармацевтичної промисловості. Незрозумілою залишилася картина щодо швидкості клінічної ефективності між такими групами порівняння: 1) два альтернативних антисиньогнійних пеніциліни (одне випробування); 2) антисиньогнійного пеніциліну і пеніциліну широкого спектра дії (одне дослідження) або карбапенему (одне випробування); 3) пеніциліни широкого спектра дії і цефалоспорини ІІ покоління (одне випробування); 4) цефалоспорини та інші бета-лактамні антибіотики (два випробування); 5) карбапенеми і антисиньогнійні пеніциліни або пеніциліни широкого спектра дії (чотири випробування); 6) фторхінолони і антисиньогнійні пеніциліни (чотири випробування) або пеніциліни широкого спектра дії (два випробування); 7) даптоміцин і ванкоміцин (одне дослідження); 8) лінезолід і комбінація амінопеніцилінів з інгібіторами бета-лактамаз (одне дослідження); 9) кліндаміцин і цефалексин (одне випробування). У дослідженні зазначено, що карбапенеми в поєднанні з антисиньогнійними агентами супроводжуються меншою кількістю побічних ефектів, ніж антисиньогнійні пеніциліни. Інше додаткове дослідження не виявило істотних відмінностей у частоті побічних ефектів, коли зазначені вище препарати порівняння застосовували поодинці, але частотота випадків діареї була нижчою в групі, яка отримувала карбапенеми (0,58 СР; 95% ДІ 0,36-0,93). Доведено, що даптоміцин спричиняє менше побічних ефектів порівняно з ванкоміцином або іншими напівсинтетичними пеніцилінами (0,61 СР; 95% ДІ 0,39-0,94). Лінезолід призводить до більшої кількості побічних ефектів порівняно з ампіцилін-сульбактамом (2,66 СР; 95% ДІ 1,49-4,73), подібні результати дотичні тайгецикліну порівняно з ертапенемом з/без ванкоміцину (1,47 СР; 95% ДІ 1,34-1,60). Порівняно з іншими антибіотиками щодо безпеки застосування дослідження суттєвої різниці не встановили. Автори дійшли висновку, що аналіз досліджень не дає змоги визначити, який системний антибіотик або схема антибактеріального лікування СДС є найкращими з точки зору клінічної ефективності й безпеки застосування. На думку авторів, невисока якість досліджень зумовлена різними підходами до сценарію дослідження, методиками виконання (тривалість лікування, терміни, упродовж яких оцінювали результат тощо) і трактування отриманих результатів. Будь-які подальші дослідження в цій галузі слід проводити з використанням стандартних критеріїв для класифікації ступеня тяжкості інфекції, визначити чіткі показники для аналізу результатів, встановити відповідну тривалість лікування [23].
Дефекти шкіри і м’яких тканин, відомі як пролежні й виразки внаслідок компресійної травми, – локалізовані ділянки пошкодження тільки шкіри або із залученням глибше розміщених тканин. Діапазон лікування включає застосування пов’язок, просякнутих препаратами з антимікробними властивостями, антисептиків і системних антибіотиків. Задля полегшення процесу прийняття оптимальних рішень, які стосуються використання антисептиків або АБТ під час лікування пролежнів, G. Norman і співавт. (2016) здійснили аналіз, який є одним із видів Кокранівських оглядів, що досліджують застосування антисептиків і антибіотиків при різних типах ран, у тому числі пролежнів. Аналіз грунтувався на результатах 12 досліджень (576 пацієнтів). У кожному дослідженні проводили одне порівняння з незначною кількістю пацієнтів у короткі терміни. За якістю доказова база варіювала від помірної до дуже низьких випробувань. Автори висловили схожу думку, що відносні ефекти системного й місцевого лікування пролежнів протимікробними засобами залишаються незрозумілими. Дослідження були невеликі за об’ємом, клінічно гетерогенні, зазвичай нетривалі, що зменшує їхню цінність для включення в рекомендації або протоколи лікування [3].
Трофічні виразки нижніх кінцівок венозного генезу – тип хронічної рани, яким протягом життя страждають близько 1% дорослого населення в розвинених країнах. Багато з цих ран контаміновані бактеріями з ознаками клінічно значущої інфекції. Наявність інфекції може гальмувати процес загоєння виразок. Для профілактики та лікування інфекції венозних трофічних виразок нижніх кінцівок використовують дві основні стратегії: системні антибіотики й актуальні антибіотики місцевої дії або антисептики. S. O’Meara і співавт. (2014) провели аналіз 45 контрольованих рандомізованих досліджень, які охоплювали 4486 пацієнтів. Деякі дослідження були невеликими за об’ємом з огляду на когорту пацієнтів, і більшість із них були виконані на високому рівні. Автори засвідчили, що на сьогодні немає жодних доказів для підтримки гіпотези стосовно рутинного використання системних антибіотиків у прискоренні процесу загоєння трофічних виразок нижніх кінцівок. Проте відсутність надійних доказів не означає, що немає необхідності у припиненні подальших досліджень з ефективності будь-якого з розглянутих агентів. З точки зору препаратів місцевої дії, наявні дані не підтримують рутинне застосування пов’язок на основі меду або срібла. Перш ніж зробити остаточні висновки про ефективність повідон-йоду, препаратів на основі перекису водню, етакридинлактату, хлорамфеніколу, фраміцетину, мупіроцину, етакридину або хлоргексидину в загоєнні трофічних виразок, необхідно проводити подальші дослідження. У світлі зростаючої проблеми стійкості бактерій до антибіотиків, згідно із світовими розробками і думкою компетентних фахівців, на сьогодні рекомендовано застосовувати антибактеріальні препарати тільки у разі клінічної значущої інфекції, а не у випадках бактеріальної колонізації [2].
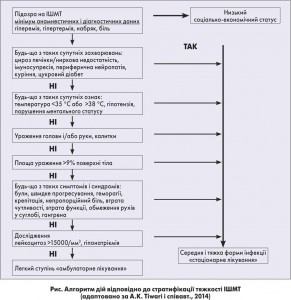
На думку A.K. Tiwari (2014) та інших дослідників, для зниження захворюваності і смертності внаслідок ІШМТ стратифікація ступеня тяжкості захворювання є необхідним компонентом для алгоритму ефективності вчасно розпочатого лікування. Позаяк патологія ІШМТ характеризується різноманітністю клінічної картини, часто виникають труднощі діагностики й складно визначити оптимальний підхід до лікування, оскільки наявні прояви інфекції можуть маскуватися у вигляді клінічних симптомів і синдромів інших захворювань [26]. Найважливішими і необхідними кроками для встановлення правильного діагнозу є знання анатомічних і функціональних особливостей шкіри і м’яких тканин, своєчасне проведення аспірації з патологічних вогнищ, біопсії тканин і рентгенографічного обстеження для визначення ступеня поширення і глибини ураження. Нижні кінцівки, промежина і черевна стінка – ділянки, які найчастіше зазнають ураження ІШМТ із тяжким клінічним перебігом та інтоксикацією організму. З огляду на зазначені вище проблеми, на рисунку подано алгоритм дій для ІШМТ.
Розрізняють легкі, середні і тяжкі форми ІШМТ з урахуванням клініко-демографічного профілю пацієнта. До найтяжчих груп хворих належать пацієнти чоловічої статі з низьким соціально-економічним статусом, які більше схильні до травматизації через свої умови праці та побуту.
До інших чинників ризику відносять куріння і цукровий діабет, температуру понад 38 °C, гіпотонію, лейкоцитоз >15000 мм3, гіпонатріємію. Наявність гангрени, міхурів із серозно-геморагічним умістом, крепітації збільшує тяжкість інфекції. Критеріями тяжкої інфекції є площа ураження >9% поверхні тіла, з ураженням кінцівок, голови, калитки й випадками, коли інфекція пов’язана із супутніми захворюваннями і гангреною. Втрата чутливості, рухів/функції ураженої кінцівки та обмеження рухів у суглобах є додатковими критеріями тяжкості інфекції.
Отже, неадекватна антибіотикотерапія може призвести до негативних результатів лікування і зростання резистентних бактерій. Стратифікація ступеня тяжкості ІШМТ – важлива складова у виборі тактики лікування (хірургічного і медикаментозного) пацієнтів, які поступають в ургентному порядку в хірургічні відділення, що дає змогу скоротити терміни лікування і показники летальності. Наявність паспорта лікарні зі спектра флори може стати орієнтиром емпіричного вибору антибіотика і допоможе клініцистам у разі необхідності зробити оптимальний вибір антибактеріального середника для лікування ІШМТ. Лікування хірургічної інфекції шкіри і м’яких тканин фокусується на хірургічному контролі джерела інфекції та антимікробній терапії, яка враховує індивідуальні чинники ризику пацієнта і мультирезистентних штамів бактерій. Препаратами вибору в подібних клінічних ситуаціях є ванкоміцин, лінезолід та інші наявні й нові антибіотики, а вища активність лінезоліду стосовно грампозитивних збудників та особливості фармакокінетики роблять його вибір кращим.
Висновки
• Лікування ІШМТ – серйозна проблема сучасної медицини з огляду на глобальне зростання резистентності грампозитивної флори до традиційних антибіотиків, зокрема метицилін-резистентних штамів стафілококів, а стратифікація ступеня тяжкості ІШМТ – важлива складова у виборі тактики лікування.
• Наявність паспорта лікарні щодо спектра флори стане орієнтиром емпіричного вибору антибіотика й допоможе клініцистам у разі необхідності зробити оптимальний вибір антибактеріального середника для лікування ІШМТ.
• У зв’язку з вищезазначеним слід вносити у протоколи лікування препарати з вираженою активністю проти MRSA з урахуванням даних локального моніторингу – ванкоміцин, лінезолід, тайгециклін тощо.
• До важливих характеристик лінезоліду належать, зокрема, активність стосовно штамів, які є стійкими до ванкоміцину, можливість проведення ступінчастої терапії (внутрішньовенно і всередину), кращі фармакокінетичні властивості й переносимість.
Список літератури знаходиться в редакції.
СТАТТІ ЗА ТЕМОЮ Інфекційні захворювання
Застуда та інші інфекції дихальних шляхів – актуальна проблема охорони здоров’я через високий рівень захворюваності, що перевищує такий інших інфекційних патологій. З метою підвищення кваліфікації лікарів загальної практики та обміну досвідом з актуальних питань лікування інфекційних захворювань у лютому була проведена науково-практична конференція «Академія сімейного лікаря. Для кого небезпечні сезонні інфекції? Загроза сезонних інфекцій. Погляд пульмонолога, інфекціоніста, алерголога, ендокринолога, кардіолога, педіатра» за участю провідних вітчизняних спеціалістів-практиків....
Гостра застуда – самообмежувальне захворювання верхніх дихальних шляхів. Застуда зазвичай має помірну тяжкість і виникає під дією низки вірусів різних родин (найчастіше – риновірусів). Основними симптомами застуди є біль у горлі, гострий кашель, чхання, закладеність та виділення з носа (рис. 1). Інкубаційний період застуди триває зазвичай 24-72 год, а сама хвороба – в межах 1 тиж. Застуда асоціюється зі значним економічним тягарем для суспільства через потребу у візитах до лікаря, витрати на фармакопрепарати і біодобавки та тимчасову непрацездатність (Al-Haddad M.S. et al., 2016). ...
Цефалоспорини займають провідну позицію серед усіх антимікробних препаратів за частотою використання. Популярність цих антибіотиків пояснюється багатьма чинниками: широким спектром антимікробної дії; бактерицидним механізмом дії; стійкістю до ферментних систем патогенів; доброю переносимістю і невеликою частотою побічних проявів; простотою та зручністю дозування. В останні роки до стандартних протоколів лікування включають цефалоспорини IV i V поколінь, але в рутинній клінічній практиці найчастіше застосовуються препарати I-III поколінь, найбільш відомими представниками яких є цефоперазон і цефтріаксон. У статті викладено порівняльну характеристику цих двох препаратів з огляду на вимоги сучасних стандартів. ...
Сучасні епідеміологічні спостереження свідчать про те, що масові спалахи інфекційних хвороб значно почастішали. Якщо раніше пандемії виникали в середньому раз на 40 років, то за 23 роки ХХІ ст. людство вже зустрілося із двома широкомасштабними спалахами: пандемією грипу А (H1N1) у 2009 році та пандемією коронавірусної інфекції (SARS-CoV-2) у 2020 році. За даними лондонської компанії Airfinity Ltd., яка займається прогнозуванням здоров’я, імовірність того, що пандемія (так само смертоносна, як і COVID-19) може виникнути в наступному десятилітті становить 27,5%. Серйозною загрозою для громадської охорони здоров’я, за даними спеціалістів Всесвітньої організації охорони здоров’я (ВООЗ), є віруси Ебола, Марбург, Ласса, Ніпа і Зіка через їхній епідемічний потенціал, але не можна забувати і про інфекції, що вважаються контрольованими....