Місце сучасних цефалоспоринів у терапії риносинуситів
Наприкінці 2016 року Генеральна Асамблея Організації Об’єднаних Націй висловила занепокоєння щодо зростання резистентності патогенних мікроорганізмів до антимікробних препаратів та ухвалила рішення про нарощування зусиль світової спільноти й активізації багатовекторної діяльності на національних рівнях щодо боротьби з цією проблемою. В інформаційному бюлетені Всесвітньої організації охорони здоров’я (ВООЗ), який було опубліковано восени 2016 року, відображено негативну динаміку рівнів антибіотикорезистентності до багатьох патогенних мікроорганізмів в усіх регіонах світу.
 У рекомендаціях ВООЗ перше місце серед заходів із протистояння зростаючій антибіотикорезистентності посідає раціональна антибіотикотерапія. Останнім часом медична спільнота часто вживає це словосполучення, проте чи завжди його розуміють правильно? Насправді багато хто з лікарів забувають, що «раціонально» – це не лише «призначення за показаннями». Це поняття охоплює і врахування локальних даних поширеності патогенних мікроорганізмів, і тривалість терапії, і, безумовно, групу лікарських засобів та конкретний препарат. Про актуальність проблеми нераціональної антибіотикотерапії та місце сучасних цефалоспоринів в терапії пацієнтів із риносинуситами (РС) нам розповів головний позаштатний спеціаліст Міністерства охорони здоров’я (МОЗ) України зі спеціальності «Оториноларингологія», завідувач кафедри оториноларингології та офтальмології з курсом хірургії голови та шиї Івано-Франківського національного медичного університету, доктор медичних наук, професор Василь Іванович Попович.
У рекомендаціях ВООЗ перше місце серед заходів із протистояння зростаючій антибіотикорезистентності посідає раціональна антибіотикотерапія. Останнім часом медична спільнота часто вживає це словосполучення, проте чи завжди його розуміють правильно? Насправді багато хто з лікарів забувають, що «раціонально» – це не лише «призначення за показаннями». Це поняття охоплює і врахування локальних даних поширеності патогенних мікроорганізмів, і тривалість терапії, і, безумовно, групу лікарських засобів та конкретний препарат. Про актуальність проблеми нераціональної антибіотикотерапії та місце сучасних цефалоспоринів в терапії пацієнтів із риносинуситами (РС) нам розповів головний позаштатний спеціаліст Міністерства охорони здоров’я (МОЗ) України зі спеціальності «Оториноларингологія», завідувач кафедри оториноларингології та офтальмології з курсом хірургії голови та шиї Івано-Франківського національного медичного університету, доктор медичних наук, професор Василь Іванович Попович.
– Найчастіше випадки нераціональної антибіотикотерапії спостерігають на первинній ланці надання медичної допомоги. По-перше, це пов’язано з величезним обсягом хворих, які звертаються до амбулаторій сімейної медицини та районних поліклінік. По-друге, лікарі первинної ланки в рамках реформування системи охорони здоров’я зобов’язані лікувати пацієнтів із новою для них патологією – синуситами, отитами, циститами тощо. По-третє, сьогодні левову частку дільничних терапевтів, особливо в регіонах, становлять лікарі похилого віку, досвід яких стає не тільки помічником, а й завадою на шляху сучасних засобів лікування. Однак і лікарі стаціонарної ланки припускаються помилок, зокрема щодо призначення антибактеріальних препаратів для парентерального застосування, найчастіше – цефалоспорину ІІІ покоління цефтриаксону. Варто зазначити, що сьогодні парентеральне призначення цефалоспоринів, коли фармацевтична промисловість виробляє по-справжньому потужні й безпечні препарати для перорального застосування, є абсолютно недоцільним.
Своєрідною страховкою від нераціональної терапії має стати дотримання рекомендацій уніфікованих клінічних протоколів, розроблених та поширених у клінічній практиці захворювань. Ці рекомендації ґрунтуються на результатах багатоцентрових рандомізованих досліджень, а в їх основу покладено принципи доказової медицини, кожну рекомендацію складено на підставі доведеної клінічної успішності, зважено з точки зору фармакоекономіки. Доказова медицина стала принципом надання медичної допомоги в Україні недавно, тим часом для Європи і США робота за уніфікованими клінічними протоколами вже давно є нормою.
Рік тому було опубліковано Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) і третинної (високоспеціалізованої) медичної допомоги «Гострий риносинусит у дорослих та дітей», затверджений наказом МОЗ України № 85 від 11.02.2016. Цей протокол став першим документом у вітчизняній оториноларингології, що відповідає принципам доказової медицини. Слід зазначити, що терапевти, сімейні лікарі та педіатри не надто зраділи публікації цього протоколу, адже по суті документ офіційно вповноважує лікарів перелічених спеціальностей надавати медичну допомогу пацієнтам із гострим РС – проблемою, яку декілька років тому вважали суто оториноларингологічною. Проте, з огляду на однорічний досвід, можна впевнено стверджувати, що протокол посів належне йому місце.
Отже, гострий РС – це запалення носа і навколоносових пазух, що характеризується двома або більше симптомами, одним з яких є або закладеність/обструкція/набряк носа, або виділення з носа (переднє/заднє назальне затікання) з можливими болем/відчуттям тиску в ділянці обличчя, послабленням або втратою нюху і/або з наявністю відповідних змін при ендоскопічному обстеженні чи на комп’ютерній томограмі. Гострий РС за етіологічним чинником поділяють на вірусний, післявірусний та бактеріальний. Усі ці форми об’єднані одними патогенетичними механізмами.
Поширеність гострого РС у світі залежно від параметрів дослідження та форми захворювання становить 6-15%. Головною причиною гострого РС є віруси, проте в певної групи пацієнтів як результат перенесеної вірусної інфекції розвивається бактеріальний гострий РС. Окремим питанням є рецидивуючий та хронічний РС, при яких бактерії виступають ключовими патогенами.
Згідно із зазначеним протоколом бактеріальний РС діагностують за наявності щонайменше трьох із таких симптомів/ознак:
- виділення з порожнини носа (переважно з одного боку) й одночасна наявність слизових чи гнійних виділень у носовій порожнині (при риноскопії);
- значний локальний біль (переважно однобічний);
- підвищення температури тіла (>38 °C);
- двофазність захворювання (погіршення перебігу після незначного покращення).
У клінічно складних випадках, при нетиповому перебігу гострого РС, використовують лабораторні дослідження: підвищення швидкості осідання еритроцитів та рівня С-реактивного білка.
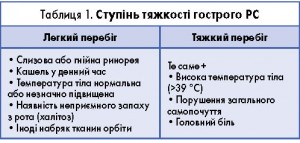
Тривалість хвороби дає змогу відокремити гостру форму РС від хронічної – до 12 тиж і більше відповідно. Рецидивуючий РС передбачає наявність щонайменше чотирьох задокументованих епізодів гострого РС, проте за умови, що кожний із цих епізодів тривав не менш як 7 днів. З метою інтерпретації даних, отриманих у ході оцінки скарг та збору анамнезу пацієнта з підозрою на гострий РС, та визначення подальшої лікувальної тактики важливо визначити ступінь тяжкості перебігу гострого РС (табл. 1).
Бактеріальна етіологія гострого, рецидивуючого чи хронічного РС з урахуванням тяжкості його перебігу є приводом до призначення антибактеріальної терапії в комплексі з препаратами іншої дії (іригаційна та комплексна фітотерапія, інколи – топічні кортикостероїди). Мета антибактеріальної терапії в цьому випадку – ерадикація інфекції у вогнищі запалення. Елімінація патогенного мікроорганізму за допомогою адекватного препарату є запорукою максимальної клінічної ефективності та засобом мінімізації вірогідності селекції антибіотикорезистентності. Основним завданням для лікаря, що призначає антибіотик, є дотримання раціонального балансу між забезпеченням максимального ефекту та запобіганням розвитку небажаних побічних реакцій препарату.
Лікування інфекцій ЛОР-органів у більшості випадків потребує обирати антибіотик емпірично, адже часу на зростання колоній мікроорганізмів для визначення чутливості до лікарських засобів стан пацієнта, як правило, не дає. Емпіричну антибіотикотерапію слід призначати з урахуванням відомих фармакокінетичних та фармакодинамічних параметрів, ефективності щодо основних бактеріальних збудників, які спричиняють саме цю патологію саме в цьому регіоні. Основними збудниками бактеріальних інфекцій ЛОР-органів у дорослих та дітей є пневмокок (20-43 і 35-42% відповідно) і гемофільна паличка (22-35 і 21-28% відповідно). Слід зазначити, що атипові збудники практично не зустрічаються при гострих інфекціях верхніх дихальних шляхів (ВДШ). Проте все-таки звертає на себе увагу великий відсоток гемофільної палички в етіологічній структурі бактеріальних РС. Важливо зазначити, що щороку фіксують зростання поширеності цього патогену як етіологічного фактора виникнення РС. H. іnfluenzae – найпоширеніший представник грамнегативної флори і другий за частотою збудник бактеріальних інфекцій ВДШ. H. іnfluenzae здатний тривалий час персистувати на слизовій оболонці носоглотки. У хворих на рекурентний тонзиліт, рецидивний назофарингіт та у дітей із торпідним перебігом РС частота колонізації H. influenzae носоглотки сягає 35-38% (Г.О. Леженко і співавт., 2012). Цікаво, що наявність вірусних інфекцій збільшує ризик переходу носійства в маніфестні форми. Тобто для переходу вірусного РС у бактеріальний не потрібна контамінація патогеном ззовні, адже на слизових оболонках можуть міститися неактивні бактеріальні колонії.
Інформація про основних збудників РС суттєво допомагає у виборі антибіотика, проте широкий асортимент останніх залишає широке поле для роздумів і вагань. Рекомендації протоколу з вибору класу антибіотика для лікування гострого РС подано в таблиці 2.
Захищені амінопеніциліни зазвичай являють собою препарати першої лінії, і це відповідає принципам раціональної антибіотикотерапії. Проте є декілька клінічних ситуацій, коли пеніциліновий старт – не дуже гарна ідея. Серед них, зокрема:
- алергія на пеніциліни (без перехресної реакції на цефалоспорини);
- нещодавне застосування пеніцилінів (наприклад, під час лікування одного з епізодів рецидивуючого РС);
- погіршення стану або стан без динаміки протягом 36-48 год лікування пеніцилінами.
Альтернативою у таких випадках має стати антибіотик цефалоспоринового ряду. Макроліди, виробники яких роблять ставку на унікальний спектр антибактеріальної активності, справді добре елімінують атипову флору. Однак як бути з тим фактом, що атипова флора, м’яко кажучи, не стандартний збудник РС? Респіраторні фторхінолони мають широкий спектр активності, проте експерти ВООЗ активно закликають не застосовувати цю групу антибіотиків для лікування рутинної патології, адже зазначені препарати сьогодні – це резерв. До того ж резерв, що може спричинити доволі серйозні небажані реакції.
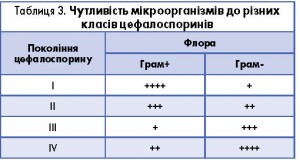
Отже, цефалоспорини. Клас цих препаратів доволі великий, тобто необхідно зробити ще один правильний вибір. Наразі існує 4 покоління цефалоспоринів, кожне з яких має свої недоліки та переваги щодо впливу на різноманітну мікрофлору, що регламентує застосування цих препаратів як стартових протимікробних засобів емпіричної антибіотикотерапії. Чутливість мікроорганізмів до різних поколінь цефалоспоринів показано в таблиці 3.
В умовах емпіричної терапії надзвичайно важливо, щоб цефалоспорин був активний як щодо грампозитивних, так і грамнегативних мікроорганізмів. Наприклад, I покоління (цефазолін, цефалексин, цефадроксил) має недостатню активність стосовно грамнегативних збудників (H. influenzae, M. catarrhalis). Препарати II покоління досить збалансовані за своєю активністю, а III генерацію представляють засоби із високим ступенем активності стосовно грамнегативної флори. Тобто це покоління є оптимальним у терапії інфекцій, де існує велика вірогідність участі грамнегативної флори. Як згадувалося вище, H. іnfluenzae – це патогенний мікроорганізм, роль якого як збудника РС в останні роки зростає. Тож абсолютно логічним виглядає вибір цефалоспорину саме ІІІ генерації.
Однак і тут на нас чекає роздоріжжя. В який же бік піти, щоб і коня зберегти, і голову не втратити? Почнімо з того, що на сьогодні в Україні найпоширеніший цефалоспорин – це цефтриаксон (до речі, він стрімко втрачає свої позиції через зростання рівня антибіотикорезистентності). Проте відповідно до міжнародних рекомендацій більшість бактеріальних інфекцій ЛОР-органів можна ефективно лікувати пероральними засобами. Парентеральні форми препаратів слід застосовувати лише в тих випадках, коли пацієнт не може приймати ліки per os (порушення ковтання, всмоктування в шлунково-кишковий тракт (ШКТ), розлади свідомості). Наразі вибір таблетованих цефалоспоринів в Україні невеликий, і найбільш вивченим серед них є цефподоксим. Як і решта β-лактамних антибіотиків, цефподоксим діє строго бактерицидно. Препарат проявляє високу активність щодо таких збудників, як грампозитивні мікроорганізми – стрептококи, Corynebacterium diphtheriae; грамнегативні – Haemophilus influenzae, Escherichia coli, нейсерії, клебсієли, Proteus, Moraxella catarrhalis, Providencia rettgeri, а також деякі анаероби (Peptostreptococcus). Помірно чутливими до цефподоксиму є метицилінчутливі стафілококи. В ході досліджень, проведених в Іспанії, було продемонстровано, що штами такого значущого збудника, як S. pneumoniae, чутливі до цефподоксиму в 99,5% випадків (A. Fenoll і співавт., 2007). При порівняльному аналізі антибактеріальної активності найбільш часто використовуваних пероральних цефалоспоринів (цефуроксиму аксетилу, цефалексину, цефіксиму) й амоксициліну/клавуланату встановлено, що цефподоксим за активністю проти H. іnfluenzae значно перевершує інші препарати з цієї групи (H. Dabernat, M. Seguy, 2007). Результати метааналізу ефективності цефподоксиму довели його ефективність у 92-100% випадків бактеріального синуситу (табл. 4). Бактеріальну ефективність цефподоксиму показано в таблиці 5.
Вітчизняний фармацевтичний ринок антибактеріальних засобів сьогодні назвичайно великий. В Україні зареєстровано велику кількість антибіотиків різних виробників, як зарубіжних, так і вітчизняних. Причому переважна більшість – це препарати виробництва Індії або інших країн Азії, які далеко не завжди дозволені для ввезення та реалізації в країнах Євросоюзу або США.
Саме тому хотілося б звернути вашу увагу на новинку цього року – препарат Цефма виробництва компанії «Сандоз», діючою речовиною якого є цефподоксим у формі проксетилу. Цефподоксиму проксетил, окрім високої ефективності лікування, характеризується ще й безпечністю застосування. Не секрет, що антибіотикотерапія доволі часто пов’язана з ризиком розвитку антибіотик-асоційованих порушень кількісного та якісного складу мікрофлори кишечника. Щоб запобігти цій проблемі, найкраще застосовувати сучасні пероральні антибіотики у вигляді проліків (prodrug), і Цефма виготовлена саме за такою технологією. Препарат потрапляє у ШКТ у неактивній формі й абсорбується в кишкову стінку шляхом відщеплення інертної частки лікарського засобу. Активація діючої речовини відбувається лише після абсорбції в стінку тонкої кишки. Наявність у просвіті кишечника лише неактивної форми препарату дає змогу запобігти безпосередньому впливу антибіотика на мікрофлору людського організму, мінімізувати ризик розвитку дисбіозу й зберегти склад мікробіоти в незмінному стані (Н.Л. Аряєв і співавт., 2009). Ця особливість препарату, крім відповідності принципу «не нашкодь», допомагає уникнути поліпрагмазії: під час використання препарату Цефма як антибіотика одночасне застосування пробіотика не викликає необхідності, що дозволяє зменшити кількість призначених препаратів і знизити фінальну вартість курсу лікування. До переваг препарату Цефма також належить низька ймовірність виникнення побічних реакцій. Тільки 5% пацієнтів з алергією на препарати пеніцилінового ряду перебувають у групі ризику щодо ймовірності виникнення перехресної алергічної реакції у відповідь на застосування цефподоксиму проксетилу. Серед нескомпрометованих щодо алергічних реакцій пацієнтів аналогічний ризик ще нижчий. Крім того, терапія цефподоксиму проксетилом не потребує коригування дози препарату для пацієнтів із печінковою недостатністю, а отже, лікарський засіб Цефма можна рекомендувати як препарат вибору для антибактеріальної терапії пацієнтів із супутніми захворюваннями печінки різного ступеня тяжкості в анамнезі.
До типових помилок антибіотикотерапії бактеріальних РС належать:
- призначення як стартової емпіричної терапії макролідів, фторхінолонів, особливо парентеральних форм (цефтриаксон);
- дом’язове чи довенне введення антибіотика;
- тривале парентеральне введення антибіотика без використання можливостей step-down-терапії;
- недотримання курсового призначення антибіотика;
- перевищення рекомендованої дози антибіотиків.
Наприкінці доповіді В.І. Попович наголосив на важливості обрання адекватного дозового режиму антибіотикотерапії.
Зазначимо, що препарат Цефма випускають у вигляді таблеток по 200 мг. Дорослим його рекомендовано приймати двічі на день в добовому дозуванні 200 мг двічі на добу. Тривалість терапії визначають індивідуально, в середньому вона становить 5-14 днів.
Варто зазначити, що Цефма – це єдиний в Україні європейський цефподоксим, який виробляють в Австрії згідно із сучасними європейськими стандартами. Цефма входить до «Оранж бук» – переліку Управління з контролю за продуктами харчування та лікарськими препаратами США (FDA), що містить лише ті препарати, якість, безпека та біоеквівалентність яких не викликає сумніву.
Підготувала Олександра Мєркулова
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Риносинусит (РС) є одним із найчастіших захворювань у первинній медичній практиці. Трьома найбільш чутливими й специфічними симптомами гострого РС є виділення з носа, закладеність носа, лицевий і головний біль. Неконтрольований гострий біль значно погіршує якість життя пацієнтів із РС: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування. Отже, полегшення болю при РС є найпершим завданням лікаря....
У всьому світі біль у горлі, зумовлений запальними захворюваннями горла (ЗЗГ), є найчастішою причиною звернень до лікарів загальної практики та оториноларингологів; із ним пов’язано ≈25% відвідувань лікаря. За даними Всесвітньої організації охорони здоров’я, >100 соматичних захворювань із провідним інфекційно-залежним і токсико-алергічним механізмом пов’язані саме із ЗЗГ. Здебільшого причина болю в горлі – гостре запалення інфекційного ґенезу: ГТ, ГФ і ГРВІ....
Антибіотикорезистентність (АБР) визнано загрозою для глобального здоров’я, яка щороку спричиняє мільйони смертей в усьому світі. Невідповідне та надмірне використання антибіотиків (АБ) зумовлює підвищення стійкості мікробних збудників і негативно впливає на ефективність цих дуже важливих лікарських засобів. Завдяки Глобальному плану дій щодо АБР Всесвітня організація охорони здоров’я (ВООЗ) працює над поліпшенням нагляду за резистентністю до протимікробних препаратів і скороченням нераціонального використання АБ. ...
Медичні інформаційні кампанії спрямовані на поширення важливих знань про охорону здоров’я серед населення. З урахуванням потреб і інтересів понад семи мільярдів людей у світі міжнародні організації шукають способи етичного обміну важливими відомостями, без упередженості та несправедливості. Обізнаність у сфері охорони здоров’я має вирішальне значення для кожного, оскільки хвороби та інфекції можуть вразити будь-кого в будь-який час. Таким чином, важливо поширювати відомості про охорону здоров’я за допомогою зрозумілих кожному усних, письмових і візуальних засобів. Ця інформація має сприяти соціальному здоров’ю і не містити дискримінаційного контенту. Заходи з підвищення обізнаності про здоров’я допомагають пацієнтам ліпше розуміти стан свого здоров’я, а також можливі варіанти та методи лікування. Кампанія з підвищення обізнаності відрізняється від маркетингу товарів для здоров’я, оскільки не спонукає купувати той чи інший продукт, а намагається сприяти свідомішому ставленню до свого здоров’я. Глобальні дні громадського здоров’я пропонують великі можливості для підвищення обізнаності та розуміння проблем здоров’я і мобілізації підтримки дій від місцевої громади до міжнародної спільноти. ...