Ремиссия при ревматоидном артрите: каковы возможности снизить дозу / отменить болезнь-модифицирующие препараты?
В настоящее время достижение ремиссии при ревматоидном артрите (РА) и изменение прогноза заболевания стали реальностью. Диагноз РА в большинстве случаев устанавливается своевременно, определены цель лечения и инструменты для мониторинга активности болезни, что позволяет рано начинать болезнь-модифицирующую терапию (БМТ) и адаптировать существующие схемы лечения с учетом индивидуальных потребностей каждого пациента (J.S. Smolen, 2010). Кроме того, биологические агенты (БА), широко вошедшие в клиническую практику, дают шанс на достижение лучших результатов лечения всем пациентам, у которых отсутствует или недостаточен ответ на стандартную терапию.
Внедрение новой стратегии лечения РА означает не только улучшение прогноза, но и снижение риска развития коморбидных состояний. Так, по данным большого популяционного исследования, уровень смертности среди больных РА после 2000 г. сопоставим с таковым в общей популяции (D. Lacaille, 2016). У пациентов, заболевших в период с 2000 по 2006 г., смертность от сердечно-сосудистых заболеваний была сопоставима с общепопуляционной (5,9 на 1000 пациенто-лет) и более чем в 2 раза ниже (5,66 на 1000 пациенто-лет) по сравнению с заболевшими в период с 1996 по 2000 г. (12,3 на 1000 пациенто-лет).
Аналогичная динамика наблюдается и в показателях смертности от онкологических заболеваний, что подтверждает роль воспаления в развитии коморбидности у пациентов с аутоиммунной патологией. Однако смертность от инфекций у больных РА превышает общепопуляционный уровень вне зависимости от сроков развития заболевания.
Согласно данным исследования NOR-DMARD в последнее десятилетие количество пациентов с РА, у которых удалось достигнуть ремиссии, увеличилось вдвое (Ann. Rheum. Dis. 2015). В исследовании RRR была показана возможность успешной отмены терапии у больных, находящихся в состоянии ремиссии (Ann. Rheum. Dis. 2010). По данным Y. Tanaka, 78% пациентов с РА на момент отмены инфликсимаба находились в состоянии устойчивой ремиссии по индексу DAS28-СОЭ. Ремиссия / низкая активность болезни (НАБ) сохранялась у 53% пациентов на протяжении 1 года после отмены терапии.
В связи с изменениями в диагностике и лечении РА возник новый сложный вопрос для пациентов и врачей: что делать после достижения ремиссии – продолжать прием болезнь-модифицирующих препаратов (БМП) в текущих дозах, снижать их или отменять терапию? Отсутствие четких рекомендаций по снижению/отмене терапии связано, с одной стороны, с недостаточным количеством данных клинических исследований по этой проблеме, а с другой – с невозможностью достижения ремиссии до внедрения стратегии «Treat to target» (лечение до достижения цели) с ранним и непрерывным назначением БМП.
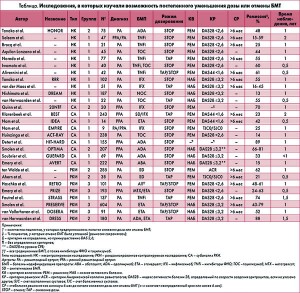
По данным многочисленных клинических исследований, высокая эффективность в достижении ремиссии БА, назначаемых в дополнение к стандартной терапии РА, доказана и не вызывает сомнений. Не менее тридцати исследований проведено для оценки сохранения эффекта после снижения дозы / отмены БА. Наибольшее количество данных относительно длительности ремиссии накоплено при применении блокаторов фактора некроза опухоли (ФНО) (табл.). Результаты исследований свидетельствуют о сохранении НАБ после отмены блокаторов ФНО в 25-60% случаев. Согласно данным некоторых исследований, таких как DOSERA, DRESS, RETRO и STRASS, у большинства пациентов прием блокаторов ФНО может быть восстановлен с прежней эффективностью в случае обострения РА (J. Haschka, 2016).
Одним из основных направлений научных исследований в настоящее время является выделение предикторов «удержания» ремиссии при снижении дозы / отмене БМП. Наиболее значимым предиктором сохранения ремиссии при снижении дозы / отмене БМП является ранее начало терапии – до 6 мес от появления первых симптомов.
Данные рандомизированых контролируемых и проспективных клинических исследований
Согласно данным B. Saleem у 59,3% метотрексат-наивных пациентов с ранним РА сохранялась стойкая ремиссия по DAS28 через 2 года после отмены блокаторов ФНО, а у 40,7% обострение развилось в среднем через 14 мес после прекращения терапии. Важным фактом является возобновление состояния ремиссии у 73% пациентов с обострением после увеличения дозы стандартных БМП; возобновление приема блокаторов ФНО понадобилось в 27% случаев. При позднем РА, рефрактерном к приему метотрексата (МТХ), удержать ремиссию в течение 2 лет после отмены удалось только у 15% пациентов. Предикторами длительной ремиссии были раннее назначение терапии, высокий уровень С-реактивного белка (СРБ) в начале лечения и нормализация иммунных нарушений (Ann. Rheum. Dis. 2010).
Воспаление оказывает прямое влияние на дифференцировку наивных CD4+ Т-клеток, приводя к образованию клеток с аномальным фенотипом (F. Ponchel, 2002). Эти клетки были названы воспалительно-связанными (inammation-related cells – IRC) и, по данным C. Burgoyne, являются предикторами обострения при лекарственно-индуцированной ремиссии у пациентов с РА (Ann. Rheum. Dis. 2008). Еще один маркер аутоиммунного заболевания – количество регуляторных Т-клеток (Treg), которое у пациентов с РА значительно снижено (S. Sakaguchi, 1995). В этом исследовании наличие устойчивой ремиссии ассоциировалось с высоким уровнем наивных Т-клеток и низким уровнем IRC (p=0,003). Уровень IRC был существенно выше у пациентов с обострением (p=0,0001).
В исследовании RETRO изучалась частота развития обострений РА после отмены всех БМП у 106 пациентов со стойкой ремиссией по DAS28 в течение 6 мес. 82% исследуемых получали МТХ, 9,9% – другие синтетические БМП, 40,6% – БА, из них 75,6% – блокаторы ФНО. Критериями исключения были прием преднизолона в дозе более 5 мг/сут и терапия ритуксимабом в анамнезе. Результаты оценивали в трех группах пациентов. У пациентов первой группы изменения в терапии не проводились, второй – дозы всех принимаемых БМП были снижены на 50%, третьей – в первые 6 мес дозы снизили на 50%, а затем препараты отменили. Обострение развилось у 38,9 и 51,9% пациентов из второй и третьей групп соответственно. В группе стабильной терапии обострение зарегистрировано в 15,8% случаев, что подтверждает данные о вторичной неэффективности терапии и волнообразном течении РА. В качестве предикторов обострения выделены позитивность по анти-ЦЦП (антитела к циклическому цитруллинированному пептиду) и, естественно, модификация дозы / отмена терапии (J. Haschka, 2016).
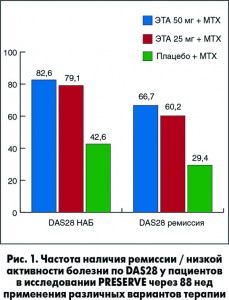
В исследовании PRESERVE изучали длительность ремиссии в течение 88 нед после отмены этанерцепта (ЭТА) при длительно текущем РА, средняя продолжительность болезни составила 6,4 года. В первой части данного исследования через 36 нед применения ЭТА в дозе 50 мг/нед 72,4% пациентов достигли ремиссии. В дальнейшем в первой группе пациенты продолжили прием ЭТА в дозе 50 мг/нед, во второй – доза была снижена до 25 мг/нед, в третьей – препарат был отменен. После достижения ремиссии эффективность применения ЭТА в дозе 50 и 25 мг/нед была сопоставимой (рис. 1). При отмене препарата ремиссия/НАБ сохранялась у 29,4 и 42,6% пациентов соответственно (Lancet, 2013).
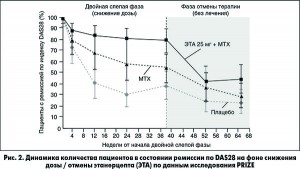
В исследовании PRIZE изучали продолжительность ремиссии после отмены ЭТА при раннем РА у пациентов со средней длительностью заболевания 6,5 мес (P. Emery, 2014). В открытой фазе комбинированной терапии длительностью 52 нед пациентам был впервые назначен МТХ в дозе 10 мг/нед с эскалацией до 25 мг/нед и ЭТА в дозе 50 мг/нед. Ремиссия по DAS28 была достигнута у 70% пациентов. В последующем 193 пациента были рандомизированы в три группы: в первой пациенты продолжили прием МТХ и ЭТА в дозе 25 мг/нед, во второй был отменен ЭТА, а в третьей отменены оба препарата. Указанная терапия проводилась 39 нед. На 39-й неделе состояние ремиссии сохранялось у 79, 54 и 38% пациентов в первой, второй и третьей группах соответственно. При этом количество больных с отсутствием нарушения функции суставов (индексом HAQ в норме) было сопоставимо в группах МТХ + ЭТА и МТХ: 78 и 72% соответственно. В группе плацебо данный показатель был существенно ниже – 45%. В финальной части исследования, с 39-й по 65-ю недели, у пациентов первой группы был отменен ЭТА. В этот период участники из группы комбинированной терапии значительно дольше удерживали ремиссию в сравнении с группой монотерапии МТХ (рис. 2). Важным результатом является отсутствие рентгенологического прогрессирования у пациентов вне зависимости от варианта терапии.
Интересные данные реальной клинической практики получены в одной из клиник Нидерландов. На фоне терапии инфликсимабом НАБ была достигнута у 51 из 94 пациентов с РА. При достижении DAS28 <3,2 дозу препарата снижали на 25% каждые 8-12 нед при условии сохранения эффекта. Более чем в 50% случаев удалось снизить дозу или отменить инфликсимаб. 39% пациентов продолжали терапию в прежней дозе. Доза была снижена на 25-75% (в среднем с 224 до 130 г на одно введение), при этом не отмечено достоверного прироста активности заболевания, а годовая стоимость лечения была снижена более чем на 5 тыс. евро. Интересен факт, что пациенты в целом осуществили 421 визит и на каждом осуществлялись контроль и при необходимости коррекция терапии. Так, глюкокортикоиды (ГК) локально были добавлены только на 8% визитов, восстановление БМП проведено не более чем на 5% и на 42 визитах проводилась коррекция дозы нестероидных противовоспалительных препаратов. Высокодостоверными предикторами обострения были курение и длительность болезни, высокодостоверным предиктором ремиссии – вера пациента в успех.
Еще одно небольшое исследование реальной клинической практики привлекает внимание оригинальным дизайном. Пациентам в состоянии ремиссии заменяли текущую терапию ЭТА и инфликсимабом на прием голимумаба 50 мг 1 раз в 4 и 8 нед (Clin. Rheumatol. 2016). По данным Н. Wakabayashi, на фоне такой терапии (52 нед) наблюдалось не только сохранение достигнутого эффекта, но и значительное увеличение количества пациентов в ремиссии: в группах с режимом 1 р/4 нед и 1 р/8 нед с 75,0 и 78,6% соответственно на неделе 0 до 93,8 и 92,9% на 52-й неделе по DAS28-СОЭ. По DAS28-СРБ 100% пациентов на 52-й неделе в обеих группах имели ремиссию. В общем группы не различались по частоте возникновения побочных явлений, однако в группе с удлинением интервалов между инъекциями не было побочных эффектов, характерных для блокаторов ФНО (инфекции верхних дыхательных путей, интерстициальные болезни легких, изменения уровней печеночных ферментов), что является дополнительным аргументом безопасности в пользу стратегии снижения дозы.
Рекомендации EULAR/ACR
Согласно рекомендациям Европейской антиревматической лиги (EULAR) по ведению пациентов с РА (2013) отмена биологических БМП не рекомендована. Одним из вариантов является снижение дозы блокаторов ФНО после достижения и удержания НАБ (DAS28 <2,6) при раннем и позднем РА. Уменьшение дозы биологических БМП возможно, если пациент находится в состоянии устойчивой ремиссии после снижения/отмены ГК, особенно на фоне комбинированной терапии с использованием синтетических БМП (J.S. Smolen et al., 2014).
Рекомендации Американской коллегии ревматологов (ACR) 2015 г. не содержат пункта об отмене БА при раннем РА. Это связано с тем, что к моменту достижения ремиссии у пациентов с ранним РА заболевание по определению уже не будет являться ранним. Относительно позднего РА рекомендуется продолжать проводимую терапию у пациентов с НАБ и уменьшать дозы стандартных БМП, блокаторов ФНО, БА и тофацитиниба у пациентов в ремиссии при продолжении приема МТХ. Не рекомендуется отменять все препараты для лечения РА. Рекомендации по снижению дозы имеют низкий уровень доказательности и основаны на мнении экспертов и клиническом опыте (J.A. Singh et al., 2016).
Концепция снижения доз БМП
Возможность снижения доз и даже в некоторых случаях отмены БМП следует рассматривать у пациентов, которые находятся в состоянии устойчивой ремиссии. Ремиссия должна наблюдаться как минимум в течение 6 мес и быть документально подтвержденной не менее чем на трех последовательных визитах в клинику.
Основным доводом для снижения дозы и отмены БМП является безопасность терапии, так как частота развития побочных явлений, включая инфекции и опухоли, зависит от дозы. Например, у пациентов, которые принимали ЭТА, показано трехкратное снижение риска развития побочных явлений при снижении дозы вдвое (B. Raffeiner, 2010). Дополнительный аргумент – высокая стоимость БА в сравнении со стандартной терапией БМП. И наиболее важным доводом при уменьшении доз БМП является возможность разграничить истинное излечение от медикаментозной супрессии воспаления (G. Schett et al., 2016).
Условия, необходимые для снижения дозы БМП:
1. Пациент удовлетворяет критериям ремиссии по DAS28 (<2,6), DAS44 (<1,4), SDAI (<3,3), CDAI (<2,8), ACR/EULAR.
2. Ремиссия должна наблюдаться как минимум в течение 6 мес и быть документально подтвержденной не менее чем на трех последовательных визитах в клинику.
3. Применение определенных БМП в стабильной дозе в последние 6 мес.
4. Отсутствие потребности в приеме ГК для поддержания ремиссии.
С целью успешной отмены / снижения доз БПМ необходимо информировать пациента о схеме снижения и тактике поведения при развитии обострения. Из практических соображений постепенное снижение дозы более предпочтительно по сравнению с быстрой отменой при приеме как синтетических, так и биологических БМП. В случае терапии биологическими БПМ приемлемы такие варианты, как снижение дозы или увеличение интервалов между введениями. Важным является тщательный мониторинг активности болезни для своевременного выявления обострений. Восстановление исходного режима применения БМП согласно данным литературы обеспечивает купирование обострения и возвращение к ремиссии у всех пациентов.
Предикторы обострения
В исследованиях HONOR и POET показано, что риск развития обострений ассоциируется с длительностью заболевания: пациенты с ранним РА имели более высокие шансы сохранения безлекарственной ремиссии. Данные регистра CORRONA свидетельствуют, что быстрый ответ на терапию БМП ассоциируется в последующем с хорошим удержанием ремиссии при снижении дозы препаратов.
Наиболее важным предиктором отсутствия обострения является «глубокая» ремиссия, без наличия признаков остаточного воспаления. Концепция связи остаточного субклинического воспаления с риском развития обострения послужила основой для определения прогностической роли инструментальных методов исследования. По данным трех исследований установлено, что наличие кровотока в синовиальной оболочке в режиме энергетической допплерографии (ЭД) является строгим предиктором обострения при отмене биологических БМП. Согласно данным B. Saleem и E. Naredo пациенты с ЭД >0 более подвержены обострениям при отмене блокаторов ФНО, нежели пациенты с ЭД=0. В комбинации с базовым уровнем DAS28 прогностическое значение допплерографии при ультразвуковом исследовании (УЗИ) суставов возрастает. В дополнение к этому исследование Alivernini и соавт. продемонстрировало, что синовиальная гипертрофия также ассоциируется с риском развития обострений при снижении дозы / отмене блокаторов ФНО. Авторы также показали, что при отсутствии синовиальной гипертрофии наблюдаются минимальные воспалительные изменения при гистологическом исследовании.
Из сывороточных биомаркеров наилучшим предиктором обострения является позитивность по анти-ЦЦП. Эти данные подтверждены в исследованиях BeSt, HIT HARD и POET. Согласно данным исследования RETRO более 70% пациентов с обострением были позитивны по анти-ЦЦП. Интересен факт, что анти-ЦЦП-негативные пациенты имели значительно более низкую частоту развития обострений вне зависимости от того, была ли исходная терапия продолжена, уменьшена или отменена. Таким образом, наличие анти-ЦЦП у пациентов в ремиссии может указывать на наличие субклинического аутоиммунного процесса, который будет препятствовать успешной отмене / снижению интенсивности терапии.
В отношении СРБ не доказана прогностическая значимость в контексте удержания ремиссии, несмотря на широкое использование для оценки активности заболевания в клинической практике.
Современная концепция ремиссии при РА
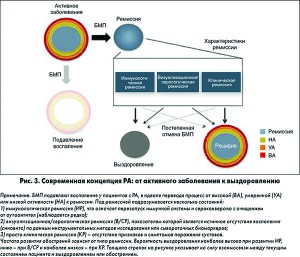
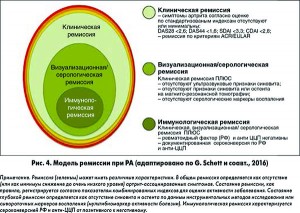
В настоящее время ремиссия при РА в основном определяется показателями клинических индексов, которые более сосредоточены на регистрации таких симптомов заболевания, как болезненные и припухшие суставы, нежели на непосредственном определении интенсивности синовиального воспаления. Истинная ремиссия – это стабильность всех составляющих: клинической, инструментальной/серологической и иммунологической (рис. 3, 4). В отличие от клинической ремиссии, основанной на определении суставного синдрома, инструментальная/серологическая ремиссия может быть констатирована только при полном отсутствии синовита (G. Schett et al., 2016). Высокая предиктивная значимость УЗИ суставов и сывороточных биомаркеров в прогнозировании риска развития обострений при снижении доз / отмене БМП подтверждает эту концепцию. И наиболее труднодостижимой является «перезагрузка» аутоиммунитета при РА – так называемая иммунологическая ремиссия (рис. 3).
Согласно этой концепции результаты исследований, проведенные с использованием более строгого определения понятия «ремиссия», основанного на отсутствии клинических признаков воспаления, нормализации сывороточных и инструментальных маркеров воспаления и даже исчезновении аутоантител (сероконверсия), позволят с высокой частотой прогнозировать достижение безлекарственной ремиссии и даже выздоровления. Тщательная оценка динамики клинико-лабораторных показателей при снижении доз / отмене БМП позволит лучше понять пути и выделить маркеры, которые указывают на разрешение воспаления при РА.
В конечном итоге результатом субоптимального контроля над заболеванием является прогрессирование суставной деструкции. В исследовании HONOR Y. Tanaka и соавт. показали отсутствие рентгенологического прогрессирования при отмене блокаторов ФНО (Ann. Rheum. Dis. 2015). В этой связи очень важно своевременно возобновить терапию при развитии обострения, чтобы не допустить формирования длительного периода высокой активности, который может являться триггером суставной деструкции.
В заключение необходимо отметить, что у пациентов в ремиссии с отсутствием синовита по данным УЗИ суставов нормализация иммунологических показателей и небольшая длительность заболевания ассоциируется с возможностью успешной отмены блокаторов ФНО при комбинации их с МТХ.
PHUA/BIO/0217/0005
СТАТТІ ЗА ТЕМОЮ Ревматологія
Сечова кислота (СК) – кінцевий продукт метаболізму пуринів, який здебільшого синтезується в печінці та виводиться нирками і кишечником [1, 2]. Гіперурикемія – підвищений рівень СК у сироватці крові – є метаболічною основою подагри, одного з найпоширеніших запальних артритів. У середні віки подагра вважалася хворобою надмірності аристократії, нині її поширеність зростає у всьому світі через зміни в харчуванні, переважання в дієті оброблених продуктів, фруктози та збільшення поширеності ожиріння [3]....
Глюкокортикоїди (ГК), які використовуються з початку 1950-х рр., стали невід’ємною частиною лікування ревматоїдного артриту (РА) [1]. Ключовою перевагою ГК є швидке настання ефекту, особливо порівняно з класичними синтетичними хворобомодифікувальними антиревматичними препаратами (ХМАРП) на кшталт метотрексату. Відповідно, ГК мають привабливий профіль для лікування спалахів хвороби або для застосування в ролі засобів для бридж-терапії на ранніх стадіях РА в очікуванні ефекту класичних синтетичних ХМАРП. Ця стратегія широко використовується після публікації результатів дослідження COBRA в 1997 р. [2]. ...
Гостре розтягнення зв’язок гомілковостопного суглоба (ГРЗГС) є поширеним, інвалідизувальним, клінічно значущим захворюванням, щодо якого по медичну допомогу щороку звертається >1 млн пацієнтів [1]; асоціюється зі значним соціально-економічним тягарем [2]. Майже 16-40% випадків ГРЗГС – спортивна травма, а час одужання є дуже важливим для спортсменів, професіоналів та осіб, котрі готуються до великих змагань. Найпоширенішими (85%) є латеральні (бічні) розтягнення зв’язок гомілковостопного суглоба; особливо часто ушкоджується передня таранно-гомілкова зв’язка – зазвичай унаслідок високошвидкісної інверсії та внутрішньої ротаційної травми [3]; ≈40% розтягнень гомілковостопного суглоба мають ризик хронізації. Характерними ознаками ГРЗГС є біль під час навантаження, нестабільність гомілковостопного суглоба та проблеми з рухливістю [4-6]....
Наприкінці жовтня минулого року Всеукраїнська асоціація ревматологів України провела науково-практичну конференцію, до якої було залучено фахівців різних галузей медицини, як-от ревматологія, загальна практика (сімейна медицина), терапія, кардіологія, медицина невідкладних станів, неврологія, функціональна й ультразвукова діагностика. Захід відбувся у змішаному форматі (онлайн / офлайн). До участі в конференції було запрошено не лише вітчизняних спікерів із різних регіонів України, а і закордонних, зокрема з Канади, США та Великої Британії. ...