Хронический гастрит, рак желудка. Как предотвратить эту последовательность?
Открытие австралийских исследователей Робина Уоррена и Барри Маршала заставило мировую медицинскую общественность пересмотреть ряд положений, касающихся патологии гастродуоденальной зоны, и выделить целую группу Helicobacter pylori (Нр)-ассоциированных заболеваний. Инфекция Нр считается важнейшим этиопатогенетическим звеном развития хронического гастрита, язвенной болезни желудка и двенадцатиперстной кишки, МАLT-лимфомы (mucosa-associated lymphoidtissue lymphoma) и некардиального рака желудка (РЖ). Широкое проведение антихеликобактерной терапии (АХТ) с целью эрадикации инфекции в ряде стран Западной Европы, США, Японии и Австралии позволило существенно снизить уровень инфицированности и заболеваемости Нр-ассоциированными заболеваниями и предотвратить их опасные исходы (желудочно-кишечное кровотечение, перфорацию, аденокарциному желудка и др.).
Эрадикационная терапия неэффективна. Хронический гастрит – рак желудка
Аспекты диагностики и лечения вышеназванной группы заболеваний постоянно совершенствуются с позиций доказательной медицины, находя свое отражение в серии согласительных совещаний. Первая согласительная конференция прошла в голландском городе Маастрихт в 1996 году. С тех пор по традиции все совещания независимо от места проведения стали носить название Маастрихтских консенсусов. В дальнейшем были разработаны рекомендации Маастрихт II (2000), Маастрихт III (2005), Маастрихт IV (2010). И наконец, последний пересмотр – Маастрихт V – состоялся в 2015 году во Флоренции (Италия), где прошла очередная встреча 43 экспертов в области диагностики и лечения инфекции Нр из 24 стран Европы, Юго-Восточной Азии и Америки. Эти рекомендации имеют огромнейшее значение для охраны общественного здоровья, так как правильное назначение эрадикационной терапии останавливает неопластическое прогрессирование предраковых изменений в определенной подгруппе пациентов.
Еще в 2007 году, до Маастрихтского консенсуса IV, Американская коллегия гастроэнтерологов издала рекомендации по лечению инфекции Нр, в которых содержались следующие положения:
- резистентность к метронидазолу является относительной и преодолевается путем увеличения дозы и применения препаратов висмута;
- рекомендуется у всех пациентов выяснять факты применения макролидов в анамнезе;
- при предшествующем приеме макролидов предпочтение следует отдавать схемам с висмутом;
- частота нежелательных реакций при квадротерапии не превышает таковую при тройной терапии.
Последнее положение очень важно, так как свидетельствует об отсутствии более выраженных побочных эффектов при применении квадротерапии с препаратом висмута по сравнению с тройной терапией.
Этапы диагностики и лечения хронического гастрита как этапы канцерпревенции
Сегодня не вызывает сомнения ассоциация между Нр и РЖ. Еще в 1994 году Международное агентство по изучению рака (IARC-WHO), которое является структурным подразделением ВОЗ, признало эту инфекцию канцерогеном 1-го порядка из-за ее эпидемиологической связи с аденокарциномой желудка и МАLT-лимфомой желудка. По мнению Л.И. Аруина (2004), в результате длительного хронического воспаления, характерного исключительно для Нр-ассоциированного гастрита, нарушается система клеточного обновления в желудке (прогрессируют изменения процессов апоптоза и пролиферации с преобладанием последней). Как следствие этого, в слизистой оболочке желудка (СОЖ) появляются мишени для действия мутагенных и канцерогенных (внешнесредовых) факторов; эпителий желудка из-за атрофии замещается метапластичным, диспластичным и, наконец, неопластичным. Предложенный P. Correa около 15 лет назад гипотетический каскад последовательности событий, приводящих в конечном итоге к развитию аденокарциномы желудка, в настоящее время является общепризнанным. Согласно ему в течение 30 лет у 50% инфицированных Нр разовьется атрофия СОЖ, у 40% – кишечная метаплазия, у 8% – дисплазия и у 1-2% – аденокарцинома желудка.
Результаты проспективных исследований свидетельствуют о том, что у больных, инфицированных Нр, риск развития РЖ повышен в 3-6 раз. Риск развития РЖ повышается параллельно тяжести атрофического гастрита. В Маастрихтском консенсусе IV указано, что между РЖ и распространенностью и тяжестью гастрита, а также атрофией и кишечной метаплазией имеется положительная ассоциация. Риск развития РЖ увеличивается у пациентов с тяжелым атрофическим гастритом астрального отдела в 18 раз. Особенно высок риск развития РЖ при развитии атрофии как в антральном, так и в фундальном отделах желудка (панатрофия, мультифокальный атрофический гастрит), в этом случае он может увеличиваться в 90 раз. Наличие кишечной метаплазии увеличивает вероятность рака желудка в 10 раз. Тяжелый и распространенный атрофический гастрит, несомненно, является предиктором развития рака желудка. В настоящее время обнаружено, что наиболее распространенные и тяжелые случаи атрофического гастрита, выявленные по оценке пепсиногенового профиля, в сочетании с отсутствием антител к Нр (возможно, из-за их спонтанного исчезновения) были связаны с гораздо большей прогрессией дисплазии и рака. Значения относительного риска (ОР) для тяжелого атрофического Нр-негативного гастрита к менее выраженному Нр-позитивному гастриту: 8,2 (3,2-21,5) против 6 в исследовании H. Watabe и соавт., 131,98 (11,95-1457,36) против 2,77 в исследовании K. Yanaoka и соавт. и 61,85 (5,6-682,64) против 14,85 в работе H. Ohata и соавт. Y. Yamaji и соавт. также обнаружили повышенный уровень заболеваемости раком желудка для Нр-позитивных случаев с незначительно выраженной атрофией, который составил 0,37% случаев в год, и более высокий – до 0,53% случаев в год – при тяжелом Нр-негативном атрофическом гастрите.
Одним из актуальнейших вопросов в рамках канцерпревенции является возможность предотвращать и тормозить развитие пренеопластических изменений СОЖ (атрофия и кишечная метаплазия) путем эрадикации Нр. Эрадикация Нр предотвращает развитие пренеопластических изменений и является эффективным элементом канцерпревенции лишь в том случае, когда она назначается до их развития. В одном из положений Маастрихтского консенсуса IV сказано, что атрофия может подвергаться регрессии, но только в теле желудка, в антральном отделе регрессия не наблюдается; кишечная метаплазия является необратимой. В Маастрихтском консенсусе V (2015) утверждается, что эрадикация Нр приводит к обратному развитию атрофии желудка в отсутствие кишечной метаплазии, а также останавливает неопластическое прогрессирование предраковых изменений в определенной подгруппе пациентов. В ряде метаанализов было показано, что атрофия желудка может быть в той или иной степени обратимой как в антральном отделе, так и в теле желудка. Кишечная метаплазия необратима, хотя ее прогрессирование приостанавливается в большой подгруппе пациентов (Маастрихт V). Распространенные предраковые изменения (атрофия, кишечная метаплазия) требуют контроля путем эндоскопического стадирования. При отборе пациентов для наблюдения должны учитываться гистологические классификационные критерии OLGA/OLGIM.
Эрадикация Нр является экономически эффективной стратегией профилактики рака желудка и должна рассматриваться во всех популяциях. Стратегия screen-and-treat рекомендуется для популяций с высоким риском развития рака желудка, а также в популяциях среднего и низкого риска. Эндоскопический скрининг рассматривается в популяциях с высоким риском развития рака желудка, особенно у пациентов с прогрессирующими пренеопластическими изменениями, такими как атрофия / кишечная метаплазия (Маастрихт V).
Как повысить эффективность эрадикационной терапии. Обзор двух исследований
Вопрос выбора схемы антихеликобактерной терапии всегда был особенно актуальным. В соответствии с Маастрихтскими консенсусами IV и V акцент при выборе схемы должен делаться на данных о резистентности штаммов Нр к кларитромицину в регионе, так как рост резистентности штаммов Нр к кларитромицину связывают со снижением эффективности стандартных схем эрадикационной терапии. Резистентность к кларитромицину снижает эффективность стандартной тройной терапии до 35-60%. Повышение резистентности Нр к кларитромицину четко прослеживается в странах Европы. В 2012 году на симпозиуме, посвященном 30-летию открытия Нр, профессор Francis Megraud докладывал о результатах исследования чувствительности Нр в большинстве стран Европы, которое проводилось в 2008-2009 гг. Общий уровень резистентности к кларитромицину составил 17%. Если рассмотреть подробнее данные по странам, то можно видеть разброс между минимальным уровнем резистентности, составившим примерно 5% в Нидерландах, и максимальным (36%) в Австрии. Таким образом, в большинстве стран северных регионов Европы резистентность довольно низкая, тогда как в странах Южной, Восточной и Центральной Европы она выше – 15%. По данным Маастрихтского консенсуса V, резистентность к кларитромицину достигла 30% в Италии и Японии, 40% – в Турции, 50% – в Китае, в Швеции и Тайване – около 15%.
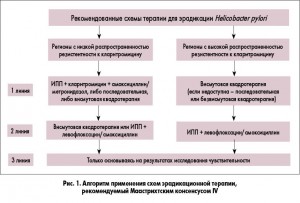
Результаты исследований показывают, что при повышении минимальной подавляющей концентрации (МПК) кларитромицина в отношении Нр выше 0,5 мг/л и особенно >2-4 мг/л происходит резкое снижение частоты эрадикации. Подобная закономерность выявлена и для фторхинолонов. Показано, что при повышении МПК левофлоксацина к Нр с <1 мг/мл до >1 мг/мл происходит снижение частоты эрадикации с 84,1 до 50%, а при изменении МПК с <8 мг/мл до >8 мг/мл частота эрадикации снижается с 82,3 до 0%. Несколько иная ситуация складывается с устойчивостью Нр к метронидазолу. Несмотря на достаточно широкое распространение устойчивых штаммов в популяции, столь драматического влияния на частоту эрадикации, как в случае макролидов и фторхинолонов, резистентность Нр к метронидазолу не оказывает. Поэтому в регионах с низкой резистентностью Нр к кларитромицину, в соответствии с консенсусом Маастрихт IV, в качестве эрадикационной терапии первой линии рекомендуется либо стандартная тройная терапия, либо квадротерапия с препаратом висмута (ИПП + висмута трикалия дицитрат + метронидазол + тетрациклин). В регионах же с высокой резистентностью Нр к кларитромицину (15-20%) в качестве эрадикационной терапии первой линии рекомендуется только квадротерапия с препаратом висмута. Однако стоит отметить, что в ряде стран, например во Франции, препараты висмута недоступны, поэтому как альтернативу первой линии терапии стоит рассматривать последовательную эрадикационную терапию (первые 5 дней – ИПП + амоксициллин, последующие 5 дней – ИПП + кларитромицин + тинидазол/метронидазол) или безвисмутовую квадротерапию (ИПП + кларитромицин + амоксициллин + метронидазол). В регионах с низкой резистентностью к кларитромицину в качестве терапии второй линии может использоваться квадротерапия на основе препаратов висмута (если она не использовалась как терапия первой линии) или как альтернатива тройная терапия с левофлоксацином (ИПП + амоксициллин + левофлоксацин). Что же касается регионов с высокой резистентностью штаммов Нр к кларитромицину, то, согласно консенсусу Маастрихт IV, терапией второй линии при неэффективности квадротерапии первой линии также является тройная терапия с левофлоксацином. Однако экспертный совет рекомендует учитывать растущий уровень резистентности к левофлоксацину, который в ближайшем будущем может поставить под угрозу эффективность данной схемы. Рекомендуемый Маастрихтским консенсусом IV алгоритм применения схем эрадикационной терапии представлен на рисунке 1.
Таким образом, четверную эрадикационную терапию с препаратом висмута можно использовать как терапию первой линии в странах и с высокой резистентностью к кларитромицину, и с низкой. При этом четверная схема с препаратом висмута в странах с низкой резистентностью к кларитромицину является терапией первой линии.
Кроме того, применение квадротерапии не только оказывает эрадикационный эффект, но и положительно влияет на течение постэрадикационного периода хронического гастрита и, что очень важно, является эффективной схемой канцерпревенции благодаря входящему в ее состав висмута субцитрату.
Реализация антибактериального эффекта препаратов висмута в отличие от антибиотиков происходит за счет местного антисептикоподобного действия. При контакте препаратов висмута с Нр происходит подавление синтеза аденозинтрифосфата, белков бактериальной клетки, нарушается бактериальная адгезия, синтез бактериальной протеазы, фосфолипазы и уреазы, повреждается внеклеточный бактериальный гликокаликс. Исследования последних лет показали, что одним из механизмов повреждения Нр является модификация метаболизма железа и никеля в бактериальной клетке. Можно предположить, что именно за счет различий в реализации антибактериального действия по сравнению с антибиотиками, а также воздействия на несколько мишеней резистентность Нр к препаратам висмута не развивается.
Применение висмута субцитрата коллоидного актуально не только в схемах классической квадротерапии, но также в качестве четвертого компонента в схемах стандартной тройной АХТ первой линии в целях оптимизации эффективности эрадикационного протокола. Недавнее исследование В. Ergul и соавт. (2013) показало существенное увеличение эффективности тройной схемы АХТ (до 90,7%) при включении висмута субцитрата. Висмута субцитрат коллоидный является важным компонентом клинических схем АХТ либо в составе традиционной квадротерапии, либо в качестве дополнительного компонента тройной терапии первой линии, что дает прирост эффективности эрадикации на 15-20%. В первую очередь, это обусловлено способностью висмута субцитрата преодолевать резистентность Нр к антибиотикам (особенно к кларитромицину). Интерес представляет также включение висмута субцитрата в схемы последовательной АХТ.
Исследования последних лет показали, что схемы терапии с висмута субцитратом обеспечивают высокий процент эрадикации Нр, выраженное уменьшение воспаления в СОЖ, а также, учитывая молекулярные механизмы действия висмута субцитрата коллоидного, обладают противоканцерогенным эффектом.
Маастрихтский консенсус V. Обзор рекомендаций
В 2016 году на 24-й Объединенной европейской гастроэнтерологической неделе в Вене в докладах была проанализирована эффективность применения метронидазола в Испании, Франции, Италии, Словении, Германии, которая составила от 83% до 89% в зависимости от ИПП и от 75% до 96% – от очередности (первая, вторая или третья линия терапии). Кроме того, были объявлены результаты применения терапии BOCA (висмут + эзомепразол + кларитромицин + амоксициллин), т.е. добавления висмута к стандартной тройной терапии, при применении которой был достигнут уровень эрадикации в Испании 96-97%, в России – 74-75%, в Украине – 90%.
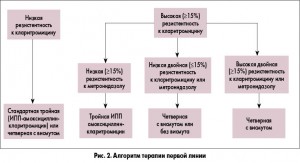
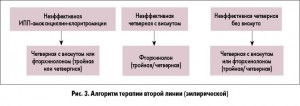
Далее представлен обзор раздела «Лечение» последнего Маастрихтского консенсуса V. Выбор схемы лечения определяется растущей резистентностью Нр к кларитромицину. Тройная терапия с кларитромицином не должна назначаться, если резистентность к кларитромицину в регионе больше 15%. В новых рекомендациях более строго подошли к разделению регионов на таковые с высокой и низкой резистентностью к кларитромицину. Ранее использовали показатель 20%, а сейчас предложили опираться в выборе на 15%. Согласно рекомендациям Европейского медицинского агентства по оценке медицинских препаратов для лечения бактериальных инфекций, выделяют три категории микроорганизмов в зависимости от их чувствительности к антибиотику: чувствительные (резистентность 0-10%), слабочувствительные (резистентность 10-50%), устойчивые (резистентность >50%). Нр попадает по чувствительности к кларитромицину во 2 категорию, исключая страны Северной Европы. Пороговым значением между высоким и низким уровнем резистентности к кларитромицину принято считать показатель в 15%. Кроме того, руководством к выбору схемы лечения должна служить индивидуальная чувствительность Нр к применяемым антибиотикам, которая зависит от употребления антибиотиков в прошлом данным индивидуумом. Поэтому у пациента, который раньше получал одну из основных схем антибиотикотерапии, должна определяться резистентность Нр к антибиотикам, несмотря на низкий уровень резистентности в данной популяции. Схемы первой и второй линии, предлагаемые Маастрихтским консенсусом V, представлены на рисунках 2 и 3.
В качестве терапии первой линии предлагается стандартная тройная терапия или висмутовая квадротерапия в странах с низкой резистентностью к кларитромицину. В странах с высокой резистентностью к кларитромицину выбор схемы определяется наличием резистентности к метронидазолу или двойной резистентности к метронидазолу и кларитромицину. В регионах с высокой резистентностью к кларитромицину предлагается назначать висмутсодержащую, безвисмутовую квадротерапию. Там, где высока двойная резистентность к кларитромицину и метронидазолу, схемой выбора является висмутсодержащая квадротерапия. Одновременная резистентность к кларитромицину и метронидазолу >15% снижает эффективность всех схем квадротерапии без препаратов висмута. Классическая квадротерапия с препаратом висмута показала высокую эффективность, несмотря на резистентность к метронидазолу в Европе. В отличие от кларитромицина, резистентность к метронидазолу может быть частично преодолена увеличением дозы, частотой и продолжительностью приема антибиотика. Так, последовательная терапия предлагает использовать метронидазол 5-7 дней, гибридная – 7 дней, сопутствующая – 10-14 дней. Однако последовательная терапия эффективнее 14-дневной трехкомпонентной схемы лишь в том случае, если уровень резистентности к метронидазолу меньше 40%. Также для преодоления резистентности рекомендуется увеличивать продолжительность лечения до 14 дней. В своем докладе на Европейской гастронеделе (2016) Р. Malfertheiner привел способы преодоления резистентности Нр к антибиотикам:
- основанная на препаратах висмута квадротерапия;
- ИПП плюс три антибиотика;
- увеличение продолжительности лечения;
- подбор терапии в зависимости от чувствительности Нр к антибиотикам;
- увеличение подавления кислотной продукции большими дозами ИПП.
Таким образом, большое внимание в Маастрихтском консенсусе V уделено квадротерапии на основе препаратов висмута. Если висмут в стране недоступен, в случае высокой двойной резистентности к кларитромицину и метронидазолу предлагается использовать левофлоксацин, рифабутин и двойную терапию с высокими дозами ИПП. Если недоступен тетрациклин, в регионах с высокой двойной резистентностью можно использовать висмутсодержащую квадротерапию, включающую фуразолидон и метронидазол, амоксициллин и метронидазол или применить тройную терапию с висмутом (препарат висмута плюс амоксициллин, кларитромицин или левофлоксацин). Резистентность к кларитромицину снижает эффективность тройной и последовательной терапии, резистентность к метронидазолу – последовательной терапии, двойная резистентность к кларитромицину и метронидазолу снижает эффективность последовательной, гибридной и сопутствующей терапии. Таким образом, еще раз подчеркивается эффективность висмутсодержащей квадротерапии.
После неудачи терапии первой линии (стандартная тройная терапия и фторхинолонсодержащая тройная или квадротерапия / висмутсодержащая квадротерапия) в качестве терапии второй линии используется висмутсодержащая квадротерапия или фторхинолонсодержащая тройная или квадротерапия. В случаях высокой резистентности Нр к фторхинолонам терапией выбора может быть комбинация висмута с другими антибиотиками или рифабутином. Висмут имеет синергический эффект с антибиотиками и преодолевает резистентность Нр к кларитромицину и левофлоксацину. Квадротерапия ИПП, амоксициллин, левофлоксацин плюс висмут показывает обнадеживающие результаты.
В случае неудачи терапии второй линии рекомендовано исследование чувствительности Нр к антибиотикам с помощью культурального метода или молекулярного определения резистентности генотипа для подбора индивидуальной терапии. Безвисмутовая квадротерапия значительно влияет на формирование двойной резистентности. Висмутсодержащая квадротерапия влияет на антибиотикорезистентность наименьшим образом. Резистентность Нр к тетрациклину очень редка и не развивается, несмотря на неудачи в лечении. При этом и резистентность к метронидазолу, если он применяеется в составе висмутсодержащей квадротерапии, не уменьшает процент эрадикации.
После неудачи терапии первой линии (с кларитромицином) и второй линии (висмутсодержащей квадротерапии) рекомендовано использование фторхинолонсодержащего режима. В регионах с известной высокой резистентностью к фторхинолонам может использоваться рифабутинсодержащая терапия спасения или комбинация висмута с различными антибиотиками. В случае неэффективности стандартной тройной терапии первой линии и фторхинолонсодержащего режима второй линии рекомендуется висмутсодержащая квадротерапия как режим третьей линии. При неудаче висмутсодержащей квадротерапии первой линии и фторхинолонсодержащей терапии второй линии рекомендована кларитромицинсодержащая тройная или квадротерапия. Другой опцией может быть комбинация висмута с различными антибиотиками.
В случае аллергии к антибиотикам пенициллинового ряда в качестве терапии первой линии может быть назначена схема ИПП + кларитромицин + метронидазол в регионах с низкой резистентностью к кларитромицину и квадротерапия в регионах с высокой резистентностью к кларитромицину. Фторхинолонсодержащий режим может использоваться как терапия второй линии в этом случае.
Статья печатается в сокращении.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...