Тестостеронова недостатність у літніх чоловіків: новий погляд на стару проблему

Старіння у здорових чоловіків традиційно асоціюється зі зниженням продукції та секреції тестостерону статевими залозами. Вікозалежне зменшення рівня тестостерону зумовлене низкою чинників: первинним ураженням тестостерон-продукуючих клітин яєчок унаслідок погіршення їхнього кровопостачання, зменшення кількості рецепторів на поверхні цих клітин і підвищення їхньої резистентності до лютропіну; дисфункціональними порушеннями в системі гіпоталамус – гіпофіз – статеві залози; підвищенням рівнів глобуліну, що зв’язує статеві гормони й, відповідно, кількості зв’язаного з ним тестостерону, що призводить до зменшення рівня біологічно активного тестостерону; порушенням співвідношення тестостерон/естрогени та розвитком відносної гіперестрогенії, що зумовлено підвищеною ароматизацією андрогенів. Естрогени, пригнічуючи секрецію гонадотропінів, додатково до інших чинників зменшують синтез тестостерону в яєчках.
Максимальна концентрація тестостерону в крові здорових чоловіків спостерігається у віці 25-30 років і починає повільно знижуватися із 35-40 років приблизно на 1-2% на рік. Однак загалом рівні тестостерону в крові тривалий час залишаються в межах нормальних коливань референтних значень, прийнятих для чоловіків молодого віку. Вікозалежне зниження рівнів тестостерону має велику індивідуальну варіабельність: у близько 20% чоловіків у віці старше 60 років рівень загального тестостерону в крові є вищим за рівень верхньої межі нормальних його коливань у молодих чоловіків. Іще один чинник вікозалежних змін рівнів тестостерону в крові пов’язаний із наявністю коморбідних станів, надлишковою вагою/ожирінням і погіршенням загального здоров’я через розвиток хронічних захворювань. Існує тісний взаємозв’язок між старінням чоловічого організму й такими захворюваннями, як серцево-судинні хвороби (в тому числі артеріальна гіпертензія), цукровий діабет (ЦД) 2 типу, онкозахворювання, ожиріння.
Частота тестостерон-дефіцитних станів у чоловіків, за різними даними, становить від 7 до 30%. У Массачусетському дослідженні старіння чоловіків (MMAS) показник гіпогонадних рівнів тестостерону в крові становив ~20% у чоловіків у віці старше 60 років, 30% – старше 70 років і 50% – старше 80 років, а поширеність низьких рівнів вільного тестостерону була ще вищою, що зумовлено зростанням рівнів глобуліну, який зв’язує стероїдні гормони. Підвищений ризик розвитку андрогенодефіциту спостерігається у чоловіків з еректильною дисфункцією, пониженим лібідо, системними захворюваннями, метаболічним синдромом (МС) та його складовими, а також на тлі лікування деякими препаратами (глюкокортикоїдами, антигіпертензивними, психотропними засобами).
Вікозалежне зниження секреції тестостерону не завжди супроводжується клінічними проявами. Однак у частини чоловіків, які старіють, зазвичай розвивається помірна або виражена недостатність тестостерону, яка проявляється симтомокомплексом патологічних станів, що характерні для класичного гіпогонадизму в молодих чоловіків: сексуальна дисфункція, м’язова слабкість, ожиріння, остеопороз, безсоння, втома, депресія, порушення когнітивних функцій. Клінічні симптоми – неспецифічні й можуть змінюватися залежно від віку пацієнта, наявності та вираженості коморбідних станів, тривалості й тяжкості тестостеронової недостатності.
Донедавна комбінацію низьких рівнів тестостерону в крові і вищеперелічених симптомів називали по-різному: чоловічий клімакс, андропауза, синдром часткової андрогенної недостатності літніх чоловіків, синдром часткового падіння андрогенів у літніх чоловіків. У 2002 році було запропоновано визначення «пізній гіпогонадизм» (late onset hypogonadism) – біохімічний синдром, пов’язаний із віком, який характеризується дефіцитом продукції андрогенів зі зменшенням чутливості рецепторів до андрогенів або без нього, що супроводжується суттєвими змінами якості життя і несприятливим впливом на функцію багатьох органів та систем організму. Це визначення відображало точку зору низки дослідників про те, що у чоловіків середнього віку (~50-65 років) і старших чоловіків (>65 років) вікозалежне падіння рівня тестостерону асоційоване із кластером симптомів та ознак, схожих до тих, які спостерігаються у чоловіків із класичною андрогенною недостатністю. Прогресуюче й залежне від віку зниження рівня концентрації тестостерону спричиняє виражене зниження енергії, погіршення самопочуття, порушення статевої функції, ендокринні та метаболічні зміни. Тестостероновий дефіцит може призводити до вираженого погіршення якості життя та дисгармонії у стосунках між партнерами.
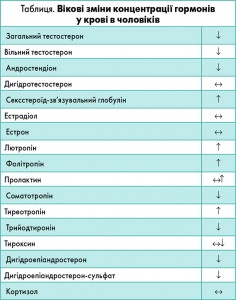
Вікові зміни функціональної активності залоз внутрішньої секреції супроводжуються зниженням продукції та секреції низки гормонів, змінами метаболізму в органах-мішенях (табл.).
Звертає на себе увагу той факт, що продукція анаболічних гормонів при старінні знижується, а продукція катаболічних – не змінюється. Деякі дослідники вважають, що така ситуація є однією з причин розвитку МС у чоловіків, які старіють.
Прояви старіння чоловічого організму в цілому визначають вікові зміни в гіпоталамічних структурах центральної нервової системи, які призводять до розвитку порушення психіки й емоційної сфери, зниження репродуктивної та сексуальної здатності, розумової і фізичної працездатності, рухливості, порушення регуляції гомеостазу та функцій внутрішніх органів.
Встановлено, що низький рівень тестостерону в крові у чоловіків середнього віку є предиктором ризику розвитку в них МС та його складових, причому ризик розвитку абдомінального ожиріння зростає в 2,7 раза, ЦД 2 типу – в 2,1 раза, артеріальної гіпертензії – в 1,8 раза, гіперліпідемії – в 1,5 раза порівняно з чоловіками з нормальною концентрацією тестостерону. Водночас у літніх чоловіків з абдомінальним ожирінням андрогенодефіцит діагностують у 52,4%, із ЦД 2 типу – у 50%, з артеріальною гіпертензією – у 42,4%, гіперліпідемією – у 40,4%. Тобто дефіцит тестостерону розвивається на тлі захворювань, асоційованих зі старінням, і водночас він сам створює преморбідну ситуацію. Встановлено зростання ризику смертності в чоловіків із рівнем тестостерону в крові <8,0 нмоль/л на 68% порівняно з групою чоловіків із нормальним рівнем гормона. За даними MMAS, встановлено, що в чоловіків із низьким рівнем тестостерону в крові вірогідність смертності від серцево-судинних захворювань (ССЗ) і загальна смертність зростають майже вдвічі, а смертність від онкозахворювань – у 3,3 раза порівняно з чоловіками з нормальним рівнем гормона. Низькі рівні загального й вільного тестостерону в крові обернено пропорційно корелювали з ураженням коронарних артерій у чоловіків незалежно від віку та вісцерального ожиріння. У чоловіків з ангіографічно підтвердженою хворобою коронарних артерій рівень тестостерону в крові був нижчим порівняно з контролем, і спостерігалася інверсивна кореляція між його рівнем та ступенем ураження артерій, причому у близько 25% із цих обстежених рівні загального тестостерону в крові залишалися в межах нижньої границі нормальних коливань, а у 50% – <11,0 нмоль/л.
У зв’язку з цим вважається, що хоч і в багатьох чоловіків старших вікових груп рівні тестостерону в крові перебувають у межах нормальних коливань, проте вони є недостатніми для нормального функціонування статевої системи. Іще однією проблемою діагностики андрогенодефіциту в чоловіків, як було зазначено вище, є індивідуальна варіабельність нормальних рівнів загального тестостерону. Загальноприйнятими є референтні значення нормальних коливань рівнів загального тестостерону в крові у дорослих чоловіків, котрі перебувають у межах від 10-12 до 30-35 нмоль/л. Це передбачає, що 2,5% умовно здорових дорослих чоловіків мають рівень загального тестостерону нижче нижньої межі норми.
Наступною можливою проблемою діагностики тестостеронодефіциту є відсутність даних про ступінь і швидкість вікозалежного зниження продукції тестостерону в чоловіків, у яких за наявності характерного симптомокомплексу рівні тестостерону в крові перебувають у «межах норми». Як аргумент на користь останньої гіпотези наводять той факт, що зниження рівня загального тестостерону більш ніж на 50% призводить до розвитку клінічної симптоматики гіпоандрогенізму.
Згідно з рекомендаціями профільних асоціацій чоловікам із низькими рівнями тестостерону в крові та ознаками андрогенної недостатності необхідно призначати терапію препаратами тестостерону, оскільки своєчасне систематичне лікування спроможне не тільки покращити симптоми андрогенодефіциту, а й призупинити розвиток коморбідних захворювань або принаймні полегшити їх прояви.
Згідно з даними Європейської асоціації урологів (2016) дефіцит тестостерону найчастіше спостерігається у літніх чоловіків із такими захворюваннями і станами:
• ЦД 2 типу;
• МС;
• ожиріння;
• вплив радіації на ділянку турецького сідла;
• у разі прийому кортикостероїдів та опіатів;
• хронічні обструктивні захворювання легень помірного та тяжкого ступеня;
• безпліддя;
• остеопороз;
• ВІЛ із саркопенією.
Для лікування чоловічого гіпогонадизму впродовж багатьох десятиліть застосовують переважно замісну терапію тестостероном. Методи маркетингу виробників із просування препаратів на фармацевтичному ринку – агресивні й водночас ефективні: продаж препаратів тестостерону в США з 2005 до 2010 року збільшився удвічі, й схожа тенденція спостерігається і в інших країнах. Прибутки від рецептурних призначень препаратів тестостерону в 1988 році становили близько 18 млн доларів США, а в 2011 році збільшилися до 1,6 млрд, і це зростання не припиняється, особливо після появи трансдермальних гелевих препаратів.
Найвищі темпи зростання кількості призначень препаратів тестостерону (+25-30% щороку) спостерігалися в 1992-2002 роках.
На підставі 70-річних клінічних досліджень встановлено, що терапія тестостероном у чоловіків із класичними формами гіпогонадизму однозначно досягає позитивних ефектів: розвиток вторинних статевих ознак; покращення статевої функції, настрою й самопочуття; збільшення маси скелетних м’язів та сили; підвищення мінеральної щільності кісток; зменшення маси жирової тканини. Крім того, замісна терапія тестостероном у молодих чоловіків (у віці до 50 років) із класичним гіпогонадизмом супроводжується низькою частотою розвитку побічних ефектів. Утім, слід зауважити, що наразі проведено небагато тривалих рандомізованих досліджень щодо застосування препаратів тестостерону в літніх чоловіків (у віці старше 65 років) із вікозалежним андрогенодефіцитом. Довгий час існували застороги стосовно потенційних побічних ефектів (насамперед розвиток раку передміхурової залози) від призначення тестостерону в чоловіків старшого віку із супутніми захворюваннями. Відтак вважали, що призначення препаратів тестостерону може бути показане в літніх чоловіків, в окремих випадках за наявності патології яєчок, гіпофіза або гіпоталамуса (опіат-індукована андрогенна недостатність або вторинний гіпогонадизм після резекції пухлини гіпофіза). Оскільки діагностика та ефективність замісної терапії тестостероном гіпогонадних станів у літніх чоловіків ґрунтуються на недостатньо контрольованих дослідженнях, то досі залишаються нез’ясованими діагностичні критерії, показання і протипоказання.
У 2013 році група дослідників провела ретроспективний аналіз даних (R. Vigen, 2014), у якому повідомлялося про зростання ризику нефатальних кардіоваскулярних ризиків у чоловіків на тлі прийому препаратів тестостерону, однак невдовзі було опубліковано результати іншого ретроспективного дослідження, які показали, що зростання частоти нефатального інфаркту міокарда на тлі замісної терапії тестостероном відрізнялося від такого самого показника до прийому препаратів тестостерону (W.D. Finkel, 2014). Відтак Управління з контролю якості продуктів харчування та лікарських препаратів США (FDA) оголосило про намір провести дослідження кардіоваскулярних ризиків за результатами застосування препаратів тестостерону.
У 2015 році в м. Прага (Республіка Чехія) відбулася Міжнародна експертна конференція з тестостеронового дефіциту та його лікування [1], на яку як експерти були запрошені урологи, ендокринологи, терапевти й науковці. Важливо, що дискусійна панель була широко представлена медичними фахівцями з різних континентів, різних галузей медицини, які виконують клінічні або експериментальні дослідження ефективності та безпечності лікування препаратами тестостерону. Проведення конференції мало на меті визначення ключових рекомендацій щодо терапії тестостероном на підставі сучасних принципів доказової медицини. За підсумками обговорення учасники конференції одностайно ухвалили консенсус (9 резолютивних висновків) із питань діагностики та лікування синдрому дефіциту тестостерону в чоловіків.
Експерти рекомендують замінити термін «замісна терапія тестостероном» терміном «тестостеронова терапія» (ТТ), термін «гіпогонадизм» – терміном «тестостероновий дефіцит» (ТД), а термін «низький тестостерон» вважати неформальним (неофіційним).
Резолюція 1
Експерти вважають, що ТД є встановленим важливим медичним станом, який негативно впливає на чоловічу сексуальність, репродукцію, фізичну функцію, призводить до зменшення маси та сили м’язів, впливає на сексуальну функцію у вигляді зниження лібідо й підвищення частоти еректильної дисфункції та розладів оргазму, призводить до компрометації загальної сексуальної активності, сприяє розвиткові абдомінального ожиріння, втомлюваності, зменшенню кісткової тканини, анемії, депресії, пониженої мотивації, погіршенню загального здоров’я та якості життя. Тестостерон впливає на багато органів та систем організму, регулює метаболізм вуглеводів, жирів і білків, впливає на ріст м’язів і адипогенез, а ТД – асоційований з інсулінорезистентністю, запаленням, дисліпідемією, МС та судинним ризиком. Достеменно встановлено, що частота і тяжкість захворювання коронарних артерій, товщина інтима-медіа каротидних артерій, атеросклероз та смертність інверсивно корелюють із концентраціями тестостерону в крові.
Резолюція 2
Симптоми та ознаки ТД є результатом низьких рівнів тестостерону, і їх можна успішно лікувати незалежно від ідентифікації етіологічного фактора ТД. Клінічні прояви ТД зростають прямо пропорційно зменшенню рівнів циркулюючих андрогенів. Зниження концентрацій тестостерону може спостерігатися за наявності відомих причин або в поєднанні із такими супутніми захворюваннями, як ЦД 2 типу, ожиріння, СНІД, хронічна недостатність нирок, тривалий прийом глюкокортикоїдів та опіоїдів, або з невідомих причин. Стан, схожий на ТД, може розвиватися у здорових волонтерів із фармакологічним зниженням рівнів тестостерону в крові, а також у чоловіків із раком простати, які приймають андроген-деприваційну терапію. Симптоми та ознаки, пов’язані із ТД, зникають з відновленням нормальних рівнів тестостерону. ТД – зумовлений дефект у системі гіпоталамус – гіпофіз – статеві залози, що проявляється класичними формами гіпогонадизму: первинним або вторинним. Отже, терапія тестостероном може бути рекомендована не тільки чоловікам з ідентифікованою етіологією.
Резолюція 3
ТД – глобальна суспільна проблема в усьому світі, однак епідеміологічні дослідження щодо його поширеності в різних дослідженнях є варіабельними, оскільки існують відмінності у використанні біохімічних порогів для тестостерону та засобів для ідентифікації ТД/гіпогонадизму. В США в чотирьох дослідженнях частота ТД становила 6-30%, а в EMAS – 2,1% на підставі врахування наявності трьох ідентифікованих сексуальних симптомів та рівнів загального тестостерону <11,0 нмоль/л. У країнах Азії частота ТД у чоловіків становить 9,5-30%, а в Австралії та Південній Америці в осіб з ожирінням, ЦД 2 типу та МС – від 14 до 43%. Ці показники можна порівняти з результатами досліджень в інших частинах світу, що є додатковим свідченням високої поширеності ТД серед чоловіків із метаболічними порушеннями. ТД може бути предиктором розвитку ЦД 2 типу, МС, особливо при врахуванні його ефектів на ожиріння, остеопорозу. В США, за деякими оцінками, витрати, пов’язані з ТД, за 20-річний період сягнули близько 190-525 млрд доларів. Однак у США тільки 12% чоловіків із ТД (поєднання симптомів і концентрація тестостерону в крові <10,4 нмоль/л) потребують тестостеронотерапії.
Резолюція 4
Терапія чоловіків із ТД – ефективна, раціональна і доказово обґрунтована. Популяційні дослідження свідчать, що сексуальні розлади є найбільш частими симптомами, асоційованими із ТД. Результати метааналізу 29 рандомізованих контрольованих досліджень (n=1930) показали, що терапія тестостероном покращує еректильну функцію, статеве бажання та оргазм.
Важливо, що ці покращення спостерігалися у чоловіків із ТД, а не в чоловіків із нормальними рівнями тестостерону. Тяжкість ТД на початку лікування асоціюється з позитивною відповіддю на терапію тестостероном. Дослідження ефектів замісної терапії тестостероном підтверджують її вірогідні позитивні ефекти порівняно із застосуванням плацебо для покращення ерекцій, лібідо, сексуальної активності та настрою. Ефекти на масу тіла, окружність талії та індекс маси тіла є суперечливими. Відмічено вірогідний позитивний ефект терапії тестостероном на рівні глюкози натще, індекс НОМА та невірогідний – на ліпідний метаболізм й артеріальний тиск.
Резолюція 5
Немає чітко визначеного порогового рівня тестостерону, який би реально розрізняв чоловіків, які відповідатимуть і не відповідатимуть на лікування тестостероном. Цей факт підтверджено Асоціацією ендокринологів США, а також багатьма іншими профільними асоціаціями. Ризик розвитку тестостерон-залежного зменшення лібідо та енергії зростає при рівнях тестостерону <15 нмоль/л, вісцерального жиру – <12 нмоль/л, депресії і ЦД 2 типу – <10 нмоль/л, еректильної дисфункції – <8 нмоль/л. Відповідь на терапію тестостероном є більш вірогідною у чоловіків з більш нижчими рівнями тестостерону.
Визначення рівнів загального тестостерону – прийнятний тест у більшості клінічних випадків. Однак через міжвидові варіації концентрації сексстероїд-зв’язувального глобуліну, рівні вільного тестостерону можуть краще відображати андрогенний статус деяких пацієнтів. Існують різні фенотипи андрогенної чутливості, переважно завдяки варіаціям функціональної активності андрогенових рецепторів. Одним із них є поліморфізм CAG-повторів в ексоні 1-АР гена. Транскрипція андроген-залежних мішеней генів зменшується in vitro зі зростанням кількості триплетів. Клінічно у разі підвищення кількості CAG-повторів андрогенова відповідь на будь-яку концентрацію тестостерону в крові (ендогенна або у відповідь на терапію тестостероном) зменшується. Три ключові концепції допомагають зрозуміти використання препаратів тестостерону й обмеження його концентрації в крові у чоловіків: 1) різні інтраіндивідуальні пороги існують для різних симптомів та ознак ТД; 2) є реальна інтраіндивідуальна варіабельність порогових рівнів тестостерону для тих самих симптомів та ознак ТД, яка частково залежить від функціональної активності андрогенового рецептора; 3) варіабельність концентрацій сексстероїд-зв’язувального глобуліну серед чоловіків впливає на концентрацію вільного тестостерону за будь-яких концентрацій загального тестостерону. Визначення вільного тестостерону може бути важливим біохімічним критерієм в оцінці чоловіків із симптомами, пов’язаними з ТД. У наукових керівництвах немає чітко встановлених однорідних порогових концентрацій тестостерону для всіх індивідуумів як первинного інструменту діагностики ТД.
Резолюція 6
Немає науково обґрунтованих рекомендацій проти застосування терапії тестостероном у чоловіків різних вікових категорій. Встановлено, що рівні тестостерону зменшуються з віком – асоційоване з віком помірне зниження середніх рівнів тестостерону характерне для чоловіків у віці старше 40 років, більш виражене зменшення спостерігається у чоловіків із коморбідними станами. Рівні вільного та біоактивного тестостерону знижуються швидше, ніж рівні загального тестостерону, що значною мірою зумовлено зростанням рівнів сексстероїд-зв’язувального глобуліну. Вік не є специфічним чинником ризику для ТД, тому термін «вікозалежний гіпогонадизм» – оманливий. Більшість чоловіків, навіть у старшому віці, мають рівні тестостерону, які перебувають у межах нормальних референтних значень. Однак низькі рівні тестостерону в чоловіків з ознаками й симптомами ТД частіше зустрічаються серед осіб з абдомінальним ожирінням, ЦД 2 типу та іншими хронічними захворюваннями незалежно від віку. Кращі клінічні та фізіологічні відповіді на терапію тестостероном були задокументовані у чоловіків молодого та середнього віку. Прикметно, що в чоловіків цих вікових категорій підвищення м’язової маси і м’язової сили на тлі терапії тестостероном не залежало від віку. Стимуляція еритропоезу спостерігається як у молодих чоловіків, так і в чоловіків старших вікових груп, однак цей феномен не можна трактувати як ускладнення у відповідь на терапію тестостероном унаслідок того, що у чоловіків старших вікових груп він частково зумовлений низьким метаболічним кліренсом екзогенного тестостерону порівняно з молодими особами. Моніторування пацієнтів здатне запобігти розвиткові побічних ефектів. У світлі очікуваного покращення якості життя та відсутності виражених негативних ефектів або як наслідок зростання вікозалежного профілю ризиків експерти не підтверджують вікового обмеження у застосуванні препаратів тестостерону в чоловіків. Крім того, результати дослідження серед чоловіків у віці старше 65 років підтверджують досягнення вірогідних позитивних ефектів терапії тестостероном без зростання кількості серйозних побічних ефектів.
Резолюція 7
Гіпотеза підвищеного ризику серцево-судинних подій, асоційованих із терапією тестостероном, наразі не підтверджена. Водночас є вагомі докази, які ґрунтуються на спостереженні за чоловіками впродовж понад 20 років і які засвідчують, що низькі рівні тестостерону асоційовані з підвищеним серцево-судинним ризиком, а вищі рівні тестостерону є кардіопротективними. У ході обсерваційних досліджень встановлено зростання показника смертності, частоти розвитку атеросклерозу, хвороби коронарних артерій, потовщення інтими-медії каротидних артерій, збільшення жирових мас та погіршення глікемічного контролю у чоловіків із низьким рівнем тестостерону. Натомість терапія тестостероном у чоловіків із ТД була асоційована з приблизно 50% зменшенням у них смертності, а також із покращенням відомих факторів ризику ССЗ, у тому числі зменшення жирових мас, підвищення відсотка «худих» жирових мас, покращення глікемічного контролю. Результати метааналізу рандомізованих досліджень продемонстрували зменшення серцево-судинних подій після терапії тестостероном у чоловіків із метаболічними порушеннями, а в іншому дослідженні – зменшення ризику інфаркту міокарда в чоловіків із найвищою категорією ризику. Встановлена редукція серцево-судинних подій у чоловіків, у яких рівні тестостерону нормалізувалися після терапії тестостероном порівняно з тими, у яких такі рівні залишалися низькими. Не встановлено асоціативних зв’язків лікування препаратами тестостерону з підвищенням ризику тромбозу вен.
Резолюція 8
Немає доказів, які підтверджують ризик підвищення рівнів простат-специфічного антигену (ПСА) у пацієнтів, котрі отримують терапію тестостероном. У ході тривалого проспективного дослідження не було встановлено асоціації між ендогенними рівнями андрогенів у крові та ризиком раку простати. Ризик розвитку раку простати у чоловіків, які приймають терапію тестостероном, не збільшувався. У здорових волонтерів зростання рівнів тестостерону до супрафізіологічних не призводило до підвищення рівнів ПСА або об’єму простати. У клінічних рекомендаціях Європейської асоціації урологів зазначено, що після успішного лікування раку простати може бути розглянута терапія тестостероном.
Резолюція 9
Отримано докази, які підтримують дослідну ініціативу для визначення можливих переваг терапії тестостероном у чоловіків із кардіометаболічними захворюваннями, включаючи ЦД 2 типу, ожиріння та МС, які є високопревалентними станами, асоційованими з високими показниками захворюваності й смертності. Незалежно від цих станів серцево-судинні події зумовлюють приблизно 40% смертності чоловіків в індустріально розвинених країнах. Спостерігається висока частота низьких рівнів тестостерону в чоловіків із ЦД 2 типу, МС, ожирінням і ССЗ, а ТД асоційований із несприятливим профілем серцево-судинного ризику й підвищеним розвитком атеросклерозу. В ході обсерваційних досліджень було встановлено наявність інверсивних кореляцій між рівнями тестостерону в крові та атеросклерозом, показниками захворювань коронарних артерій і смертністю. Крім того, шестирічне ретроспективне дослідження у тестостерон-дефіцитних чоловіків із ЦД 2 типу виявило, що в осіб, які отримували терапію тестостероном, удвічі покращувався показник виживання порівняно з чоловіками, які не отримували такого лікування.
Дискусія
Серед експертів досі триває жвава дискусія щодо переваг та ризиків застосування препаратів тестостерону в чоловіків. Вищенаведені рекомендації (резолюції) – результат узгодження позицій фахівців різних спеціальностей стосовно призначення терапії тестостероном чоловікам із клініко-лабораторними ознаками його дефіциту. Консолідована думка членів експертної панелі була прийнята одностайно на підставі багаторічного досвіду, численних наукових досліджень та на засадах доказової медицини. З таких позицій спірним виглядає повідомлення FDA, що терапія тестостероном показана лише чоловікам з одним або більше специфічними симптомами/станами, асоційованими з ТД, і її не слід призначати при вікозалежному андрогенодефіциті [2]. Також було зазначено, що симптоми й маніфестація ТД зумовлені недостатніми/неадекватними концентраціями тестостерону в сироватці крові, які не залежать від етіопатогенетичних факторів. Слід зауважити, що хоч FDA і відіграє ключову роль у регуляції галузі фармакотерапії, проте не має безпосереднього впливу на практичну медицину. Концепції стосовно медичних результатів потребують медичної експертизи, яку й було представлено у вищезгаданому консенсусному документі.
За останні 20 років було ідентифіковано низку нових причин ТД, і в майбутньому очікується розширення їх спектра. З позиції синдромологічного підходу до терапії ТД наразі доцільним вбачається можливість застосування терапії тестостероном у більшості чоловіків із симптомокомплексом, характерним для ТД, без чітко ідентифікованого етіологічного чинника.
Накопичений досвід терапії тестостероном свідчить про її порівняно хорошу ефективність як у молодих чоловіків, так і у пацієнтів із ТД старших вікових груп. Окрім того, більшість поширених станів/захворювань, за яких вдаються до терапії тестостероном, у тому числі еректильна дисфункція, знижене лібідо, ЦД 2 типу, хронічна ішемічна хвороба серця, є вікозалежними. Наразі важливим є визнання, що терапія тестостероном має широкий діапазон застосування, не всі межі якого достатньо вивчені. В дослідженні P.J. Snyder і співавт. було продемонстровано позитивний ефект терапії тестостероном у чоловіків похилого віку на статеву функцію (ерекцію, лібідо та сексуальну активність) [3].
Одним із найбільш відповідальних рішень у клінічній практиці є визначення кандидатів для терапії тестостероном на підставі встановлення рівня загального тестостерону в крові. Чимало професійних асоціацій публікують клінічні рекомендації, в яких пропонують різні порогові рівні, нижче яких діагноз може бути лабораторно підтверджений. Однак наразі поширена думка про те, що досі немає специфічного порога тестостерону, відносно якого можна надійно розподілити чоловіків із і без ТД та бути предиктором ефективності подальшої терапії. Ця проблема зумовлена значною міжіндивідуальною варіабельністю рівня тестостерону, варіабельністю біоактивності тестостерону, що значною мірою ґрунтується на концентраціях сексстероїд-зв’язувального глобуліну у сироватці крові та генетичними варіаціями в кількості CAG-повторів в AR-гені, а також генному поліморфізмі, який, у свою чергу, впливає на чутливість до андрогенів. Відсутність встановлених лімітів рівнів загального тестостерону заохочує клініцистів до обговорення клінічних ознак та симптомів, додатково до біохімічних результатів при визначенні кандидатів для лікування.
Упродовж десятиліть найпоширенішим застереженням стосовно терапії тестостероном вважалося те, що вона може сприяти виникненню раку простати або прискорити швидкий розвиток вже наявного захворювання. Наразі не знайдено доказів підвищеного ризику раку простати у чоловіків, які отримують терапію тестостероном [4], або у чоловіків із вищими ендогенними концентраціями андрогенів порівняно з тими, у яких ці рівні нижчі [5]. Також з’явилися нові докази стосовно підтвердження асоціації між низькими рівнями тестостерону й негативними прогностичними факторами раку простати, такими як високий показник за шкалою Глісона й високий відсоток розвитку рецидиву після хірургічного лікування [6].
Можливий негативний вплив терапії тестостероном на стан серцево-судинної системи був продемонстрований лише в чотирьох дослідженнях за більш ніж 20 річний період [7]. Навпаки, більшість останніх досліджень повідомляють про менший відсоток серцево-судинних подій у чоловіків з андрогенодефіцитом на тлі замісної терапії тестостероном [8] або у чоловіків із вищими ендогенними рівнями тестостерону [7]. На думку авторів, концентрації тестостерону в крові інверсивно корелюють з атеросклерозом, патологією коронарних артерій, товщиною інтима-медіа каротидних судин і смертністю. Американська асоціація клінічних ендокринологів та Американська колегія ендокринологів на підставі огляду літературних джерел опублікували власну думку про відсутність незаперечних доказів зростання ризику виникнення ССЗ у чоловіків, які отримують терапію тестостероном [9]. Також останні дослідження повідомляють про менший ризик розвитку ССЗ у чоловіків, у котрих нормалізувався рівень тестостерону в крові після терапії порівняно з чоловіками, які мали постійно низькі рівні тестостерону [10, 11].
Крім того, поодинокі публікації не повідомляють про підвищений ризик тромбоемболічних ускладнень унаслідок терапії тестостероном [12]. У деяких дослідженнях було встановлено, що у чоловіків із ТД, які отримали терапію тестостероном, показник смертності зменшувався приблизно наполовину порівняно з тими, кому не було призначено такої терапії [13, 14].
На підставі цих даних автори дійшли висновку про необхідність проведення широких проспективних плацебо-контрольованих досліджень кардіопротективних ефектів терапії тестостероном у чоловіків із ризиком ССЗ та низькими рівнями тестостерону.
Література
1. Morgentaler A., Zitzmann М., Traish A.M., Fox A. International expert consensus conference on testosterone deficiency and its treatment held in Prague, Czech Republic // Aging Male, 2015. – Vol. 18. – № 4. – Р: 205-216. Epub 2015 Nov 20.
2. Nguen C.P., Hirsch M.S., Money D. et al. Testosterone and «age-related hypogonadism» – FDA concerns. // N. Engl. J. Med. 2015. – Vol. 373.– P. 689-691.
3. Snyder P.J., Bhasin S., Cunningham G.R. et al. Testosterone trials Investigators. Effects of testosterone treatment in older men // N. Engl. J. Med. 2016. – Vol. 374. – P. 611-624.
4. Cui Y., Zong H., Yan H., Zhang Y. The effect of testosterone replacement therapy on prostate cancer: a collaborative review and meta-analysis // Prostate Cancer Prostatic Dis. 2014. – Vol. 17. – P. 132-143.
5. Endogenus Hormones and Prostate Cancer Collaborative Group. Endogenus sex hormones and prostate cancer: a collaborative analisis of 18 prospective studies. J. Natl. Cancer Inst. 2008. – Vol. 100 (3). – P. 170-183.
6. Khera M., Crawford D., Morales A. et al. A new era of testosterone and prostate cancer: from physiology to clinical implications // Eur. Urol. 2014. – Vol. 65. – P. 115-123.
7. Morgentaler A., Miner M.M., Caliber M. et al. Testosterone therapy and cardiovascular risk advances and controversies // Mayo Clin Proc. 2015. – Vol. 90. – P. 224-251.
8. Corona G., Maseroli E., Rastrellі G. et al. Cardiovascular risk associated with testosterone-boosting medications: a systematic review and meta-analysis // Expert Opin Drug. Saf. 2014. – Vol. 13. – P. 1327-1351.
9. Goodman N., Guay A., Dandona P. et al. Reproductive Endocrinology Scientific Committee. American Association of Clinical Endocrinologist and American College of Endocrinology position statement on the association of testosterone and cardiovascular risk // Endocr. Pract. 2015. – Vol. 21. – P. 1066-1073.
10. Anderson J.L., May H.T., Lappe D.L. et al. Impact of testosterone replacement therapy on miocardial infarction, stroke, and death in men with low testosrerone concentrations in a integrated health care system // Am. J. Cardiol. 2016. – Vol. 117. – P. 794-799.
11. Sharma R., Oni O.A., Gupta K. et al. Normalization of testosterone level is associated with reduced incidence of miocardial infarction and mortality in men // Eur. Heart. J. 2015. – Vol. 36. – P. 2706-2715.
12. Baillargeon J., Urban R.J., Morgentaker A. et al. Risk of venous thromboembolism in men receiving testosterone therapy // Mauo Clin Proc. 2015. – Vol. 90. – P. 1038-1045.
13. Muraleedharan V., Marsh H., Kapoor D. et al. Testosterone deficiency is associated with increased risk of mortality and testosterone replacement improves survival in men with type 2 diabetes. // Eur.J.Endocrinol. 2013. – Vol. 43. – P. 153-164.
14. Shores M.M., Smith N.L., Forsberg C.W. et al. Testosterone treatment and mortality in men with low testosterone levels // J. Clin. Endocrinol. Metabol. 2012. – Vol. 97. – P. 2050-2058.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....
Метформін – протидіабетичний препарат першої лінії, який пригнічує глюконеогенез у печінці і в такий спосіб знижує рівні глюкози в крові. Крім того, він знижує ризик кардіоваскулярних подій, чинить нефропротекторний ефект і здатен подовжувати тривалість життя. Завдяки цим властивостям метформін нині розглядають як мультифункціональний препарат і дедалі частіше застосовують для лікування та профілактики різноманітних захворювань....
Сучасне лікування хворих на цукровий діабет (ЦД) 2 типу включає зміну способу життя і медикаментозну терапію для контролю глікемії та профілактики ускладнень. Проте дослідження показують, що на практиці небагато хворих досягають контролю захворювання (частково через погану прихильність до лікування). Частка пацієнтів, які дотримуються протидіабетичної терапії, коливається від 33 до 93% (упродовж 6-24 міс) [1, 2]....