Статины при остром коронарном синдроме: вторичная профилактика или экстренная помощь?
За последние 10-15 лет накоплен большой массив данных о так называемых плейотропных эффектах статинов, которые наблюдаются независимо от их основного предназначения – снижать атерогенный холестерин крови. Показано, что статины не только уменьшают прогрессирование атеросклероза сосудов, но и ингибируют различные патологические пути и процессы, приводящие к дестабилизации атеросклеротических бляшек в коронарных артериях и развитию острого коронарного синдрома (ОКС). Статины оказывают воздействие на механизмы эндотелиальной дисфункции, участвуют в каскадах системного воспалительного ответа, коагуляции и тромбообразования. В серии проспективных контролируемых исследований препараты этой группы продемонстрировали безопасность, а в некоторых – и способность улучшать исходы при раннем назначении после ОКС. Кроме того, публикуются работы, в которых показаны положительные эффекты статинов не только как средства вторичной профилактики, но и как непосредственной терапии инфаркта миокарда (ИМ) в острой фазе, у клинически нестабильных пациентов.

Статины для ранней вторичной профилактики
В многочисленных наблюдательных исследованиях (RIKS-HIA, GUSTO IIb, PURSUIT и др.) раннее начало приема статинов после ОКС ассоциировалось с улучшением исходов, в том числе с меньшей смертностью в первые 6-12 мес наблюдения. Эффекты статинов при ОКС изучались в нескольких проспективных исследованиях. Не все из них подтвердили, что статины уменьшают частоту повторных больших сердечно-сосудистых событий после ОКС (табл.). А точнее, это справедливо только в отношении дозы 80 мг/сут аторвастатина, которая улучшала исходы в исследованиях MIRACL (по сравнению с плацебо) и PROVE-IT (по сравнению с более «легким» режимом гиполипидемической терапии – правастатином в дозе 40 мг).
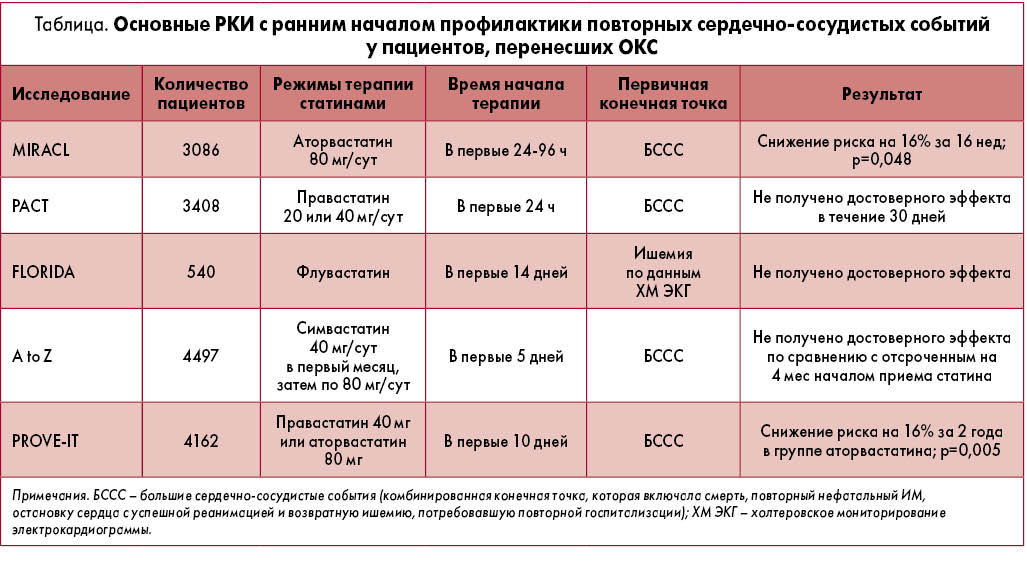
Также опубликовано несколько метаанализов рандомизированных контролируемых исследований (РКИ) с ранним назначением статинов при ОКС. Они четко показали, что назначение статинов не влияет на частоту нефатальных ИМ, инсультов и показатели смертности в первые 4 мес после ОКС. Но в более поздний период защитный эффект становится отчетливым, достигает статистической достоверности на шестом месяце терапии и длится до 2 лет (такой была максимальная длительность исследований). Относительный риск повторного ИМ, инсульта или смерти у пациентов, принимавших статины, уменьшался на 16% (N. Vale et al., 2011; M. Briel et al., 2012).
При наличии этих доказательств (полученных более 10 лет назад) и рекомендаций класса IA назначать статины как можно раньше (в европейских и американских руководствах по ведению пациентов с ОКС) вызывает недоумение низкий процент пациентов, которые принимают интенсивную (40-80 мг аторвастатина или 20-40 мг розувастатина) терапию после перенесенного ОКС. И эта проблема актуальна не только для Украины, но и для специализированных кардиологических клиник США и Канады (J.R. Shiu, G.J. Pearson et al., 2012; R. Bukata, 2015).
Следует отметить, что вышеупомянутые исследования статинов при ОКС были рассчитаны на раннее начало терапии – в первые дни после госпитализации, но не в отделении интенсивной терапии. До приема первой дозы большинство пациентов были стабилизированы, а в некоторых исследованиях стабильная гемодинамика была обязательным критерием включения. Учитывая многочисленные нелипидные эффекты статинов, способствующие стабилизации бляшек и их заживлению после недавно перенесенного разрыва (именно повреждение атеросклеротической бляшки с последующим тромбообразованием является причиной ОКС и внезапной смерти), а также их антикоагулянтные и антиагрегантные свойства, есть все основания ожидать пользу от применения статинов в острейшей фазе ОКС, у нестабильных пациентов, начиная с отделения реанимации и интенсивной терапии или катетеризационной лаборатории.
Статины в неотложной терапии ОКС: экспериментальные и клинические предпосылки
S. Hayashidani и соавт. (2002) были среди первых экспериментаторов, обнаруживших положительные эффекты статинов сразу после начала ишемии миокарда. В эксперименте с перевязкой коронарной артерии лучше выживали мыши, которым немедленно после наложения лигатуры вводили дозу флувастатина. Bell и Yellon на изолированном мышином сердце продемонстрировали свойство аторвастатина уменьшать зону реперфузионного повреждения миокарда (R.M. Bell, D.M. Yellon, 2003). Эти результаты подтвердило исследование in vivo, в котором симвастатин предотвращал реперфузионное поражение при экспериментальном инфаркте у крыс (S. Wolfrum et al., 2004).
Авторы обсуждают возможные механизмы «быстрых» эффектов статинов при ОКС. Во-первых, положительное влияние статинов на эндотелиальную функцию в фазу ишемии, по-видимому, не связано с регулированием матричных РНК (мРНК), кодирующих эндотелиальную NO-синтетазу (eNOS). Ранее было установлено, что этот путь требует нескольких часов (U. Laufs et al., 1998). Быстрое повышение активности eNOS объясняется влиянием статинов на сигнальный путь PI 3-kinase/Akt, который обеспечивает фосфорилирование eNOS в течение минут.
В клинических исследованиях получены данные о влиянии статинов на липидный профиль и воспаление уже в первые 24 ч ОКС. В пилотном проспективном исследовании первую дозу церивастатина назначали при поступлении пациентов с ОКС и уже через сутки получали достоверное снижение уровней С-реактивного белка (СРБ) и интерлейкина-6 по сравнению с контрольной группой (P. Ostadal et al., 2003).
Иранские исследователи изучали влияние высоких и низких доз аторвастатина на уровень высокочувствительного СРБ у пациентов с ОКС. Аторвастатин в дозе 40 мг/сут у пациентов с ОКС наряду со снижением содержания в крови атерогенного холестерина липопротеинов низкой плотности существенно снижал уровень высокочувствительного СРБ, отражающий острую фазу воспалительной реакции. Правда, это не повлияло на клинические исходы в группах высокодозовой и низкодозовой терапии аторвастатином, что, по-видимому, обусловлено недостаточной статистической мощностью исследования (B. Zamani et al. Int. J. Res. Med. Sci. 2016).
Если раньше считалось, что эффект снижения уровня холестерина наступает через несколько недель терапии статинами, то сегодня исследователи говорят о вмешательстве в липидный обмен в масштабах дней и часов. Такая картина особенно характерна для больных ОКС. При назначении флувастатина в дозе 80 мг пациентам с ОКС уже через сутки наблюдали достоверное снижение уровней общего холестерина, холестерина липопротеинов низкой и высокой плотности на 14,5; 17,2 и 10% соответственно по сравнению с контрольной группой (P. Ostadal et al., 2007). D. Vondrakova и соавт. повторили эти результаты с 80 мг аторвастатина (2010). В отличие от исследований по длительной терапии статинами, обращает на себя внимание снижение уровня холестерина липопротеинов высокой плотности у пациентов с ОКС, что авторы объясняют не действием статинов, а естественной реакцией в острой фазе ишемии (P. Ostadal, 2012). Возможно, быстрое снижение атерогенных фракций холестерина под влиянием первой дозы статина имеет значение в механизмах стабилизации коронарных бляшек при ОКС. Терапия статинами при длительном их использовании способна стабилизировать атероматозную бляшку, уменьшить ее объем и положительно повлиять на другие параметры, что было показано в метаанализе исследований с внутрисосудистой ультразвуковой оценкой морфологии атером (M. Banach et al., 2015).
В серии экспериментов показаны антитромботические свойства статинов, их влияние на протромбиновый фрагмент (F1+2), фибринопептид А и комплекс тромбин-антитромбин III, за счет чего подавляется образование тромбина у пациентов с пограничными или высокими значениями холестерина (A. Szczeklik et al., 1999; J. Musial et al., 2001). Статины влияют не только на коагуляцию, но и на фибринолитическую активность крови: стимулируют синтез тканевого активатора плазминогена (ТАП) и одновременно понижают уровень ингибитора ТАП (H. Seeger et al., 2001; F. Wiesbauer et al., 2002). Предполагается, что эти эффекты могут иметь значение как при медикаментозном, так и при фармакоинвазивном лечении ОКС.
Влияние на клинические исходы
Какой бы мощной не была база экспериментальных данных о положительных эффектах статинов в острую фазу ишемии миокарда, их клиническую перспективу в лечении ОКС определяют контролируемые клинические исследования с оценкой выживаемости и частоты повторных сердечно-сосудистых событий.
Первое многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование по изучению эффектов статинотерапии, назначенной для лечения ОКС, проводилось с флувастатином в группе 156 пациентов, которым стартовую дозу препарата 80 мг назначали сразу же при поступлении в стационар (Fluvastatin in the therapy of Acute Coronary Syndrome – FACS). Двойная слепая фаза исследования длилась 30 дней, а затем пациентам предлагали продолжать прием флувастатина в открытом режиме. Первичным критерием эффективности было влияние статина на уровни провоспалительных цитокинов (СРБ, интерлейкин-6 и др.), однако они остались без изменений в обеих группах. Вместе с тем терапия флувастатином ассоциировалась с достоверно меньшей частотой комбинированной конечной точки – сердечно-сосудистых событий на протяжении года наблюдения (11,5 против 24,4% в группе плацебо; 95% доверительный интервал, ДИ 0,17-0,95; p=0,038). Несмотря на малую выборку и другие ограничения, результаты исследования FACS подтвердили пользу стратегии назначения статинотерапии «как можно раньше» при ОКС.
Статины в отделении интенсивной терапии?
При ИМ с элевацией сегмента ST ранняя реваскуляризация методом чрескожного коронарного вмешательства (ЧКВ) стала стандартом лечения, улучшающим выживаемость больных. Закономерно, что интервенционные кардиологи первыми начали изучение эффектов предварительной и обычно высокой («нагрузочной») дозы статинов при ОКС. Совершенно очевидно, что здесь речь идет уже не о ранней вторичной профилактике, а о тех самых «быстрых» механизмах действия статинов, которые помогают восстановлению тканевого (миокардиального) кровотока, защищают миокард от реперфузионного повреждения, предотвращают прогрессирующее тромбообразование и уменьшают перипроцедурные осложнения на фоне перкутанных вмешательств.
Из наиболее значимых исследований следует отметить ARMYDA-ACS, в котором продемонстрировано достоверное уменьшение частоты перипроцедурных ИМ после кратковременной терапии аторвастатином у ранее не получавших статины пациентов с ОКС перед ЧКВ, а также ARMYDA-RECAPTURE, показавшее, что нагрузочная доза аторвастатина улучшает исходы у пациентов, которые до ЧКВ постоянно принимали статины.
Одной из главных проблем неотложной кардиологии является так называемый феномен «no-reflow» – «невосстановленный кровоток», который заключается в отсутствии адекватного кровоснабжения ткани миокарда после успешного восстановления проходимости инфаркт-обусловившей артерии как на фоне тромболизиса, так и при проведении интервенционных вмешательств и ассоциируется с плохими исходами. На сегодняшний день патофизиология феномена «no-reflow» остается недостаточно изученной. Считается, что он имеет многофакторное происхождение. Возможные объяснения – это тромбоз и эмболизация микроциркуляторного русла ишемизированного миокарда фрагментами разрушенной бляшки и тромба с последующей местной активацией коагуляционного каскада крови и провоспалительных факторов в присутствии повышенного уровня липопротеинов, отеком клеток эндотелия сосудов в зоне реперфузии (P.H. Jones et al., 2003; B. Zhao et al., 2011; S.S. Zhou et al., 2015).
Осенью 2016 г. были опубликованы результаты корейско-американского многоцентрового рандомизированного исследования RESIST-ACS, в котором изучали эффекты нагрузочной дозы аторвастатина перед ЧКВ у пациентов с ОКС без элевации сегмента ST. Терапия аторвастатином в нагрузочной дозе 80 мг за 12-24 ч, затем 40 мг за 2 ч до выполнения ЧКВ предотвращала микроваскулярную дисфункцию и вторичное повреждение миокарда (Bong-Ki Lee et al. Korean Circ. J. 2016).
Китайские авторы недавно опубликовали результаты исследования, в котором изучали эффекты предпроцедурной дозы аторвастатина при ИМ с элевацией ST. Отсутствие восстановления кровотока по ангиографическим критериям TIMI ≤2 и MBG ≤1 отмечалось достоверно реже в группе пациентов, которые перед ЧКВ получали 40 мг аторвастатина. Различия по этим показателям были статистически достоверными по сравнению с контрольной группой и группой традиционного в Китае дозирования аторвастатина (20 мг). Важно также, что частота сердечно-сосудистых событий после процедуры в группе высокодозовой терапии аторвастатином была достоверно меньшей, чем в группах сравнения. По мнению авторов исследования, это можно объяснить улучшением липидного профиля, что эффективно предотвращает тромбоз микроциркуляторного русла после ИМ (W. Liu et al. Experimental and Therapeutic Medicine, 2017; 13: 97-102).
Проведенное в нашем отделе рандомизированное исследование по раннему (сразу при поступлении в стационар) применению высокоинтенсивной гиполипидемической терапии (аторвастатин 80 мг или комбинация 40 мг аторвастатина + 10 мг эзетимиба) по сравнению со среднеинтенсивной терапией (аторвастатин 40 мг или комбинация его с эзетимибом 10 мг) у больных ОКС с элевацией сегмента ST, подвергнутых интервенционному вмешательству, свидетельствует о безопасности такого лечения и преимуществах более высоких доз статинов для улучшения восстановления микроциркуляции после реперфузии (уменьшение синдрома «no-reflow» по данным ангиографического критерия MBG), уменьшения постинфарктной дилатации левого желудочка. Результаты исследования готовились к печати и докладу на Европейском конгрессе кардиологов в г. Барселона в августе 2017 г.
Можно ли представить в обозримом будущем рекомендацию давать первую дозу статина всем пациентам, которые госпитализируются с подозрением на ОКС, по аналогии с ацетилсалициловой кислотой (АСК)? Перед командой персонала отделений интенсивной терапии и инвазивных кардиологов этот вопрос стоит несколько по-иному: можно ли давать первую дозу статина всем пациентам с ОКС, учитывая то, что только части из них показано ЧКВ? И не будет ли вреда от нагрузочной дозы, если реваскуляризация по каким-то причинам откладывается или невозможна? (Как, например, нет вреда от принятой дозы АСК, если инфаркт не подтвердился). Пока соответствующие рекомендации не приняты, результаты двух метаанализов позволяют и тем и другим чувствовать себя уверенно, начиная высокодозовую терапию статинами сразу при поступлении в отделение реанимации и интенсивной терапии.
Пользу предварительной дозы статинов перед ЧКВ подтвердил метаанализ 13 рандомизированных исследований (G. Patti et al. Circulation, 2011; 123 (15): 1622). Правда, его недостатком было исключение больных ОКС с элевацией сегмента ST, так как исследователи считали, что в этом случае недостаточно времени, чтобы нагрузочная доза статина успела абсорбироваться и проявить свои плейотропные эффекты до выполнения ЧКВ. Также исключались пациенты, которые уже принимали статины. Метаанализ показал, что у пациентов с ИМ без элевации ST ургентная статинотерапия снижала частоту наступления комбинированной конечной точки – смерть, ИМ, повторная реваскуляризация – на 41% (отношение шансов, ОШ 0,59; 95% ДИ 0,38-0,92; p=0,02). И в абсолютных цифрах результат впечатляет: 0,9% в группе статинотерапии по сравнению с 5,7% в контрольной. Посчитано, что для предотвращения одного неблагоприятного исхода нагрузочную дозу статина необходимо назначить 16 пациентам.
В более поздний метаанализ 14 РКИ (A.M. Benjo et al. Cath. Cardiovasc. Interv. 2015; 85 (1): 53) были включены данные 3146 пациентов, которые раньше не принимали статины. Нагрузочную дозу аторвастатина (80 мг) или розувастатина (20-40 мг) в этих исследованиях получали пациенты перед выполнением ЧКВ по поводу стабильной стенокардии, ОКС без элевации сегмента ST или по смешанным показаниям. Перипроцедурный ИМ (первичная конечная точка) возник у 7,5% пациентов, рандомизированных к приему нагрузочной дозы статинов, по сравнению с 15,8% случаев в контрольной группе (ОШ 0,44; 95% ДИ 0,35-0,56; p<0,00001). Достоверное уменьшение частоты перипроцедурных ИМ наблюдалось в подгруппах пациентов со стабильной стенокардией (ОШ 0,33; p<0,00001), ОКС без элевации ST (ОШ 0,32; p<0,0001), а также в смешанной популяции (ОШ 0,66; p=0,02). Прием статина перед ЧКВ также ассоциировался с уменьшением частоты комбинированной конечной точки – смерть, спонтанный ИМ или повторная реваскуляризация (ОШ 0,59; 95% ДИ 0,38-0,92; p=0,02), но это наблюдалось только в подгруппе пациентов с ОКС без элевации ST (ОШ 0,18; p=0,0005).
Дополнительный аргумент в пользу назначения первой дозы статина перед ЧКВ – это данные о снижении частоты контраст-индуцированной нефропатии в результате внутривенного введения контрастирующих препаратов для ангиографии. В исследовании PRATO-ACS назначение розувастатина в нагрузочной дозе 40 мг до выполнения коронарографии и ЧКВ с переходом на 20 мг/сут привело к значимому снижению количества случаев острого повреждения почек с 15,1 до 6,7% в последующие 3 дня. Пользу статинов подтвердил и недавний метаанализ (Y.H. Liu et al., 2015).
Статины и антитромбоцитарная терапия
Поскольку статины влияют на функцию тромбоцитов и обладают собственным антиагрегантным эффектом, закономерно встает вопрос об их взаимодействиях с компонентами антитромботической терапии, которая назначается пациентам со стабильной ишемической болезнью сердца (ИБС) и ОКС. Кроме того, известно, что один из самых популярных препаратов – аторвастатин – метаболизируется с участием фермента системы печеночного цитохрома CYP3A4 – того самого, который образует активный метаболит клопидогреля. Таким образом, возможно фармакокинетическое взаимодействие указанных препаратов, в результате чего антитромбоцитарный эффект клопидогреля может снижаться.
Хронические фармакодинамические эффекты аторвастатина и розувастатина у пациентов со стабильной ИБС и нормальной исходной агрегацией тромбоцитов на фоне двойной антитромбоцитарной терапии изучались в исследовании PEARL (F. Pelliccia et al. Eur. J. Pharmacol. 2014; 725: 18-22). В течение месяца прием статинов не повлиял на реактивность тромбоцитов.
В январе этого года опубликованы результаты рандомизированного одноцентрового открытого исследования STATIPLAT (C. Godino et al. Clinical Cardiology, 2017. DOI: 10.1002/clc.22709), в котором изучались «острые» эффекты нагрузочных доз статинов на показатели агрегации тромбоцитов у пациентов со стабильной ИБС, которым предстояло ЧКВ. Включались пациенты, принимавшие двойную антитромбоцитарную терапию – АСК и клопидогрель. Эффекты статинов оценивали в трех группах: аторвастатин 80 мг, розувастатин 40 мг и без назначения статина (контрольная). Исследование не обнаружило существенного вмешательства нагрузочных доз статинов в антитромбоцитарные эффекты хронической терапии АСК и клопидогрелем. С другой стороны, авторы поднимают вопрос о роли антитромбоцитарного эффекта статинов в улучшении исходов после ЧКВ, но пока на него нет ответа.
В исследовании ESTATE высокая доза аторвастатина перед ЧКВ также не повлияла на антиагрегантный эффект нагрузочной дозы клопидогреля, несмотря на фармакокинетическую предпосылку – конкуренцию за CYP3A4 (R.P. Kreutz et al. Clin. Pharmacol. 2016; 8: 45-50).
Таким образом, нагрузочная доза статинов, по-видимому, вполне безопасна в остром периоде ОКС, у статин-наивных пациентов и у тех, кто уже длительно принимал статины на фоне антитромбоцитарной терапии.
Вместо заключения
Несмотря на существующие доказательства пользы, превентивное применение статинов при поступлении пациента с ОКС в стационар еще не стало рутинной практикой. Исполнительный редактор американского интернет-журнала Emergency Physicians Monthly доктор Richard Bukata недавно выразил свое отношение к вопросу назначения статинов при ОКС на страницах издания: «Когда я поступлю в ваше отделение интенсивной терапии с моим ОКС, пожалуйста, дайте мне АСК и высокую дозу статина, как только я войду в эту дверь. В этой ситуации я не вижу никакого вреда, но вижу потенциальную пользу. Я не заинтересован ожидать результатов исследований, которые это окончательно подтвердят».
Подготовил Дмитрий Молчанов
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...




