Конгрес Асоціації урологів України – 2017: у фокусі міждисциплінарність
15-17 червня 2017 року в м. Києві у приміщенні Торгово-промислової палати відбувся конгрес Асоціації урологів України. Захід був організований за підтримки Національної академії медичних наук (НАМН) України, Міністерства охорони здоров’я (МОЗ) України, Державної установи «Інститут урології НАМН України», Асоціації урологів України, Асоціації сексологів та андрологів України, Національної медичної академії післядипломної освіти ім. П.Л. Шупика МОЗ України.
Патологія органів сечовидільної системи у структурі захворюваності населення України посідає не останню позицію. Серед найбільш актуальних проблем – сечокам’яна хвороба (СКХ), інфекції сечовидільної системи, онкологічні захворювання й нетримання сечі.
Кожна з цих проблем заслуговує на окреме обговорення. Перелічені патології здатні призвести до формування хронічної ниркової недостатності, на яку в Україні хворіють понад півмільйона громадян, 5 тис. з яких потребують хронічного гемодіалізу. Ця соціально-економічна й медична проблема з року в рік набуває дедалі більшої актуальності.
Під час роботи конгресу були представлені доповіді, присвячені проблемам застосування сучасних методів діагностики та лікування уролітіазу, інфекцій сечовидільної системи та проведення медикаментозної терапії при порушеннях сечовиділення.
Наукова частина заходу вирізнялася насиченістю, різноплановістю, мультидисциплінарністю і широкоформатністю. Під час симпозіуму фармацевтичної компанії «Астеллас» були розглянуті актуальні питання лікування і профілактики рецидивів інфекції сечовивідних шляхів, гіперактивного сечового міхура (ГАСМ), синдрому нижніх сечових шляхів (СНСШ).
 Професор кафедри хірургії та урології Буковинського державного медичного університету (м. Чернівці), доктор медичних наук В.І. Зайцев присвятив свій виступ актуальним питанням лікування ГАСМ.
Професор кафедри хірургії та урології Буковинського державного медичного університету (м. Чернівці), доктор медичних наук В.І. Зайцев присвятив свій виступ актуальним питанням лікування ГАСМ.
– Проблема гіперактивного сечового міхура – важливе соціальне та медичне питання, яке донедавна офіційна медицина практично не вирішувала, хоча від цього захворювання потерпає чимало українців. Досі цій проблемі приділяли несправедливо малу увагу, що зумовлено як власне медичними причинами (захворювання не призводить до смертельних наслідків і рідко – до інвалідності), так і психологічними проблемами відповідної категорії пацієнтів (відчуття незручності, сорому, відтак – замовчування факту захворювання).
Відсутність адекватної інформації у пресі та медичних джерелах призвело до того, що більшість лікарів, на жаль, досі не здатні адекватно діагностувати й лікувати ГАСМ. Лише в останні 10-15 років ГАСМ почали приділяти достатньо уваги, що можна пояснити значними успіхами медицини в розробленні нових методів лікування захворювання і кращим розумінням особливостей виникнення та перебігу ГАСМ. Завдяки накопиченню значного досвіду практичного використання М-холінолітичних препаратів (у тому числі нових даних багатоцентрових клінічних досліджень) було розширено та уточнено показання до їхнього використання не тільки у жінок (як традиційно вважалося), а й у чоловіків. Важливим кроком стало запровадження нового покоління М-холінолітичних препаратів зі значно покращеним співвідношенням ефективність/толерантність, а також нового класу препаратів, які ефективні при цих розладах – стимуляторів β3-адренорецепторів детрузора.
Зрозуміло, що появу дизурії у чоловіків традиційно пов’язували із захворюваннями передміхурової залози (ПЗ), наприклад, запальними або з новоутвореннями, насамперед доброякісною гіперплазією ПЗ (ДГПЗ). Це привело до появи терміна «симптоми з боку нижніх сечових шляхів» (тобто дизурія, що пов’язана із ДГПЗ), а також до внесення змін до протоколів терапії ДГПЗ. Сьогодні на перший план виходить лікування саме означених симптомів, а не тільки самої ПЗ, як це було раніше. Ще 10-15 років тому лікування дизурії у чоловіків було спрямоване на ліквідацію першопричини (як тоді вважалося). У разі простатиту насамперед призначали антибактеріальну терапію із додаванням великої кількості інших препаратів та фізіотерапії; при ДГПЗ спершу застосовували лише оперативне лікування, яке з 1980-х років поступово замінили різноманітними медикаментозними методиками.
ГАСМ – синдром порушення функції нижніх сечових шляхів, який характеризується наявністю таких скарг:
- імперативні позиви до сечовипускання (ургентність);
- раптовий позив до сечовипускання, який неможливо відкласти (інакше виникне самовільне виділення сечі, так зване неутримання сечі) – вважається основним та обов’язковим у діагностиці ГАСМ і може супроводжуватися іншими скаргами;
- нетримання сечі – будь-яке мимовільне виділення сечі;
- полакіурія (почащене сечовипускання) – сечовипускання протягом дня >8 разів;
- ніктурія (синонім – ноктурія) – сечовипускання >1 раза вночі.
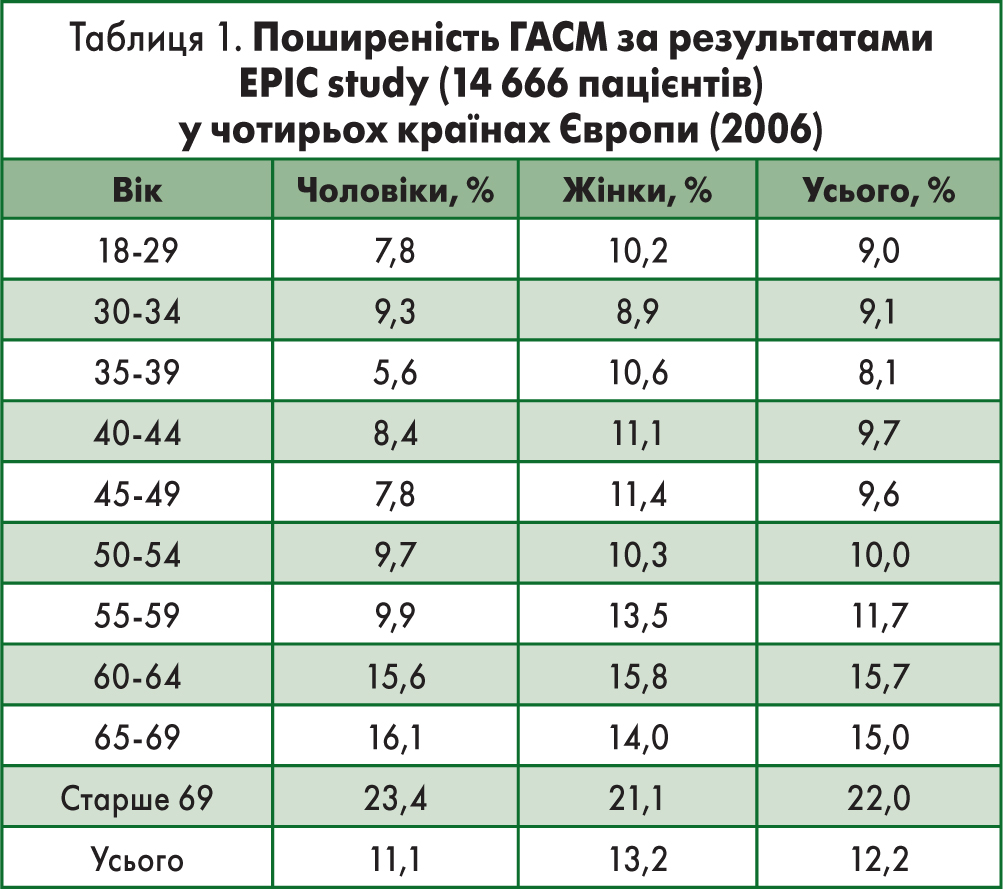 Наскільки важливою є проблема ГАСМ стало зрозуміло тільки після отримання результатів масштабних соціологічних досліджень, проведених упродовж останніх 10-15 років серед різних популяційних груп (табл. 1).
Наскільки важливою є проблема ГАСМ стало зрозуміло тільки після отримання результатів масштабних соціологічних досліджень, проведених упродовж останніх 10-15 років серед різних популяційних груп (табл. 1).
Поширеність ГАСМ у чоловіків має два піки: перший припадає на вік 30-34 років, другий – 50-54 років; і надалі з віком частота розвитку ГАСМ збільшується. У жінок такої закономірності немає, а частота розвитку ГАСМ у них зростає у віці після 60 років.
Було проведено мультиваріантний аналіз впливу дизурії на життя чоловіків (n=13 000). Сім – максимальний бал, при якому дизурія викликає порушення еректильної функції. Вона має навіть більший вплив на еректильну функцію, ніж вік чоловіків. Менше впливають на розвиток ГАСМ паління, цукровий діабет, захворювання серцево-судинної системи.
Слід згадати прояви ГАСМ після проведення трансуретральної резекції ПЗ. Не завжди патологія ПЗ є причиною дизурії. У 20-30% прооперованих пацієнтів, яких обстежили на піку дизурії, упродовж 3,5 року все ще спостерігалися такі симптоми, як ніктурія (68%) та ургентність (52%). Отже, незважаючи на проведення операції, симптоми дизурії залишились.
Одним із перших препаратів, спрямованих саме на лікування порушень функції сечового міхура у чоловіків, був тамсулозину гідрохлорид. В Японії тамсулозин застосовують із 1983 року, в Європі – з 1995 року. В 2006 році з’явилися генерики. В наш час застосовуються й інші α1-адреноблокатори, але цей препарат залишається основним.
Після початку активного використання α1-адреноблокаторів, зокрема тамсулозину, упродовж 1987-1997 років значно збільшилася різноманітність медикаментозних методів лікування та мінімальних інвазивних втручань.
Поява холінолітиків (ХЛ), які позиціонували насамперед як «жіночі» препарати, значно збільшила можливості лікування ургентності й частого сечовипускання. Тож сьогодні антихолінергічні засоби (М-холінолітики) є препаратами вибору лікування ГАСМ згідно з протоколами.
ХЛ властиві такі загальні ознаки:
- їхня ефективність проявляється тільки під час застосування; після закінчення курсу лікування ефект доволі швидко зникає (хоча наш власний досвід довів, що у великої частини пацієнтів (як правило, це молоді жінки) прийом якісних ХЛ протягом щонайменше 3 міс запобігає рецидиву дизурії або ж вона проявляється менш активно і не потребує подальшого лікування);
- лікування має тривати не менш як 3-6 міс.
До загальних побічних ефектів ХЛ (значно менш виражені в сучасних ХЛ) належать:
- найчастіше – сухість у роті;
- рідко – закрепи, нудота, діарея;
- дуже рідко – розпливчастість предметів (пелена перед очима), сонливість, головний біль, серцебиття, сухість шкіри.
Розглянемо питання використання ХЛ у чоловіків, відповівши на такі запитання:
- Чи це використання так само ефективне, як і у жінок?
- Чи не зростає кількість ускладнень при лікуванні ДГПЗ?
- Чи зберігається їхня терапевтична дія при тривалому прийомі (ефект звикання)?
- Чи не прогресують побічні ефекти?
Препаратами для лікування ГАСМ згідно із сучасними рекомендаціями є:
- антимускаринові препарати: толтеродин, троспіум, дарифенацин, оксибутинін;
- адренергічні препарати: мірабегрон.
На сьогодні золотим стандартом ХЛ є соліфенацину сукцинат (Везикар). У ході великої кількості досліджень була продемонстрована його вірогідно більша ефективність і менша частота розвитку побічних ефектів порівняно з оксибутиніном і детрузитолом. Препарат справляє тривалий ефект, денна доза препарату вживається 1 раз на добу. За результатами більш як 10 багатоцентрових досліджень соліфенацину сукцинату була підтверджена ефективність препарату в лікуванні усіх симптомів ГАСМ. Важливі дані були отримані під час великого дослідження STAR, у ході якого порівнювали ефективність соліфенацину сукцинату і найкращий до появи останнього ХЛ толтеродин у пролонгованій формі (в Україні не зареєстрована).
Дослідження проводилося в 17 країнах Європи за участю 1355 пацієнтів протягом 12 тиж, але згодом було продовжене до року. На підставі даних дослідження було встановлено, що за абсолютною більшістю показників соліфенацину сукцинат (Везикар) виявився кращим за толтеродин, ефективним при лікуванні усіх симптомів ГАСМ, а обидва ці препарати за ефективністю зменшення усіх симптомів були вірогідно кращими, ніж плацебо. Також було проведено аналіз розвитку побічних дій для визначення безпечності застосування препарату в чоловіків. Встановлено, що у більшості пацієнтів відзначалася гарна переносимість препаратів, не спостерігалося розвитку толерантності при тривалому використанні, у понад 60% пацієнтів зникло нетримання сечі, 40% учасників з ургентними позивами позбулися їх наприкінці лікування. Було зафіксовано (11%) незначну кількість випадків основної побічної дії ХЛ – сухості у роті.
На підставі проведених досліджень можна зробити висновок, що Везикар має кращий профіль безпеки, а також він більш ефективний стосовно лікування всіх симптомів ГАСМ і більш зручний у застосуванні (приймають 1 раз на день).
Повернемося до питання виникнення частоти ГАСМ у чоловіків. Важливою причиною його виникнення є розвиток хронічних запальних захворювань ПЗ.
Патологія органів сечовидільної системи у структурі звідно до даних Європейської асоціації урологів 2015 року причиною 8; 13; 14% усіх візитів до уролога (Італія, США, Фінляндія відповідно) є хронічний простатит (ХП).
Лікування ХП відповідно до протоколу Європейської асоціації урологів включає насамперед призначення антибіотиків. Групою вибору є фторхінолони (протягом 4-6 тиж), а препаратом вибору залишається ципрофлоксацин. Тетрацикліни рекомендуються у разі підозри на інфікування внутрішньоклітинними мікроорганізмами. Про можливе застосування комбінації антибактеріальних препаратів у документі не згадується. Також тут містяться α-адреноблокатори й фінастерид (при ХП категорії ІІІа). Внутрішньопростатичні ін’єкції не рекомендовані, інші типи препаратів не згадуються. Проте якщо вважати атипові мікроорганізми (АМ) одними з основних збудників ХП, то необхідно призначати лише сучасні фторхінолони (але не ципрофлоксацин), які виявляють щодо них достатню активність. Крім того, важливим напрямом терапії на першому етапі лікування є елімінація трихомонад, які виконують контейнерну функцію для АМ. Водночас антитрихомонадні препарати також не згадуються в означеному протоколі. Швидше за все, це пов’язано з виділенням сексуально-трансмісивних запальних захворювань в окрему групу.
Синдром хронічного тазового болю (СХТБ) – наявність постійних або часто повторюваних епізодів болю в структурах тазу. Для його лікування застосовують:
- α-адреноблокатори, які зменшують симптоматику в 1,7-1,8 раза і покращують якість життя;
- антибіотики: фторхінолони (4-5 тиж), тетрацикліни – у разі підозри на внутрішньоклітинні мікроорганізми;
- нестероїдні протизапальні препарати, опіоїди, фітопрепарати, пентосан полісульфат, міорелаксанти, фізіотерапію, психотерапію тощо.
Численні дослідження показали ефективність застосування адреноблокаторів у інших груп чоловіків (що часто перетинається із ДГПЗ) за наявності ХП або СХТБ. Наразі адреноблокатори нарівні з антибіотиками є основними (і часто єдиними) рекомендованими препаратами для лікування ХП, а також вони показані для терапії СХТБ. Інших препаратів для лікування ГАСМ та дизурії ці рекомендації не містять.
Наш практичний досвід, а також дослідження інших авторів констатують велику частку пацієнтів із простатитом і СХТБ, у яких наявні симптоми накопичення – насамперед часті денні й нічні сечовипускання. У таких пацієнтів нечасто спостерігається ургентність і нетримання сечі, проте негативний вплив дизурії на якість життя, емоційний стан і сексуальну функцію не слід недооцінювати.
Причини застосування ХЛ у лікуванні ХП і СХТБ: зменшують полакіурію, ургентність, нетримання сечі; можливо, зменшують негативний вплив дизурії на сексуальну дисфункцію (потребує подальшого дослідження); можливо, утамовують біль (потребує дослідження). Перспективність використання цих препаратів є безсумнівною.
Під час лікування ГАСМ призначають мірабегрон (Бетміга®) – перший і єдиний представник нового класу – блокаторів β3-адренорецепторів (БАБ). БАБ становлять 97% усіх адренорецепторів у самому детрузорі. Вони активні у фазі наповнення, їх стимуляція приводить до активного розслаблення сечового міхура й збільшення його ємності при постійному низькому тиску в ньому, не чинять типових для ХЛ побічних ефектів.
Бетміга® – реальна та єдина альтернатива ХЛ, випускається у двох дозуваннях – 25 мг (для пацієнтів із нирковою недостатністю) і 50 мг. Можливе тривале застосування – від 12 до 52 тиж. Для обох доз у клінічних дослідженнях отримано вірогідне зменшення полакіурії, ніктурії, нетримання сечі, збільшення об’єму сечового міхура; ефект не зменшується при тривалому використанні; значно покращують якість життя пацієнтів; викликають менше побічних ефектів порівняно з ХЛ (як-от сухість у роті, закрепи, зміни з боку центральної нервової системи).
Основними перевагами препарату є:
- ефективний у пацієнтів, які не отримували ефекту від ХЛ чи погано їх переносили;
- ефективний як у чоловіків, так і у жінок;
- ефективний і безпечний у тому числі в пацієнтів похилого віку;
- кількість розвитку побічних ефектів – на рівні плацебо;
- його можна комбінувати з 1) ХЛ – для лікування ГАСМ; 2) з адреноблокаторами – для лікування чоловіків із ДГПЗ/СНСШ.
На підставі досліджень, проведених у 2017 році, було встановлено, що β-адренорецептори справляють такий вплив:
- розслабляють гладкі м’язи простати;
- розслабляють детрузор;
- покращують еректильну функцію за рахунок релаксації тканин статевого члена;
- розслабляють м’язи уретри та сприяють уретральній релаксацї (полегшенню відходження конкрементів у сечоводах).
Отже, завдяки застосуванню цих препаратів у майбутньому можна буде впливати на стан сечового міхура, м’язів ПЗ при ХП, уретри при ГАМС, сечоводів при уретральних камінцях, корегувати еректильну дисфункцію (викликати розслаблення тканин статевого члена).
Підбиваючи підсумки, можна зробити такі висновки стосовно лікування ГАСМ/СНСШ у чоловіків:
- ХЛ/БАБ + α1-адреноблокатори при ДГПЗ/СНСШ – доведений ефект за відсутності ускладнень;
- ХЛ/БАБ (+ α1-адреноблокатори) при дизурії після трансуретральної резекції ПЗ (ТУРПЗ);
- ХЛ/БАБ + α1-адреноблокатори при ХП, СХТБ тощо – можливий ефект для зменшення дизурії, болю та еректильної дисфункції.
До 1980-х років успішно використовували аденомектомію, з 1990-х – ТУРПЗ. У XXI столітті використовують α1-адреноблокатори, останні 10 років застосовуємо ХЛ. Поява БАБ забезпечила більше можливостей для лікування пацієнтів із ГАСМ/СНСШ.
 Завідувач кафедри нефрології Національної медичної академії післядипломної освіти ім. П.Л. Шупика МОЗ України професор Д.Д. Іванов представив доповідь на тему «Інфекція сечовивідних шляхів: лікування і профілактика рецидивів».
Завідувач кафедри нефрології Національної медичної академії післядипломної освіти ім. П.Л. Шупика МОЗ України професор Д.Д. Іванов представив доповідь на тему «Інфекція сечовивідних шляхів: лікування і профілактика рецидивів».
– Інфекції сечової системи – мікробно-запальне ураження органів сечових шляхів без уточнення топічного рівня ураження. Відсутність вітчизняних протоколів лікування інфекцій сечовивідних шляхів додає певних проблем лікарям-практикам, оскільки не враховує місцевих особливостей та резистентності мікрофлори. У зв’язку з цим орієнтир на європейські рекомендації не завжди доцільний, потрібно якнайшвидше розробляти власні протоколи лікування. Аналізуючи терапію пацієнтів відповідно до європейських протоколів та методики лікування в Україні, бачимо переваги нашої практики лікування інфекції сечових шляхів (ІСШ). У 2017 році Європейська асоціація урологів змінила погляди на ведення безсистемної бактеріурії, яку запропоновано не лікувати, а також на призначення антибіотиків за будь-якої ІСШ. Натомість в Україні широко застосовують уроантисептики, комбіновану терапію фітопрепаратами, практику щеплення.
Безсимптомна бактеріурія (ББ) відповідно до клінічних досліджень здатна захищати від суперінфекції симптоматичної ІСШ, тому лікування ББ слід проводити тільки у разі доведеної користі для пацієнта, аби уникнути ризику резистентності до антимікробних препаратів.
Терапію не призначають у таких випадках:
- невагітним жінкам;
- людям, які страждають на діабет;
- пацієнтам будинків престарілих;
- у разі ІСШ, при яких застосовують катетери.
Терапію призначають:
- перед урологічними процедурами;
- вагітним жінкам (?).
Призначення ББ вагітним жінкам не впливає на ризик передчасних пологів, але позначається на якості їхнього життя. У 2016 році було зроблено акцент на необхідності часто повторювати бактеріальний посів сечі.
 Цистит – неспецифічне мікробне запалення слизової оболонки сечового міхура. Терапію уретрального синдрому/циститу проводять фосфоміцином у дозі 3,0 г на день. Доведена його ефективність порівняно з іншими препаратами, проти E. coli – 77%, клінічно – 70%.
Цистит – неспецифічне мікробне запалення слизової оболонки сечового міхура. Терапію уретрального синдрому/циститу проводять фосфоміцином у дозі 3,0 г на день. Доведена його ефективність порівняно з іншими препаратами, проти E. coli – 77%, клінічно – 70%.
Для лікування циститу використовують і комбінацію фурагіну з магнію гідроксикарбонатом у дозі 100 мг 3 рази на добу, триметоприм/сульфаметоксазол, цефіксим у дозі 20-30 мг/кг або 6 днів ніфуратель 200 мг 3 рази на добу. Профілактичне лікування: комбінація фурагіну з магнію гідроксикарбонатом, триметоприм/сульфаметоксазол у дозі 1 мг/кг, цефіксим у дозі 2 мг/кг, цефуроксим у дозі 5 мг/кг на ніч або засоби на основі лікарських рослин.
При першому епізоді циститу краще спочатку призначити уроантисептик, аніж застосовують антибіотик. Якщо відбувся другий епізод, цефалоспорини III покоління (цефіксим) + профілактична доза (й одночасно діагностика статевих інфекцій, за їх наявності – фторхінолон), посткоїтально – цефалоспорини III покоління. Чоловікам призначають фторхінолони або цефалоспорини, нітрофурани не використовують, оскільки помічена їх низька здатність до накопичення в сечовому міхурі.
Профілактичне лікування проводять у випадку трьох епізодів циститу на рік або двох епізодів за 6 міс (європейські рекомендації щодо цього питання не змінюються з 2008 року). Ми широко використовуємо вакцинацію. Її проводять аутовакцинами і такими офіцинальними вакцинами, як Уро-Ваксом®. Після її здійснення спостерігаємо на 50% зменшення рецидування інфекцій верхніх та нижніх сечових шляхів. Ми використовуємо таку схему вакцинації: 3 міс 1 раз на день уранці натщесерце і ще 3 міс по 10 днів. При досягненні позитивного результату, зменшенні рецидування або його припиненні рекомендуємо пацієнтам щорічно восени і навесні проводити по 30 днів додаткову ревакцинацію при підтримці імунітету. Таку схему застосовують тому, що сформувати імунітет до кишкової мікрофлори непросто.
Клінічна ефективність Уро-Ваксом®:
- зменшує кількість рецидивів ІСШ порівняно з плацебо;
- зменшує частоту бактеріурії, дизурії і лейкоцитурії;
- зменшує необхідність застосування антибіотиків;
- забезпечує надійний захист від рецидивів ІСШ від 3 до 12 міс;
- добре переноситься пацієнтами.
Пієлонефрит – неспецифічне мікробне запалення нирки з переважним осередковим ушкодженням тубулоінтерстиційної тканини, чашечок і миски.
 Відомі три напрями в лікуванні пієлонефриту: дезінтоксикація, протизапальна терапія (парацетамол і німесулід), антибіотикотерапія. Для дезінтоксикації та цитопротекції використовуємо реосорбілакт внутрішньовенно (6-8 мл/кг 3-4 дні) або ксиліт. У пацієнтів із цукровим діабетом з метою дезінтоксикації призначаємо ксиліт, а не реосорбілакт. Із протизапальною метою – парацетамол 3-4 дні в комбінації з німесулідом.
Відомі три напрями в лікуванні пієлонефриту: дезінтоксикація, протизапальна терапія (парацетамол і німесулід), антибіотикотерапія. Для дезінтоксикації та цитопротекції використовуємо реосорбілакт внутрішньовенно (6-8 мл/кг 3-4 дні) або ксиліт. У пацієнтів із цукровим діабетом з метою дезінтоксикації призначаємо ксиліт, а не реосорбілакт. Із протизапальною метою – парацетамол 3-4 дні в комбінації з німесулідом.
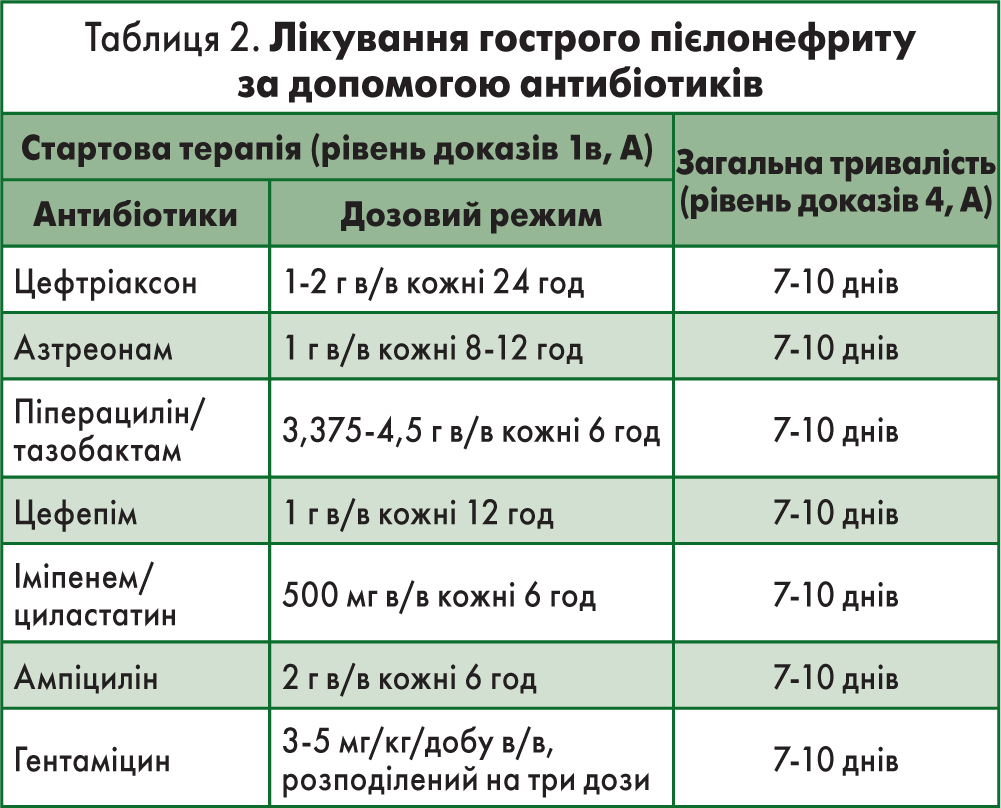
Антибіотикотерапія – ступінчаста, протягом 10 діб (табл. 2). Пацієнти похилого віку мають отримувати дозу, підібрану відповідно до тяжкості інфекції та кліренсу креатиніну. Інфузійно при лікуванні пієлонефриту можна застосовувати таку схему: левофлоксацин у дозі 750 мг 7 діб, реосорбілакт у дозі 200,0 мл 2 рази на добу – 3 доби, парацетамол у дозі 1 г 2 рази на добу – 3 доби. При неускладненому перебігу захворювання виліковування становить 90%.
Профілактична терапія пієлонефриту триває від 3 до 12 міс і включає: уроантисептики в профілактичній дозі – ніфуратель 200 мг або комбінація фурагіну з магнію гідроксикарбонатом 50-100 мг на ніч, триметоприм/сульфаметоксазол у дозі 120-480 мг на ніч, препарати на рослинній основі. З метою післякоїтальної профілактики застосовують Супракс (цефіксим), якщо статеві акти трапляються не більш ніж 4 рази на місяць; при більшій частоті рекомендовано проводити щоденну профілактику. Уро-Ваксом® призначають не лише для пацієнтів із рецидивами, а й для жінок у пременопаузі й менопаузі. Уро-Ваксом® застосовують 3 міс щоранку, а далі – 3 міс по 10 діб. Таке профілактичне лікування показане за наявності більш як двох рецидивів протягом року або у разі ускладненого перебігу пієлонефриту. Тривалість лікування становить 3-12 міс. Також можна проводити вакцинацію, аутовакцинацію, використовувати фаги.
 Завідувач кафедри загальної, дитячої та онкологічної урології Харківської медичної академії післядипломної освіти, кандидат медичних наук І.М. Антонян представив доповідь «Симптом нижніх сечових шляхів на тлі ДГПЗ: як лікувати хворого?».
Завідувач кафедри загальної, дитячої та онкологічної урології Харківської медичної академії післядипломної освіти, кандидат медичних наук І.М. Антонян представив доповідь «Симптом нижніх сечових шляхів на тлі ДГПЗ: як лікувати хворого?».
– ДГПЗ – найбільш часте захворювання у чоловіків похилого і старечого віку. У статистичних звітах це захворювання посідає перше місце, випереджаючи СКХ і запальні процеси сечовивідної системи.
За статистикою Всесвітньої організації охорони здоров’я, чоловіки >50 років, що страждають на ДГПЗ, становлять близько 40-50%; >70 років – близько 75%; >80 років – близько 90%.
Наявність СНСШ зумовлена статичним і динамічним компонентом обструкції вихідного отвору сечового міхура. Збільшення ПЗ є статичним компонентом обструкції. Симпатична нервова система у відповідь на збільшення ПЗ викликає гіпертонус сечових шляхів, що є динамічним компонентом обструкції. Унаслідок обструкції вихідного отвору сечового міхура збільшується індекс інтравезикальної обструкції, що, у свою чергу, призводить до розвитку СНСШ.
EpiLUTS провели дослідження (n=14 139 чоловіків), за підсумками якого були встановлені причини розвитку СНСШ. Серед них, зокрема, ДГПЗ, неврологічні розлади (у тому числі депресія, безсоння), рак ПЗ, артрити, діабет, астма, синдром подразненого кишечника, ІСШ, хронічна слабкість, порушення роботи серцево-судинної системи (у тому числі артеріальна гіпертензія). Серед чоловіків >40 років зафіксовано 71% випадків розвитку СНСШ. У 49% чоловіків були наявні симптоми як випорожнення, так і симптоми накопичення.
Спостереження, що проводилися протягом 11 років стосовно ГАСМ, виявили, що загальна частота гіперактивності зростає з віком – із 15,6 до 44,4%.
Європейська асоціація урологів у 2014 році розробила алгоритм обстеження чоловіків >40 років із СНСШ, який містить такі етапи:
1. Опитування з QoL (за шкалою IPSS).
2. Анамнез і фізикальне обстеження (нейрогенний сечовий міхур, СНСШ, викликаний прийомом препаратів, серцево-судинні захворювання з нічною поліурією, захворювання статевого члена, рак ПЗ, що підлягає пальпації).
3. Загальний аналіз сечі (інфекції сечових шляхів, гематурія, цукровий діабет).
4. Біохімічний аналіз крові з визначенням Na+, креатиніну, простатичного специфічного антигену (погіршення функції нирок, простатит).
5. Ультразвукове дослідження (сечовий міхур, ПЗ, нирки) – ДГПЗ, пухлини ПЗ та сечового міхура, затримка сечі, камінь сечового міхура, дивертикул сечового міхура, камінь сечоводу, гідронефроз.
6. Урофлоуметрія (стриктура уретри, порушення випорожнення).
7. Ведення пацієнтом щоденника сечовипускання (нічна поліурія, полідипсія – поліурія, нецукровий діабет).
8. Доброякісне утворення.
Розглянемо принципи сучасного лікування ДГПЗ. Підтримувальна тактика ведення пацієнтів передбачає: динамічне спостереження, поведінкову терапію, навчання, заспокоєння, поради стосовно способу життя, періодичне спостереження.
Медикаментозне лікування включає: α1-блокатори, інгібітори 5α-редуктази, антимускаринові препарати, фітотерапію, аналог вазопресину, комбіновану медикаментозну терапію.
Хірургічне лікування охоплює: трансуретральну резекцію ПЗ, відкриту аденомектомію, трансуретральну мікрохвильову терапію, інші методики хірургічного лікування.
У країнах Європи застосовують такі види терапії ДГПЗ: у Франції – динамічне спостереження (43,8%), медикаментозну терапію (53,8%), хірургічне лікування (2,4%); у Німеччині – динамічне спостереження (21,7%), медикаментозну терапію (52,7%), хірургічне лікування (5,6%); у Великій Британії – динамічне спостереження (54,6%), медикаментозну терапію (46,9%), хірургічне лікування (2,5%); в Італії – динамічне спостереження (11,1%), медикаментозну терапію (87,3%), хірургічне лікування (1,6%); в Іспанії – динамічне спостереження (8,9%), медикаментозну терапію (88,1%), хірургічне лікування (3%); у Польщі – динамічне спостереження (31,2%), медикаментозну терапію (66,4%), хірургічне лікування (2,4%).
Найбільший страх пацієнтів – це страх невчасного виявлення раку ПЗ. Упродовж перших 5 років динамічного спостереження за 107 пацієнтами з інтравезикальною обструкцією прооперовано 10 осіб (9,3%), а наступних 10 років – не більш як 17%. При повторних уродинамічних дослідженнях у пацієнтів цієї групи були виявлені незначні зміни. Встановлення швидкості потоку сечі дає змогу розпізнати пацієнтів із небезпекою прогресування захворювання, при якому показане хірургічне втручання.
Історія медикаментозної терапії в лікуванні ДГПЗ веде свій початок з 1976 року, коли були проведені перші клінічні дослідження адреноблокаторів, а згодом, у 1987 році, – перше дослідження селективних адреноблокаторів. Холіноблокатори з’явилися пізніше, а в останні роки використовують комбінації препаратів адреноблокаторів і ХЛ.
Групи препаратів, які містять рекомендації Європейської асоціації урологів (2014), включають: очікувальну тактику, зміну способу життя; α1-адреноблокатори, інгібітори 5α-редуктази, ХЛ, α1-адреноблокатори з інгібіторами 5α-редуктази, α1-адреноблокатори з ХЛ, інгібітори фосфодіестерази‑5 (з тамсулозином або без нього), аналоги вазопресину – десмопресину.
При опитуванні пацієнтів були встановлені симптоми наповнення, які найбільше непокоять при СНСШ: скупчення сечі – 51,3% (нокурія, ургентні позиви до сечовипускання, збільшення частоти сечовипускань, нетримання сечі), випорожнення – 25,7% (утруднений початок сечовипускання, сповільнення потоку сечі, необхідність натужуватися під час сечовипускання, підкапування сечі наприкінці акту сечовипускання), після сечовипускання – 16,9% (відчуття неповного випорожнення сечового міхура, підкапування сечі наприкінці акту сечовипускання). Наразі відомо, що лише 10% чоловіків із ГАСМ (симптоми наповнення) отримують лікування.
Інформація для роздумів:
- 75% пацієнтів із ДГПЗ мають симптоми ГАСМ або уродинамічно підтверджену гіперактивність
- детрузора;
- 65% пацієнтів відмічали неадекватний контроль своїх симптомів після лікування α1-адреноблокаторами протягом 3 міс, зниження показника за шкалою IPSS <3 пунктів (Lee et al. 2004);
- 30% пацієнтів незадоволені результатами трансуретральної резекції через персистування симптомів ГАСМ (S.H. Alloussi et al. 2010);
- 48% чоловіків, у яких до операції симптомів ГАСМ не було, після операції починають їх відчувати;
- симптоми накопичення потребують набагато більше уваги, ніж симптоми сечовипускання (Irwin et al. 2006).
 Призначення комбінованої терапії медикаментозного лікування дає можливість усунути симптоми випорожнення і наповнення. Так, використання α1-адреноблокаторів (тамсулозин ОКАС – Омнік Окас) сприятиме розслабленню гладкої мускулатури ПЗ, простатичної уретри і шийки сечового міхура, а в комбінації із М-холіноблокаторами (соліфенацин – Везикар), які знижують скоротливість стінки сечового міхура, будуть усунуті симптоми випорожнення і наповнення.
Призначення комбінованої терапії медикаментозного лікування дає можливість усунути симптоми випорожнення і наповнення. Так, використання α1-адреноблокаторів (тамсулозин ОКАС – Омнік Окас) сприятиме розслабленню гладкої мускулатури ПЗ, простатичної уретри і шийки сечового міхура, а в комбінації із М-холіноблокаторами (соліфенацин – Везикар), які знижують скоротливість стінки сечового міхура, будуть усунуті симптоми випорожнення і наповнення.
Для зручного застосування пацієнтами цих препаратів був створений Везомні, який представлений у формі двошарової таблетки, до складу якої входить 6 мг соліфенацину сукцинату, що відповідає 4,5 мг соліфенацину й 0,4 мг тамсулозину гідрохлориду, що відповідає 0,37 мг тамсулозину.
Застосування комбінації соліфенацину і тамсулозину вивчали у дослідженні NEPTUNE. Науковці, які провели понад тисячу досліджень, ставили перед собою первинні та вторинні цілі.
Первинні цілі:
- оцінити ефективність комбінації соліфенацину в дозі 6 або 9 мг і тамсулозину ОКАС у дозі 0,4 мг порівняно з монотерапією тамсулозином ОКАС у дозі 0,4 мг у чоловіків віком 45 років і старше із СНСШ/ДГПЗ, пов’язаними з накопиченням сечі та випорожненням.
Вторинні цілі:
- оцінити безпеку і переносимість комбінації соліфенацину в дозі 6 або 9 мг і тамсулозину ОКАС у дозі 0,4 мг;
- оцінити ефективність комбінації соліфенацину в дозі 6 або 9 мг і тамсулозину ОКАС у дозі 0,4 мг порівняно з плацебо.
Мішенями для фіксованої комбінації Везомні є:
1) соліфенацин у дозі 6 мг переважно впливає на симптоми з боку сечового міхура, зокрема імперативні позиви на сечовипускання, часте сечовипускання, що вдалося визначити завдяки шкалі TUFS; 2) тамсулозин ОКАС у дозі 0,4 мг здебільшого впливає на симптоми з боку ПЗ, включаючи утруднений початок сечовипускання, слабкий струмінь сечі й крапельне виділення сечі наприкінці сечовипускання, що було визначено завдяки шкалі IPSS. Препарат Везомні й тамсулозин ОКАС значно зменшують кількість балів за шкалою IPSS порівняно з плацебо.
Чоловіки, які приймають ХЛ з приводу терапії урогенітальних захворювань, мають ретельно обстежуватися в перші 30 днів лікування стосовно затримки сечі. У перші 30 днів (раннє лікування) використання ХЛ асоціювалося із відносним ризиком затримки сечі 8,3 (95% довірчий інтервал, ДІ 4,8-14,2), а при тривалому використанні (понад 30 днів) відносний ризик становить 2,0 (95% ДІ 1,2-3,1). Ризик гострої затримки сечі був таким, як і при призначенні низьких/середніх або високих доз ХЛ (2,8 vs 3,0).
Протипоказаннями до застосування препаратів є глаукома, гіпотензія, необхідність гемодіалізу. Комбіновану терапію не рекомендовано призначати, якщо об’єм залишкової сечі >200 мл, клінічно виражена інфравезикальна обструкція (Qmax<5 мл/с).
Можна зробити висновок, що застосування комбінованої терапії для пацієнта є доволі вартісним, проте з погляду позитивного результату ефективність лікування зростає від 30 до 80%.
Отже, минулий конгрес, з оглядом основних подій якого ми ознайомили читачів у попередньому номері газети, мав міждисциплінарні риси. Під час симпозіуму компанії «Астеллас» було висвітлено відразу декілька важливих проблем сучасної урології, розглядалися сучасні тенденції в лікуванні та результати важливих клінічних досліджень. Фаховий склад спікерів і зацікавленість аудиторії укотре підтвердили, що формат проведення симпозіуму є зручним і сучасним, а його наукове наповнення – важливим для фахівців сучасної урологічної практики.
Підготувала Оксана Шимків
Тематичний номер «Урологія. Нефрологія. Андрологія» № 3-4 (10-11), листопад 2017 р.
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
Кальцій є одним із найважливіших елементів в організмі людини, оскільки підтримує належний стан кісток і зубів, зменшує ризик остеопорозу, а також знижує імовірність розвитку серцево-судинних хвороб і ожиріння (Institute of Medicine, 2011; Zhang F. et al., 2019; Teegarden D., 2003). Значна кількість людей потребує кальцієвих добавок, але водночас боїться каменеутворення. Сечокам’яна хвороба (СКХ) – поширене в наш час захворювання; більшість каменів становлять кальцій-оксалатні (Wei L. et al., 2022)....
Рак передміхурової залози (РПЗ) – злоякісне новоутворення, що розвивається з епітелію передміхурової залози. РПЗ вважається одним із найпоширеніших видів раку у чоловіків та однією з головних причин смерті у чоловіків похилого віку в Україні і світі. Лікарі загальної практики – сімейної медицини, лікарі інших спеціальностей мають бути обізнані щодо основних факторів ризику та початкових клінічних проявів РПЗ з метою їх раннього виявлення та направлення пацієнта до закладу охорони здоров’я (ЗОЗ), що надає спеціалізовану медичну допомогу, а також сприяти виконанню усіх рекомендацій фахівців онкологічного профілю під час протипухлинного лікування та організації належної паліативної допомоги пацієнтам, які виявляють бажання перебувати вдома на термінальних стадіях захворювання. ...
У статті представлено коментарі до дослідження TRAVERSE* , яке оцінювало ризик виникнення довгострокових серцево-судинних подій у чоловіків із гіпогонадизмом, що застосовують тестостерон-замісну терапію....
Переважна більшість хворих урологічного профілю страждають від больового синдрому. Гострий біль, який може виникнути внаслідок перенесеного хірургічного втручання на передміхуровій залозі або сечовому міхурі, при гострих запальних захворюваннях сечовивідних шляхів або при нирковій кольці (НК), вимагає невідкладної аналгезії з використанням ефективного та безпечного препарату, який не викликає серйозних побічних явищ. Хронічний біль, який є основним симптомом хронічного простатиту (ХП) та синдрому хронічного тазового болю (СХТБ) у чоловіків, суттєво впливає на якість життя, сексуальну сферу та психоемоційний стан пацієнтів, що також потребує проведення раціональної знеболювальної терапії. Нестероїдні протизапальні препарати (НПЗП), зокрема диклофенак натрію, довели свою ефективність за рахунок вираженої знеболювальної й протизапальної дії при оперативних втручаннях в урології, у хворих урологічного профілю з хронічною патологією (ХП/СХТБ) або невідкладними станами. ...




