Антибиотикотерапия острых инфекций мочевыводящих путей: есть ли альтернатива фторхинолонам и цефалоспоринам?
Инфекции мочевыводящих путей (ИМП) являются второй по частоте после инфекций респираторного тракта причиной назначения антибактериальных препаратов (АБП) в амбулаторной практике. Ограниченный выбор новых АБП, снижение их активности и рост резистентности микрофлоры затрудняют выбор схемы терапии, особенно если речь идет о рецидивирующих инфекциях. Женщины, у которых острый цистит (ОЦ) встречается значительно чаще, порой получают по нескольку курсов антибиотиков (АБ) ежегодно, что неизбежно ведет к селекции резистентных штаммов и способствует развитию побочных эффектов. Есть ли выход? Каковы реальные возможности современных препаратов нитрофуранового ряда и сульфаметоксазола в комбинации с триметопримом?
Неосложненная и осложненная ИМП у женщин – один из наиболее распространенных поводов обращения к специалистам разного профиля. Дизурические симптомы инфекций нижних мочевых путей (ИНМП) значимо ухудшают качество жизни пациенток, снижают трудоспособность, дестабилизируют эмоциональный фон. Сегодня ОЦ определяется как инфекционно-воспалительный процесс, местом локализации которого чаще всего является слизистая мочевого пузыря. Анатомические особенности мочеиспускательного канала у женщин – его относительно малая длина и близкое расположение к анальному отверстию – фактор, способствующий более частому развитию цистита. У пациенток репродуктивного возраста предрасполагающими факторами являются также половой акт, использование спермицидов, смена полового партнера, ИМП в анамнезе у матери, ИМП в детском возрасте. В постменопаузе к факторам риска относятся: недержание мочи, атрофический вульвовагинит, цистоцеле (В. Foxman, 2005; T.N. Hooton, 2010). К 25 годам 30% женщин имеют в анамнезе хотя бы 1 эпизод ОЦ; его распространенность сегодня выражается в соотношении 700 случаев на 1 тыс. женщин репродуктивного возраста (V.V. Rafalsky, 2010).
При неосложненных ИНМП 70-95% возбудителей составляют штаммы кишечной палочки (G. Кahlmeter, 2003). Другие виды микроорганизмов – Staphylococcus epidermidis, Staphylococcus saprophyticus, Enterococcus faecalis, Klebsiella, Enterobacter, Enterococci встречаются реже: от 2 до 20% (А.Г. Панин и соавт., 2006). По данным литературы, лечение ОЦ успешно далеко не у всех больных, а рецидивирующее течение имеет место у 30-50% женщин. При этом повторение заболевания отмечено у трети пациенток в течение 6 мес после первичного эпизода (В.В. Рафальский, Л.С. Страпунский, 2004). Применение курсов антибактериальной терапии часто приводит к нарушению качественного и количественного состава микрофлоры организма, возникновению аллергических реакций, появлению резистентности у возбудителей, изменению этиологического фактора, развитию локального и системного иммунодефицита (А.С. Переверзев и соавт., 2002), что необходимо учитывать, назначая повторные курсы антимикробного лечения.
Каковы же критерии выбора АБП для терапии ОЦ? Это:
- спектр чувствительности уропатогенов;
- эффективность препарата согласно данным клинических исследований;
- переносимость антимикробного препарата;
- минимальный риск развития «сопутствующего ущерба» (нарушения микрофлоры желудочно-кишечного тракта, влагалища, развитие кандидозной инфекции и т.д.);
- доступность препарата;
- стоимость препарата (К.Л. Локшин, 2015).
Согласно рекомендациям Европейской ассоциации урологов (EAU) препаратом выбора в терапии неосложненных ИНМП является фосфомицин. АБП широкого спектра действия (фторхинолоны – офлоксацин, левофлоксацин, а также цефалоспорины – цефтибутен и цефиксим) рассматриваются как альтернативные препараты, применение которых целесообразно при неэффективности средств первой линии терапии. Это обусловлено, с одной стороны, возможностью развития дисбиоза влагалища и кишечника на фоне приема фторхинолонов и цефалоспоринов, с другой стороны, селекцией резистентности микрофлоры к АБ. Так, согласно исследованию «Дармис» (И.С. Палагин и соавт., 2012) не менее 10% штаммов E. сoli обнаруживают устойчивость к фторхинолонам. Именно ухудшающаяся ситуация с антибиотикорезистентностью, а также возможность развития нежелательных явлений на фоне приема повторных курсов АБ заставляют врачей с осторожностью использовать в широкой клинической практике современные фторхинолоны и цефалоспорины.
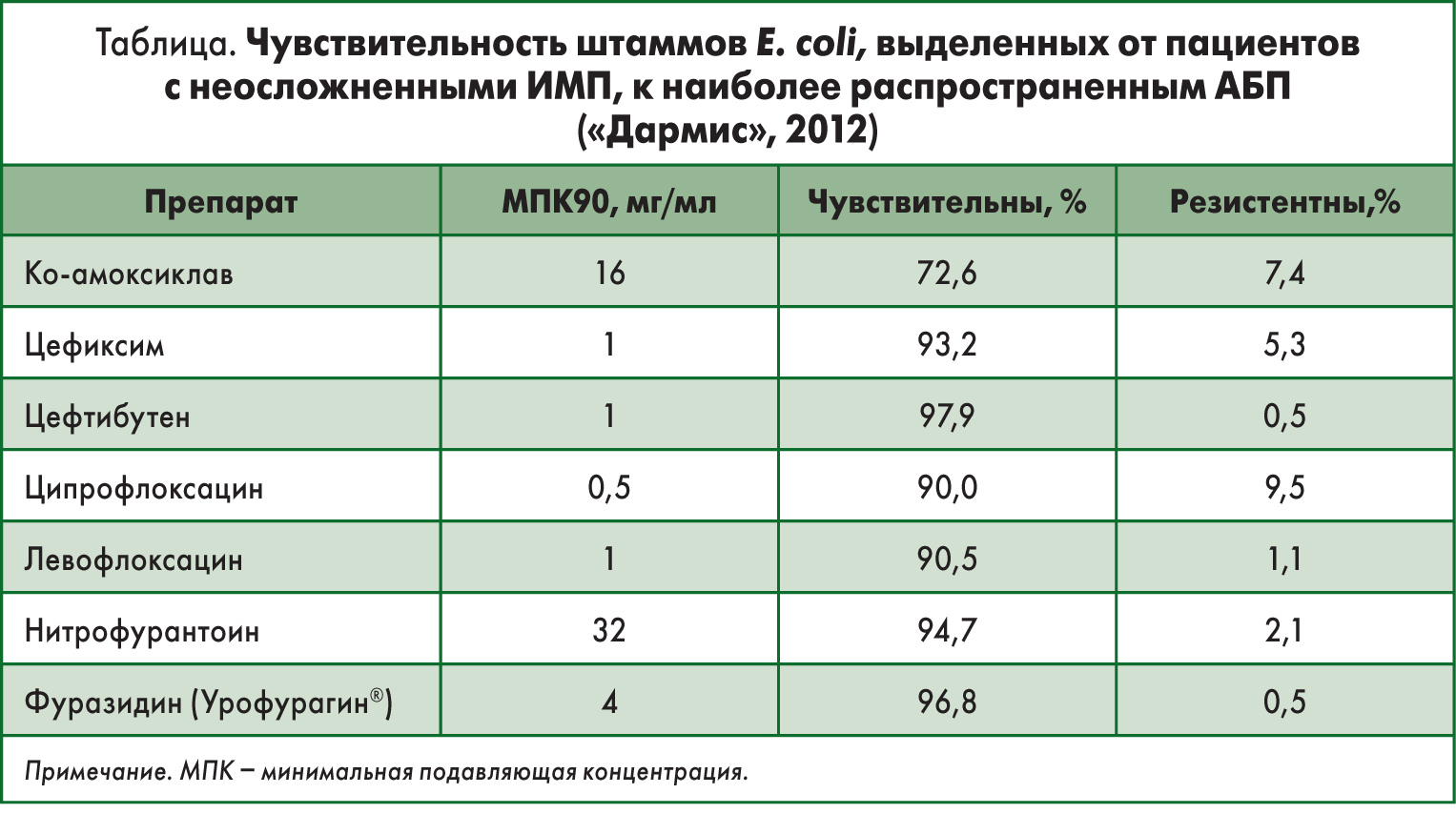
Еще одним ограничивающим фактором применения указанных групп АБ является их «резервность». Учитывая высокую проникающую способность фторхинолонов и цефалоспоринов, целесообразно резервирование этих препаратов для эпизодов более серьезных инфекций – пиелонефритов, осложненных ИМП и т.д. (А.О. Данилов, 2017). Вместе с тем использование в терапии ОЦ фосфомицина трометамола, нитрофурантоина и фуразидина обусловлено высокой чувствительностью уропатогенов к указанным препаратам. Как показали результаты упомянутого выше многоцентрового исследования «Дармис», чувствительность основного возбудителя ИНМП E. coli к фуразидину составила 96,8%, Staphylococcus spp. – 100%. Сопоставимые показатели чувствительности зафиксированы к фосфомицина трометамолу и нитрофурантоину. При этом указанные препараты лишены нежелательных побочных эффектов, таких как влияние на микрофлору организма (отсутствует риск развития дисбиоза влагалища и кишечника) (А.О. Данилов, 2017). Чувствительность штаммов E. coli к различным антимикробным препаратам (по данным исследования «Дармис») представлена в таблице.
В настоящее время на фармацевтическом рынке ЕС имеется макрокристаллический нитрофурантоин (макродантин), который в Украине отсутствует. В нашей стране используется только обычный нитрофурантоин (фурадонин), обладающий малой биодоступностью и высокой частотой развития нежелательных побочных реакций, что значительно сужает область его применения (Л.А. Страчунский, В.В. Рафальский, 2009). Существенным недостатком фосфомицина, по мнению многих специалистов, является невозможность курсового приема (препарат применяется однократно в дозе 3 г), что может способствовать рецидиву ИМП.
Сегодня отечественный фармацевтический рынок предлагает новый препарат фуразидина Урофурагин®, который производится в Польше в полном соответствии с GMP-стандартами. Урофурагин® высокоэффективен в отношении основных патогенов ИНМП, обладает высокой биодоступностью и адекватной стоимостью, что в значительной мере повышает комплайенс пациентов. Кроме того, при необходимости можно продлить курс терапии Урофурагином. Примечательно, что у этого достаточно нового препарата уже имеется собственная доказательная база.
Так, в работе А.О. Данилова (2017) была изучена эффективность препарата Урофурагин® (фуразидин) в лечении острой неосложненной ИНМП (ОЦ). Исследование проводилось на базе урологического отделения ООО «СМ-Клиника» (г. Москва). Были задействованы 52 пациентки в возрасте от 18 до 62 лет с установленным диагнозом ОЦ (средний возраст участниц – 31,5 года). Время начиная с появления первых симптомов заболевания до обращения за медицинской помощью составило 12 ч – 3 суток. Диагноз устанавливался на основании наличия клинических симптомов заболевания (учащенное болезненное мочеиспускание, боль над лоном, примесь крови в моче), а также результатов лабораторных исследований: общего анализа мочи, бактериологического посева мочи на микрофлору и чувствительность к АБ. Лейкоцитурия присутствовала в 100% случаев. E. сoli была высеяна у 46 пациенток (88,5%). Другие возбудители – Enterococcus faecalis, Klebsiella, St. saprophyticus встречались значительно реже – у 2 (3,8%) пациенток, у 1 (1,9%) больной и 3 (5,7%) больных соответственно.
Все пациентки прошли УЗИ мочевого пузыря и были проконсультированы врачом-гинекологом. Критериями исключения из исследования являлись: повышение температуры тела >37,5 °C (ситуация расценивалась как острый пиелонефрит), выявление сопутствующей гинекологической патологии – вульвовагинита, сальпингоофорита и т.д., самостоятельный прием пациентками каких-либо АБП или иммуномодуляторов на момент обращения. В соответствии с наличием либо отсутствием макрогематурии больные были рандомизированы на 2 группы: в 1-ю группу (n=9) вошли пациентки с острым геморрагическим циститом, во 2-ю (n=44) – с ОЦ без макрогематурии. Пациенткам 1-й группы был назначен Урофурагин® в дозе 100 мг 3 р/ сут в течение 7 дней, пациенткам 2-й – в течение 5 дней. Участницы обеих групп получали симптоматическую терапию: свечи с нестероидными противовоспалительными препаратами (индометацин, диклофенак) 2 р/ сут в продолжение 2-3 дней. Эффективность применения Урофурагина оценивалась на основании регресса клинических проявлений заболевания, а также показателей контрольного анализа мочи.
Оценка результатов проводимого лечения в 1-й группе пациенток в динамике показала: на 2-е сут отмечались уменьшение дизурии, исчезновение макрогематурии, на 3-4-е – полное исчезновение симптомов. Контрольный анализ мочи, взятой на 8-й день, зафиксировал нормализацию лабораторных показателей. В контрольном посеве мочи роста микрофлоры обнаружено не было. Назначенная терапия хорошо переносилась больными. Побочные эффекты на фоне приема препарата в данной группе отсутствовали. Оценка результатов терапии во 2-й группе в динамике показала: на 2-е сут у 39 (88%) пациенток отмечалось купирование дизурии, у 5 (11%) почти 3 сут терапии сохранялась резь в конце мочеиспускания. У 4 (9%) участниц были отмечены нежелательные побочные эффекты, связанные с приемом препарата: тошнота, снижение аппетита. Степень их выраженности была незначительной и отмены препарата не потребовала.
После окончания лечения у всех пациенток фиксировалась положительная динамика лабораторных показателей. Так, у 43 (97%) участниц показатели общего анализа мочи не имели отклонений от нормы, у 1 (2%) больной сохранялась небольшая лейкоцитурия, несмотря на положительную динамику лабораторных показателей. В контрольном посеве мочи роста микрофлоры выявлено не было.
Авторы исследования сделали вывод, что в обеих группах пациенток с острым циститом Урофурагин® показал высокую клиническую эффективность. Уже на 2-е сут у большинства больных отмечались признаки клинического улучшения – купирование гематурии, уменьшение дизурии, устранение болевого синдрома. Нормализация лабораторных показателей после проведенного лечения отмечена у 51 (98%) участницы исследования. При этом эрадикация возбудителей по результатам посева мочи отмечалась в 100% случаев.
Частота возникновения нежелательных явлений была незначительной (7,6%). Побочные эффекты – тошнота, снижение аппетита носили невыраженный характер и не потребовали отмены препарата. В процессе лечения эпизодов возникновения кандидозного вульвовагинита, ятрогенной диареи, а также признаков дисбиоза кишечника отмечено не было.
Еще одним важным преимуществом применения фузидина является быстрое начало действия. ИНМП, как известно, зачастую протекают с выраженной симптоматикой, поэтому указанная характеристика приобретает особое значение. Так, после приема внутрь фурагин очень быстро всасывается и достигает максимальной концентрации в сыворотке крови в течение 0,5 часа. Эти концентрации являются незначительными с терапевтической точки зрения и составляют не более 4,2 мкм/ мл. Выведение же препарата составляло в среднем около 6,25 мг/мл. То есть препарат работает таргетно, концентрируясь преимущественно в моче. По сведениям литературы прием производных нитрофурана с пищей потенциально увеличивает биодоступность на 40-50% и увеличивает выведение препарата, то есть повышает его концентрацию в моче, влияя на эффективность и ускоряя начало действия.
! Основные преимущества Урофурагина:
• уникальный механизм действия, обеспечивающий низкий уровень риска селекции антибиотикорезистентности;
• узкий спектр действия, позволяющий не нарушать количественный и качественный состав микрофлоры кишечника и влагалища;
• высокая таргетность – максимальная концентрация вещества в месте инфекции;
• минимальная ингибирующая концентрация в моче превышает таковую в плазме в несколько раз;
• наиболее благоприятный профиль безопасности среди всех нитрофуранов;
• доступная цена и европейское качество.
Однако не только препараты нитрофуранового ряда сегодня задекларированы в Рекомендациях EAU-2017 в качестве препаратов первой линии для лечения ИНМП. При известной чувствительности локальных уропатогенов к ко-тримоксазолу экспертная группа EAU-2017 рекомендует применение триметоприма или его комбинации с сульфаметоксазолом. Особенно это актуально для пациентов с рецидивирующими урогенитальными инфекциями, ведь на прием к врачу они зачастую приходят со списком антибиотиков, принимаемых ими за последние несколько месяцев. Именно в такой ситуации идеальным решением может стать назначение Бисептола. При этом сроки лечения как правило 3 до 5 дней, при этом оптимальная продолжительность приема АБП по мнению ряда авторов составляет 3 дня (Bonkat et al., 2017).
Эффективность коротких курсов ко-тримоксазола была оценена в недавнем сравнительном исследовании А. Vachhani и соавт. (2015). 175 пациентов с неосложненной ИМП (с острым циститом и явлениями дизурии, подтвержденной бактериурией и характерными УЗИ-признаками) были рандомизированы на 3 группы и получали назначенное антибактериальное лечение (ко-тримоксазол, норфлоксацин или левофлоксацин) в течение 3 дней. Перед началом терапии всем пациентам был произведен бактериальный посев на флору. В целом E. coli (74,29%) оказалась наиболее распространенным организмом. Другие бактерии встречались значительно реже: Klebsiella spp (11,43%), Streptococcus spp. (6,29%), Staphylococcus saprophyticus (5,14%) и Pseudomonas spp. (2,86%). После 3 дней лечения показатели эрадикации возбудителя составили 86,2; 87,7 и 83,3% для пациентов, получавших, соответственно, ко-тримоксазол, норфлоксацин и левофлоксацин. Ни в одной из групп не было отмечено серьезных побочных реакций, потребовавших отмены лечения.
! Авторы сделали вывод, что короткие курсы (3 дня) ко-тримоксазола в терапии неосложненных ИМП являются эффективной мерой для элиминации основных видов уропатогенов. По эффективности короткие курсы ко-тримоксазола не уступают таковым у фторхинолонов. Однако в качестве первой линии лечения неосложненных ИМП должен быть использован именно ко-тримоксазол, так как фторхинолоны, не имея явных преимуществ, должны быть отнесены к группе препаратов резерва.
Стоит отметить, что неосложненный пиелонефрит легкой и средней степени тяжести требует более длительного лечения ко-тримоксазолом – 7-14 дней. Около 10-15 лет назад появились сообщения о росте уровней резистентности микроорганизмов к ко-тримоксазолу, что привело к некоторым ограничениям в его использовании. Но подобные ограничения коснулись большого количества антибиотиков, что было связано с общим резонансом в отношении растущих уровней антибиотикорезистентности ко всем без исключения классам антибиотиков. Ко-тримоксазол не только не исчез с фармацевтического рынка Европы, но и сумел сохранить свое место в европейских рекомендациях по ведению бактериальных инфекций различных органов и систем организма.
Бисептол как комбинация двух синергично действующих веществ (сульфаметоксазола и триметоприма) обладает уникальным антимикробным бактерицидным спектром и высокой, проверенной временем безопасностью. Наиболее ярким критерием хорошего профиля безопасности является разрешение к применению препарата в детской практике (Бисептол® в таблетках рекомендован начиная с 6-летнего возраста, в форме суспензии применяется с 2-месячного возраста). Рационализация назначения Бисептола привела к тому, что в последние годы отмечается повышение уровней чувствительности к ко-тримоксазолу, причем среди штаммов микроорганизмов, вызывающих развитие как ИМП, так и инфекций других систем организма (прежде всего – респираторной). Это важно понимать в разрезе возрастающего числа сообщений об аллергических реакциях на антибиотики цефалоспоринового ряда и случаях резистентности к фторхинолонам.
Таким образом, Урофурагин® и Бисептол® являются эффективными и безопасными АПБ и безусловной альтернативой цефалоспоринам и фторхинолонам в эмпирической терапии острой неосложненной ИНМП. При этом Бисептол® является антибактериальным средством с огромной доказательной базой и высокой степенью безопасности. Повсеместный рост чувствительности уропатогенов к Бисептолу позволяет рекомендовать его в качестве препарата первой линии для лечения ИНМП при известной чувствительности локальных уропатогенов к ко-тримоксазолу. Урофурагин®, обеспечивая высокий уровень эрадикации основного возбудителя ИМП – кишечной палочки, позволяет сохранять стабильность микрофлоры основных сред организма, что имеет первостепенное значение для пациентов, страдающих острыми инфекциями. Лечение ИМП Урофурагином и Бисептолом не только соответствует принципам доказательной медицины, но и позволяет обеспечить высокий уровень комплайенса к терапии со стороны пациентов благодаря удобству применения, относительно коротким курсам лечения и доступной цене. И конечно же, нельзя забывать о том, что использование эффективных и безопасных АПБ в широкой клинической практике – шаг к преодолению антибиотикорезистентности, являющейся на сегодня глобальной медико-социальной проблемой.
Справка ЗУ
Говоря об антибиотикотерапии ИМП, важно помнить о потенциальной опасности широкого назначения фторхинолонов для системного применения. Напоминаем, что Управлением по контролю пищевых продуктов и лекарственных препаратов США (FDA) 12 мая 2016 г. было опубликовано сообщение с рекомендацией ограничить применение АБ группы фторхинолонов при большинстве неосложненных инфекций, поскольку эти препараты могут вызвать развитие инвалидизирующих побочных эффектов. По мнению экспертов FDA, в целом риск неблагоприятных явлений, связанных с применением АБП класса фторхинолонов, преобладает над их пользой для пациентов с острым синуситом, острым бронхитом и неосложненными ИМП. При указанных состояниях фторхинолоны должны использоваться в качестве резервных препаратов у больных, которые не могут получать другую терапию. Проведенное FDA исследование безопасности продемонстрировало, что системное применение фторхинолонов (в таблетках, капсулах или инъекционно) ассоциируется с развитием инвалидизирующих и потенциально необратимых побочных эффектов (иногда сочетанных). Нежелательные реакции могут возникать со стороны сухожилий, мышц, суставов, периферических нервов и центральной нервной системы. Вследствие этого FDA считает необходимым в инструкции по медицинскому применению всех препаратов группы фторхинолонов и в листки-вкладыши для пациента внести изменения, отражающие эту новую информацию о безопасности. При этом отмечается, что исследования безопасности фторхинолонов продолжаются и FDA будет извещать общественность по мере появления дополнительной информации.
Подготовила Александра Меркулова
Тематичний номер «Урологія. Нефрологія. Андрологія» № 3-4 (10-11), листопад 2017 р.
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
Кальцій є одним із найважливіших елементів в організмі людини, оскільки підтримує належний стан кісток і зубів, зменшує ризик остеопорозу, а також знижує імовірність розвитку серцево-судинних хвороб і ожиріння (Institute of Medicine, 2011; Zhang F. et al., 2019; Teegarden D., 2003). Значна кількість людей потребує кальцієвих добавок, але водночас боїться каменеутворення. Сечокам’яна хвороба (СКХ) – поширене в наш час захворювання; більшість каменів становлять кальцій-оксалатні (Wei L. et al., 2022)....
Рак передміхурової залози (РПЗ) – злоякісне новоутворення, що розвивається з епітелію передміхурової залози. РПЗ вважається одним із найпоширеніших видів раку у чоловіків та однією з головних причин смерті у чоловіків похилого віку в Україні і світі. Лікарі загальної практики – сімейної медицини, лікарі інших спеціальностей мають бути обізнані щодо основних факторів ризику та початкових клінічних проявів РПЗ з метою їх раннього виявлення та направлення пацієнта до закладу охорони здоров’я (ЗОЗ), що надає спеціалізовану медичну допомогу, а також сприяти виконанню усіх рекомендацій фахівців онкологічного профілю під час протипухлинного лікування та організації належної паліативної допомоги пацієнтам, які виявляють бажання перебувати вдома на термінальних стадіях захворювання. ...
У статті представлено коментарі до дослідження TRAVERSE* , яке оцінювало ризик виникнення довгострокових серцево-судинних подій у чоловіків із гіпогонадизмом, що застосовують тестостерон-замісну терапію....
Переважна більшість хворих урологічного профілю страждають від больового синдрому. Гострий біль, який може виникнути внаслідок перенесеного хірургічного втручання на передміхуровій залозі або сечовому міхурі, при гострих запальних захворюваннях сечовивідних шляхів або при нирковій кольці (НК), вимагає невідкладної аналгезії з використанням ефективного та безпечного препарату, який не викликає серйозних побічних явищ. Хронічний біль, який є основним симптомом хронічного простатиту (ХП) та синдрому хронічного тазового болю (СХТБ) у чоловіків, суттєво впливає на якість життя, сексуальну сферу та психоемоційний стан пацієнтів, що також потребує проведення раціональної знеболювальної терапії. Нестероїдні протизапальні препарати (НПЗП), зокрема диклофенак натрію, довели свою ефективність за рахунок вираженої знеболювальної й протизапальної дії при оперативних втручаннях в урології, у хворих урологічного профілю з хронічною патологією (ХП/СХТБ) або невідкладними станами. ...