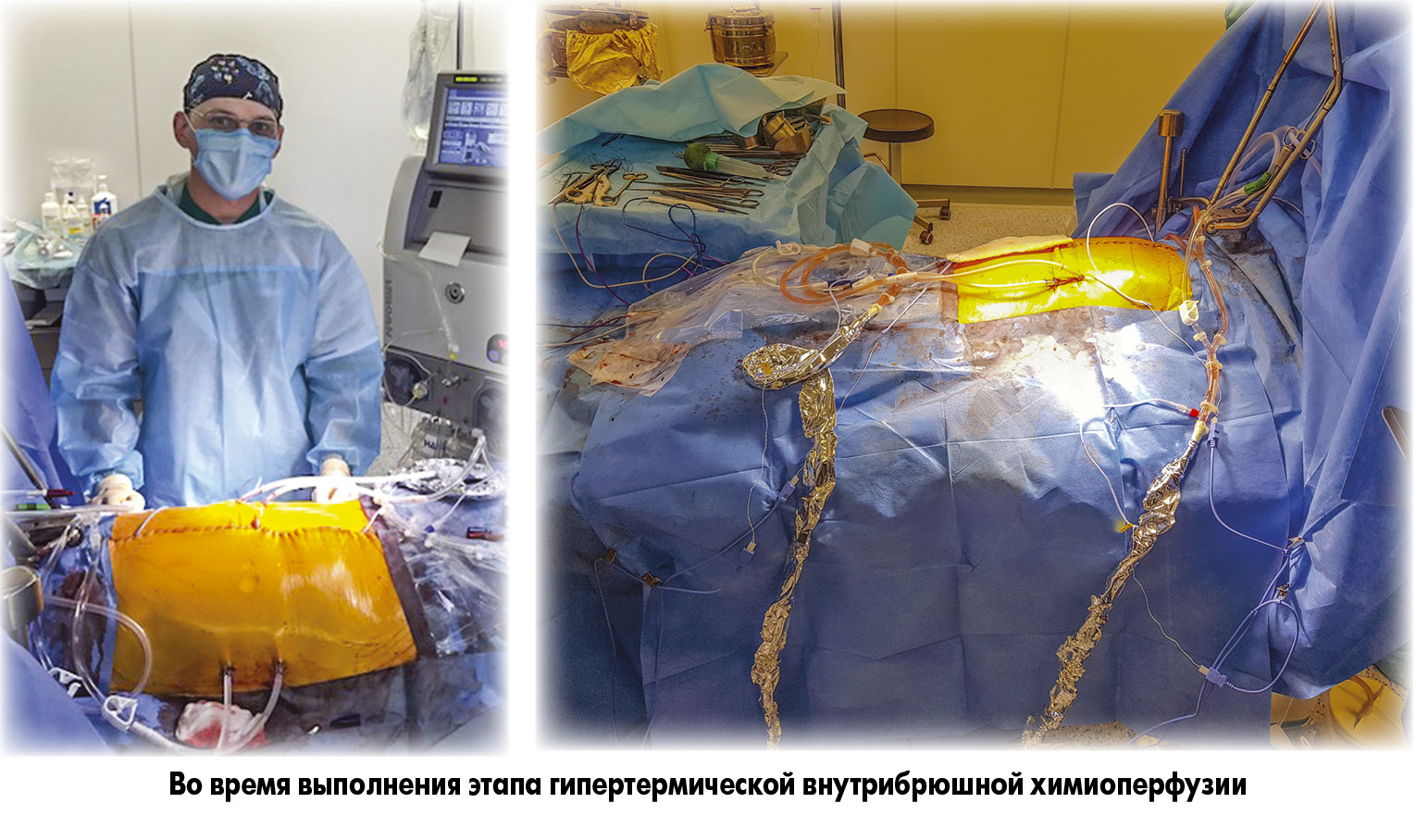
Программа циторедуктивной хирургии и внутрибрюшной гипертермической химиоперфузии в Национальном институте рака
 С сентября 2017 г. в Национальном институте рака (НИР) стартовала программа лечения больных с карциноматозом. Об этом нашему корреспонденту рассказал хирург-онколог, глава мультидисциплинарного консилиума по лечению перитонеального карциноматоза НИР Вячеслав Игоревич Копецкий.
С сентября 2017 г. в Национальном институте рака (НИР) стартовала программа лечения больных с карциноматозом. Об этом нашему корреспонденту рассказал хирург-онколог, глава мультидисциплинарного консилиума по лечению перитонеального карциноматоза НИР Вячеслав Игоревич Копецкий.
Насколько остро стоит вопрос карциноматоза в Украине?
По данным Национального канцеррегистра, с 1990-х гг. только в нашем институте пролечено 635 пациентов с раком желудка (РЖ), 3098 пациенток с раком яичников (РЯ), 233 пациента с колоректальным раком (КРР), 4 пациента с мезотелиомой брюшины и 2 пациента с псевдомиксомой брюшной полости. Исходя из этой статистики, можно констатировать, что проблема карциноматоза достаточно актуальна, а если учитывать многие факторы в лечении таких больных, то этих пациентов намного больше. К примеру, при гинекологических операциях, выполняемых в неспециализированных центрах, часто не проводится ревизия брюшной полости. Подобные ситуации возникают и при лапароскопических операциях на прямой кишке. Согласно статистическим данным европейских стран, на 100 тыс. регистрируется 5 случаев псевдомиксомы брюшной полости, в Украине – только 2 случая. Из этого следует, что остальным больным не устанавливается диагноз и они не получают соответствующего лечения.
Как появилась идея о внедрении технологии гипертермической интраперитонеальной химиотерапии (HIPEC) в НИР и почему Вы решили заняться ее реализацией?
Медиана выживаемости у больных с негинекологическим карциноматозом в среднем не превышает 10 мес, а учитывая то, что много пациентов с КРР и РЖ сталкиваются с этой проблемой, мы стали искать пути ее решения. Около 2 лет назад началось наше общение с Вадимом Гущиным, хирургом-онкологом из Mercy Medical Center (г. Балтимор, США). Из его публикаций и данных исследований стало понятно, что пациенты с карциноматозом, которым была применена циторедуктивная хирургия и технология HIPEC, имеют большую продолжительность жизни. Вадим Гущин оказывал консультативную помощь в запуске программы, провел несколько семинаров с хирургической и анестезиологической бригадой. После этого началась работа по выбору и покупке аппарата для HIPEC. В этом вопросе нам содействовало руководство НИР, без которого воплощение этой идеи в жизнь было бы невозможным.
Отличается ли эффективность при разных нозологиях и как изменяется течение заболевания при применении HIPEC?
Да, данные по эффективности HIPEC при первичных злокачественных опухолях разной локализации отличаются. К примеру, при перитонеальном карциноматозе у больных с КРР медиана выживаемости составляет 13,5-18,8 мес, последняя в 2 и больше раза выше при применении этой методики. Так, большую роль играет РСІ (peritonel cancer index – индекс перитонеального карциноматоза), чем он ниже, тем выше шансы пациента на излечение. При применении этой методики у пациенток с эпителиальным раком яичников медиана выживаемости колеблется от 46 до 78 мес в зависимости от степени дифференцировки опухоли и РСІ. До недавних пор мы в принципе не могли оказать помощь пациентам с мезотелиомой брюшины, потому что классические методы, такие как нормотермическая внутрибрюшная химиотерапия и хирургическое лечение, не позволяли достичь медианы выживаемости более 16 мес. При проведении циторедукции и НІРЕС медиана выживаемости колеблется от 20 до 79 мес. В лечении псевдомиксомы брюшной полости химиоперфузия является основным методом лечения, а хирургическое лечение – дополнительным. Лечение карциноматоза при РЖ успешно проводится в Японии, в европейских странах пока не получены удовлетворительные результаты применения HIPEC у больных с РЖ.
Скажите, пожалуйста, может ли врач областной, городской больницы или врач-онколог поликлиники направить к вам больного? Какие критерии включения пациента в программу лечения перитонеального карциноматоза в НИР?
Пациентов к нам направлять можно и нужно, поскольку мы являемся единственным государственным учреждением в Центральной и Восточной Украине, в котором проводится лечение перитонеального карциноматоза с использованием НІРЕС. В программу могут быть включены пациенты в возрасте 18-70 лет с диагнозом мезотелиомы брюшины, псевдомиксомы брюшины, карциноматоза при РЯ (первичный или платиночувствительный), КРР с карциноматозом и до 3 метастазов в печень. Также в программу могут быть включены пациенты с КРР высокого риска, когда планируется профилактическая симультанная НIPEC или НIPEC как этап стратегии second look (стадия рТ4, опухолевые депозиты на брыжейке, метастазы в яичники, положительный перитонеальный смыв, перфорации опухоли до или во время операции). Состояние пациента по шкале ECOG (Eastern Cooperative Oncology Group) дожно быть не выше 2.
Каких пациентов Вы не возьметесь лечить, какие критерии исключения из программы?
Критериями исключения прежде всего являются тяжелое состояние больного (по шкале ECOG выше 2); возраст – до 18 лет и старше 70; ИМТ больше 30; декомпенсированная сопутствующая патология; кроме этого, карциноматоз при некоторых солидных опухолях из-за отсутствия достоверной информации о применении НІРЕС (перитонеальный карциноматоз с синхронными неколоректальными паренхиматозными метастазами, карциноматоз при первичном платинорефрактерном и платинорезистентном РЯ). Кроме того, в программу не могут быть включены пациенты с такими осложнениями, как уретерогидронефроз по данным КТ, клинические и инструментальные признаки кишечной непроходимости, что свидетельствует об инвазивном характере заболевания, при котором эффективность процедуры равняется нулю, как и при асците брюшной полости независимо от локализации.
Какой объем оперативного вмешательства может быть выполнен пациенту и как проводится процедура НІРЕС?
Максимальный объем операции, который может перенести пациент: оментэктомия, спленэктомия, листальная панкреатоспленэктомия, перитонеумэктомия с левого и правого купола диафрагмы, холецистэктомия, правосторонняя гемиколэктомия или субтотальная колэктомия, дистальная резекция желудка или гастрэктомия, задняя эвисцерация таза. При циторедукции возможно удаление любого органа, кроме печени, почек, мочевого пузыря и мочеточников, вмешательство на этих органах свидетельствует о нецелесообразности такой операции. Процедура начинается с циторедукции, которая выполняется в максимальном объеме с целью достижения СС‑0, после этапа циторедукции в брюшную полость вводится химиотерапевтический препарат, нагретый до 42-43 °С. Время экспозиции, а также температура и другие параметры регулируются автоматически. Что касается самой установки НІРЕС, то существует 3 основных типа систем: открытая, закрытая и смешанная. Основной характеристикой является безопасность для медицинского персонала, наибольшая безопасность – у закрытой системы, которую используем мы, потому что такая система обеспечивает минимальный контакт персонала с химиопрепаратами.
Отмечались ли Вами осложнения при проведении циторедукции с последующей НІРЕС?
Естественно, проведение большого объема оперативного вмешательства с использованием НІРЕС сопряжено с высоким риском осложнений. Данные исследований сообщают о высоком риске несостоятельности дигестивных анастомозов. Однако пока у наших пациентов, которые приняли участие в программе лечения перитонеального карциноматоза в НИР, осложнений, требующих хирургической и медикаментозной коррекции, не возникало, все были выписаны домой.
В завершение нашей беседы хотелось бы узнать Ваше мнение о перспективах развития лечения перитонеального карциноматоза в нашей стране.
Прежде всего необходимо расширение показаний к применению гипертермической химиоперфузии, эту методику следует применять, помимо лечения перитонеального карциноматоза, при опухолях другой локализации. Очень интересным и перспективным методом является направление изолированной перфузии конечностей при опухолях мягких тканей конечности, которое пока еще в Украине представлено очень ограниченно.
Подготовила Анна Кальченко
Тематичний номер «Онкологія» № 5 (51), грудень 2017 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...