Лікування анафілаксії на первинній ланці
Анафілаксія – це важка генералізована чи системна реакція гіперчутливості, що загрожує життю [1, 2]. Усі рекомендації щодо анафілаксії підкреслюють тяжкість епізодів цього стану та супутній ризик смерті [1-5]. Оскільки анафілаксія характеризується швидким розвитком порушень дихання та кровообігу, боротися з нею слід також максимально швидко. Проте цей стан часто важко розпізнати через варіабельність діагностичних критеріїв, що призводить до відстрочення призначення правильного лікування та збільшення ризику смерті.
Лікарям первинної ланки відводиться надзвичайно важлива роль у профілактиці та лікуванні анафілаксії, однак цьому питанню присвячено мало досліджень. Систематичний огляд публікацій стосовно лікування анафілаксії виявив певну кількість прогалин у цій області, зокрема брак знань щодо розпізнавання анафілактичних реакцій, лікування епінефрином (адреналіном) та застосування аутоінжекторів адреналіну (АІА) [6]. Найбільш часто вирішенням цієї проблеми вбачається розвиток міждисциплінарної комунікації та навчання медичного персоналу.
Пильність щодо анафілаксії як небезпечного для життя стану зростає серед лікарів різних спеціальностей, а в нещодавніх публікаціях зазначено, що цей стан не є таким рідкісним, як вважалося раніше. Епідеміологічні дані свідчать про частоту подібних реакцій у межах 1,5-7,9 випадку на 100 тис. пацієнто-років у Європі та 1,6-5,1 випадку на 100 тис. пацієнто-років у США [16, 17]. Однак статистика захворюваності та смертності від анафілаксії досі недосконала. Різна методологія, вибір специфічних популяцій та часте застосування кумулятивних показників поширеності перешкоджають екстраполяції даних більшої частини досліджень на загальну популяцію.
На сьогодні більшість популяційних досліджень, які документують алергічні реакції відповідно до Міжнародної класифікації хвороб Х перегляду, подають суперечливі дані, що унеможливлює точне визначення поширеності тяжких алергічних реакцій на кшталт анафілаксії [17-20]. Однак у деяких з них підрахунок частоти анафілактичних реакцій проводиться за допомогою інших підходів, наприклад аналізу історій хвороби у відділеннях невідкладної допомоги чи підрахунку кількості призначених АІА. Згідно зі звітами відділень невідкладної допомоги частота анафілаксії становить 0,04-0,5% усіх випадків госпіталізацій [20-28]. Значну варіабельність можна пояснити різницею в популяціях та методології досліджень, особливостями різних відділень, труднощами в розпізнаванні пацієнтів з анафілаксією. Інформації щодо смертності від анафілаксії також дуже мало, і показники за даними різних авторів значно відрізняються: 0,04-2,7 випадку/млн/рік [29-31]. Підраховано, що 1 із 3 тис. пацієнтів стаціонару в США переносить анафілактичну реакцію з ризиком смерті близько 1%, що зумовлює 500-1000 смертей щорічно тільки в цій країні [32]. Бразильські автори стверджують, що рівень смертності від анафілаксії становить 1,1 випадку/млн/рік, при цьому більшість реакцій викликана ліками, а летальні випадки зазвичай реєструються в медичних закладах [31].
Перебіг анафілаксії здебільшого відбувається за IgE-залежним імунологічним механізмом, хоча можливі IgE-незалежний механізм та безпосередня стимуляція мастоцитів. Тригерами можуть бути харчові продукти, отрута комах, що жалять, та ліки [2] Кілька досліджень продемонстрували складність сигнальних шляхів мастоцитів та базофілів, а також чутливість цієї системи до регуляторних механізмів.
В активації мастоцитів та вивільненні медіаторних речовин (IgE та IgG, фактор стовбурових клітин, білки комплементу, цитокіни, нейропептиди, опіоїди) бере участь велика кількість молекул, що взаємодіють з рецепторами на клітинній поверхні [33]. Більшість цих механізмів на сьогодні точно не встановлена [34-37].
Діагностика анафілаксії
Оскільки анафілаксія є станом, який швидко розвивається та уражає кілька систем організму, клінічний діагноз базується на оцінці ознак та симптомів, що виникають упродовж 2 год після контакту з алергеном чи тригером [38]. Швидке встановлення діагнозу забезпечує оптимальне лікування. До симптомів анафілаксії належать: порушення дихання (респіраторний дистрес), гіпотензія, тахікардія, ціаноз, кропив’янка, ангіонабряк, нудота, блювання та біль у животі. Шкірні прояви спостерігаються в більшості випадків, а наступними за частотою є кардіоваскулярні та респіраторні симптоми [39]. Встановлення діагнозу ускладнюється, якщо відсутні дерматологічні ознаки, наприклад у разі гіпотензивного шоку без жодних інших симптомів при контакті з відомим чи ймовірним алергеном. Респіраторні (утруднений вдих, дистонія, слинотеча) та кардіоваскулярні прояви (раптове суттєве зниження артеріального тиску, тахікардія) є потенційно життєзагрожуючими проявами анафілаксії та мають розглядатися особливо уважно [1-5].
Однією з основних проблем розпізнавання зазначеного стану є те, що сполучення симптомів та проявів не завжди однакове, тому лікарю, який спостерігає подібні стани рідко, реакції низької та помірної тяжкості складно ідентифікувати як анафілаксію. Таким чином, для діагностики слід використовувати затверджені клінічні критерії. Представлені нижче критерії мають достатню чутливість та точність для діагностики анафілаксії у відділенні невідкладної допомоги [40].
Діагностичні критерії анафілаксії (адаптовано)
Імовірність анафілаксії є високою, коли перебіг патологічного стану відповідає будь-якому з наведених комплексів ознак.
1. Гострий початок захворювання (від кількох хвилин до кількох годин) із залученням шкіри та/або слизових оболонок (наприклад, генералізована кропив’янка, свербіння, почервоніння, набряк губ, язика, язичка):
а) порушення дихання (задишка, свистяче дихання, бронхоспазм, стридор, знижений піковий об’єм видиху, гіпоксемія);
б) знижений артеріальний тиск (АТ) чи асоційовані з ним симптоми з боку органів-мішеней (гіпотонія, колапс, синкопе, нетримання сечі).
2. Два чи більше з таких проявів швидко (від кількох хвилин до кількох годин) розвиваються після контакту з імовірним для цього пацієнта алергеном:
а) залучення шкіри та/або слизових оболонок (наприклад, генералізована кропив’янка, свербіння, почервоніння, набряк губ, язика, язичка);
б) порушення дихання (задишка, свистяче дихання, бронхоспазм, стридор, знижений піковий об’єм видиху, гіпоксемія);
в) знижений АТ чи асоційовані з ним симптоми з боку органів-мішеней (гіпотонія, колапс, синкопе, нетримання сечі);
г) стійкі шлунково-кишкові симптоми (кольки у животі, блювання).
3. Зниження АТ після контакту з відомим для цього пацієнта алергеном (від кількох хвилин до кількох годин):
а) немовлята та діти: низький АТ чи зниження систолічного АТ на ≥30% (низький систолічний АТ визначається як < 70 мм рт. ст. для дітей віком 1 міс – 1 рік; <70 + (2 × вік) мм рт. ст. для дітей віком 1-10 років; <90 мм рт. ст. для дітей віком 11-17 років);
б) дорослі: систолічний АТ <90 мм рт. ст. чи зниження на >30% від вихідного рівня цього пацієнта.
Протягом кількох останніх десятиліть були розроблені in vitro та in vivo методи для підтвердження клінічного діагнозу анафілаксії та встановлення її етіології [41]. Точні клінічні дані разом з доступними лабораторними методиками здатні забезпечити правильне встановлення діагнозу. Діагностика анафілактичних реакцій in vitro передбачає кількаразове (серійне) визначення рівнів медіаторів, що виділяються при анафілаксії, а саме: триптази, гістаміну, хімази, карбоксипептидази A3, тромбоцитактивуючого фактора та інших продуктів мастоцитів.
Визначення рівня триптази в сироватці або плазмі крові рекомендоване для діагностики системної анафілаксії, хоча результати мають інтерпретуватися індивідуально і з врахуванням інших відповідних обстежень [41]. Під час анафілактичної реакції пік рівня сироваткової триптази спостерігається через 60-90 хв після її початку, а його зниження починається через 120 хв. Отже, цей метод потребує взяття зразків крові упродовж 1-2 год від початку реакції та через 24 год для фіксації піку та подальшого зниження [42]. Однак нормальний рівень сироваткової триптази в першому зразку не виключає анафілаксії. Інші біомаркери (гістамін та його метаболіти, хімаза, карбоксипептидаза, цистеїнілові лейкотрієни, простагландини, тромбоцитактивуючий фактор) мають менш значущу та більш варіабельну прогностичну цінність у діагностиці анафілаксії [42].
Для профілактики повторних анафілактичних реакцій необхідною є ідентифікація агентів, здатних їх викликати. Відповідне обстеження слід проводити через 3-4 тиж після гострого епізоду, щоб дати час відновитися активності мастоцитів [43, 44]. Етіологічний діагноз можна підтвердити за допомогою серологічних методів, зокрема визначення алергенспецифічного сироваткового IgE, клітинних тестів, що дозволяють виміряти рівень вивільнення медіаторів, які виділяються базофілами (лейкотрієни, гістамін), тест активації базофілів [41]. Ці методи пропонують цікаву альтернативу в діагностиці потенційних тригерів анафілаксії. Тест активації базофілів забезпечує важливі переваги для пацієнтів з анафілактичними реакціями на β-лактамні засоби, нестероїдні протизапальні препарати (НПЗП), нейромускулярні блокатори та ліки, для яких не існує методики, здатної виявити рівень специфічного IgE [45]. Хоча тести in vitro є більш безпечними, слід точно встановити їх чутливість та специфічність.
Основні методики дослідження алергії та реакції гіперчутливості in vivo включають шкірні та провокаційні тести [41], які повинні призначатися, проводитися та інтерпретуватися досвідченими професіоналами.
При діагностиці анафілаксії слід обов’язково враховувати супутні фактори, як-от: наявність коморбідних станів (бронхіальна астма, інфекційні процеси, серцево-судинні хвороби, мастоцитоз), певні фізичні навантаження, вживання алкоголю, гормональний цикл, психогенний стрес, прийом специфічних препаратів (НПЗП, інгібітори ангіотензинперетворюючого ферменту, β-блокатори), здатні призвести до тяжчої реакції чи до анафілаксії на тлі прийому менших доз алергену. Одним з найбільш відомих таких факторів анафілаксії є фізичне навантаження. Залежна від вживання їжі індукована фізичним навантаженням анафілаксія вважається окремим клінічним синдромом (46).
Наприклад, сенсибілізація до омега‑5 гліадину зазвичай проявляється як залежна від вживання пшениці індукована фізичним навантаженням анафілаксія [47]. Загалом кажучи, механізми, що зумовлюють вплив кофакторів на розвиток анафілаксії, досі точно не встановлені [48].
Невідкладне лікування анафілаксії
Анафілаксія є невідкладним станом, що загрожує життю, тому швидка оцінка стану пацієнта та відповідне втручання є критично важливими. Усі медичні працівники мають бути підготовленими до виявлення та лікування хворих з анафілактичними реакціями. Незначна на перший погляд клінічна маніфестація здатна непередбачувано прогресувати до фатального анафілактичного шоку протягом кількох хвилин [49]. Важкість анафілактичних епізодів може відрізнятися в різних хворих, і навіть в одного пацієнта вона може бути різною [50].
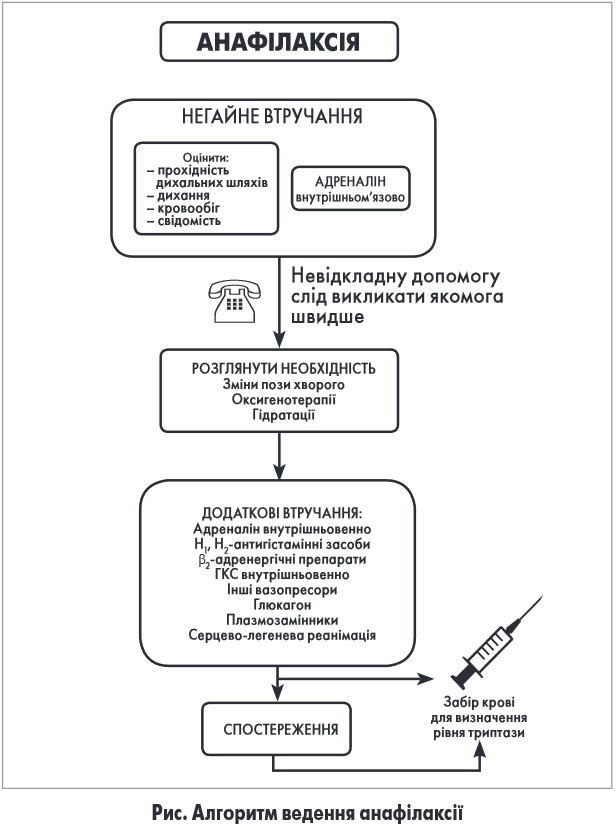 Лікування пацієнта з анафілаксією має розпочинатися з припинення контакту з відомим чи ймовірним тригером, якщо це можливо [51]. Надалі необхідно оцінити кровообіг, прохідність дихальних шляхів, дихання, стан свідомості, шкірні прояви, вагу [44].
Лікування пацієнта з анафілаксією має розпочинатися з припинення контакту з відомим чи ймовірним тригером, якщо це можливо [51]. Надалі необхідно оцінити кровообіг, прохідність дихальних шляхів, дихання, стан свідомості, шкірні прояви, вагу [44].
Після введення адреналіну слід покласти пацієнта на спину з піднятими нижніми кінцівками. Не варто дозволяти хворим сидіти, стояти та перебувати у вертикальному положенні. У разі блювання чи задишки необхідно подбати про те, щоб хворий перебував у зручному положенні з піднятими нижніми кінцівками. Це дозволить запобігти шоку внаслідок перерозподілу крові та синдрому порожньої порожнистої вени / порожнього шлуночка [52].
Слід негайно викликати допомогу та постійно чи якомога частіше моніторувати життєво важливі показники пацієнта (АТ, частоту серцевих скорочень, оксигенацію). Якщо потрібно, призначити кисень та внутрішньовенні інфузії, провести серцево-легеневу реанімацію [53]. Алгоритм дій при анафілаксії представлений на рисунку.
Двофазна анафілаксія – це повторний розвиток симптомів анафілаксії через кілька годин після зникнення первинних симптомів без повторного контакту з тригером [1].
Враховуючи, що двофазна анафілаксія не є незвичним станом [21, 54], пацієнти, в яких симптоми минули, повинні підлягати моніторингу та медичному спостереженню в спеціалізованому центрі з відповідно навченим персоналом, відділенням невідкладної допомоги та можливістю госпіталізації. Тривалість моніторингу повинна залежати від важкості симптомів [55].
Фармакологічне лікування анафілаксії: адреналін як засіб вибору
Доказова база щодо використання різних засобів для лікування анафілаксії ґрунтується на обсерваційних, епідеміологічних, фармакологічних, посмертних дослідженнях, вивченні тваринних моделей [56]. Значна тяжкість анафілактичних реакцій практично унеможливлює оцінку лікування адреналіном у проспективних рандомізованих подвійних сліпих плацебо-контрольованих дослідженнях. [57].
Адреналін є засобом вибору для невідкладного лікування анафілаксії та єдиним медикаментом, що має вазоконстрикторний ефект, викликаючи зворотній розвиток набряку слизової оболонки дихальних шляхів та гіпотензії [58 59]. Крім того, адреналіну властиві інотропна та хронотропна дія на серце, бронходилатуючий вплив та стабілізуюча дія на мастоцити і базофіли [60, 61].
Доказова база свідчить, що відтермінування ін’єкції адреналіну асоціюється з більшою частотою госпіталізацій та вищим рівнем смертності [62, 63]. І навпаки, догоспітальне введення адреналіну супроводжується кращими наслідками для пацієнта [64, 65].
Адреналін слід вводити внутрішньом’язово в латеральний широкий м’яз стегна (musculus vastus lateralis), тобто зовнішню його частину, у зв’язку з вазодилататорним ефектом цього засобу, який реалізується в скелетних м’язах і сприяє швидкому всмоктуванню та розвитку безпосередньої фармакологічної дії. У підшкірних тканинах адреналін, навпаки, діє як вазоконстриктор, що може сповільнювати його всмоктування [66-68].
Доза адреналіну для лікування анафілаксії в медичному закладі становить 0,01 мг/кг в разі внутрішньом’язового призначення в розведенні 1:1000. Максимальна доза становить 0,3 мг для дітей та 0,5 мг для підлітків та дорослих. При застосуванні АІА пацієнти вагою 7,5-25 кг повинні отримувати 0,15 мг, вагою більше 25 кг – 0,3 мг [3]. Ін’єкцію адреналіну можна повторювати ще 1 чи 2 рази через 5-15 хв у пацієнтів, що не відповіли на першу дозу, у хворих з швидким прогресуванням реакції чи в разі двофазної анафілаксії [69]. Третя доза адреналіну потребується менш часто [70, 71]. Відсутність відповіді на адреналін є індикатором потреби в госпіталізації до відділення інтенсивної терапії, де пацієнт може отримати подальшу допомогу, у т. ч. внутрішньовенну інфузію адреналіну [72].
Використання терапевтичних доз адреналіну здатне викликати побічні ефекти, подібні до ознак підвищення рівня ендогенного адреналіну: тривожність, головний біль, запаморочення, тремор, блідість, серцебиття [57, 60, 61, 73]. Рідше, зазвичай при передозуванні чи введенні внутрішньовенного болюсу, адреналін може спричинити шлуночкові аритмії, набряк легень, злоякісну гіпертензію, внутрішньочерепну кровотечу, хоча такі побічні явища вкрай рідко спостерігаються в дітей та здорових дорослих [59, 61, 74, 75].
Абсолютних протипоказань до призначення адреналіну при анафілаксії не існує (50). Однак слід оцінювати співвідношення користь/ризик у пацієнтів із серцево-судинними захворюваннями [76]. Серце є потенційним органом-мішенню при анафілаксії; якщо не ввести адреналін, може розвинутися гострий коронарний синдром [77].
Засоби другого ряду для лікування анафілаксії
Антигістамінні препарати (анти-H1 та анти-H2) та глюкокортикоїди (ГКС) – це засоби другого ряду, оскільки вони не є життєзберігаючими, тому не повинні застосовуватися як початкове чи єдине лікування [58, 78, 79].
Доказів на користь застосування H1-антигістамінних засобів при анафілаксії немає. Ці препарати полегшують свербіння, почервоніння обличчя та кропив’янку, однак вони не діють на обструкцію дихальних шляхів чи гіпотензію. Дія Н1-гістаміноблокаторів повільніша, ніж адреналіну. Крім того, рекомендації щодо вживання цих препаратів при анафілаксії, у т. ч. що стосується призначуваних доз, екстрапольовані з рекомендацій стосовно кропив’янки. Певна кількість Н1-гістаміноблокаторів першого покоління представлена у формі для парентерального введення, яку можна застосовувати при анафілаксії. Ці засоби часто викликають незначні побічні ефекти (сонливість, сплутаність свідомості), але тяжкі небажані реакції (судоми, гіпотензія, кардіотоксична дія) розвиваються рідко.
Н1-гістаміноблокатори є більш безпечними, проте вони не мають форм для парентерального введення. Антигістамінні препарати до цих пір залишаються засобами, що найчастіше помилково застосовуються при анафілактичних реакціях у відділеннях невідкладної допомоги [58, 80, 81].
Існують докази, що ефект H2-гістаміноблокаторів щодо шкірних симптомів посилюється в разі сумісного призначення з H1-гістаміноблокаторами, але роль цих засобів при анафілаксії на сьогодні точно не визначена [79, 82].
ГКС традиційно призначаються з метою запобігання двофазній чи відтермінованій анафілаксії, хоча їх ефективність ніколи не була доведена. Досвід прийому ГКС при астмі свідчить, що початок фармакологічної дії може спостерігатися через кілька годин після їх застосування; отже, ці засоби не впливають або незначно впливають на первинні симптоми анафілаксії [78].
Інгаляція β2-адренергічних агоністів (сальбутамол, тербуталін) здатна впливати на анафілаксію шляхом зменшення бронхоспазму. Однак призначення цих засобів у жодному разі не повинно передувати введенню адреналіну [2].
Довгострокове лікування анафілаксії
Лікування анафілаксії продовжується і після перенесеного гострого епізоду. Основним моментом у запобіганні подальшим анафілактичним реакціям є підтверджений етіологічний діагноз та уникнення тригерів. У деяких випадках довгострокове етіотропне лікування здатне забезпечити захист у разі випадкових контактів з алергеном, приміром алергенспецифічна імунотерапія при анафілаксії, індукованій отрутою перетинчастокрилих комах. Пацієнт також повинен знати, як поводитися в разі повторної появи симптомів [2-5, 83].
Усім хворим, що перенесли епізод анафілаксії, слід рекомендувати визначення специфічних тригерів подібних реакцій. Тригери анафілаксії можуть бути визначені спеціалістами-алергологами, які також повинні інформувати пацієнта щодо можливих перехресних реакцій та безпечних альтернатив, особливо при гіперчутливості до ліків. Такий підхід продемонстрував свою користь у зниженні ризику тяжкої анафілаксії [86]. Найбільш застосовуваними способами визначення алергенів є детальний анамнез гострих епізодів, результати шкірних тестів, визначення алергенспецифічних IgE, провокаційні тести. Оптимальним часом для подібної діагностики вважається приблизно 4 тиж після гострого епізоду [5].
Уникнення деяких тригерів здатне негативно впливати на якість життя пацієнтів [50]. У таких випадках можна застосовувати імуномодулююче та/або етіотропне лікування, у т. ч. з десенсибілізацією до ліків [87], імунотерапію отрутою комах [88], харчову пероральну імунотерапію харчовими продуктами [89], анти-IgE терапію [90].
Враховуючи непередбачувану природу анафілаксії, пацієнти мають бути готові діяти в будь-який момент, особливо в разі відсутності медичних працівників. У міжнародних рекомендаціях зауважено, що складений письмово план дій є ефективним засобом покращення наслідків для пацієнта [2-5].
 План дій при анафілаксії є письмовим документом, який може допомогти пацієнту чи особам, що надаватимуть допомогу, у разі розвитку алергічної реакції (табл. 1). Наявні на сьогодні плани дій здатні покращувати наслідки при інших алергічних хворобах, наприклад бронхіальній астмі, отже, мають потенціал щодо зниження частоти та важкості анафілактичних реакцій, а також рівня тривожності пацієнта і осіб, що надають допомогу [91].
План дій при анафілаксії є письмовим документом, який може допомогти пацієнту чи особам, що надаватимуть допомогу, у разі розвитку алергічної реакції (табл. 1). Наявні на сьогодні плани дій здатні покращувати наслідки при інших алергічних хворобах, наприклад бронхіальній астмі, отже, мають потенціал щодо зниження частоти та важкості анафілактичних реакцій, а також рівня тривожності пацієнта і осіб, що надають допомогу [91].
У побутових умовах для введення адреналіну перевага надається АІА (якщо доступні), оскільки самостійне користування ампулами, голками та шприцами пацієнтом чи його родичами часто супроводжується помилками [2-5]. Сучасні АІА представлені в трьох дозуваннях: 0,15, 0,3 мг та 0,5 мг (у меншості країн). Адреналін для самостійного введення може використовуватися і в умовах медичного закладу [92].
 Препарати адреналіну для самостійного введення слід призначати пацієнтам з анамнезом анафілаксії та високою ймовірністю повтору подібного епізоду, особливо в разі індукції нападу харчовими продуктами чи укусами комах, а також хворим з ідіопатичною анафілаксією.
Препарати адреналіну для самостійного введення слід призначати пацієнтам з анамнезом анафілаксії та високою ймовірністю повтору подібного епізоду, особливо в разі індукції нападу харчовими продуктами чи укусами комах, а також хворим з ідіопатичною анафілаксією.
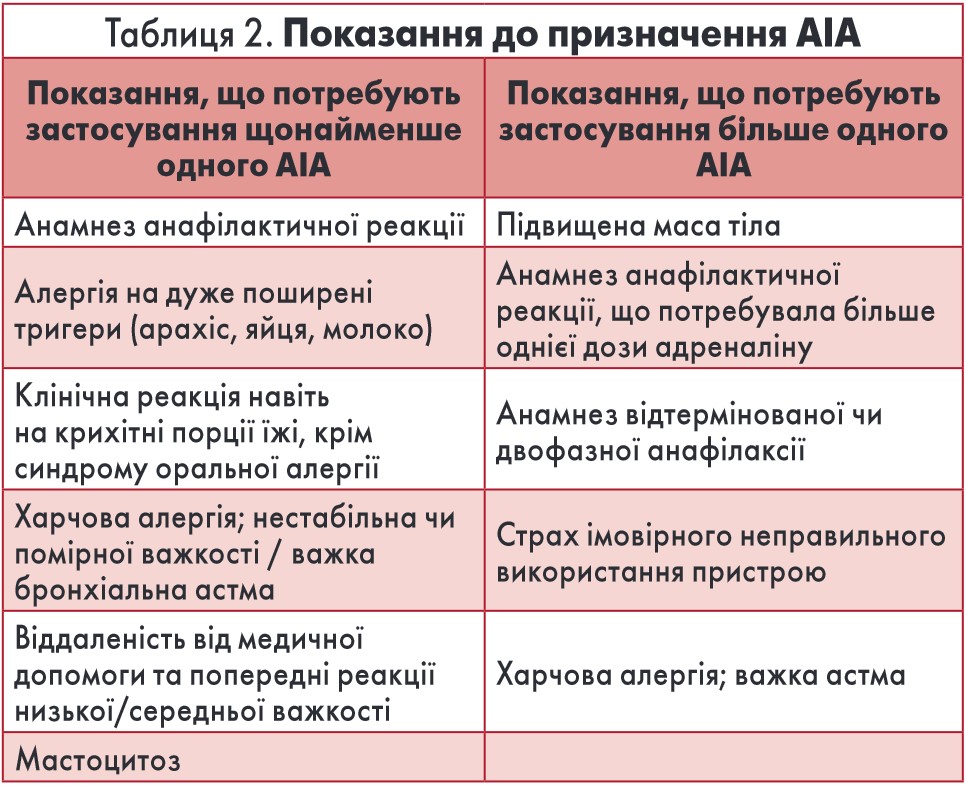
АІА також варто рекомендувати особам, що живуть у віддалених регіонах без доступу до медичних служб, пацієнтам з мастоцитозом, певним хворим без анамнезу анафілаксії. Серед останніх – особи з попередніми генералізованими шкірними реакціями після контакту з мінімальними кількостями харчових продуктів, а також пацієнти з алергією на тригери, уникнути яких складно через їх значну поширеність (арахіс, яйця, молоко) [2-5]. Основні показання до призначення таких приладів представлені в таблиці 2 [93].
Загалом призначення АІА повинно ґрунтуватися на об’єктивних даних анамнезу після ретельної оцінки співвідношення користь/ризик, оскільки потреба в цих приладах і користування ними асоціюються з погіршенням якості життя [94].
За даними останніх досліджень проведення навчальних заходів серед пацієнтів дозволяє знизити захворюваність та смертність від анафілаксії, хоча довготермінові переваги таких заходів ще мають бути встановлені [95, 96]. Навчання пацієнтів має розпочинатися після завершення гострого епізоду анафілаксії до виписки зі стаціонару, і медичні працівники відділення невідкладної терапії повинні бути підготовлені до його правильного проведення. Пацієнтів навчають розпізнавати симптоми анафілаксії; визначати потребу у введенні адреналіну та зверненні за медичною допомогою; розпізнавати та уникати ймовірних кофакторів, що значно збільшують ризик тяжкої анафілаксії [50].
Протягом останніх кількох років доступними джерелами пов’язаної зі здоров’ям інформації стали Інтернет та соціальні мережі [97]. Кілька досліджень, що фокусувалися на впливі цих технологій на пацієнтів з анафілаксією, підтверджують сприятливу дію спеціалізованого навчання за допомогою Інтернету та мобільних додатків [98-100].
Анафілаксія в окремих контингентів населення
У певних груп пацієнтів є клінічні особливості, що впливають на стратегію лікування анафілаксії у відділенні невідкладної допомоги. Їх необхідно враховувати при оцінюванні ризику анафілаксії та рекомендуванні запобіжних заходів.
Зокрема, маленькі діти можуть бути неспроможними правильно описати симптоми анафілаксії. Крім того, її ознаки в дітей неспецифічні (дратівливість, плач, сонливість), тому їх часом важко інтерпретувати, а це сповільнює встановлення діагнозу та призначення відповідного лікування. Затверджених клінічних критеріїв анафілаксії для цієї вікової категорії немає. Диференційний діагноз зазначеного стану в немовлят та маленьких дітей повинен включати вроджені вади, аспірацію стороннього тіла, ентероколіт, викликаний білками їжі [101].
Харчова алергія є найбільш поширеною причиною анафілаксії в дітей (близько 20% усіх випадків) і значною проблемою охорони здоров’я в школах [102, 103, 104]. При цьому працівники більшості закладів освіти недостатньо підготовлені до надання невідкладної допомоги при анафілаксії [105], не мають планів невідкладних заходів, адреналіну. Усе це сповільнює встановлення діагнозу та госпіталізацію дітей до відділення невідкладної допомоги. Для покращення готовності до надання невідкладної допомоги в школах варто вживати певних заходів на основі співпраці між батьками, персоналом школи, алергологами та педіатрами [106].
Підлітки характеризуються більшим ризиком анафілаксії через специфічні характеристики цієї вікової групи [98, 107, 108]. Поведінка підлітків потенційно призводить до недбалого ставлення до тригерів анафілаксії. Також вони можуть приховувати своє захворювання, уникати застосування АІА, звертатися за медичною допомогою лише на пізніх стадіях. Ці фактори здатні сповільнити розпізнавання епізоду анафілаксії. Лікування цього стану в підлітків може бути ускладнено неправильною інформацією (свідоме зниження інтенсивності симптомів при їх описі, приховування тригерів) [109, 110]. Слід зазначити, що фактором підвищення тяжкості анафілаксії може бути перший досвід вживання алкоголю [93].
На думку науковців, старечий вік не збільшує ризик анафілаксії [111]. Однак він асоціюється з більшим ризиком смерті, ймовірно, внаслідок наявності коморбідних станів, вживання великої кількості ліків, більшого ризику госпіталізації, змін імунної системи, що призводять до прозапального стану [112]. У пацієнтів старечого віку з анафілаксією, що лікуються у відділенні невідкладної допомоги, вік чи навіть анамнез кардіоваскулярного захворювання не є абсолютним протипоказанням до призначення адреналіну. Однак слід ретельно зважити переваги та недоліки цього методу [76].
Розповсюдженість анафілаксії, особливо ідіопатичної, вища в пацієнтів з мастоцитозом, ніж у загальній популяції [113]. У цих осіб також частіше спостерігається гіперчутливість до НПЗП та отрути перетинчастокрилих комах. При оцінці стану хворих з мастоцитозом потрібно врахувати, що в них анафілактичні реакції можуть бути особливо тяжкими, з частими кардіоваскулярними проявами. Крім того, у значній кількості випадків ідентифікувати тригер не вдається [114, 115]. Хворим з мастоцитозом слід завжди призначати щонайменше один АІА [116].
Висновки
Анафілаксія не є таким рідкісним станом, як вважалося раніше. Це порушення не завжди легко розпізнати, особливо, якщо єдиний його прояв – гіпотензія. Анафілаксія – це мультисистемний патологічний стан, який може проявлятися як різні комбінації симптомів. При анафілаксії на перший погляд помірні симптоми можуть непередбачувано прогресувати до фатального анафілактичного шоку. Критично важливими для пацієнта є швидке встановлення правильного діагнозу та швидке втручання. Після оцінки кровообігу, дихання та стану свідомості, а також ліквідації ймовірної причини реакції варто внутрішньом’язово ввести адреналін, який є препаратом вибору без абсолютних протипоказань. Однак у пацієнтів із серцево-судинними захворюваннями слід все-таки оцінити співвідношення користь/ризик.
Антигістамінні засоби та ГКС є препаратами другого ряду. Після епізоду анафілаксії потрібно рекомендувати використання АІА.
Етіологічні чинники, запідозрені при огляді у відділенні невідкладної допомоги, можуть відрізнятися від реальної причини реакції. При цьому госпіталізованому пацієнту слід запропонувати ретельне обстеження щодо алергічних хвороб. Особливу увагу варто приділити кофакторам, оскільки вони здатні значно погіршувати перебіг анафілаксії. Загалом кажучи, анафілаксія – комплексна патологія, яку повинен добре розпізнавати та лікувати будь-який медичний працівник, тому існує значна потреба у відповідному навчанні.
Список літератури знаходиться в редакції.
Alvarez-Perea A., Tanno L. K., Baeza M. L. How to manage anaphylaxis
in primary care. Clin Transl Allergy. 2017; 7: 45.
Переклала з англ. Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 1 (422), січень 2018 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Реімбурсація – це повне або часткове відшкодування аптечним закладам вартості лікарських засобів або медичних виробів, що були відпущені пацієнту на підставі рецепта, за рахунок коштів програми державних гарантій медичного обслуговування населення. Серед громадськості програма реімбурсації відома як програма «Доступні ліки». Вона робить для українців лікування хронічних захворювань доступнішим....
Тіамін (вітамін В1) – важливий вітамін, який відіграє вирішальну роль в енергетичному обміні та метаболічних процесах організму загалом. Він необхідний для функціонування нервової системи, серця і м’язів. Дефіцит тіаміну (ДТ) спричиняє різноманітні розлади, зумовлені ураженням нервів периферичної та центральної нервової системи (ЦНС). Для компенсації ДТ розроблено попередники тіаміну з високою біодоступністю, представником яких є бенфотіамін. Пропонуємо до вашої уваги огляд досліджень щодо корисних терапевтичних ефектів тіаміну та бенфотіаміну, продемонстрованих у доклінічних і клінічних дослідженнях....
Актуальність проблеми порушень моторної функції шлунково-кишкового тракту (ШКТ) за останні десятиліття значно зросла, що пов’язано з великою поширеністю в світі та в Україні цієї патології. Удосконалення фармакотерапії порушень моторики ШКТ та широке впровадження сучасних лікарських засобів у клінічну практику є на сьогодні важливим завданням внутрішньої медицини....
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....




