Переваги комбінованого пробіотика Опефера у профілактиці та лікуванні ожиріння (експериментальне обґрунтування)
 Метаболічні порушення при ожирінні можуть спричиняти розвиток низки хвороб, а саме: захворювань серцево-судинної системи (артеріальної гіпертонії, атеросклерозу, ішемічної хвороби серця), інсульту, цукрового діабету 2 типу, захворювань опорно-рухового апарату (остеохондрозу хребта та обмінно-дистрофічного поліартриту), хвороб гепатобіліарної системи (дискінезії жовчного міхура, хронічного холециститу, жовчнокам’яної хвороби), пухлин різної локалізації, зокрема легенів, молочної залози, тіла матки та яєчників, а також передчасну смерть. Тривалість життя осіб із цією патологією на 3-5 років, а при тяжких формах ожиріння на 15 років менша порівняно з особами з нормальною масою тіла (М.М. Гинзбург, 2000; Yang, 2007).
Метаболічні порушення при ожирінні можуть спричиняти розвиток низки хвороб, а саме: захворювань серцево-судинної системи (артеріальної гіпертонії, атеросклерозу, ішемічної хвороби серця), інсульту, цукрового діабету 2 типу, захворювань опорно-рухового апарату (остеохондрозу хребта та обмінно-дистрофічного поліартриту), хвороб гепатобіліарної системи (дискінезії жовчного міхура, хронічного холециститу, жовчнокам’яної хвороби), пухлин різної локалізації, зокрема легенів, молочної залози, тіла матки та яєчників, а також передчасну смерть. Тривалість життя осіб із цією патологією на 3-5 років, а при тяжких формах ожиріння на 15 років менша порівняно з особами з нормальною масою тіла (М.М. Гинзбург, 2000; Yang, 2007).
Ожиріння – хронічне захворювання обміну речовин, що характеризуєтьcя надмірним розростанням жирової тканини. До розвитку цієї патології призводить енергетичний диcбаланc між надлишком енергії, що надходить в організм з їжею, та витратами цієї енергії. У такому випадку надлишок енергії акумулюється у вигляді накопичення адипозної тканини. Розвиток ожиріння є індивідуальним та залежить від cтадії перебігу, віку, раціону, фізичної активноcті та генетичних факторів. Надмірне вживання жирів хоча і є важливою причиною ожиріння, проте останнім часом вчені довели, що безконтрольне використання харчових добавок, а саме підсилювача смаку глутамату натрію (Е 621), теж є причиною надмірної маси тіла (Т.М. Фалалєєва, 2010).
 Глутамат натрію (підсилювач смаку) внесено до переліку дозволених в Україні харчових добавок тільки у 2000 році згідно з постановою Кабінету Міністрів України № 342 від 17.02.2000. Глутамат натрію (C5H8NO4Na, Е 621) широко використовується у виробництві різних продуктів харчування (бульйонних кубиків, консервів, заморожених продуктів, чіпсів, соусів, супів, фаст-фуду тощо). Складно знайти консерви, напівфабрикати або готові продукти, вироблені промисловим шляхом, які не містили б цю харчову добавку. При цьому вміст глутамату натрію може значно перевищувати допустимі норми, що може призводити до розвитку захворювань травного тракту.
Глутамат натрію (підсилювач смаку) внесено до переліку дозволених в Україні харчових добавок тільки у 2000 році згідно з постановою Кабінету Міністрів України № 342 від 17.02.2000. Глутамат натрію (C5H8NO4Na, Е 621) широко використовується у виробництві різних продуктів харчування (бульйонних кубиків, консервів, заморожених продуктів, чіпсів, соусів, супів, фаст-фуду тощо). Складно знайти консерви, напівфабрикати або готові продукти, вироблені промисловим шляхом, які не містили б цю харчову добавку. При цьому вміст глутамату натрію може значно перевищувати допустимі норми, що може призводити до розвитку захворювань травного тракту.
Вивчення здатності глутамату натрію спричиняти ожиріння триває вже кілька десятиліть. Показано, що у щурів із ожирінням, індукованим глутаматом натрію, розвивається інсулінорезистентність до периферичного засвоєння глюкози, зокрема у 3-місячних щурів спостерігали гіперінсулінемію (K. Oida, 1984). При цьому підвищувалася чутливість адипоцитів до інсуліну, що збільшувало їх ємність для транспорту глюкози та синтезу ліпідів (T. Nakagawa, 2000).
Характер харчування населення у наші дні викликає серйозну стурбованість: зростаюче споживання фаст-фуду, що супроводжується зменшенням частки овочів, фруктів, молочних і кисломолочних продуктів у раціоні, вкрай негативно позначається на стані здоров’я. Дійсно, за останні 10 років частота захворювань шлунково-кишкового тракту (ШКТ) серед дітей та дорослих зросла. У 2011 році в Україні зареєстровано 7 089 010 хворих на гастроентерологічну патологію, 18956,3 на 100 тис. дорослого населення. Станом на кінець 2011 року на диспансерному обліку перебувало 5 028 034 пацієнтів із захворюваннями органів травлення, тобто 70,9% від загальної кількості зареєстрованих осіб. Починаючи з 2006 року поширеність гастроентерологічних захворювань зросла на 11,2% (Ю.М. Степанов, 2013). Значна частина лікарів пов’язують це насамперед із порушенням характеру харчування. На тлі порушення режиму та якості дієти розвиваються не лише гастроентерологічні порушення та метаболічні розлади, зокрема ожиріння, а й дисбіотичні розлади.
У зв’язку з викладеним вище пошук нових нетоксичних засобів профілактики розвитку ожиріння є одним із найважливіших завдань сучасної медицини. У науковій літературі зараз активно дискутується питання впливу пробіотиків на жировий обмін та ожиріння (S.W. Kim, 2013; E. Angelakis, 2012; R. Luoto, 2010; 2012). F. Backhed та співавт., провівши дослідження у 2004 році, були піонерами у вивченні ролі мікрофлори товстої кишки в регуляції обміну речовин. Показано, що мікрофлора кишечнику змінюється в осіб із надмірною масою тіла та що мікробіоценоз кишки можна вважати екологічним чинником, який модулює розвиток ожиріння.
Встановлено, що внаслідок тривалого перебування на дієті з високим вмістом жирів істотно змінювався склад мікрофлори товстої кишки у мишей, зокрема знижувалася кількість Bifidobacterium i Lactobacillus, які, як відомо, мають багато фізіологічно позитивних ефектів, у тому числі поліпшують бар’єрну функцію слизової оболонки кишки, та збільшувалася кількість Firmicutes і Proteobacteria, продуктами метаболізму у яких є багато токсичних речовин (M. Hildebrandt, 2009; P. Turnbaugh, 2008). Автори виявили, що додавання пребіотика олігофруктози до дієти з високим вмістом жирів забезпечувало відновлення кількості біфідобактерій, усувало ендотоксемію та сповільнювало розвиток ожиріння. Отримані результати дозволяють припустити, що підвищення кількості біфідобактерій може зменшити проникність кишечнику та знизити рівень циркулюючого ендотоксину. Крім того, при зростанні кількості біфідобактерій підвищується чутливість до глюкози, посилюється секреція інсуліну, знижується приріст маси тіла і продукція прозапальних медіаторів (P.D. Cani, 2007; F. Fak, 2012; Y. Kadooka, 2010). У роботах останніх років також були встановлені позитивні ефекти пробіотичних бактерій стосовно розвитку ожиріння. Так, застосування Lactobacillus gasseri SBT2055 та Lactobacillus paracasei SSP paracasei F19 (F19) запобігає розвитку індукованого дієтою ожиріння (R. Luoto, 2010; F. Fak, 2012).
З огляду на важливу роль мікробіоти в порушенні обміну речовин перспективним є використання для профілактики та лікування хворих з ожирінням природних та безпечних біологічних засобів на основі коменсальної мікробіоти слизових оболонок людини – пробіотиків, для яких є доведеною: здатність нормалізувати кишкову мікрофлору; впливати на обмін білків, ліпідів, вуглеводів; збалансовувати запальну реакцію організму за рахунок впливу на продукцію про- та протизапальних цитокінів; змінювати мікроекологічне оточення різних органів та систем організму. Обґрунтуванням використання пробіотиків є також характер порушення мікробіоти ШКТ при метаболічних розладах, що проявляється в істотному зниженні кількості Bifidobacterium та Lactobacillus на тлі підвищення кількості Firmicutes і Proteobacteria (M. Hildebrandt, 2009; P. Turnbaugh, 2008).
На сьогодні на фармацевтичному ринку розвинених країн світу представлено кількасот пробіотичних засобів із задекларованим досить високим рівнем імунологічних властивостей, спрямованих на посилення індукції прозапальних цитокінів. Водночас лише декілька пробіотичних штамів із науково-дослідних лабораторій та одиниці готових форм пробіотичних засобів, які можуть впливати на метаболізм окремих речовин та продукцію протизапальних цитокінів, рекомендовано використовувати для корекції порушення обміну речовин. На фармацевтичному ринку України представлено понад 50 пробіотичних засобів.
Серед цих засобів, які використовують для оптимізації кишкового мікробіоценозу, виділяють пребіотики, пробіотики, синбіотики (N.A. Nagalingam, 2012). Термін «пребіотик» у науковий обіг увели Гібсон і Роберфройд. Поняття «пребіотик» визначають як «вибірково ферментований інгредієнт, що приводить до конкретних змін у складі та/або активності шлунково-кишкової мікрофлори, тим самим приносячи користь здоров’ю організму хазяїна» (A.S. Neish, 2009). На сьогодні лише вуглеводневі сполуки є предметом досліджень пребіотичної активності. У більшості досліджень вивчали фруктани (інулін або фруктоолігосахариди, отримані з різних культур або сахарози) та галактоолігосахариди. Для цих інгредієнтів селективна ферментація і відповідні зміни мікробіоти, пов’язані з потенційною користю для здоров’я, були підтверджені в дослідженнях на людях. Пребіотик є субстратом, який піддається селективній ферментації, стимулюючи ріст і активність конкретного мікроорганізму або групи мікроорганізмів, що становлять інтерес, та забезпечує бажаний ефект для здоров’я. Не виключено також, що пребіотики безпосередньо впливають на здоров’я, наприклад, через імунну систему (H.J. Flint, 2012).
Загалом результати більшості досліджень на людях (переважно з використанням фруктанів) підтверджують ефект щоденного вживання пребіотиків відносно зниження апетиту, зменшення маси тіла або маси жирової тканини шляхом зміни концентрації біологічно активних пептидів ШКТ у крові та підвищення толерантності до глюкози (H.J. Flint, 2012).
Існує доказова база клінічного застосування пребіотиків у дітей для лікування та профілактики захворювань. Накопичено дані щодо ефективності пребіотиків при різних захворювань у дітей. Так, R. Orel і L.V. Reberak (2016) провели пошук досліджень, присвячених використанню пребіотиків у дітей, у базах MEDLINE, PubMed, UpToDate, Cochrane Database of Systemic Reviews, the Cochrane Controlled Trials Register. Аналіз результатів досліджень, які мали належну методологічну якість, показав, що пребіотики мають такі позитивні ефекти:
- зменшують біль при кольках у немовлят, що проявляється у зниженні кількості епізодів плачу;
- збільшують частоту дефекації та/або пом’якшують консистенцію випорожнень при закрепах у немовлят і дітей переддошкільного віку, зменшують частоту закрепів загалом і поліпшують травлення;
- сприяють кращому всмоктуванню мінералів (кальцію, заліза) у кишечнику;
- сприяють набору маси тіла у немовлят;
- знижують частоту гастроінтестинальних інфекцій та призначення антибіотиків;
- зменшують частоту респіраторних інфекцій;
- знижують ризик розвитку алергічних захворювань.
Значний інтерес становить використання синбіотиків з метою оздоровлення мікробіому. Синбіотики представлені комбінованими засобами, які отримані шляхом оптимального поєднання пробіотиків і пребіотиків і мають властивості двох складових. Результатом їх взаємодії є покращення властивостей засобу щодо нормалізації складу мікрофлори, підвищення її захисних функцій, у тому числі імунітету, знешкодження патогенних мікроорганізмів (K.R. Pandey, 2015).
Увагу клініцистів привертає комбіноване застосування про- і пребіотиків, оскільки завдяки цьому досягається синергічний і, відповідно, кращий терапевтичний ефект. Механізм синергічної дії про- і пребіотиків схематично зображено на рисунку 1 на прикладі їх впливу на імунну систему при ротавірусному гастроентериті (G. Gonzalez-Ochoa et al., 2017).
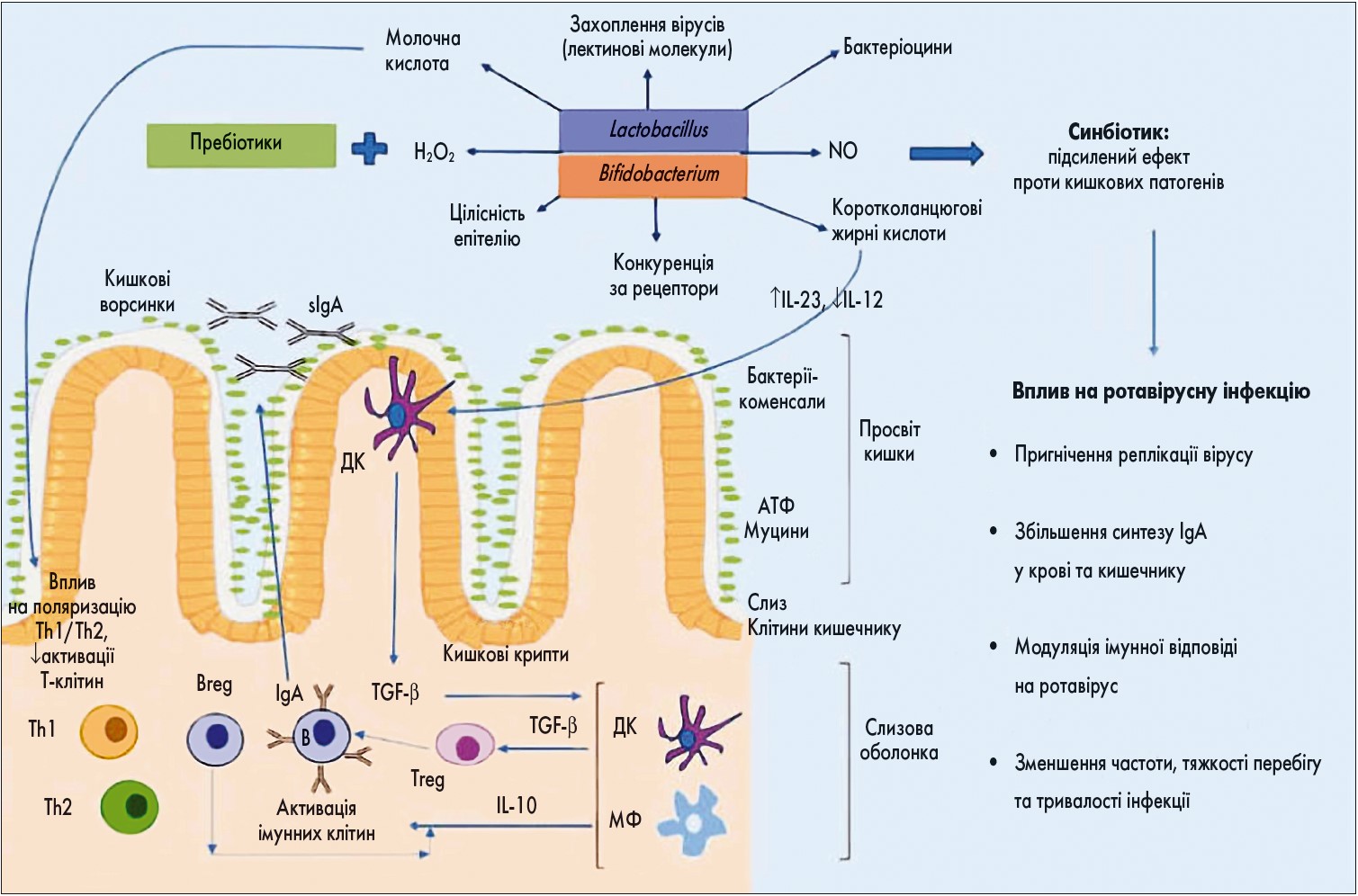 Рис. 1. Механізм синергічної дії про- і пребіотиків (G. Gonzalez-Ochoa et al., 2017)
Рис. 1. Механізм синергічної дії про- і пребіотиків (G. Gonzalez-Ochoa et al., 2017)
Ефективність застосування синбіотиків показано при гострій діареї у дітей віком від 2 місяців до 5 років. Пацієнти були рандомізовані на дві групи: I група (n=79) отримувала синбіотик (Bifidobacterium lactis + інулін), а II група (n=77) – плацебо 1 раз/добу протягом 5 днів. До призначення лікування випорожнення дітей тестували на наявність Rotavirus, Adenovirus, Entamoeba histolytica, Salmonella, Shigella, Campylobacter, Clostridium difficile, Cryptosporidium і паразитів. У дітей, які приймали синбіотик, відзначено меншу тривалість діареї (3,9±1,2 дні vs 5,2±1,3 дні, p<0,001), нижчу частоту епізодів випорожнень на 3-й день захворювання (5,5±2,9 vs 8,3±3,01, p<0,001), меншу кількість дітей із діареєю на 5-й день лікування (17,7 vs 38,9%, р=0,002). Найменша тривалість діареї на тлі прийому синбіотика була у дітей із ротавірусною інфекцією (р=0,001). Крім того, тривалість діареї була меншою у тих пацієнтів, які розпочали лікування синбіотиками протягом перших 24 год захворювання, ніж у тих, які зробили це пізніше (A. lek et al., 2014).
Результати наших та інших досліджень підтверджують, що комбіновані мультиштамові пробіотики мають більш виражений ефект, ніж пробіотики, що містять монокультуру пробіотичних бактерій, для лікування та профілактики ожиріння (О.А. Cавченюк, 2014; N. Kobyliak, 2016, 2017; H.M. Timmerman, 2004). Тому доцільно використовувати комбіновані пробіотики, які містять у своєму складі біфідо- та лактофлору і пребіотики. Одним із таких синбіотиків є Опефера (компанія World Medicine).
Опефера – комбінований пробіотик, який містить живі ліофілізовані бактерії (Lactobacillus rhamnosus, Lactobacillus plantarum, Streptococcus thermophilus, Lactobacillus acidophilus, Bifidobacterium spp. Bifidobacterium bifidum, Bifidobacterium longum, Bifidobacterium infantis), Saccharomyces boulardii: сухий екстракт квіток ромашки аптечної (Matricaria chamomilla L.), інулін.
Лакто- та біфідобактерії у складі Опефери мають високу антагоністичну активність проти широкого спектру патогенних та умовно-патогенних мікроорганізмів, пригнічують життєдіяльність стафілококів, шигел, ротавірусів, протея, ентеропатогенної кишкової палички, деяких дріжджоподібних грибів, запобігають їх адгезії до слизової оболонки кишечнику. Лакто- та біфідобактерії створюють сприятливі умови для розвитку корисної мікрофлори кишечнику, підтримують і регулюють фізіологічну рівновагу кишкової мікрофлори, сприяють нормалізації мікробіоценозу ШКТ, а також підвищують неспецифічну резистентність організму, мають імуномодулювальні властивості, синтезують амінокислоти, вітаміни (К, групи В, у тому числі пантотенову кислоту), які сприяють всмоктуванню заліза, кальцію, вітаміну D. Лакто- і біфідобактерії активізують пристінкове травлення, беруть участь у ферментативному розщепленні білків, жирів, вуглеводів та процесах метаболізму жовчних кислот і холестерину. Кисле середовище, яке створюють лактобактерії, сприяє розвитку біфідобактерій, що становлять 85-95% кишкової мікрофлори організму.
Streptococcus thermophilus володіє максимальною лактазною активністю і синтезує полісахариди, які є необхідним компонентом для росту лактобактерій. Таким чином ці види бактерій проявляють симбіоз, компенсують метаболізм і стимулюють ріст один одного.
Saccharomyces boulardii при проходженні через ШКТ чинять біологічну захисну дію щодо нормальної кишкової мікрофлори. Генетично зумовлена стійкість Saccharomyces boulardii до дії антибіотиків дозволяє застосовувати їх одночасно з антибіотиками для захисту нормального мікробіоценозу кишечнику.
Екстракт квіток ромашки аптечної (Matricaria chamomilla L.) містить ефірну олію, до складу якої входить хамазулен, прохамазулен, інші терпени та сесквітерпени, а також флавоноїди, полісахариди, макро- та мікроелементи, каротин, аскорбінову кислоту, β-ситостерин, холін, органічні кислоти. Цей комплекс біологічно активних речовин має спазмолітичні, протизапальні, антимікробні, в’яжучі, потогінні, жовчогінні та седативні властивості, підвищує секрецію травних залоз, покращує апетит, усуває спазми кишечнику, пригнічує процеси бродіння, поліпшує функціональний стан ШКТ.
Інулін – рослинний полісахарид, полімер D-фруктози, який позитивно впливає на функціональний стан мікрофлори ШКТ та як пребіотик стимулює ріст сахаролітичної мікрофлори.
Дія інуліну на людський організм:
- підвищує імунітет, запускає захисні механізми;
- має гепатопротекторні властивості, відновлює клітини печінки;
- виводить з організму радіонукліди і важкі метали;
- бере участь у ліпідному обміні, сприяє схудненню;
- прискорює процес травлення і виведення калових мас, запобігаючи запорам і процесам гниття;
- бере участь в обміні вуглеводів;
- зменшує інтоксикацію: виводить токсини, патогенні мікроорганізми, гриби, шлаки;
- знижує ризик утворення різного роду пухлин;
- регулює рівень фосфоліпідів, тригліцеридів і холестерину у крові;
- покращує засвоєння вітамінів і мінералів.
Серед сучасних комбінованих пробіотиків Опефера вирізняється завдяки своєму унікальному складу, який не має аналогів на українському ринку.
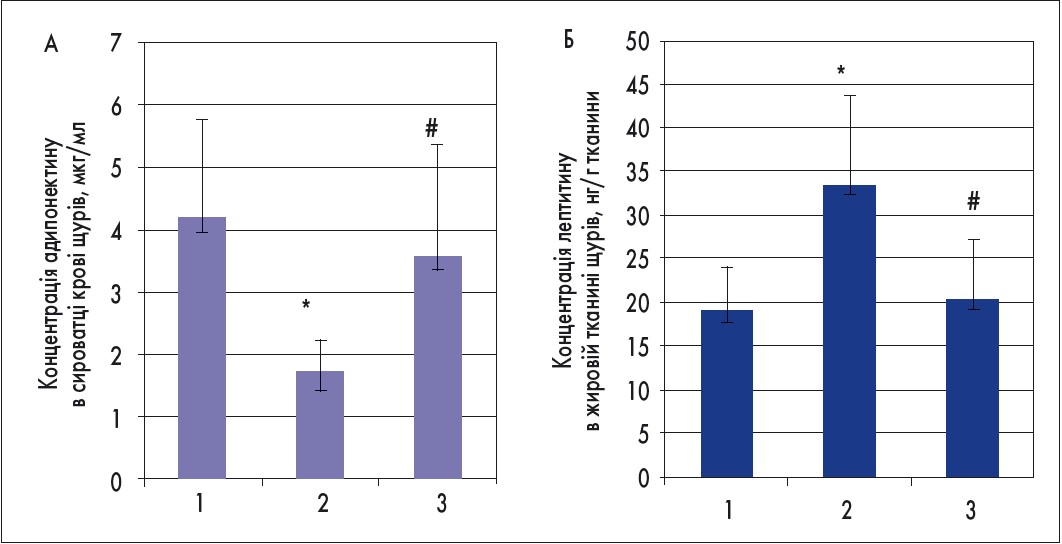
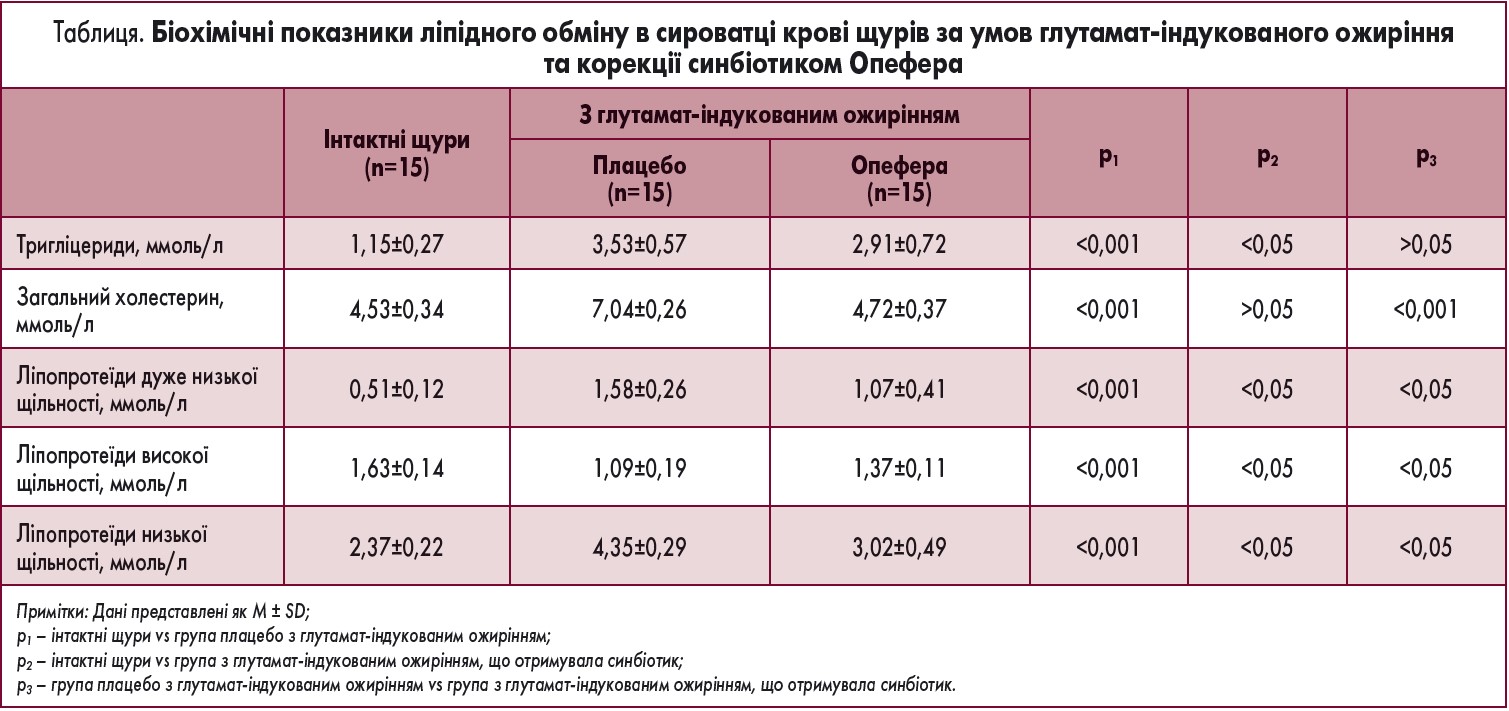
У зв’язку з викладеним вище метою дослідження було вивчити вплив синбіотика Опефера на розвиток експериментального ожиріння у щурів, спричиненого глутаматом натрію. Введення глутамату натрію (4 мг/г) на 2, 4, 6, 8, 10-й день життя призводило до розвитку ожиріння у 4-місячних щурів, що підтверджують також інші автори (K. Oida, 1984; N. Kobyliak, 2016, 2017). Синбіотик Опефера вводили 1-місячним тваринам, що отримували глутамат натрію в неонатальному періоді. Терапію пробіотиком Опефера проводили 3 курсами, один курс – 2 тижні, 1 раз на місяць. Підтвердженням зменшення ожиріння було значуще зниження індексу маси тіла та маси вісцерального жиру (рис. 2). Окрім цього, введення синбіотика Опефера забезпечувало нормалізацію ліпідного обміну в сироватці крові щурів. Найбільш виражений ефект синбіотика стосувався рівня холестерину в сироватці крові, який був статистично значущо відновлений до рівня в інтактних щурів. У тварин, яким вводили синбіотик Опефера, концентрація ліпопротеїдів дуже низької щільності (ЛПДНЩ) зменшувалася на 32,3% (p<0,05), ліпопротеїдів низької щільності (ЛПНЩ) – на 30,6% (p<0,05), а ліпопротеїдів високої щільності (ЛПВЩ) підвищувалася на 25,7% (p<0,05) порівняно з групою плацебо (табл.). Введення комбінованого пробіотика Опефера сприяло відновленню гормональної активності жирової тканини. Так, концентрація адипонектину в сироватці крові та лептину в жировій тканині при введенні пробіотика не відрізнялася від їх рівнів у інтактних щурів (рис. 3).
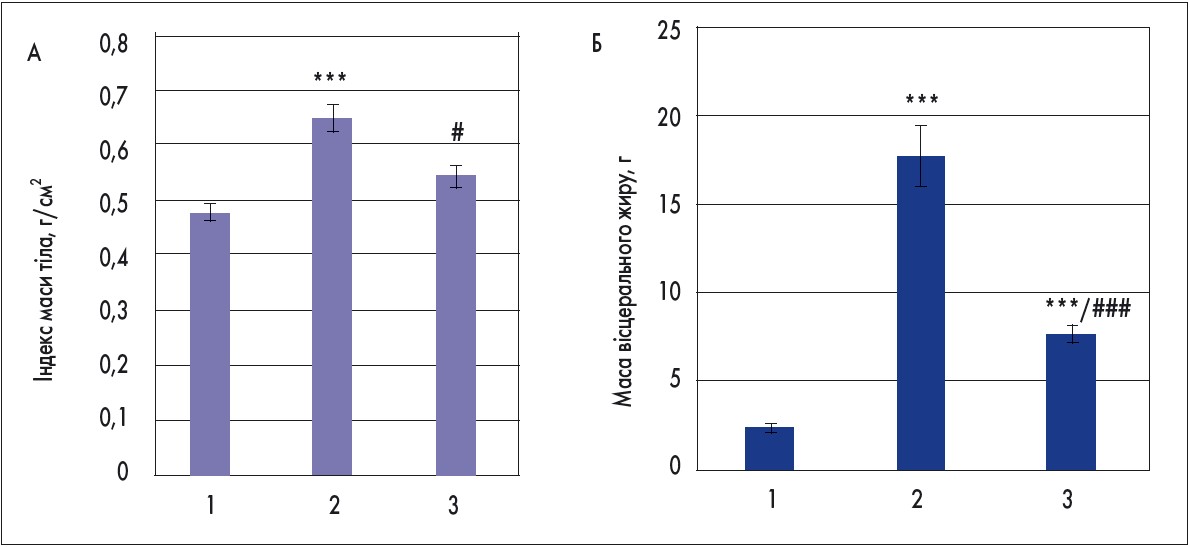 Рис. 2. Індекс маси тіла (А) та маса вісцерального жиру (Б) у щурів за умов глутамат-індукованого ожиріння та корекції синбіотиком Опефера
Рис. 2. Індекс маси тіла (А) та маса вісцерального жиру (Б) у щурів за умов глутамат-індукованого ожиріння та корекції синбіотиком Опефера
Примітки: 1-ша група – інтактні щури; 2-га – глутамат натрію; 3-тя – глутамат натрію + Опефера (n=10, M ± SD);
*** – p<0,05 порівняно з інтактними щурами; # – p<0,05, ### – p<0,001 порівняно з групою глутамату натрію.
Рис. 3. Концентрація адипоцитарних гормонів (А – адипонектин у сироватці крові, Б – лептин у жировій тканині щурів) за умов глутамат-індукованого ожиріння та корекції синбіотиком Опефера
Примітки: 1-ша група – інтактні щури; 2-га – глутамат натрію; 3-тя – глутамат натрію + Опефера (n=10, M ± SD);
* – p<0,05 порівняно з інтактними щурами; # – p<0,05 порівняно з групою глутамату натрію.
Таким чином, курсове введення синбіотика Опефера (впродовж 2 тижнів 1 раз на місяць) зумовлювало підвищення рівня адипонектину в крові, зниження концентрації лептину в жировій тканині та нормалізацію ліпідного обміну в тварин, яким у неонатальному періоді вводили глутамат натрію. Отримані результати свідчать про ефективність синбіотика Опефера у запобіганні ожирінню.
Висновки. Отримані у дослідженні дані є експериментальним обґрунтуванням доцільності застосування синбіотика Опефера для лікування та профілактики ожиріння. Таким чином, в арсеналі лікаря-практика є ефективний та безпечний продукт, який можна призначати дітям віком від 1 року. Спосіб застосування та рекомендована добова доза: дітям раннього віку (від 1 року до 3 років): по 1 капсулі 2 р/добу; дітям віком від 3 до 12 років: по 1 капсулі 3 р/добу; дорослим та дітям віком від 12 років: по 1-2 капсули 3 р/добу.
Список літератури знаходиться в редакції.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (47), березень 2018 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Реімбурсація – це повне або часткове відшкодування аптечним закладам вартості лікарських засобів або медичних виробів, що були відпущені пацієнту на підставі рецепта, за рахунок коштів програми державних гарантій медичного обслуговування населення. Серед громадськості програма реімбурсації відома як програма «Доступні ліки». Вона робить для українців лікування хронічних захворювань доступнішим....
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....