Дайджест
Комбинированный прием ривароксабана с ацетилсалициловой кислотой снижает риск инсульта и других кардиоваскулярных событий у пациентов со стабильной ишемической болезнью сердца
В конце 2017 г. были опубликованы результаты исследования, в котором применение комбинации ривароксабана и ацетилсалициловой кислоты (АСК) снижению частоты развития ишемического инсульта, инфаркта миокарда (ИМ) и смерти у пациентов со стабильным течением атеросклеротического поражения сосудов по сравнению с монотерапией АСК, при этом риск внутричерепного кровоизлияния не повышался.
Дизайн и методы. Двойное слепое рандомизированное исследование COMPASS длилось с марта 2013 по май 2016 года и включило 27 395 пациентов из 602 учреждений 33 стран. Средний возраст участников составил 68,2 года. 89,8% пациентов принимали гиполипидемическую терапию; 72,2% – ингибиторы ангиотензинпревращающего фермента или блокаторы рецепторов ангиотензина. Уровень систолического артериального давления в среднем составлял 136 мм рт. ст., диастолического АД – 78 мм рт. ст., средний уровень общего холестерина – 4,2 ммоль/л.
У 90,6% участников было диагностировано заболевание коронарных артерий, у 27,3% – заболевание периферических артерий. Критериями исключения из исследования служили: высокий риск кровотечения; недавно перенесенные инсульт тяжелая сердечная недостаточность; болезнь почек (скорости клубочковой фильтрации <15 мл/мин); прием двойной антитромбоцитарной терапии, антикоагулянтов; другие заболевания и состояния, которые, по мнению исследователей, связаны с плохим прогнозом.
Участники были рандомизированы на 3 группы в зависимости от назначенной терапии: 1-я группа получала АСК в дозе 100 мг/сут; 2-я – ривароксабан в дозе 5 мг 2 р/сут; 3-я – комбинацию ривароксабана 2,5 мг 2 р/сут и АСК 100 мг/сут.
Первичными конечными точками были смерть, инсульт, ИМ. Исследование досрочно прекращено вследствие явного преимущества комбинированной терапии после наблюдения в среднем на протяжении 23 месяцев.
Результаты. В группе пациентов, принимавших ривароксабан и АСК, первичная конечная точка достигалась реже, чем в группе АСК: 379 (4,1%) случаев против 496 (5,4%) соответственно (относительный риск (ОР) 0,76; 95% доверительный интервал (ДИ) 0,66-0,86; р<0,001). Однако в группе комбинированной терапии отмечена большая частота случаев крупного кровотечения: 288 (3,1%) случаев против 170 (1,9%) в группе монотерапии (ОР 1,70; 95% ДИ 1,40-2,05; р<0,001). Крупными считались все кровотечения, потребовавшие обращения за неотложной медицинской помощью или госпитализации в стационар. По частоте возникновения внутричерепного или фатального кровотечения между двумя группами не выявлено существенной разницы. В группе ривароксабан + АСК зарегистрировали 313 (3,4%) случаев смерти против 378 (4,1%) случаев в группе монотерапии АСК (ОР 0,82; 95% ДИ 0,71-0,96; р=0,01). Между группами монотерапии ривароксабаном и АСК отсутствовало значимое отличие в достижении первичной конечной точки, однако отмечена большая частота случаев возникновения крупного кровотечения у пациентов, получавших только ривароксабан: 255 (2,8%) пациентов против 170 (1,9%) больных из группы АСК (ОР 1,51; 95% ДИ 1,25-1,84; р<0,001).
Выводы. У пациентов со стабильным течением атеросклеротического заболевания сосудов частота наступления смерти, инсульта, ИМ была на 24% ниже у тех, кто получал комбинацию ривароксабана и АСК, по сравнению с пациентами, принимавшими только АСК (4,1 против 5,4% соответственно). Однако частота крупных кровотечений на фоне применения комбинации препаратов оказалась выше на 70% (3,1 против 1,9% соответственно). Коэффициент чистого клинического эффекта был на 20% ниже в группе ривароксабан + АСК по сравнению с группой монотерапии АСК (4,7 против 5,9% соответственно). Монотерапия ривароксабаном в дозе 5 мг 2 р/сут не приводила к улучшению сердечно-сосудистых исходов, но вызывала более значительные кровотечения по сравнению с АСК.
Rivaroxaban with or without Aspirin in Stable Cardiovascular Disease. Eikelboom J., Connolly S., Bosch J. et al. N. Engl. J. Med. 2017; 377:1319-1330.
Злоупотребление алкоголем – важный модифицируемый фактор риска деменции
Результаты недавнего когортного исследования, проведенного во Франции, дают основание предположить, что чрезмерное потребление алкоголя приводит к развитию всех типов деменции, особенно высоким является риск рано манифестирующей деменции.
Предположительно связь между потреблением алкоголя и риском развития деменции можно объяснить тем, что этанол и его метаболит ацетальдегид обладают прямым нейротоксическим действием, что обусловливает структурное и функциональное повреждение головного мозга. Кроме того, употребление алкоголя связано с дефицитом тиамина, что приводит к развитию синдрома Вернике – Корсакова. Алкоголизм также является фактором риска (ФР) развития эпилепсии, травмы головы, а также печеночной энцефалопатии у пациентов с циррозом печени. Употребление алкоголя косвенно связано с сосудистой деменцией из-за ассоциаций с такими ФР, как артериальная гипертензия, геморрагический инсульт, фибрилляция предсердий и сердечная недостаточность. Наконец, алкоголизм ассоциируется с курением табака, склонностью к депрессии и низким уровнем образования – возможными ФР развития деменции. Полученные результаты стали поводом для обсуждения вопроса о введении специфического диагноза «алкогольная деменция», однако употребление алкоголя не включено в перечень ФР развития слабоумия.
Целью исследования, выполненного M. Schwarzinger и соавт., было изучение связи между злоупотреблением алкоголем и развитием деменции с акцентом внимания на раннюю манифестацию заболевания (<65 лет).
Данные ретроспективного анализа опубликованы 20 февраля в Lancet Public Health. Исследователи проанализировали базу данных по всем случаям госпитализаций в больницы Франции. База данных включала около 30 млн человек за 6-летний период наблюдения (2008-2013 гг.). Среди них 80% составили пациенты старше 60 лет. С целью идентификации заболевания использовались диагностические коды по Международной классификации болезней 10-го пересмотра. Манифестацию деменции определяли по первичной регистрации диагноза в период с 2008 по 2013 год; деменцию, установленную пациентам младше 65 лет, классифицировали как раннюю. Ассоциации злоупотребления алкоголем и других ФР с риском развития деменции были проанализированы в многомерных моделях Кокса у пациентов, госпитализированных в 2011-2013 гг., без учета ранее установленного заболевания (2008-10 гг.).
Результаты. Из 31 624 156 взрослых пациентов, выписанных из клиник Франции в период с 2008 по 2013 год, у 1 109 343 диагностирована деменция; эти пациенты были включены в анализ. Из 57 353 (52%) случаев раннего начала деменции 22 338 (38,9%) было связано со злоупотреблением алкоголем; другие пациенты имели дополнительные расстройства, связанные с употреблением алкоголя: 10 115 (17,6%). Последние были наиболее сильными модифицируемыми ФР развития деменции (ОР 3,34; 95% ДИ 3,28-3,41 для женщин и ОР 3,36; ДИ 3,31-3,41 для мужчин). Кроме того, злоупотребление алкоголем имело непосредственную связь со всеми другими ФР развития деменции (все – p<0,0001).
Исследователи пришли к выводу, что расстройства, ассоциированные с употреблением алкоголя, следует считать значимым ФР развития всех типов деменции, и прежде всего рано манифестирующей. Поэтому скрининг на опасное употребление алкоголя должен стать частью рутинной медицинской помощи.
Contribution of alcohol use disorders to the burden of dementia in France 2008-13: a nationwide retrospective cohort study. Schwarzinger M. et al. Lancet Public Health. 2018 Mar;3(3): e124-e132.
Гистопатологические изменения в мозговой ткани при эпилепсии
В 2015 г. Всемирная организация здравоохранения (ВОЗ) признала эпилепсию серьезной проблемой здравоохранения. Приблизительно 50 млн человек во всем мире в настоящее время страдают эпилепсией, и более 30% из них не достигают достаточного контроля судорог на фоне медикаментозной терапии. У некоторых пациентов с резистентной очаговой эпилепсией может применяться хирургическое лечение, и в ряде случаев успешные операции снижают риск смерти. Хотя эффективность хирургической коррекции эпилепсии уже установлена в ретроспективных анализах, проведенных в высокоспециализированных хирургических центрах, лишь немногие из этих центров предоставили подробную информацию о типах обнаруженных патологических изменений головного мозга. Детализация гистопатологических находок, лежащих в основе припадков, необходима для лучшего понимания резистентной к медикаментозной терапии фокальной эпилепсии.
В 2006 г. в рамках исследовательской программы Европейского союза создан Европейский эпилептический банк мозга (The European Epilepsy Brain Bank, EEBB) для стандартизации описания гистопатологической картины образцов, полученных во время операции, и изучения эпилептогенных поражений головного мозга. Создание базы данных также побудило экспертов Международной противоэпилептической лиги (International League against Epilepsy, ILAE) разработать международную классификацию клинико-патологических подтипов фокальной кортикальной дисплазии и подтипов склероза гиппокампа.
Методы. Были исследованы образцы из базы данных EEBB, в которую вошли 4944 мужчины и 4579 женщин, перенесших хирургическое лечение эпилепсии в период с 1990 по 2014 год в 36 специализированных центрах 12 стран Европы. Гистопатологические диагнозы определяли путем исследования образцов в местных больницах (41%) или в Немецком референтном центре по изучению нейропатологии при эпилепсии (59%). Учитывались такие клинические данные: возраст на момент операции и на момент манифестации эпилепсии, продолжительность заболевания, пол, локализация поражения, год операции. Гистопатологический диагноз основывался на результатах световой микроскопии тканей, окрашенных гематоксилином и эозином, или дополнительных гистохимических и иммуногистологических методов. Гиппокампальный склероз трактовался как сегментарная потеря нейронных клеток в анатомических секторах гиппокампа (согласно классификации ILAE). Опухоли головного мозга упорядочены в соответствии с классификацией ВОЗ опухолей центральной нервной системы. Фокальная дисплазия коры была определена в соответствии с классификацией ILAE.
Результаты. Заболевание манифестировало в 18-летнем возрасте у 75,9% пациентов, среди них в 72,5% случаев было проведено хирургическое вмешательство во взрослом возрасте. Средняя длительность эпилепсии до операции составляла 20,1 года у взрослых и 5,3 года – у детей. Височная доля была вовлечена в патологический процесс в 71,9% случаев. Было установлено 36 гистопатологических диагнозов в 7 разных категориях, среди них: склероз гиппокампа (36,4% пациентов; 88,7% – взрослые), опухоли (23,6%; в основном ганглиоглиомы), мальформации кортикального происхождения в 19,8% случаев (фокальная кортикальная дисплазия; 52,7% составили дети). У 7,7% пациентов гистопатологический диагноз установлен не был.
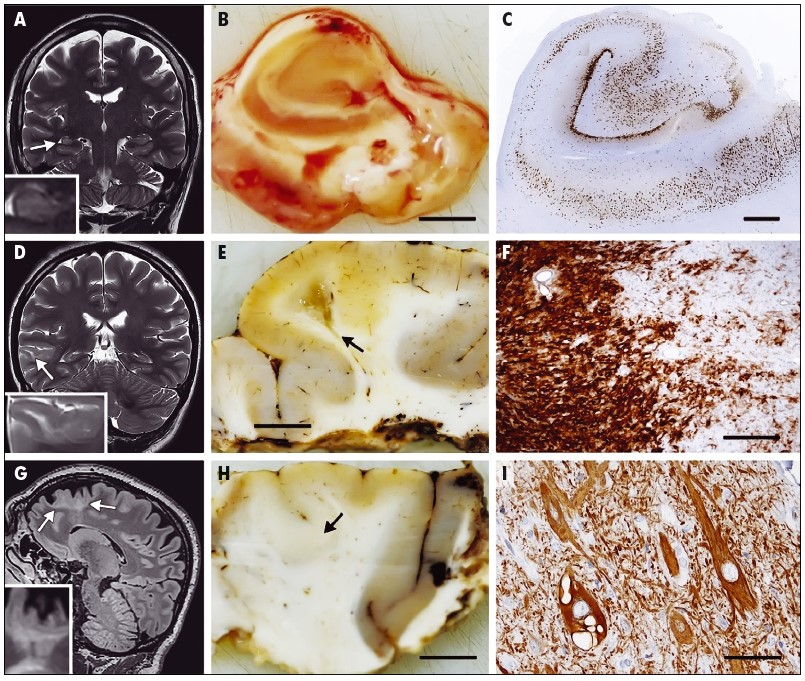
Рис. Внутрицитоплазматическое накопление нейрофиламента, что характерно для дисморфных нейронов при фокальной кортикальной дисплазии ІІ типа: А. Магнитно-резонасная томография (МРТ) – скан 51-летнего мужчины со склерозом гиппокампа и эпилепсией правой височной доли с 12 лет; В. Срез гиппокампа того же пациента; С. Иммуногистохимический анализ отображает сегментарную потерю нейронов зоны СА‑1 гиппокампа; D. Ганглиоглиома у девочки 12 лет с эпилепсией правой височной доли с 8-летнего возраста; Е. Кистозное образование подкоркового белого вещества этой же пациентки; F. Диффузная опухолевая инфильтрация коры (ганглиоглиома І ст. по классификации ВОЗ); G. Фокальная кортикальная дисплазия ІІ типа у пациента с эпилепсией левой фронтальной доли; H. Образец этого же пациента. Утолщенная бледная неокортикальная зона, трудно отличимая от белого вещества
Выводы. Склероз гиппокампа – наиболее распространенный гистопатологический диагноз у взрослых пациентов с медикаментозно резистентной фокальной эпилепсией. У детей чаще всего выявлялась фокальная кортикальная дисплазия. Опухоли оказались второй по распространенности причиной в обеих группах.
Histopathological Findings in Brain Tissue Obtained during Epilepsy Surgery. Blumcke I., Spreafico R. et al. October 26, 2017. N. Engl. J. Med. 2017; 377:1648-1656.
Подготовила Марина Сподаренко
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 1 (44), березень 2018 р.
СТАТТІ ЗА ТЕМОЮ Неврологія
Проблема когнітивних розладів є однією з найважливіших у сучасній клінічній медицині. Це зумовлено не тільки збільшенням частки людей старшого віку серед населення, а й посиленням ролі стресу та інших патогенетичних чинників. У березні відбувся семінар «Академія сімейного лікаря. Біль в грудній клітині. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста», у якому прийняли участь провідні вітчизняні науковці і фахівці різних галузей. У рамках заходу професор кафедри військової терапії Української військово-медичної академії Міністерства оборони України, кандидат медичних наук Мар’яна Миколаївна Селюк представила доповідь «Війна та когнітивні порушення. Причина чи наслідок? Як вирішити проблему?». Подаємо огляд цієї доповіді у форматі «запитання – відповідь»....
Хоча нестероїдні протизапальні препарати (НПЗП) мають численні серйозні побічні ефекти, вони належать до найчастіше застосовуваних препаратів у всьому світі (McGettigan P., Henry D., 2013). Через часте застосування побічні дії НПЗП становлять значну загрозу для громадського здоров’я. Так, уже декілька декад тому було описано підвищення артеріального тиску та ризик загострень серцевої недостатності на тлі прийому цих препаратів (Staessen J. et al., 1983; Cannon P.J., 1986)....
У лютому відбувся медичний форум Ukraine Neuro Global 2024, організований ГО «Українська асоціація медичної освіти» (м. Київ). Під час заходу обговорювалися найактуальніші проблеми сучасної неврології. У рамках форуму відбувся сателітний симпозіум «Актуальні питання фармакотерапії в неврології». Слово мала в.о. завідувача кафедри неврології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Марина Анатоліївна Тріщинська з доповіддю «Краніоцервікалгії: особливості діагностики та лікування»....
Запаморочення є поширеним та іноді стійким симптомом після струсу мозку чи легкої черепно-мозкової травми (лЧМТ). Терміном «запаморочення» часто описують декілька симптомів, як-от головокружіння (вертиго; ілюзія руху), порушення рівноваги (нестійкість, нестабільність) і, власне, запаморочення (пресинкопальний стан). Запаморочення після струсу мозку є клінічним викликом, оскільки існує багато причин цього розладу, а його ведення залежить від етіології [1-3]. Однією з таких причин є пошкодження периферичної вестибулярної системи (внутрішнього вуха). У разі травм, отриманих під час війни, лЧМТ часто пов’язана з вибуховою дією, яка може пошкоджувати внутрішнє вухо. Лікарям важливо розуміти вестибулярні наслідки вибухової лЧМТ, оскільки ЧМТ є дуже характерною для сучасних війн [4]....