Вторичная профилактика инсульта в вопросах и ответах
 Инсульт является одной из основных причин смертности и инвалидизации населения земного шара. По данным Всемирной организации здравоохранения (ВОЗ), в мире насчитывают более 17 млн больных, которые перенесли мозговой инсульт (МИ). Согласно прогнозам экспертов ВОЗ количество инсультов в будущем будет возрастать, что обусловлено постарением населения планеты и ростом распространенности в популяции таких факторов риска, как артериальная гипертензия (АГ), дислипидемия, сахарный диабет, болезни сердца, курение, стрессовые ситуации и др.
Инсульт является одной из основных причин смертности и инвалидизации населения земного шара. По данным Всемирной организации здравоохранения (ВОЗ), в мире насчитывают более 17 млн больных, которые перенесли мозговой инсульт (МИ). Согласно прогнозам экспертов ВОЗ количество инсультов в будущем будет возрастать, что обусловлено постарением населения планеты и ростом распространенности в популяции таких факторов риска, как артериальная гипертензия (АГ), дислипидемия, сахарный диабет, болезни сердца, курение, стрессовые ситуации и др.
В Украине ежегодно около 100 тыс. пациентов переносят МИ. В 2016 году заболеваемость МИ на 100 тыс. населения составила 278,6. В структуре всех МИ лидирующее положение по частоте встречаемости занимает ишемический инсульт (ИИ). Каждый перенесенный ИИ повышает риск развития повторного инсульта, инфаркта миокарда (ИМ) и других сердечно-сосудистых событий. 25-28% всех МИ – это повторные нарушения мозгового кровообращения. Предупредить их развитие возможно путем проведения мероприятий, относящихся к разряду стратегий вторичной профилактики МИ.
? Что такое вторичная профилактика ИИ?
Вторичная профилактика ИИ – система мероприятий, направленная на предотвращение развития повторного инсульта и других сердечно-сосудистых событий у больных, которые перенесли транзиторную ишемическую атаку (ТИА) или инсульт.
? Почему рекомендации по вторичной профилактике МИ включают пациентов, которые перенесли не только МИ, но и ТИА?
Эпидемиологические исследования продемонстрировали высокий риск развития инсульта после ТИА. Так, в течение 48 ч у 10% пациентов после ТИА развивается инсульт, в течение года – у 12-20%, в течение 5 лет – у 30-40%. При этом чаще всего МИ происходят в первую неделю после ТИА. Риск развития инсульта после ТИА сопоставим с риском развития инсульта после инсульта. Кроме того, у 30-38% больных после ТИА развиваются кардиальные события. Поэтому ТИА, как и МИ, в настоящее время признана неотложным состоянием и требует неотлагательного проведения вторичной профилактики.
? Какие существуют рекомендации по вторичной профилактике МИ?
В 2012 году Министерством здравоохранения Украины был утвержден Унифицированный клинический протокол по оказанию помощи больным с МИ (Приказ № 602), в котором изложены основные положения вторичной профилактики МИ. Однако за 5 лет некоторые позиции изменились или добавились. В 2014 году Американской ассоциацией сердца / Американской ассоциацией инсульта (AHA/ASA) были выпущены рекомендации по предупреждению инсульта у лиц, которые перенесли МИ или ТИА. В 2016 году Европейским обществом кардиологов (ESC) был выпущен обновленный вариант рекомендаций по ведению больных с фибрилляцией предсердий (ФП), в которых большой раздел посвящен профилактике инсульта.
В данной статье изложены современные подходы к вторичной профилактике МИ, в том числе и новые положения.
? Какие мероприятия определяют стратегию вторичной профилактики МИ?
Стратегия вторичной профилактики состоит из: 1) определения подтипа первого инсульта или ТИА (атеротромботический, кардиоэмболический, лакунарный, криптогенный); 2) коррекции факторов сердечно-сосудистого риска; 3) назначения статинов; 4) применения антитромбоцитарных препаратов у пациентов с атеротромботическим, лакунарным, криптогенным механизмом МИ или ТИА; 5) применения антикоагулянтов у пациентов с кардиоэмболическим МИ или ТИА; 6) проведения каротидной эндартерэктомии (КЭ) или каротидной ангиопластики.
? Учитывается ли в рекомендациях коррекция образа жизни пациентов?
В рекомендациях AHA/ASA большое внимание уделено изменению образа жизни пациентов, которые перенесли МИ или ТИА, в частности: снижение веса при наличии ожирения; соблюдение средиземноморской диеты, богатой фруктами, овощами и нежирными молочными продуктами; ограничение потребления поваренной соли; регулярная аэробная физическая активность.
Курение. Курящим пациентам рекомендовано бросить курить и избегать пассивного курения (класс рекомендации І, уровень доказательств А).
Употребление алкоголя. Пациентам, которые ранее злоупотребляли крепкими спиртными напитками, следует отказаться от алкоголя или уменьшить его употребление (І, С). В то же время легкое или умеренное употребление алкоголя (не более бутылки пива, стакана вина или 30-60 мл крепких напитков в сутки) снижает риск развития инсульта (І, А). Больным, которые не употребляют спиртные напитки, не следует рекомендовать такую профилактику (IIb, B).
Избыточный вес. Риск развития инсульта линейно увеличивается начиная с показателя индекса массы тела >20 кг/м2. Рекомендуется выявлять ожирение, проводить оценку индекса массы тела. Также рекомендуется снижать массу тела путем снижения калорийности питания, увеличения физической активности (ІІb, С).
Физическая активность. Пациентам, которым не противопоказаны физические нагрузки, следует рекомендовать 3-4 р/нед по 40 мин/день заниматься физической активностью. Достаточной нагрузкой считается та, что вызывает повышенное потоотделение и существенное увеличение частоты пульса. Рекомендуется воздержаться от значительных физических нагрузок (ІІа, С). Если пациент не может передвигаться, рекомендуется комплекс физических нагрузок под наблюдением специалиста.
Питание. Рекомендуется оценивать нутритивный статус больных, перенесших инсульт, для выявления признаков переедания или недостаточного питания (IIa, С). При выявлении дефицита питания строго рекомендуется индивидуальная коррекция диеты (I, B). Целесообразно ограничить употребление соли до <2,4 г/сут. Более строгое ограничение (<1,5 г/сут) также полезно и может способствовать лучшему контролю артериального давления (АД) на фоне антигипертензивной терапии (IIa, С). Следует рекомендовать пациентам придерживаться средиземноморской диеты, которая предусматривает употребление большого количества овощей и фруктов, продуктов из цельного зерна, а также молочных продуктов с низким содержанием жиров, мяса птицы, бобовых, рыбы и орехов. Ограничивается потребление красного мяса и сладостей (IIa, С).
Апноэ во время сна. Апноэ во сне выявляют с частотой 50-75% среди больных, перенесших инсульт или ТИА. Нарушения дыхания во сне ассоциируются с депрессией, повышенной смертностью и худшими функциональными исходами инсульта. Полисомнография может быть рекомендована всем пациентам, даже при отсутствии жалоб на храп (IIb, В). При выявлении апноэ можно рекомендовать использование аппаратов, создающих постоянное положительное давление в дыхательных путях (CIPAP), в качестве эффективного метода лечения (IIb, В).
? Какие факторы сосудистого риска чаще всего требуют коррекции у больных с перенесенными МИ или ТИА?
АГ, дислипидемия, сахарный диабет, апноэ во сне, болезни сердца и др. – наиболее часто встречаемые факторы сердечно-сосудистого риска, воздействие которых продолжается и после перенесенных мозговых катастроф, поэтому требуется их постоянная коррекция.
? До каких цифр необходимо снижать АД у больных после инсульта?
Лечение АГ с целью вторичной профилактики приводит к снижению риска повторного инсульта на 30-40%. Коррекция АД у больного, перенесшего ИИ, направлена не только на снижение АД, но и на его нормализацию. Поэтому рекомендуется регулярный контроль уровня АД у таких пациентов. Пересмотрены целевые значения АД, к которым следует стремиться у пациентов, перенесших инсульт и ТИА: <140/90 мм рт. ст. (IIa, В), а для лиц с перенесенными лакунарными инсультами рекомендуется более низкий уровень систолического АД – <130 мм рт. ст. (IIb, В). Необходим индивидуальный подход к снижению АД с учетом исходного уровня. Данные доказательной медицины дают основание рекомендовать для снижения АД диуретики либо комбинацию диуретиков и ингибиторов ангиотензинпревращающего фермента (I, A). Выбор антигипертензивного препарата определяется индивидуально с учетом их переносимости и коморбидности.
Однако не следует значительно снижать АД у больных с гемодинамическим механизмом развития инсульта или у больных с билатеральным стенозом сонных артерий.
? Каким образом следует проводить коррекцию уровня глюкозы крови?
Необходимо регулярно контролировать уровень глюкозы крови. Коррекцию уровня глюкозы крови рекомендуется осуществлять посредством изменения образа жизни и назначения индивидуальной фармакотерапии.
? Каким пациентам рекомендована терапия статинами?
Терапия статинами рекомендована пациентам, у которых перенесенные ТИА или инсульт обусловлены атеросклерозом и у которых содержание липопротеинов низкой плотности в крови превышает 100 мг/дл (2,6 ммоль/л) независимо от наличия или отсутствия атеросклеротических поражений других локализаций (I, B). Больным с уровнем холестерина липопротеинов низкой плотности <100 мг/дл без доказательств наличия других атеросклеротических поражений также показана терапия статинами для вторичной профилактики инсульта, но с меньшим уровнем доказательств (I, С).
? Какой препарат из группы статинов эффективен, согласно данным доказательной медицины, во вторичной профилактике МИ?
На основании исследования SPARCL показано, что аторвастатин снижает риск развития МИ на 23-25%. Доза аторвастатина назначается индивидуально и может колебаться от 10 до 80 мг/сут.
? Каким пациентам показаны антитромбоцитарные препараты и на сколько процентов они снижают риск развития повторного инсульта?
Пациентам с атеротромботическим или лакунарным механизмом развития перенесенных ТИА или МИ показаны антитромбоцитарные препараты.
Метаанализ 287 многоцентровых исследований с участием 135 тыс. пациентов показал, что применение антитромбоцитарных препаратов позволяет снизить риск развития повторного МИ на 25%.
? Какие антитромбоцитарные препараты применяются во вторичной профилактике МИ?
Ацетилсалициловая кислота – АСК (50-325 мг 1 р/сут), клопидогрель (75 мг 1 р/сут), комбинированный препарат АСК 50 мг + дипиридамол 200 мг с модифицированным высвобождением 2 р/сут.
Выбор антитромбоцитарного препарата должен основываться на оценке подтипа МИ или ТИА, факторов сосудистого риска у каждого больного, эффективности, безопасности и стоимости каждого препарата.
? Показана ли двойная антитромбоцитарная терапия во вторичной профилактике?
Проведенное исследование CHANCE в 114 центрах Китая с включением 5170 пациентов после малого ишемического инсульта или ТИА показало, что комбинация АСК с клопидогрелем эффективна для начальной терапии с первых суток после легкого инсульта или ТИА в течение 90 дней (IIb, B). Не рекомендуется использовать комбинацию АСК с клопидогрелем длительно, так как при этом повышается риск кровотечений (III, A).
Также комбинация клопидогреля и АСК рекомендована пациентам с нестабильной стенокардией, Q-негативным ИМ или недавно проведенным стентированием с продолжительностью терапии до 9 мес.
? Как долго необходимо принимать антитромбоцитарную терапию?
Настолько долго, насколько сохраняется риск развития повторного инсульта. Минимум 9 мес.
? Какие препараты эффективны во вторичной профилактике у больных с перенесенными кардиоэмболическими ТИА или МИ?
Оральные антикоагулянты (при поддержании международного нормализованного отношения (МНО) на уровне 2,0-3,0) снижают риск повторного инсульта у пациентов с неклапанной ФП (как при постоянной, так и при пароксизмальной форме), а также при большинстве других состояний, сопровождающихся кардиальной эмболией.
Терапия антикоагулянтами может быть наиболее эффективной у пациентов с атеромой аорты, аневризмой основной артерии или диссекцией артерий шеи.
? Почему так важно проводить профилактику МИ у пациентов с ФП?
Наличие ФП повышает риск развития ИИ в 5 раз, а повторного – в 2,5 раза. Инсульт, развившийся на фоне ФП, является более тяжелым и чаще приводит к летальному исходу или тяжелой инвалидизации. Кроме того, у пациентов с перенесенными ТИА или МИ с ФП существенно повышается риск развития тромбоэмболических осложнений (ИМ, нестабильной стенокардии, внезапной смерти). Поэтому больные с ФП являются пациентами высокого риска развития мозговых катастроф, коронарных событий.
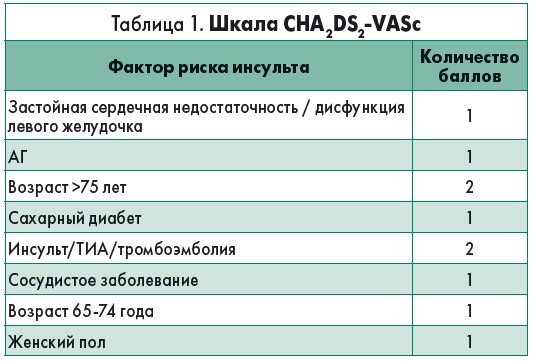
? Как можно оценить риск развития инсульта у больных с ФП?
Для оценки риска развития МИ у больных с ФП используется шкала CHA2DS2-VASс (табл. 1).
? Каким пациентам с ФП в соответствии со шкалой CHA2DS2-VASс показана антикоагулянтная терапия?
Согласно последним рекомендациям ESC по лечению ФП пероральная антикоагулянтная терапия показана всем мужчинам с оценкой ≥2 балла и женщинам с оценкой ≥3 балла по шкале CHA2DS2-VASc (класс рекомендации I, уровень доказательств А).
Необходимо индивидуально рассмотреть назначение пероральной антикоагулянтной терапии мужчинам с оценкой 1 балл и женщинам с оценкой 2 балла по шкале CHA2DS2-VASc (класс рекомендации IIb, уровень доказательств В).
? Оценку по каким еще шкалам необходимо провести пациенту с ФП перед назначением антикоагулянтной терапии?
Подходы к назначению антитромботической терапии у больных с ФП во многом зависят от степени риска кровотечений. Поэтому параллельно с оценкой по шкале CHA2DS2-VASc необходимо определять у каждого пациента риск кровотечений по шкале HAS-BLED (табл. 2).
Риск кровотечений считается высоким при ≥3 баллах.
? Какие антитромботические препараты используют для профилактики инсульта у больных с ФП?
Антитромботическая терапия является эффективным способом снижения риска развития инсульта и других тромбоэмболических осложнений у больных с постоянной и пароксизмальной формами ФП, что подтверждается данными многочисленных исследований. Оральные антикоагулянты (варфарин, дабигатран, ривароксабан, апиксабан) и антитромбоцитарный препарат (АСК в дозе 300 мг) снижают риск развития инсульта.
? Насколько эффективен варфарин в снижении риска развития инсульта у больных с ФП?
В ходе метаанализа данных проведенных исследований было показано, что применение непрямого антикоагулянта варфарина снижает риск развития МИ на 62% у больных с ФП. При этом риск экстракраниальных кровотечений составил 0,3% в год и 0,1% в группе контроля. Прием варфарина позволил снизить общую смертность на 26%. Необходимо строго контролировать при приеме варфарина величину МНО и поддерживать этот показатель в пределах 2,0-3,0.
? Какие недостатки варфарина ограничивают его широкое применение у пациентов с ФП?
В рутинной практике рекомендованный уровень МНО при приеме варфарина в терапевтической дозе, по данным зарубежных исследователей, обеспечивается только в 37% случаев. Это обусловлено многочисленными факторами: взаимодействием варфарина с другими лекарственными препаратами, пищевыми продуктами, отсутствием возможности для регулярного контроля МНО и др. К недостаткам, ограничивающим его применение в клинической практике, относятся: медленное начало и окончание действия, узкий терапевтический диапазон, значительные индивидуальные различия, множество взаимодействий с пищевыми продуктами и другими лекарствами, необходимость в частой коррекции дозы и др. Также у таких пациентов резко увеличивается риск серьезных кровотечений при падении.
? В чем преимущества новых оральных антикоагулянтов (НОАК)?
Анализ проведенных многочисленных исследований показал, что НОАК превосходят по безопасности и не уступают по эффективности варфарину во вторичной профилактике инсульта при ФП. При этом назначение НОАК не требует постоянного контроля антикоагулянтного эффекта. Как следует из последних рекомендаций ESC по ведению пациентов с ФП, необходимо отдавать предпочтение НОАК перед варфарином у пациентов с перенесенным инсультом или ТИА и ФП.
? Какие НОАК и в каких дозах назначают пациентам с ФП?
Ривароксабан в дозе 15-20 мг 1 р/сут, дабигатран в дозе 110 или 150 мг 2 р/сут, апиксабан 2,5 мг 2 р/сут, эдоксабан 30 или 60 мг 1 р/сут.
? Почему во вторичной профилактике у пациентов с ФП используют разные дозы НОАК?
Все зависит от уровня клиренса креатинина. У пациентов с клиренсом креатинина <50 мл/мин доза НОАК должна быть ниже. У пациентов с высоким риском кровотечений (оценка по шкале HAS-BLED ≥3 баллов) также следует рассмотреть снижение дозы НОАК.
Поэтому во время лечения НОАК пациент должен находиться под наблюдением врача с обязательным контролем функции почек. При клиренсе креатинина ≥50 мл/мин – контрольные осмотры каждые 6 мес, при клиренсе креатинина <50 мл/мин – каждые 3 мес.
? Когда нужно начинать прием антикоагулянтов для вторичной профилактики у больных с ФП?
Сроки назначения антикоагулянтов зависят от тяжести мозговой катастрофы, которая определяется по шкале NIHSS. После ТИА антикоагулянты назначаются сразу после проведения нейровизуализации и исключения церебральной геморрагии. После легкого инсульта – на 3-5-й день от начала симптомов. После инсульта средней тяжести – на 5-7-й день от начала симптомов. После тяжелого инсульта – на 2-4-ю неделю от начала симптомов.
? К стратегиям вторичной профилактики относится КЭ. Каким больным она показана?
Показания для КЭ: стеноз сонной артерии >70%, без грубого неврологического дефицита. КЭ проводится больным только в стационарах, где риск операционных осложнений составляет 6%.
Рекомендуется выполнение операции КЭ для некоторых пациентов со стенозом 50-69% (у мужчин с полушарной симптоматикой КЭ может иметь преимущества). Операция КЭ при стенозе 50-69% должна выполняться только в центрах с показателем периоперационных осложнений (любой инсульт и смерть) <3%.
Рекомендован прием антитромбоцитарных препаратов как до, так и после операции КЭ.
Операция КЭ не рекомендована пациентам со стенозами сонных артерий <50%. Таким больным следует назначать медикаментозную профилактику, которая включает антиагреганты, статины и препараты, влияющие на другие выявленные факторы риска (I, А).
?В какие сроки после МИ наиболее эффективна КЭ?
Операция выполняется как можно раньше, лучше всего в течение первых 2 нед после последнего ишемического события (ТИА или МИ).
? В каких случаях проводятся каротидная ангиопластика и стентирование?
В случаях, когда КЭ противопоказана или же при наличии стеноза в отрезке сосуда, недоступном для хирургического вмешательства, можно выполнить чрескожную транслюминальную ангиопластику (ЧТА) и установку стента. Кроме того, ЧТА и установка стента показаны больным с рестенозом после проведенной КЭ.
Такие больные должны получать комбинацию клопидогреля и АСК до и в течение 1 мес после стентирования.
Эндоваскулярные методы лечения могут использоваться у пациентов с симптомным интракраниальным стенозом.
? Чем определяется выбор метода реваскуляризации?
Необходимо учитывать возраст больных при выборе метода реваскуляризации. У пациентов старше 70 лет необходимо отдавать предпочтение КЭ, особенно если анатомические особенности артерий неблагоприятны для выполнения эндоваскулярного вмешательства. У более молодых лиц следует рассмотреть возможность выполнения ЧТА (IIа, В).
? Какой должна быть тактика вторичной профилактики у пациентов со стенозами позвоночных артерий (ПА)?
Стеноз ПА является причиной до 9% заднециркуляторных инсультов.
У пациентов с симптомными стенозами ПА строго рекомендуется придерживаться общих принципов вторичной профилактики инсульта, которые предусматривают назначение антитромбоцитарных средств, снижение уровня холестерина, контроль АД и коррекцию образа жизни (I, C).
Эндоваскулярное стентирование ПА может быть предложено, если симптомы ишемии сохраняются на фоне адекватной медикаментозной терапии (IIb, C).
Открытые вмешательства (вертебральная эндартерэктомия или шунтирование) рассматриваются как альтернатива при неэффективности медикаментозной терапии, но доказательная база также ограничена (IIb, C).
? Какой должна быть тактика вторичной профилактики у пациентов с атеросклерозом интракраниальных сосудов головного мозга?
Пациентам с инсультом или ТИА, вызванными стенозом крупных внутричерепных артерий (ВА) 50-99% просвета, строго рекомендуется профилактическое назначение АСК в дозе 325 мг/сут (I, B). У больных с перенесенными в последние 30 дней инсультом или ТИА и стенозом 70-99% просвета артерии в первые 3 мес для оптимизации профилактики повторных инсультов можно комбинировать АСК с клопидогрелем в дозе 75 мг/сут (ІІb, B).
У пациентов с инсультом или ТИА, которые обусловлены стенозом 50-99% просвета крупной ВА, польза клопидогреля, комбинации АСК с дипиридамолом или цилостазола не установлена (ІІb, С).
? Какой должна быть тактика вторичной профилактики при наличии других факторов риска?
Пациентам с атеромами дуги аорты и перенесенным инсультом показано назначение антитромбоцитарных препаратов (I, А) и статинов (I, В). Хирургическая эндартерэктомия в качестве вторичной профилактики инсульта не рекомендуется (III, С).
Больным с диссекциями сонных или позвоночных артерий после перенесенного инсульта рекомендуется прием антитромбоцитарных препаратов или антикоагулянтов в течение 3-6 мес.
Пациентам с перенесенным инсультом или ТИА и открытым овальным окном, которые не принимают антикоагулянты, показано назначение антитромбоцитарных средств (I, В).
Больным с открытым овальным окном и известными источниками венозной тромбоэмболии (с тромбозом глубоки вен нижних конечностей) показано назначение антикоагулянтов с учетом характеристик перенесенного инсульта (I, А). Если антикоагулянты противопоказаны, следует рассмотреть возможность установки улавливающего фильтра нижней полой вены (IIа, С).
Назначение фолиевой кислоты с витаминами группы B для коррекции гипергомоцистеинемии не оправдано (III, В).
? Насколько можно снизить риск развития инсульта, если соблюдать все рекомендации по вторичной профилактике МИ?
Суммарное снижение риска повторных инсультов при условии четкого следования рекомендациям составляет >50%.
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 1 (44), березень 2018 р.
СТАТТІ ЗА ТЕМОЮ Неврологія
Стрес і тривожність чинять потужний несприятливий вплив і на самопочуття окремих індивідуумів, і на загальний стан здоров’я всієї популяції світу. Цей несприятливий вплив значно підсилили пандемія COVID‑19 та війна в Україні (Celuch M. et al., 2023)....
16-17 лютого в Києві відбувся науково-практичний майстер-клас «Хронічний стрес сьогодення: обрані запитання про здоров’я жінки в різні вікові періоди». Під час заходу виступили фахівці різних спеціальностей, було обговорено важливі аспекти жіночого здоров’я як психологічного, так і фізичного. Доповіді присвячувалися різноманітним питанням, зокрема репродуктивним проблемам, онкологічним захворюванням, психосоматичним розладам. Під час події виступила засновниця Академії довголіття Dr. Skytalinska, віцепрезидент Асоціації дієтологів України, лікар-дієтолог Оксана Василівна Скиталінська. Доповідь Оксани Василівни була присвячена впливу тривалого стресу на харчування та пов’язані з цим наслідки для здоров’я жінок. Окрім пояснення механізмів негативного впливу стресу, під час доповіді лікарка також надала важливі практичні рекомендації стосовно здорового харчування....
Події останніх 5 років є неабияким викликом для психічного стану кожного українця: спочатку – пандемія коронавірусу та запроваджені через неї карантинні обмеження, а далі – повномасштабне російське вторгнення, що триває уже понад 2 роки. Все це спричиняє погіршення психічного здоров’я населення. Такі надзвичайні ситуації, що характеризуються загрозою з невизначеною тривалістю, створюють масивне стресове навантаження, яке підсилюється відчуттям самотності та відчуженості, підвищують тривожність, а також є підґрунтям розвитку психічних розладів. Відомо, що ці стани порушують розумову діяльність, тобто перешкоджають концентрації та аналізу інформації. ...
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....