Cовременные подходы к терапии системных заболеваний соединительной ткани: достижение целей быстро и безопасно
По материалам научно-практической конференции «Родственные группы системных заболеваний соединительной ткани: определение статуса и менеджмент на основе международных стандартов» (22-23 марта, г. Киев)
На заседаниях научно-практической конференции, в которой приняли участие не только ревматологи, но и врачи общей практики, были рассмотрены самые разнообразные вопросы диагностики и лечения ревматических заболеваний: от современных рекомендаций до практических аспектов.
 О возможностях коррекции болевого синдрома при аксиальном спондилоартрите (АСА) рассказал заведующий кафедрой внутренней медицины № 3 Национального медицинского университета им. А.А. Богомольца (г. Киев), доктор медицинских наук, профессор Олег Борисович Яременко.
О возможностях коррекции болевого синдрома при аксиальном спондилоартрите (АСА) рассказал заведующий кафедрой внутренней медицины № 3 Национального медицинского университета им. А.А. Богомольца (г. Киев), доктор медицинских наук, профессор Олег Борисович Яременко.
Лектор отметил, что применение нестероидных противовоспалительных препаратов (НПВП) остается важным аспектом лечения спондилоартритов, что отражено в современных международных рекомендациях. Согласно руководству Международного общества по изучению спондилоартритов и Европейской противоревматической лиги (ASAS/EULAR, 2016) НПВП являются средствами первой линии в терапии АСА. Данные доказательной медицины говорят о том, что сила рекомендаций в отношении эффективности НПВП при АСА сопоставима с таковой для ингибиторов фактора некроза опухоли-α (иФНО-α). В обновленных рекомендациях ASAS/EULAR по лечению АСА указывается, что у пациентов с болью и скованностью НПВП должны использоваться в максимальных дозах; при хорошем ответе и отсутствии противопоказаний целесообразен их длительный прием. При неэффективности минимум двух курсов и/или плохой переносимости НПВП показан переход ко второй фазе лечения: при периферических поражениях могут быть использованы инъекции глюкокортикоидов (ГК) и/или сульфасалазин, при исключительно аксиальных поражениях – биологические болезнь-модифицирующие противоревматические препараты (БМПРП), в частности, рекомендовано начинать терапию с иФНО-α. У больных с высокой активностью заболевания и отсутствием ответа на терапию фазы II рассматривают вопрос о назначении другого иФНО-α или ингибитора интерлейкина‑7.
Важная роль НПВП в лечении АСА подчеркивается и в американских рекомендациях (2015), в которых указано, что при активном АСА показано непрерывное применение НПВП, а при сохранении активности заболевания на протяжении более 3 мес – назначение иФНО-α. У пациентов со стабильной формой АСА НПВП могут применяться по требованию (M.M. Ward et al., 2015).
Профессор О.Б. Яременко обратил внимание слушателей на то, что в Украине БМПРП назначаются и применяются нечасто, что связано с высокой стоимостью этих препаратов. В такой ситуации особую актуальность приобретают высокоэффективные НПВП, безопасные при длительном применении. С этой точки зрения вызывают интерес результаты метаанализа (R. Wang et al., 2016), посвященного сравнению эффективности и безопасности 20 НПВП при спондилоартрите. В метаанализ были включены 26 исследований с участием 3410 пациентов (средний возраст – 41 год, средняя продолжительность спондилоартрита – 11 лет), и было установлено, что в парных сравнениях единственным препаратом, который достоверно превосходил большинство других НПВП по обезболивающему эффекту, был эторикоксиб (Аркоксия®). По результатам данного метаанализа исследователи разместили НПВП на условной оси координат «выраженность обезболивания» и «выраженность побочных эффектов». В соответствии с этими критериями эторикоксиб (Аркоксия®) был помещен в квадрант с максимальным обезболивающим эффектом и минимальным риском побочных явлений (рис. 1).
Рис. 1. Относительная эффективность и безопасность НПВП
Докладчик озвучил также результаты недавнего исследования, проведенного в Испании (J. Gratacos et al., 2016). Участниками исследования стали 57 пациентов с АСА (средний возраст – 43 года) и неэффективной предшествовавшей терапией НПВП (минимум два курса), в связи с чем рассматривался вопрос о переводе на терапию иФНО-α. Пациентам был назначен эторикоксиб (Аркоксия®) в дозе 90 мг/сут на 4 нед; при наличии эффекта курс продлевали до 24 нед. Через 4 нед 46%, а через 24 нед – 33% пациентов достигли хорошего клинического ответа и уже не нуждались в переводе на терапию иФНО-α. Интересно, что через 24 нед наблюдения у 30% участников наблюдалась нормализация уровня С-реактивного белка, хотя, как известно, для традиционных НПВП подобный эффект не характерен.
В 2018 году были получены данные, свидетельствующие об эффективности эторикоксиба (Аркоксия®) в лечении пациентов пожилого и старческого возраста с хронической болью при остеоартрите, у которых ответ на предшествующее применение НПВП или опиатов оказался недостаточным (W.N. Huang, T.K. Tso, 2018). В данное исследование включили пациентов от 79 до 96 лет. Этим больным эторикоксиб назначали в дозе 60 мг/сут на 4 нед, что привело к снижению выраженности боли в 4,5 раза, а также двукратному улучшению функции суставов и уменьшению скованности по шкале WOMAC.
По мнению профессора О.Б. Яременко, высокая аналгетическая эффективность эторикоксиба обусловлена двойным механизмом действия препарата и влиянием не только на периферический, но и на центральный механизм формирования боли. Считается, что примерно у 70% пациентов с хронической суставной болью, в том числе при спондилоартрите, в патогенез боли вовлечены оба механизма.
Центральная сенситизация связана с увеличением чувствительности сенсорных нейронов (прежде всего задних рогов спинного мозга под воздействием болевой импульсации от периферических болевых рецепторов суставов), что приводит к гиперпродукции простагландина Е2 в спинном мозге под влиянием циклооксигеназы‑2. Основными клиническими маркерами центральной сенситизации являются повышение болевой чувствительности на участках, отдаленных от пораженного сустава, и усиление временной суммации боли. Центральная сенситизация может являться причиной неэффективности традиционных обезболивающих средств – парацетамола, ибупрофена и даже опиатов. Очевидно, что эторикоксиб, быстро проникающий в спинномозговую жидкость и воздействующий на центральный механизм формирования боли, имеет преимущество перед перечисленными препаратами.
В ходе доклада были подробно рассмотрены результаты двойного слепого рандомизированного плацебо-контролируемого исследования влияния эторикоксиба (Аркоксии) на механизмы боли у пациентов с болевой формой остеоартрита колена (L. Arendt-Nielsen et al., 2016). Эторикоксиб назначали в дозе 60 мг/сут. В данном исследовании оценивали две группы показателей: количественные биомаркеры боли и клинические параметры. В качестве количественных биомаркеров боли использовали уровень болевого порога, временную суммацию боли, условную модуляцию боли. Клинические показатели оценивали с помощью опросников Brief Pain Inventory, WOMAC, painDETECT. Также оценивалась боль во время ходьбы по ровной поверхности и при подъеме по лестнице. В результате было показано, что эторикоксиб (Аркоксия®) значительно уменьшает локальную и центральную сенситизацию, а также снижает эффект временной суммации боли. Лечение эторикоксибом сопровождалось улучшением клинических показателей, причем наилучшие результаты были получены у пациентов с более высокими исходными показателями центральной сенситизации. Таким образом, чем более была выражена центральная сенситизация, тем большим был обезболивающий эффект при использовании эторикоксиба.
 Важной темой обсуждения на конференции стала терапия сопутствующей патологии при лечении ревматических заболеваний. Этой проблеме посвятил доклад главный научный сотрудник отдела некоронарных болезней сердца и ревматологии ГУ «ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины» (г. Киев), доктор медицинских наук, профессор Олег Петрович Борткевич.
Важной темой обсуждения на конференции стала терапия сопутствующей патологии при лечении ревматических заболеваний. Этой проблеме посвятил доклад главный научный сотрудник отдела некоронарных болезней сердца и ревматологии ГУ «ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины» (г. Киев), доктор медицинских наук, профессор Олег Петрович Борткевич.
Докладчик подробно остановился на проблеме развития системного остеопороза (ОП) при ревматоидном артрите (РА), нарушениях кальциево-фосфорного обмена при данном заболевании и современных возможностях их коррекции.
ОП является характерным заболеванием при РА в связи с аутоиммунным воспалительным процессом, ограничением двигательной функции, приемом некоторых препаратов, прежде всего ГК. В связи с этим пациенты с РА должны не реже чем один раз в два года (некоторые категории пациентов – чаще) проходить рентгенденситометрию костей (DEXA) для раннего выявления и мониторинга ОП. Профилактика прогрессирования ОП включает адекватный уровень приема кальция и витамина D, механическую защиту суставов и позвоночника (индивидуально подобранные ортезы, корсеты), физические упражнения (силовые без весовой нагрузки – отягощений), достаточное воздействие солнечного света, а также отказ от курения и злоупотребления алкоголем.
Согласно рекомендациям Американской ассоциации клинических эндокринологов и Американской коллегии эндокринологов (AACE/ACE Postmenopausal Osteoporosis CPG, 2016) адекватное потребление кальция является основой диетических рекомендаций любой программы по предупреждению или лечению ОП и важной составляющей здорового образа жизни для сохранения здоровья костей в любом возрасте. Для всех взрослых в возрасте старше 50 лет рекомендованная суточная доза кальция составляет 1200 мг (подразумевается потребление кальция с пищей и при необходимости в форме добавок). Доказано, что прием добавок, содержащих необходимые дозы кальция, приводит к повышению минеральной плотности костной ткани, на 15% снижает общий риск переломов, на 30% – риск переломов бедра.
Между тем во всем мире констатируется недостаточное потребление кальция. Так, в США взрослые потребляют в среднем лишь 600 мг кальция в сутки. В Украине 81% женщин в менопаузе получают менее 700 мг кальция в сутки, 47% – менее 400 мг/сут.
Сегодня ученые сходятся во мнении, что у мужчин и женщин со средним и высоким риском развития ОП прежде всего необходима модификация образа жизни. Согласно современным рекомендациям одним из мероприятий по модификации образа жизни является коррекция потребления кальция (1000-1200 мг/сут) и витамина D (600-800 МЕ/сут) с помощью диеты или приема кальциевых комплексов. Особенно это касается категорий пациентов (как мужчин, так и женщин), у которых по разным причинам снижена протекторная функция половых гормонов. В категорию риска попадают в первую очередь женщины с ранней (часто после хирургического вмешательства по поводу фибромиомы) менопаузой. Оптимизация потребления кальция особенно важна для пациентов, длительно принимающих ГК, так как последние стимулируют выведение кальция с мочой. ГК-индуцированный ОП – распространенная проблема, и, согласно рекомендациям Американской коллегии ревматологов (L. Buckley et al., 2017), к группе риска развития ОП относятся все взрослые пациенты, принимающие ГК в дозе более 2,5 мг/сут (в пересчете на преднизолон) на протяжении 3 мес и более.
Докладчик подчеркнул важность соблюдения «коридора нормы» в потреблении кальция: суточная доза более 1500 мг на 40% повышает общую смертность, а менее 700 мг – повышает сердечно-сосудистый риск. Напротив, соблюдение «коридора нормы» и поступление кальция в дозе 500-1000 мг/сут, по данным 10-летнего исследования с участием 9 тыс. женщин в менопаузе, повышало выживаемость этих пациенток в сравнении с женщинами, не получавшими добавки кальция. При этом показатели смертности не зависели от приема витамина D.
При рассмотрении средств, рекомендованных для регуляции кальциево-фосфорного обмена при ОП, профессор О.П. Борткевич отметил, что сегодня на смену средствам первого (простой кальций) и второго (кальций в комбинации с витамином D3) поколений пришли представители третьего поколения, в состав которых входит MCH-Сal™ – микрокристаллический гидроксиапатит кальция в комбинации с факторами роста. MCH-Сal™ способствует стимуляции остеобластов и торможению резорбции костной ткани. Применение MCH-Сal™ рекомендуют для регуляции кальциево-фосфорного обмена при дефиците кальция в организме, ОП, а также для улучшения сращения костей при переломах.
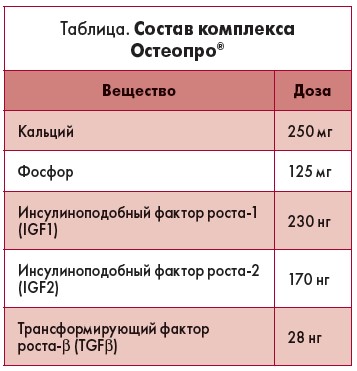 В Украине присутствует комплекс Остеопро®, в состав которого входит MCH-Сal™ (табл.).
В Украине присутствует комплекс Остеопро®, в состав которого входит MCH-Сal™ (табл.).
В ходе доклада были озвучены результаты исследования, проведенного в Оклендском университете (Новая Зеландия), которое продемонстрировало влияние MCH-Сal™ на рост и дифференциацию остеобластов. Согласно полученным данным MCH-Сal™ дозозависимо увеличивает площадь минерализованной костной ткани в культуре первичных остеобластов. Результаты полимеразно-цепной реакции показали, что MCH-Сal™ вызывает усиление экспрессии генов-маркеров дифференциации остеобластов. С помощью метода флуоресцентной микроскопии было установлено увеличение минерализации в трехмерных культурах остеобластов под воздействием MCH-Сal™.
Результаты исследования свидетельствуют о том, что белковые компоненты MCH-Сal™ действуют как анаболические факторы формирования костной ткани, и MCH-Сal™ стимулирует дифференцировку остеобластов и формирование нового костного матрикса. Таким образом, применение комплекса, содержащего MCH-Сal™ (Остеопро®), можно рассматривать как один из эффективных подходов в костнорепаративной медицине.
 В рамках секции, посвященной сложным клиническим случаям в ревматологии, доцент кафедры внутренней медицины № 3 Национального медицинского университета им. А.А. Богомольца, кандидат медицинских наук Дмитрий Леонидович Федьков провел мастер-класс «Локальная инъекционная терапия с использованием ГК».
В рамках секции, посвященной сложным клиническим случаям в ревматологии, доцент кафедры внутренней медицины № 3 Национального медицинского университета им. А.А. Богомольца, кандидат медицинских наук Дмитрий Леонидович Федьков провел мастер-класс «Локальная инъекционная терапия с использованием ГК».
Докладчик отметил, что внутрисуставные инъекции ГК применяются в Украине значительно реже, чем в западных странах, и преимущественно их выполняют травматологи, реже – ревматологи, а врачи общей практики с данной методикой практически незнакомы.
Д.Л. Федьков подробно остановился на некоторых нюансах проведения внутрисуставных инъекций ГК и озвучил практические рекомендации по проведению процедуры: 1) соблюдать правила асептики и антисептики, для суставов стопы проводить двойную обработку места введения йодом и спиртом, отдавать преимущество предварительно наполненным шприцам; 2) всегда аспирировать максимально возможное количество жидкости; 3) не использовать для внутрисуставного введения анестетики из-за их доказанного хондродеструктивного воздействия; 4) не следует вращать иглу внутри сустава; 5) антибиотики вводить в сустав нецелесообразно; 6) промывание сустава не является правилом, его обычно проводят при инфекционных артритах в стационаре; 7) после внутрисуставного введения ГК с целью замедления распространения препарата по лимфатическим путям необходимо максимально ограничить движения в суставе до 24 ч; 8) доза ГК для введения зависит от размера сустава и составляет: для крупных (коленных/голеностопных) суставов – 1 мл, средних (локтевых/ лучезапястных) – 0,5-1 мл, мелких (межфаланговых/ плюснефаланговых) – 0,1-0,5 мл.
Рекомендуемые интервалы: инъекции ГК в коленный и тазобедренный суставы следует делать не чаще 1 раза в 3 мес, в другие суставы – не чаще 1 раза в 1,5-2 мес.
При неэффективности первой инъекции повторное введение в тот же сустав возможно через 1-2 нед. Следует рассмотреть смену доступа, возможно – препарата.
При неэффективности двух инъекций следует прекратить введение и пересмотреть диагноз.
Безусловно, внутрисуставные инъекции ГК пролонгированного действия не должны быть единственным методом лечения заболеваний суставов (кроме посттравматических или постоперационных синовитов/артритов, периартритов, ганглионитов, не ассоциированных с хроническими артропатиями тендовагинитов и бурситов, а также случаев непереносимости базисных препаратов).
Внутрисуставные инъекции ГК могут быть выполнены на фоне приема НПВП (после инъекции их следует при первой возможности отменить) и/или «хондропротекторов» (SYSADOA), в том числе внутрисуставных инъекций гиалуроновой кислоты. Физиотерапевтические процедуры, за исключением фонофореза с гидрокортизоном, могут назначаться не ранее чем через 3 дня после внутрисуставной инъекции ГК пролонгированного действия.
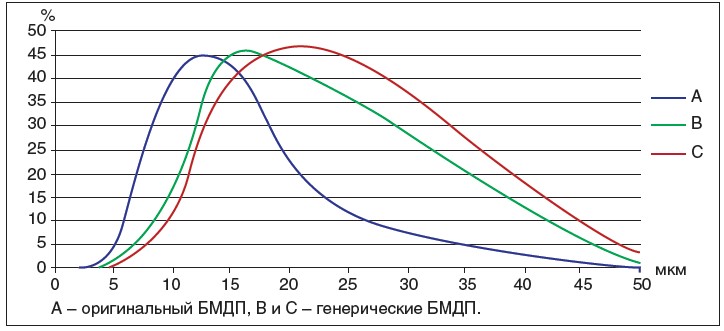
Особое внимание при проведении внутрисуставной инъекции ГК пролонгированного действия следует уделять выбору препарата, отдавая предпочтение оригинальным средствам, которые доказали свою эффективность и безопасность. В пользу такого решения свидетельствуют данные некоторых исследований, демонстрирующие наличие значительных отличий между оригинальными препаратами и генериками, которые могут отразиться на результатах процедуры. Так, при сравнении оригинального и двух генерических препаратов, содержащих бетаметазона дипропионат (БМДП) и бетаметазона натрия фосфат, было выявлено, что БМДП в оригинальном препарате характеризуется значительно более низкой скоростью осаждения суспензии в шприцах после добавления лидокаина. При микроскопии было обнаружено, что основную массу суспензии оригинального БМДП составляют частички меньшего размера (от 5 мкм), чем у генериков (от 10 мкм) (рис. 2).
Рис. 2. Отличия в размерах частиц суспензий БМДП (счетчик частиц)
При тестировании биодоступности бетаметазона была также обнаружена разница в растворимости кристаллов бетаметазона: за тестовое время растворилось 99,8% кристаллов бетаметазона оригинального препарата и только 66 и 53% кристаллов – у генериков.
Больший размер и худшая растворимость кристаллов БМДП в исследованных генерических препаратах могут стать причиной снижения терапевтического эффекта из-за неравномерного распределения суспензии в суставе (вследствие уменьшения площади взаимодействия с синовиальной оболочкой) и хондродеструктивного воздействия вследствие низкой растворимости суспензии.
В Украине оригинальный БМДП зарегистрирован под торговым названием Дипроспан®, который выпускается как в ампулах, так и в инновационной форме – в виде предзаполненного шприца. Преимущества такой формы препарата включают удобство в использовании, уменьшение времени подготовки манипуляции, существенное снижение риска развития инфекционных осложнений. В комплект входят две иглы с силиконовым покрытием и специальной антитравматичной заточкой, что позволяет снизить риск травматизации тканей. Также очень удобной в использовании является специальная усиленная система крепления иглы на конусе шприца, которая усиливает плотность фиксации и предупреждает подтекание препарата при инъекции.
Подводя итоги обзора, следует отметить, что прошедшая конференция продемонстрировала очередные достижения украинской ревматологии, большое желание ученых внедрять самые современные подходы к диагностике и лечению ревматических заболеваний в клиническую практику и стремление практических врачей повышать уровень образования и совершенствовать практические навыки.
Подготовила Екатерина Ткаченко
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (56) Квітень 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...