У пацієнтів з болем диклофенак забезпечує потужну антидепресивну й анксіолітичну дію
Серед усіх захворювань депресивні розлади займають третє місце за економічними та соціальними втратами. У більшості країн розповсюдженість депресії протягом життя людини становить 8-12%. Стандартне лікування депресії включає 5 основних класів антидепресантів, які діють на моноамінові нейротрансмітерні шляхи. Приблизно половина пацієнтів, які приймають антидепресанти, припиняють лікування передчасно через пізній початок ефекту, побічні реакції та страх залежності. Згідно з результатами дослідження STAR*D, у якому вивчалися селективні інгібітори зворотного захоплення серотоніну, інгібітори зворотного захоплення дофаміну-норадреналіну та інгібітори зворотного захоплення серотоніну-норадреналіну, навіть за високого комплаєнсу і доброї переносимості частота ремісії депресії після двох спроб призначення антидепресантів становить близько 50%. У дослідженнях, де використовували 4 класи антидепресантів, цей показник вдалося підвищити до 67%. На жаль, це означає, що третина пацієнтів мають резистентну до лікування депресію. До того ж доведено, що всі антидепресанти незалежно від класу підвищують ризик повторного інсульту (Juang H.-T. et al., 2015), тож при їх призначенні потрібно враховувати і цей фактор.
 У пацієнтів з депресією як основну або допоміжну терапію часто застосовують лікарські засоби, що не є класичними антидепресантами, наприклад кетамін, міноциклін і нестероїдні протизапальні препарати (НПЗП), зокрема целекоксиб, аспірин і диклофенак.
У пацієнтів з депресією як основну або допоміжну терапію часто застосовують лікарські засоби, що не є класичними антидепресантами, наприклад кетамін, міноциклін і нестероїдні протизапальні препарати (НПЗП), зокрема целекоксиб, аспірин і диклофенак.
У систематичному огляді й метааналізі O. Kohler і співавт. (2014) оцінювали вплив протизапальної терапії на депресивні симптоми. В аналіз включили 14 рандомізованих контрольованих досліджень, з них у 10 вивчалися НПЗП. Виявилося, що в пацієнтів з великим депресивним розладом або депресивними симптомами протизапальна терапія значно зменшує прояви депресії як в разі окремого призначення, так і у вигляді додавання до лікування традиційними антидепресантами.
Прийом протизапальних препаратів збільшував частоту відповіді в 6,59 раза, вірогідність досягнення ремісії – в 7,89 раза. Ефект НПЗП був найбільш вираженим протягом перших 6-8 тижнів терапії. Ризик побічних ефектів, асоційованих з НПЗП, був дуже низьким. Автори дійшли висновку, що протизапальні препарати можна призначати для посилення ефективності антидепресантів або когнітивно-поведінкової терапії, особливо в пацієнтів із м’язово-скелетними чи запальними симптомами.
У 2017 році I. V. Chohen і співавт. проаналізували базу даних системи повідомлення небажаних подій (FAERS) Управління з контролю якості продуктів харчування і лікарських засобів США (FDA) і виявили значне зниження частоти депресії в пацієнтів, які отримували кетамін, міноциклін, ботулінічний токсин або диклофенак, порівняно з хворими, яким призначались інші препарати проти болю.
Нещодавно ця ж група дослідників здійснила повторний аналіз FAERS (2012-2017 рр.), а також бази даних AERS (2004-2012 рр.) з метою більш докладного вивчення порівняльного впливу різних НПЗП на симптоми депресії і тривоги (Makunts T. et al., 2018).
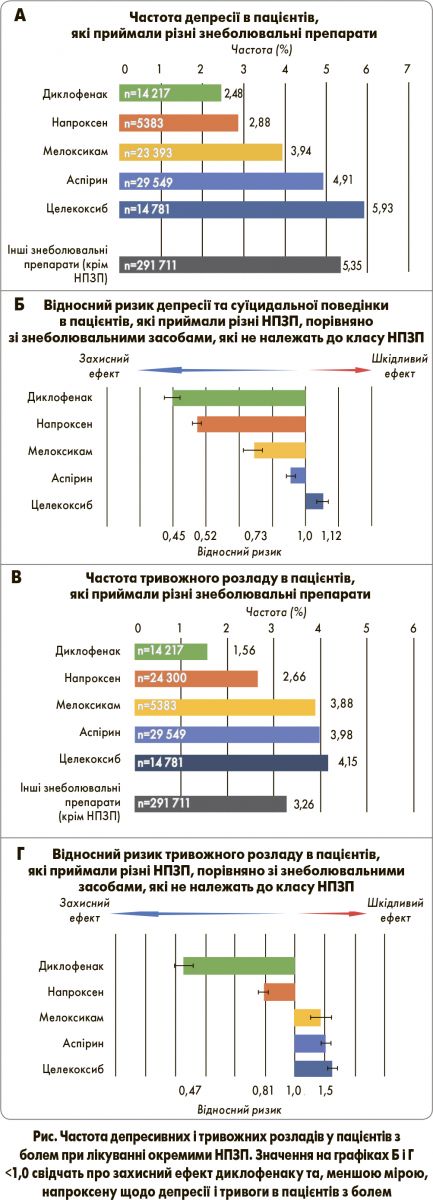
Загалом було проаналізовано 9 220 343 повідомлення про небажані події. З них 582 889 належали пацієнтам, які отримували лікування з приводу болю в спині, головного болю, болю в суглобах, фіброміалгії, периферичної нейропатії, болю в кінцівках і т. ін. Пацієнтів, які одночасно приймали будь-які антидепресанти, з дослідження виключали. У результаті до аналізу включили 430 783 повідомлення, які розділили на 2 групи залежно від того, приймали пацієнти НПЗП (n=139 072) або інші знеболювальні препарати (n=291 711). У групі НПЗП оцінювали ефекти окремих представників цього класу, зокрема диклофенаку, напроксену, аспірину, целекоксибу та мелоксикаму. Для кожного НПЗП розрахували частоту депресії та тривоги, а також відносний ризик цих подій порівняно з такими для лікування знеболювальними препаратами інших класів.
Проведений аналіз показав, що порівняно з іншими препаратами в пацієнтів, які отримували НПЗП, зменшувалася частота депресії і підвищувалася частота тривоги. Різниця була невеликою в абсолютних цифрах, проте статистично значимою. Натомість у пацієнтів, які приймали диклофенак, достовірно зменшувалася частота як депресії, так і тривоги; до того ж захисний ефект щодо депресії був значно більшим порівняно з НПЗП в цілому. Порівняно з іншими знеболювальними препаратами (не НПЗП) лікування диклофенаком асоціювалося зі зниженням ризику депресії на 55% і тривоги на 53%. Мелоксикам та аспірин дещо зменшували частоту депресії, проте підвищували частоту тривоги. Лікування целекоксибом асоціювалося з одночасним підвищенням ризику депресії / суїцидальної поведінки та тривоги (рис.).
Отже, аналіз баз даних FAERS та AERS з великою вибіркою пацієнтів з болем (понад 400 тис.) показав, що окремі НПЗП, передусім диклофенак, забезпечують виражені захисні ефекти щодо депресії та тривоги. Важливо, що ці ефекти не є специфічними для всього класу НПЗП.
На думку авторів дослідження, унікальні психіатричні ефекти диклофенаку і напроксену є підставою для впровадження нової термінології. Цей клас препаратів можна називати анксіолітичними антидепресивними нестроїдними протизапальними препаратами – АА-НПЗП (Anxiolytic Antidepressant Non-steroidal Anti-inflammatory Drugs, AA-NSAID). З огляду на високу коморбідність тривоги/депресії та хронічних больових синдромів клініцисти мають враховувати, що деякі НПЗП можуть погіршувати депресивні та/або тривожні симптоми. У цій ситуації переведення пацієнтів з продепресивних НПЗП на АА-НПЗП може мати додаткові переваги щодо покращення депресивних і тривожних симптомів.
Підготував Олексій Терещенко
Можливі пояснення антидепресивного й анксіолітичного ефектів диклофенаку
Диклофенак був розроблений у 1973 р. як знеболювальний препарат і з того часу широко використовується в усьому світі. Диклофенак є збалансованим інгібітором циклооксигенази (ЦОГ) 1 і 2 типу, завдяки чому забезпечує потужні антипіретичний, аналгетичний і протизапальний ефекти та при цьому добре переноситься. Крім вищезгаданого аналізу FAERS, антидепресивний ефект диклофенаку порівняно з кетаміном вивчався в рандомізованому контрольованому дослідженні M. Jafarinia і співавт. (2016) у пацієнтів з хронічним болем.
Після перорального прийому диклофенак швидко досягає максимальної концентрації в крові (tmax=0,89 год) і проникає крізь гематоенцефалічний бар’єр (Marzo A. et al., 2002; Novakova I. et al., 2014). В експериментальних дослідженнях було встановлено, що диклофенак нормалізує індуковане інтерфероном α підвищення метаболізму моноамінів у центральній нервовій системі (De La Garza R., Asnis G. M., 2003).
У клінічних дослідженнях було доведено, що в пацієнтів з депресією підвищуються рівні запальних медіаторів, зокрема фактора некрозу пухлини (TNF) та інтерлейкіну 1β (IL‑1β). Крім того, розвитку депресії сприяє втрата дофамінергічних нейронів, що пояснює підвищену частоту депресивних симптомів у пацієнтів з хворобою Паркінсона та ефективність такого класу антидепресантів, як інгібітори зворотного захоплення дофаміну та норадреналіну.
В експериментальному дослідженні S. Naafem і співавт. (2015) було встановлено, що диклофенак запобігає втраті дофамінергічних нейронів, нормалізує рівні дофаміну та серотоніну і зменшує концентрації TNF та IL‑1β в головному мозку, і ці ефекти можуть пояснювати його потужний і швидкий (уже після 7 днів лікування) антидепресивний ефект.
На відміну від інших НПЗП диклофенак, крім ЦОГ‑1 і ЦОГ‑2, додатково інгібує 5-ліпоксигеназу (5-ЛОГ) – фермент, що відповідає за продукцію прозапальних лейкотрієнів. Підвищена активність сигнального шляху 5-ЛОГ, який включає білок FLAP, асоціюється з атеросклерозом і підвищеним ризиком інсульту (Radmark O., Samuelsson B., 2007). Крім кардіоваскулярної системи, 5-ЛОГ також експресується в центральній нервовій системі, де функціонує незалежно від системної активності (Chinnici C. M. et al., 2007). У головному мозку 5-ЛОГ бере участь у регуляції рецепторів нейротрансмітерів, зокрема глутамату, і впливає на відкладання β-амілоїду (Chinnici C. M. et al., 2007; Firuzi O. et al., 2008). В експериментальних дослідженнях інгібування 5-ЛОГ забезпечувало антидепресивний ефект (Manev R. et al., 2007). Крім того, продемонстрований зв’язок між активністю сигнального шляху 5-ЛОГ/FLAP/cFOS та симптомами тривоги. Отже, здатність диклофенаку інгібувати 5-ЛОГ може забезпечувати додаткові анксіолітичні й антидепресивні властивості.
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (434-435), липень 2018 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Реімбурсація – це повне або часткове відшкодування аптечним закладам вартості лікарських засобів або медичних виробів, що були відпущені пацієнту на підставі рецепта, за рахунок коштів програми державних гарантій медичного обслуговування населення. Серед громадськості програма реімбурсації відома як програма «Доступні ліки». Вона робить для українців лікування хронічних захворювань доступнішим....
Тіамін (вітамін В1) – важливий вітамін, який відіграє вирішальну роль в енергетичному обміні та метаболічних процесах організму загалом. Він необхідний для функціонування нервової системи, серця і м’язів. Дефіцит тіаміну (ДТ) спричиняє різноманітні розлади, зумовлені ураженням нервів периферичної та центральної нервової системи (ЦНС). Для компенсації ДТ розроблено попередники тіаміну з високою біодоступністю, представником яких є бенфотіамін. Пропонуємо до вашої уваги огляд досліджень щодо корисних терапевтичних ефектів тіаміну та бенфотіаміну, продемонстрованих у доклінічних і клінічних дослідженнях....
Актуальність проблеми порушень моторної функції шлунково-кишкового тракту (ШКТ) за останні десятиліття значно зросла, що пов’язано з великою поширеністю в світі та в Україні цієї патології. Удосконалення фармакотерапії порушень моторики ШКТ та широке впровадження сучасних лікарських засобів у клінічну практику є на сьогодні важливим завданням внутрішньої медицини....
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....




