Зіставні клінічні переваги в разі застосування еналаприлу в цільовій дозі та в дозі, нижчій за цільову, у пацієнтів із серцевою недостатністю в дослідженні SOLVD
Вступ
Серцева недостатність (СН) – це хронічний стан, який є однією з провідних причин захворюваності та смертності [14]. Відомо, що інгібітори ангіотензинперетворювального ферменту (ІАПФ) знижують ризик смерті та частоту госпіталізацій у пацієнтів із СН та зниженою фракцією викиду (ФВ). В основних рекомендаціях з лікування СН зазначено, що терапію ІАПФ слід розпочинати з низьких доз з переходом на вищі цільові дози в разі переносимості [5, 6]. Ця рекомендація частково ґрунтується на результатах подвійного сліпого дослідження SOLVD (Studies of Left Ventricular Dysfunction), в якому пацієнтів було рандомізовано в групи 2,520 мг плацебо чи ІАПФ еналаприлу щодня [7].
Хоча дизайн дослідження SOLVD передбачав вивчення препарату у вищих дозах (20 мг/добу), кінцева середня добова доза еналаприлу становила 11 мг, а під час останнього візиту цільові дози отримували лише 49% пацієнтів обох груп [7]. Отже, сприятливий вплив еналаприлу, відзначений під час випробування SOLVD, не обов’язково є наслідком дії високих доз. Наскільки нам відомо, порівняння 2 доз еналаприлу, що застосовували в SOLVD, ніколи раніше не публікувалися. Метою зазначеного аналізу було вивчити зв’язок прийому цільової та нижчої за цільову доз еналаприлу з наслідками для пацієнта в дослідженні SOLVD.
Методи
Зазначена робота ґрунтується на доступному для широкого загалу описі дослідження SOLVD, отриманому від Національного інституту серця, легень та крові (National Heart, Lung, and Blood Institute), який також спонсорував цей аналіз. Деталі дизайну, методи та результати SOLVD були описані раніше [7].
Загалом кажучи, 2569 пацієнтів із СН зі зниженою ФВ (≤35%), переважно із симптоматикою ІІІІІ класу за NYHA, які перенесли фазу прерандомізаційної стабілізації (прийом еналаприлу в дозі 5мг/добу протягом тижня, одинарне засліплення), були рандомізовані в групи плацебо (n=1284) або еналаприлу (n=1285) у стартовій дозі 5-10 мг/добу (подвійне засліплення).
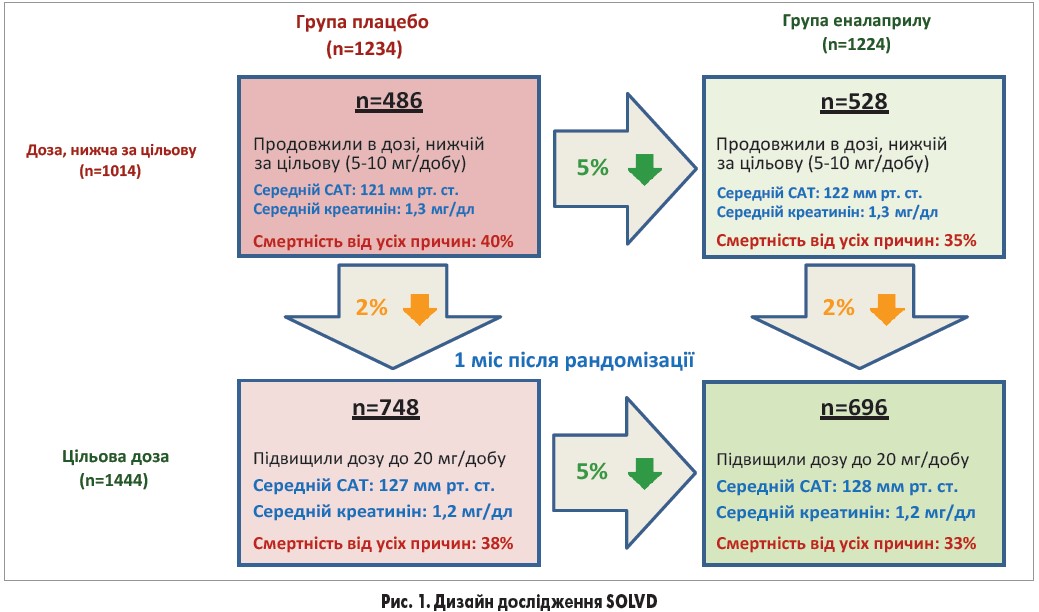
Упродовж місяця після рандомізації відповідно до запротокольованого процесу збільшення доз дослідники в подвійному сліпому режимі збільшували дозу препарату до 20 мг/добу, якщо в пацієнтів не спостерігалося симптоматичної гіпотензії чи погіршення функції нирок [7, 8]. Вказаний аналіз обмежений 2458 з 2569 осіб, які підлягали збільшенню дози. 61% (748 з 1234) пацієнтів групи плацебо та 57% (696 з 1224) учасників групи еналаприлу отримували цільову дозу препарату (20 мг/добу) (рис. 1). Загалом цільову дозу було призначено 58,7% (1444 з 2458) хворих.
Кінцеві точки
Первинною кінцевою точкою аналізу вважалася смертність від усіх причин протягом щонайбільше 4,6 року (у середньому – 2,7 року) спостереження, яка була також первинною кінцевою точкою, власне, дослідження SOLVD [7]. Вторинними кінцевими точками були кардіоваскулярна смертність та смертність від СН; кількість госпіталізацій з приводу СН, інших кардіоваскулярних та будьяких причин; комбінована кінцева точка (госпіталізація з приводу СН + смертність від усіх причин). Усі кінцеві точки були зафіксовані авторами дослідження в кожному центрі його проведення на основі заповнених статистичних таблиць та опитувань членів сім’ї учасників.
Статистичний аналіз
Вихідні характеристики груп учасників дослідження, які отримували цільову та нижчу за цільову дози препарату, порівнювали окремо в групах еналаприлу та плацебо за допомогою тесту хіквадрат або t-тесту Стьюдента. Оскільки дози як еналаприлу, так і плацебо підвищували в подвійному сліпому режимі, для оцінювання дозозалежності відповіді були застосовані 2 окремі підходи.
Поперше, вивчено зв’язок прийому еналаприлу з кінцевими точками окремо в групах цільової дози та дози, нижчої за цільову. Це здійснили за допомогою порівняння наслідків прийому еналаприлу в цільовій дозі з використанням плацебо в цільовій дозі, а далі – порівняння наслідків застосування еналаприлу в дозі, нижчій за цільову, з прийомом плацебо в дозі, нижчій за цільову.
Подруге, автори вивчили зв’язок цільової дози з кінцевими точками окремо в групах еналаприлу та плацебо. Зазначене відбулося за допомогою порівняння наслідків прийому еналаприлу в цільовій дозі з вживанням еналаприлу в дозі, нижчій за цільову, а також порівняння результатів прийому плацебо в цільовій та нижчій за цільову дозах.
Для обох підходів було застосовано мультиваріантну модель пропорційних ризиків Кокса, стандартизовану відповідно до всіх вихідних характеристик учасників дослідження. Для створення кривих виживання груп цільових та нижчих за цільову доз (окремо серед користувачів еналаприлу та плацебо) були використані ті ж самі моделі.
Оскільки систолічний артеріальний тиск (САТ) та креатинін сироватки крові були двома ключовими змінними, що застосовувалися для прийняття рішення стосовно підвищення дози, було проведено додатковий аналіз, який передбачав стандартизацію за цими показниками, з метою оцінювання впливу САТ та креатиніну на зв’язок між дозою та первинними кінцевими точками.
Автори також порівняли загальну кількість госпіталізацій з приводу СН, кардіоваскулярних і усіх причин, протестувавши статистичну достовірність за допомогою t-тесту Стьюдента та тесту Вілкоксона. Дані вважалися достовірними в разі p <0,05. Для всіх проведених аналізів використовували програмне забезпечення IBM SPSS Statistics для Windows, версія 22.0 (IBM Corp., США).
Результати
Вихідні характеристики
У дослідження було включено 2458 пацієнтів середнім віком 60±10 років із середньою ФВ 25±7%; 20% – жінки, 15% – афроамериканці. Середній САТ був вищим, а середній креатинін сироватки нижчим серед хворих, які отримували цільову дозу як плацебо, так і еналаприлу, що відображало потребу та можливість збільшення дози. Загалом середні дози препаратів для пацієнтів груп плацебо та еналаприлу становили 15,6 та 15,2 мг/добу відповідно (p=0,077).
Середня доза препаратів у групі доз, нижчих за цільову, становила 8,8 мг/добу, у групі цільової дози – 20,0 мг/добу (показники не відрізнялися статистично в групах плацебо та еналаприлу). Усі пацієнти групи цільової дози отримували 20 мг препарату на добу. Більшість хворих групи доз, нижчих за цільову, приймали 10 мг препарату на добу (n=774; 76 та 77% пацієнтів груп плацебо та еналаприлу відповідно). Іншими застосовуваними дозами, нижчими за цільову, були 2,5 мг/добу (n=23), 5 мг/добу (n=215), 7,5 мг/добу (n=1), 15 мг/добу (n=1).
Еналаприл та смертність від усіх причин в оригінальній когорті SOLVD
Як було повідомлено в попередніх публікаціях, серед 2569 пацієнтів, залучених до участі в SOLVD, первинної кінцевої точки (смертність від усіх причин) було досягнуто в 40 та 35% пацієнтів груп плацебо та еналаприлу відповідно (співвідношення ризиків (СР) для еналаприлу в порівнянні з плацебо становило 0,84; 95% довірчий інтервал (ДІ) 0,740,96; p=0,008) [7].
Еналаприл та смертність від усіх причин у когорті збільшення дози
Серед 2458 пацієнтів, включених у цей аналіз, смертність від усіх причин була зафіксована в 39% хворих групи плацебо та 34% учасників, які приймали еналаприл (СР 0,83; 95% ДІ 0,730,95; p=0,005).
Еналаприл та кінцеві точки в групі цільової дози
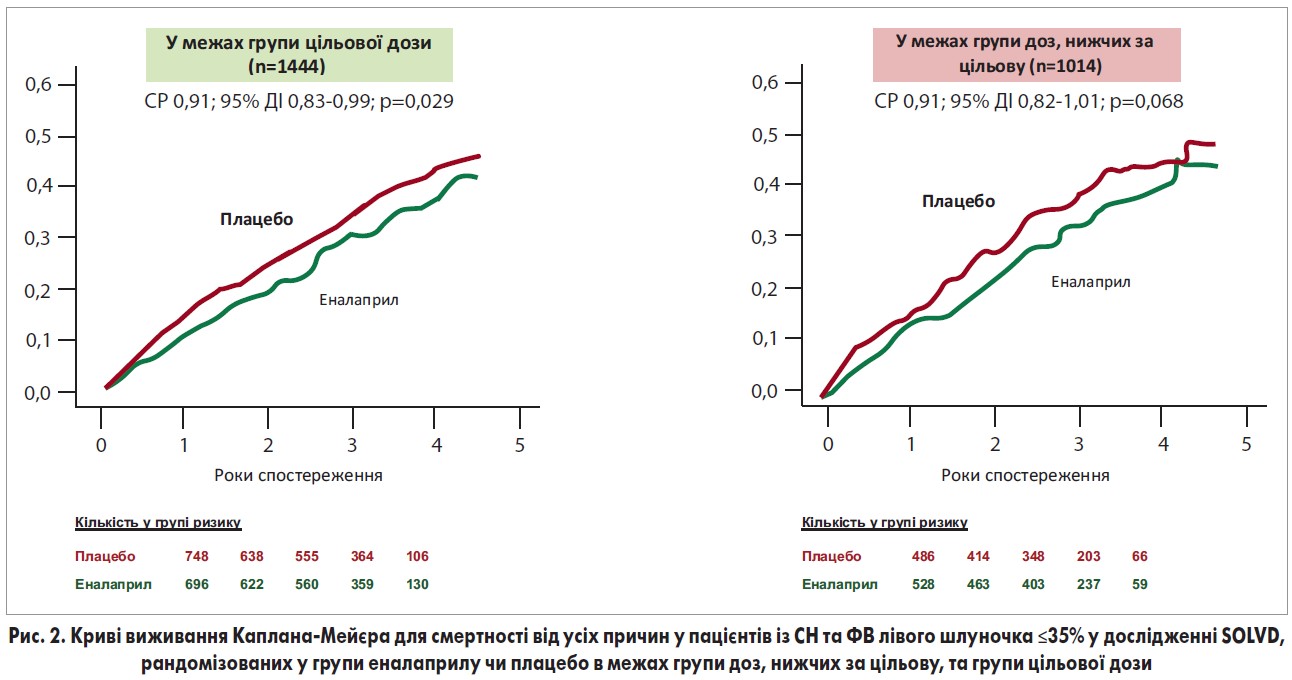
Серед пацієнтів групи цільової дози (n=1444) рівень смертності від усіх причин становив 38% у групі плацебо та 33% в групі еналаприлу (СР 0,91; 95% ДІ 0,830,99; p=0,029) (рис. 2). Ця асоціація залишилася незмінною після мультиваріантної стандартизації ризиків (стандартизоване СР 0,90; 95% ДІ 0,820,98; p=0,017). Прийом еналаприлу в цільовій дозі також асоціювався з меншим ризиком госпіталізацій з приводу СН (стандартизоване СР 0,75; 95% ДІ 0,680,83; p<0,001), та, відповідно, з меншою частотою досягнення комбінованої кінцевої точки (госпіталізація з приводу СН + смертність від усіх причин; стандартизоване СР 0,70; 95% ДІ 0,600,81; р<0,001).
Еналаприл та кінцеві точки в групі доз, нижчих за цільову
Серед хворих відносно меншої групи доз, нижчих за цільову (n=1014), смертність від усіх причин становила 40 та 35% у групах плацебо та еналаприлу відповідно (СР, асоційоване з прийомом еналаприлу в дозі, нижчій за цільову, 0,91; 95% ДІ 0,821,01; р=0,068) (рис. 2). Цей зв’язок залишився незмінним після мультиваріантної стандартизації ризиків (стандартизоване СР 0,90; 95% ДІ 0,811,00; р=0,057).
Еналаприл у дозах, нижчих за цільову, також асоціювався зі зменшенням ризику госпіталізацій з приводу СН (стандартизоване СР 0,79; 95% ДІ 0,710,89; р<0,001) та частоти досягнення комбінованої кінцевої точки (госпіталізація з приводу СН + смертність від усіх причин; СР 0,68; 95% ДІ 0,570,81; р<0,001).
Цільова доза та кінцеві точки в групі еналаприлу
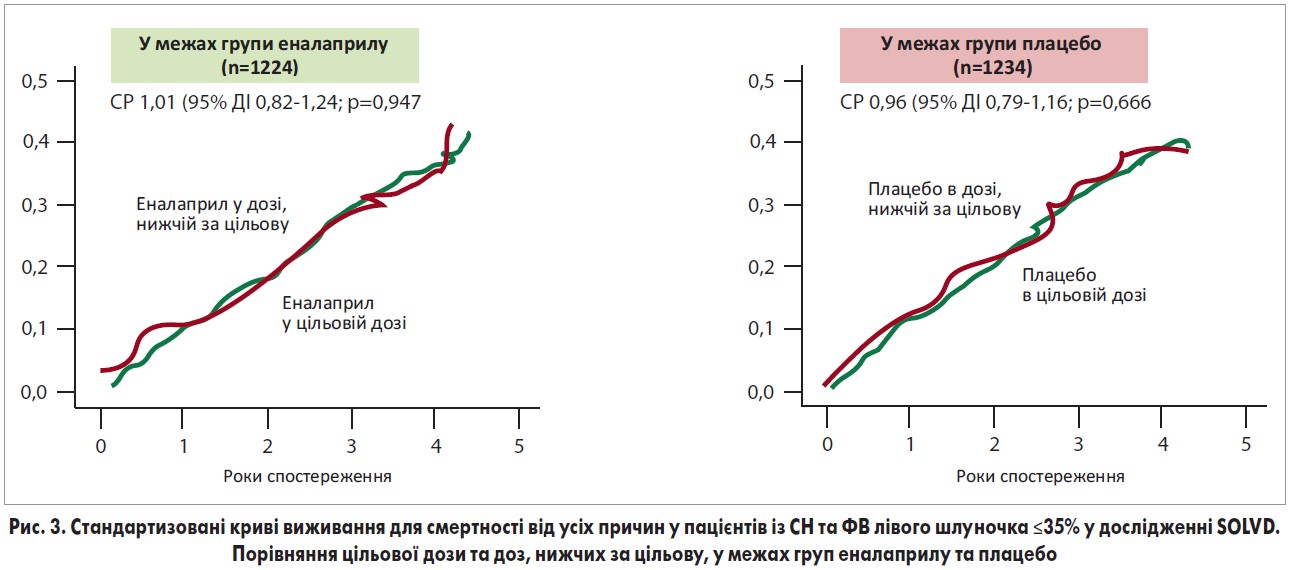
Серед пацієнтів групи еналаприлу (n=1224) смертність від усіх причин становила 35% у групі доз, нижчих за цільову, та 33% в групі цільових доз (СР, асоційоване з прийомом еналаприлу в цільовій дозі, 0,89; 95% ДІ 0,741,09; р=0,26). У разі мультиваріантної стандартизації СР для цього зв’язку становило 1,01 (95% ДІ 0,821,24; p=0,95) (рис. 3). СР, стандартизоване за САТ та сироватковим креатиніном, виявилося на рівні 0,97 (95% ДІ 0,801,18; р=0,76). Прийом еналаприлу в цільовій дозі не асоціювався зі зниженням частоти досягнення комбінованої кінцевої точки (госпіталізація з приводу СН чи смертність від усіх причин): СР 1,04; 95% ДІ 0,871,23; р=0,70.
Цільова доза та кінцеві точки в групі плацебо
Серед учасників групи плацебо (n=1234) смертність від усіх причин була відзначена в 40 та 38% пацієнтів груп доз нижче цільової та цільової дози відповідно (СР, асоційоване з прийомом плацебо в цільовій дозі, 0,91; 95% ДІ 0,76-1,09; р=0,28). У разі мультиваріантної стандартизації СР для цього зв’язку становило 0,96 (95% ДІ 0,79-1,16; р=0,67) (рис. 3). Як і в групі еналаприлу, СР, стандартизоване за вихідним показником САТ і сироватковим креатиніном, співпадало з рівнем СР після мультиваріантної стандартизації (СР 0,98; 95% ДІ 0,81-1,18; р=0,79).
Зв’язок із загальною кількістю госпіталізацій
Серед 2458 пацієнтів, включених до аналізу, у хворих групи еналаприлу спостерігалося на 32% менше госпіталізацій з приводу СН (634 проти 931 у групі плацебо; p<0,001). Між групами різного дозування різниці в частоті госпіталізацій не виявлено (як для еналаприлу, так і для плацебо).
Цільова доза та кінцеві точки в дослідженнях SOLVD, ATLAS, NETWORK та HEAAL
У жодному з вказаних досліджень високі дози ІАПФ чи блокаторів рецепторів ангіотензину ІІ (БРА) не зменшували ризик смерті [9-11]. Частота досягнення комплексної кінцевої точки (смертність + госпіталізація з приводу СН) достовірно зменшилась у 2 з цих досліджень [9, 10]. Оцінка зниження ризику госпіталізацій з приводу СН не була представлена в дослідженні ATLAS [9], а в HEAAL відзначалося достовірне, хоча і незначне 1% зниження частоти подібних госпіталізацій на 100 пацієнто-років спостереження в групі високих доз лозартану [11].
Обговорення
Рost hoc аналіз результатів SOLVD демонструє, що еналаприл у порівнянні з плацебо асоціювався з однаковим зниженням ризику смерті в групі цільової дози та групі доз, нижчих за цільову. Величина абсолютного зниження ризику в цих групах доз була аналогічною результатам дослідження в цілому [7].
При аналізі зв’язку цільових доз і доз, нижчих за цільову, зі смертністю в разі відсутності стандартизації було виявлено однакове помірне статистично незначуще зниження в групах плацебо та еналаприлу, що відображає погрішності відбору пацієнтів та сліпе збільшення дози препаратів.
Брак доказів більших переваг у зниженні смертності на тлі вищої дози, виявлений під час цього аналізу, загалом відповідає результатам попередніх рандомізованих контрольованих досліджень, що порівнювали цільові дози ІАПФ і БРА та дози тих самих засобів, нижчі за цільову [9-11]. Менша частота досягнення комбінованої кінцевої точки в деяких з цих досліджень була зумовлена незначним зниженням частоти госпіталізацій з приводу СН.
Отже, зазначені результати свідчать, що цільова доза ІАПФ не асоціюється з подальшим зменшенням смертності в порівнянні з результатом, досягнутим у разі прийому дози, нижчої за цільову, а інші клінічні переваги цільової дози, якщо й наявні, є помірними.
Відповідно до протоколу сліпе збільшення дози еналаприлу та плацебо в дослідженні SOLVD ґрунтувалося на стані пацієнтів, а саме на відсутності симптоматичної гіпотензії та/або порушення функції нирок. Тобто цей процес міг призвести до відбору пацієнтів з кращим прогнозом до групи цільової дози. Крім того, у хворих, які приймали цільову дозу як еналаприлу, так і плацебо, спостерігалися вищі вихідні показники САТ і нижчі рівні сироваткового креатиніну – характеристики, що пов’язані з кращим прогнозом у пацієнтів із СН [12, 13].
Незначуще абсолютне зниження смертності на 2% (за відсутності стандартизації) при застосуванні еналаприлу в цільовій дозі в порівнянні з прийомом препарату в дозі нижче цільової свідчить, що зниження ризику, пов’язане зі збільшенням дози, було помірним.
Однак можливе інше пояснення, а саме ймовірні погрішності відбору пацієнтів. По-перше, помірна асоціація цільової дози та зниження смертності зникла в разі стандартизації за САТ та сироватковим креатиніном, а по-друге, аналогічні асоціації цільової дози та смертності були зафіксовані в групі плацебо як до стандартизації, так і після неї.
У дослідженні SOLVD еналаприл призводив до значного зниження частоти госпіталізацій з приводу СН [7]. Автори відзначили, що еналаприл у порівнянні з плацебо в обох групах доз (цільова та нижче цільової) асоціювався з однаковим зниженням ризику госпіталізацій з приводу СН; зазначене може свідчити про те, що вища доза не забезпечує більших переваг щодо цього наслідку.
На користь відсутності дозозалежного ефекту свідчить також спостереження, що ні цільова доза еналаприлу, ні цільова доза плацебо жодним чином не впливали на частоту госпіталізацій з приводу СН у порівнянні з дозами аналогічних речовин, нижчими за цільові. Однак, як пояснюється далі, ці результати стосовно госпіталізацій з приводу СН не повністю співпадають з висновками деяких попередніх рандомізованих контрольованих досліджень щодо дозування препаратів [9, 11].
Як було вказано раніше, жодне з 3 рандомізованих контрольованих досліджень, що порівнювали ефекти високих та низьких доз ІАПФ та БРА, не виявило переваг стосовно смертності [9-11]. Два з цих досліджень повідомили про зниження смертності чи частоти госпіталізацій з приводу СН [9, 10], що було зумовлено помірним зниженням ризику госпіталізацій. Однак у жодному з вказаних випробувань не було групи плацебо для порівняння з нею групи низькодозового препарату.
Результати цього аналізу свідчать, що застосування еналаприлу як у цільовій дозі, так і в дозі, нижчій за цільову, асоціювалося з однаковим зниженням ризику госпіталізацій з приводу СН. Дані відповідають результатам нещодавнього дослідження, яке встановило однакову ефективність комбінації сакубітрилу/валсартану в порівнянні з еналаприлом як у групі доз, нижчих за цільову (СР 0,80; 95% ДІ 0,70-0,93; р<0,001), так і в групі цільових доз (СР 0,79; 95% ДІ 0,71-0,88; р<0,001) [14].
Результати цього аналізу мають важливе значення для клінічної практики. Застосування вищих (цільових) доз ІАПФ та БРА пов’язане з помірним зростанням ризику побічних ефектів, у т. ч. гіпотензії, запаморочення, гіперкаліємії, зростання рівня сироваткового креатиніну [9, 15, 16]. Крім того, використання вищих доз зазначених ліків може перешкоджати збільшенню доз бета-блокаторів, антагоністів альдостерону, а також переведенню пацієнта на застосування комбінації БРА та інгібітора неприлізину [6, 17].
Згідно з нещодавнім оновленням настанов з лікування СН рекомендовано застосовувати останню комбінацію (валсартан + сакубітрил) для заміни ІАПФ в амбулаторних пацієнтів з м’якою/помірною хронічною СН зі зниженою ФВ, які переносять високі цільові дози ІАПФ [6, 17].
Дослідження SOLVD було проведено в еру більш ранньої тактики ведення пацієнтів із СН, що може обмежувати інтерполяцію його результатів на сучасних хворих із СН зі зниженою ФВ. Однак це випробування залишається наріжним каменем доказової бази застосування ІАПФ у пацієнтів із СН зі зниженою ФВ. Що важливо, застосування цільових доз ІАПФ у SOLVD часто використовується як аргумент на користь призначення більших доз цих медикаментів, хоча дані стосовно досягнення кінцевих точок у хворих, які приймали цільові дози та дози, нижчі за цільові, раніше не публікувалися.
Зазначений аналіз ґрунтується на результатах дослідження SOLVD і роз’яснює деякі аспекти інтерпретації цих результатів. Оскільки доза в дослідженні не визначалася випадково (рандомізовано), можливі погрішності внаслідок відбору пацієнтів для збільшення дози. Однак на це не слід звертати увагу, адже автори не виявили жодних клінічних переваг серед пацієнтів, які отримували вищу (цільову) дозу та могли мати нижчий ризик через особливості відбору.
Зрештою, аналогічні зв’язки цільової дози еналаприлу та дози, нижчої за цільову, зі смертністю, виявлені в цій роботі, відповідають результатам вивчення цільових доз та доз, нижчих за цільові, препаратів груп ІАПФ та БРА в зниженні смертності в дослідженнях ATLAS, NETWORK та HEAAL [9-11].
Отже, у пацієнтів із СН зі зниженою ФВ, включених у дослідження SOLVD, застосування еналаприлу в цільовій дозі в порівнянні з плацебо в цільовій дозі, а також використання еналаприлу в дозі, нижчій за цільову, у порівнянні з плацебо в дозі, нижчій за цільову, асоціювалося з однаковим зниженням ризику смерті, частоти госпіталізацій з приводу СН чи комбінованої кінцевої точки (госпіталізація з приводу СН + смерть). Автори також виявили, що застосування еналаприлу в цільовій дозі в порівнянні з прийомом еналаприлу в дозі, нижчій за цільову, не асоціювалося з поліпшенням наслідків для пацієнта чи зменшенням загальної кількості госпіталізацій.
Як і результати досліджень ATLAS, NETWORK та HEAAL, отримані дані свідчать, що використання ІАПФ пов’язане з клінічними перевагами для тих, хто може переносити вищу дозу, і для тих, хто не може переносити вищих доз чи не відповідає критеріям для їхнього призначення. Асоційоване зі збільшенням дози зростання клінічних переваг, якщо й наявне, то є помірним.
Lam P.H., Dooley D.J., Fonarow G.C. et al. Similar clinical benefits from below-target and target dose enalapril in patients with heart failure in the SOLVD Treatment trial. European Journal of Heart Failure, 2017.
Переклала з англ. Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 15-16 (436-437), серпень 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...