Розлади здоров’я, асоційовані з синдромом подразненого кишечнику: аналіз реєстру даних первинної ланки надання медичної допомоги
Згідно з сучасними уявленнями, синдром подразненого кишечнику (СПК) є наслідком порушення цереброінтестинальної взаємодії, що клінічно характеризується появою рецидивуючого абдомінального болю, асоційованого зі змінами частоти дефекації та характеру випорожнень [1]. За приблизними оцінками, його поширеність у загальній популяції становить 10% [2].
Вважається, що розвиток СПК є результатом складної взаємодії між біологічними (наприклад, підвищеною проникністю кишечнику, центральною сенситизацією тощо), психологічними (наприклад, тривожністю) та соціальними факторами (наприклад, несприятливими подіями в ранньому дитинстві, відсутністю соціальної підтримки) – тобто йдеться про біопсихосоціальну модель цього захворювання [3]. Згідно з цим концептуальним уявленням, СПК асоціюється з різноманітними медичними, психологічними та соціальними проблемами, включаючи фіброміалгію [4], тривожність і депресивні розлади [5], а також ризик стати жертвою сексуального або фізичного насилля [6]. Whitehead та співавт. [7] порівняли поширеність 76 медичних проблем у пацієнтів із СПК і спеціально підібраних за аналогічними характеристиками осіб контрольної групи, які не мали СПК. Дослідники виявили, що в осіб з СПК частіше виникають різноманітні інфекції (включаючи цистит, уретрит, простатит і респіраторні інфекції), а також розвивається інсульт. Автори цього дослідження припустили, що пацієнти з СПК є уважнішими щодо виявлення у себе соматичних симптомів і можуть мати нижчий поріг скарг для звернення до лікарів – феномен, який не спостерігається при запальних захворюваннях кишечнику (ЗЗК) [7].
Загалом відомо, що коморбідні медичні проблеми можуть виникати ще до розвитку СПК, паралельно з ним або вже після встановлення цього діагнозу, і це може деякою мірою пролити світло на їх роль в етіології СПК. Так, в одному дослідженні повідомлялося, що в осіб без СПК у початкових умовах рівні тривожності були предикторами наявності діагнозу СПК через 12 років, тоді як в осіб з СПК без початкової тривожності наявність цього функціонального гастроінтестинального розладу дозволяла прогнозувати її появу [8]. Інші автори виявили, що розвитку СПК часто передують тривожність [9-11], незадовільна якість сну, нездужання [12] та диспепсія [13]. Таким чином, дослідження супутніх захворювань при СПК може допомогти інтерпретувати медичні проблеми пацієнтів (з урахуванням спільної етіології з СПК і тенденцій у повідомленні лікарів про наявні симптоми).
Однак у більшості досліджень виявлено лише окремі медичні проблеми, пов’язані з СПК, або у них початково використовували катамнестичний дизайн. Отже, наразі складно оцінити, чи слід розглядати ці медичні проблеми як окремі суб’єкти, які мають спільні фактори, котрі збільшують схильність до розвитку СПК, чи пацієнти з СПК справді мають загальне підсилення рівня сприйняття симптомів [7], чи треба розглядати СПК як системне захворювання, при якому можуть виникати проблеми з боку багатьох органів і систем, чи паттерни коморбідності у різних підгрупах пацієнтів відрізняються [14]. Таким чином, існує потреба «вписати» окремі коморбідні стани, що мають місце при СПК, в інтегральну концепцію та зрозуміти, коли саме вони виникають у часі, в зв’язку з встановленням діагнозу СПК. Тому наше дослідження має 3 додаткові мети, досягти яких ми запланували шляхом розгляду реєстру даних первинної ланки надання медичної допомоги в Бельгії. По-перше, мета цього дослідження полягала у тому, щоб ідентифікувати, які саме медичні проблеми асоціюються з СПК. По-друге, ми вивчили, яким чином ці медичні проблеми об’єднуються в межах інтегративної мережі супутніх захворювань при СПК (далі по тексту – карта коморбідності СПК). По-третє, ми з’ясували частоту наявності цих медичних проблем протягом тих років, що передували встановленню діагнозу СПК, та у подальші роки.
Методи
Реєстр даних первинної ланки надання медичної допомоги
У цьому дослідженні як джерело інформації був використаний реєстр даних первинної ланки надання медичної допомоги Intego [15], що функціонує у Фландрії (Бельгія) [16]. Лікарі загальної практики (ЛЗП) використовують програмне забезпечення MediDoc [17] для введення в цей реєстр діагнозів пацієнтів, включаючи ті діагнози, що були встановлені фахівцями вузького профілю (вони вводилися ЛЗП після госпіталізації хворих). Реєстр охоплював період з 1999 по 2015 рр., хоча діагностичні відомості до 1999 р. також враховувалися у дослідженні. Діагнози походили з тезаурусу (уніфікованого зведення термінів) з приблизно 65 000 термінів, які були реструктуризовані шляхом обчислень у 680 унікальних діагнозів згідно з Міжнародною класифікацією первинної медичної допомоги (ICPC‑2 )[18]. Кожен діагноз у ICPC має код, який позначає систему органів однією літерою (наприклад, D – код для системи травлення), а тип діагнозу – цифрою (коди до 30 є діагнозами, що ґрунтуються на симптомах, далі – симптоми, а коди після 70 – діагнози, що ґрунтуються на діагностованих розладах, тобто поділені на інфекції, новоутворення та інші нозології). Іншими зафіксованими в реєстрі даними були ідентифікаційний номер (ІН) ЛЗП, ІН пацієнта, стать, рік народження, рік встановлення діагнозу та роки першого й останнього контакту з ЛЗП.
З метою забезпечення якості й узгодженості даних ми включали лише дані від ЛЗП з оптимальним виконанням реєстрації, яке визначалось за наявністю в середньому більше ніж 1 діагнозу на пацієнто-рік, а також за часткою діагнозів, зареєстрованих без використання ключових слів (менше ніж 50%) та за узгодженими параметрами протягом останніх 3 років. Загалом були включені дані від 79 ЛЗП, що зафіксували 4 254 325 діагнозів згідно з ICPC у 319 068 окремих пацієнтів.
Ключові терміни, використані у цій публікації, наведено у таблиці 1.
Мета 1. Проблеми зі здоров’ям, асоційовані з СПК
Відбір пацієнтів і діагнозів згідно з ICPC. З-поміж 319 068 пацієнтів в аналіз були включені особи з наявністю даних за період як мінімум 10 років з метою зменшення кількості хибнонегативних випадків діагностування СПК. Поріг 10 років був обраний тому, що протягом цього часу поширеність СПК стабільно становила 9% – показник, який узгоджується з результатами епідеміологічних досліджень [2]. У результаті була сформована вибірка з 151 496 пацієнтів, 13 701 з яких мав щонайменше 1 раз вказаний діагноз СПК (код ICPC D93) у своїй електронній медичній документації. Дані 13 701 пацієнта з СПК були зіставлені з такими 2 контрольних груп: пацієнтів без гастроентерологічного діагнозу та пацієнтів з органічним захворюванням ШКТ, але без додаткового СПК (визначено в табл. 1). Зіставлення даних виконували у співвідношенні 1:1 залежно від статі та ІН ЛЗП, віку пацієнта на момент внесення першого запису до документації, року першого звернення та року останнього звернення за медичною допомогою, а також від тривалості періоду контакту та періоду даних. Остаточний аналіз включав дані 11 244 та 7808 пацієнтів з контрольних груп без гастроентерологічних діагнозів і з діагнозом органічного захворювання ШКТ відповідно.
З 680 окремих діагнозів згідно з ICPC ми включили лише діагнози з наявністю як мінімум 20 таких випадків у підібраних групах пацієнтів, оскільки при розрахунку коефіцієнтів ризику ділення на малі числа може призводити до отримання екстремальних значень.
Аналіз даних. Для пацієнтів з СПК та осіб контрольної групи ми отримали інформацію щодо довгострокової поширеності кожного з діагнозів ICPC. Довгострокова поширеність визначається як поширеність протягом періоду, за який ми маємо дані (тобто це не поширеність протягом життя), котрий становить як мінімум 10 років на одного пацієнта. Були обчислені коефіцієнти ризику. Їх статистичну значущість не перевіряли з двох причин: по-перше, статистична значущість майже гарантована з урахуванням великого розміру вибірки, а по-друге – коефіцієнти ризику не будуть відтворюваними і стануть предметом різноманітних систематичних помилок через неоднакову частоту консультацій у ЛЗП при порівнянні групи з позитивним діагнозом із групою без такого діагнозу. Щоб подолати ці обмеження, ми використали методику, яка зазвичай застосовується у генетиці, – аналіз функціонального збагачення [19]. Ця методика підсумовує ранговий порядок коефіцієнтів ризику і становить єдину статистичну процедуру, а не тестування гіпотез для багатовимірних даних. Така методика була застосована до всіх діагностичних категорій (n=16, тобто за літерою кодів ICPC), а також до підрозділів у межах певної категорії, тобто симптомів, інфекцій, новоутворень та інших діагнозів (n~64, тобто 4 набори даних для кожної категорії).
Мета 2. Взаємозв’язок проблем зі здоров’ям у межах карти коморбідності СПК
Відбір пацієнтів і діагнози ICPC. Діагнози за ІСРС були включені на основі їх асоціації з СПК, який є верхнім тертилем коефіцієнтів ризику в меті 1, а довгострокова поширеність становить як мінімум 5% у пацієнтів з СПК. Загалом 28 діагнозів ICPC задовільняли ці критерії. Інші 118 діагнозів ICPC містилися у верхньому тертилі коефіцієнтів ризику в меті 1, проте мали поширеність нижче 5%. Вони були згруповані у 18 новостворених діагностичних пулах (табл. 2).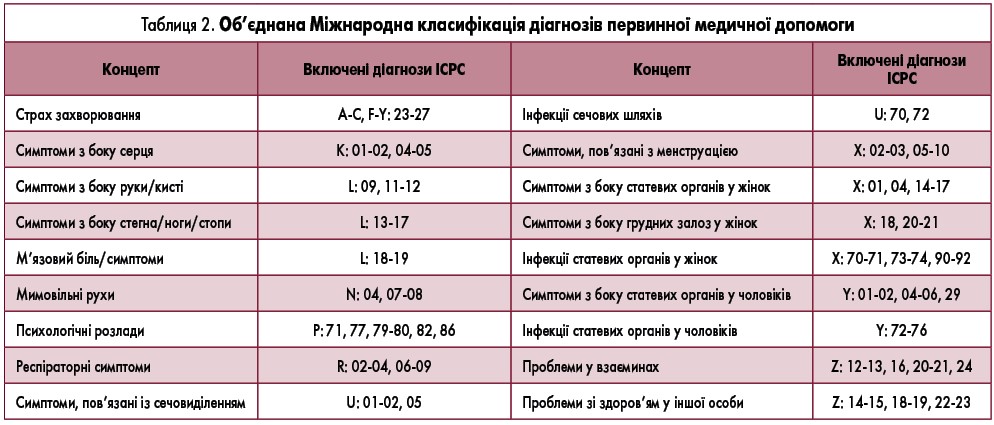
Крім того, ми додали до діагнозів діарею та закреп (коди D11 та D12), щоб зрозуміти, як відрізняється коморбідність у пацієнтів з СПК з різними паттернами консистенції калу. Таким чином, до аналізу увійшло 46 діагнозів ICPC або пулів.
Для кожного з 46 діагнозів ICPC, скажімо, «Х», ми зіставляли пацієнтів з СПК, які мали діагноз «Х», з пацієнтами з СПК без діагнозу «Х» за критеріями, аналогічними таким в меті 1.
Аналіз даних. Ми виконали системний аналіз, щоб підсумувати дані про супутні захворювання при СПК в інтегративній перспективі і вивчити, яким чином їх слід інтерпретувати. Коротко кажучи, ми обчислили коефіцієнти ризику (як в меті 1) для всіх 46 діагнозів ICPC. Отримана в результаті цього матриця коефіцієнтів ризику була логарифмічно трансформована з метою отримання вагової матриці. Коефіцієнти ризику, що ґрунтувалися на менш ніж 20 випадках, були переведені у втрачені дані, і в таких випадках ми вводили середнє значення вагової матриці, оскільки системний аналіз несумісний з відсутніми значеннями. Для створення зваженої системи з 46 діагнозів ICPC використовували R-пакет qgraph [20] із застосуванням алгоритму Фрухтермана – Рейнгольда [21]. У підсумку ми виділили субсистеми діагнозів ICPC на підставі клінічних/концептуальних засад.
Мета 3. Частота проблем зі здоров’ям у роки перед встановленням діагнозу СПК та після нього
Відбір пацієнтів і діагнози ICPC. З-поміж 319 068 пацієнтів 17 301 пацієнт мав діагноз СПК. Пацієнти, які мали діагноз СПК до періоду контакту, були виключені з аналізу, оскільки щільність діагностичних даних до 1999 р. була набагато нижчою. Результатом цього стало формування вибірки з 10 861 пацієнта з СПК, дані яких були зіставлені з даними осіб контрольної групи. Підхід до їх зіставлення відрізнявся від такого в меті 1, оскільки для отримання надійних значень щодо частоти необхідно набагато більше даних, ніж щодо поширеності. Нижче підсумовані розбіжності у стратегії зіставлення між метою 1 та 3. По-перше, 10-річний період даних не був необхідним для пацієнтів з СПК, оскільки він не відіграє ролі в аналізі за один рік, але може застосовуватися щодо осіб контрольної групи з метою запобігання випадкам хибнонегативного діагностування СПК. По-друге, учасники контрольної групи були представлені особами без СПК, а не пацієнтами без будь-якого гастроентерологічного діагнозу з метою максимального збільшення розміру вибірки. По-третє, зіставлення даних здійснювалося у співвідношенні 1:3 як оптимальний розмір вибірки і з погляду надійності. По-четверте, зіставлення даних було також строгим щодо віку, оскільки тут ми отримуємо дані за один рік, а не в довгостроковій перспективі. По-п’яте, ми включали лише контактні дані в межах 10 років до та після першого встановлення діагнозу СПК або (для осіб контрольної групи без СПК) за 10 років до та після того року, в який відповідному пацієнту з СПК був встановлений цей діагноз. По-шосте, діагнози ICPC були об’єднані у пул з використанням субсистем з мети 2 для того, щоб збільшити потужність аналізу; ми також включили інфекції ШКТ (коди D70 та D73) та новоутворення ШКТ (коди від D74 до D78). Ми включили дані 8779 та 26 337 пацієнтів з СПК та осіб контрольної групи, охопивши 89 379 та 268 137 людино-років відповідно.
Аналіз даних. Як у пацієнтів з СПК, так і в осіб контрольної групи без СПК ми обчислили показники частоти на один діагноз ICPC для від -10 до +10 років відносно року діагностування СПК (при 95% довірчому інтервалі) [22]. Роки від -10 до -8, від -7 до -6, від +6 до +7 та від +8 до +10 були об’єднані у пул з метою підвищення статистичної достовірності. Для новоутворень ШКТ ми об’єднали у пул роки від -10 до -1 та від +1 до +10 і виключили рік 0 через міркування потужності та систематичної помилки (є повідомлення про діагностичну плутанину внаслідок наявності перехресних симптомів між СПК і новоутвореннями ШКТ [23]). Показники частоти були розділені залежно від загальної кількості негастроентерологічних діагнозів, встановлених для відповідної групи пацієнтів на певний момент часу, з метою отримання інформації про причини звернення до ЛЗП, а не просто про частоту як таку. Отже, цей аналіз контролює розбіжності в тенденціях консультування ЛЗП пацієнтів з СПК та осіб контрольної групи. Скоректовані показники захворюваності для пацієнтів з СПК та осіб контрольної групи без СПК були розділені, що дозволило отримати дані про скоректовані коефіцієнти захворюваності при 95% довірчому інтервалі. Таким чином, скоректований показник захворюваності вищий за 1,0 свідчить про високу частоту певної патології у пацієнтів з СПК порівняно з особами контрольної групи без СПК, яка не пояснюється узагальненим збільшенням кількості діагнозів ICPC.
Результати
Реєстр даних первинної ланки надання медичної допомоги
СПК був діагностований у 17 301 пацієнта у віці, медіана якого склала 39 років. Органічне захворювання ШКТ було діагностовано у 24 615 пацієнтів (медіана віку – 45 років). Дві третини пацієнтів з СПК становили жінки. Медіана кількості окремих діагнозів згідно з ICPC на одну особу склала 42, 18 і 34 у пацієнтів з СПК, пацієнтів без діагнозу захворювання ШКТ та пацієнтів з органічним захворюванням ШКТ відповідно. З них 25% становили симптоми (коди за ICPC <30), а 75% – інфекції, новоутворення або інші діагнози (коди за ICPC >70).
Мета 1. Проблеми зі здоров’ям, асоційовані з СПК
Пацієнти з СПК мали вищу поширеність 98% діагнозів ICPC порівняно з особами контрольної групи без будь-якого діагностованого захворювання ШКТ. При цьому медіана (та міжквартильний діапазон) коефіцієнтів ризику склала 1,80 (1,48; 2,34). Пацієнти з СПК мали вищу поширеність 79% діагнозів ICPC порівняно з особами контрольної групи з органічним захворюванням ШКТ; медіана (та міжквартильний діапазон коефіцієнтів ризику) – 1,15 (1,03; 1,32).
Коефіцієнт ризику для соматизованого розладу (код за ICPC P75) входив у топ‑10 при порівнянні пацієнтів з СПК з особами обох контрольних груп – без гастроентерологічного діагнозу (4,45) та з органічним захворюванням ШКТ (2,24). Коефіцієнт ризику для вагітності (код за ICPC W78), який розглядався як можливий індикатор технічної системної помилки (оскільки вагітність не може мати ні медичного стосунку до СПК, ні піддаватися впливу з боку персональних тенденцій у консультуванні конкретного ЛЗП [24]), був помірно підвищений при порівнянні пацієнток з СПК з особами контрольної групи без діагностованого захворювання ШКТ (1,45), але не при їх порівнянні з особами з наявним органічним захворюванням ШКТ (1,02).
В цілому у пацієнтів з СПК частіше порівняно з особами контрольної групи без гастроентерологічного захворювання зустрічалися такі діагностичні категорії: психологічні проблеми (P; p<0,001), захворювання жіночих статевих органів (X; p=0,02), патологія чоловічих статевих органів (Y; p=0,05) та соціальні проблеми (Z; p=0,02). Крім того, частіше фіксували симптоми таких категорій: м’язово-скелетні (L; p<0,001), респіраторні (R; p=0,001), загальні (A; p=0,007), урологічні (U; p=0,03) та серцево-судинні симптоми (K; p=0,04). Інфекції жіночих і чоловічих статевих органів зустрічалися частіше (p<0,05), проте цього не спостерігалося щодо новоутворень (у будь-якій категорії). При порівнянні пацієнтів з СПК з особами контрольної групи з наявним органічним захворюванням ШКТ паттерни збільшення частоти вказаних проблем були аналогічними, але різниця – меншою. Результати наведено в таблиці 3.
Мета 2. Взаємозв’язок проблем зі здоров’ям у межах карти коморбідності СПК
Карта коморбідності СПК містила 46 діагнозів ICPC. Психосоціальні та соціальні діагнози ICPC разом зі страхом хвороби сформували окремий перший кластер – «психосоціальні проблеми». Симптоми з боку жіночих і чоловічих статевих органів та інфекції разом з урологічними симптомами й інфекціями сформували другий кластер – «урогенітальні симптоми та інфекції». М’язово-скелетні симптоми сформували третій кластер – «м’язово-скелетні симптоми». Інші різні типи симптомів, такі як загальні, респіраторні, серцево-судинні, неврологічні та шкірні симптоми, разом зі струсом головного мозку, периферичним невритом/нейропатією та гемороєм сформували кластер за назвою «інші соматичні симптоми». Медіани показників відносного ризику у межах зазначених кластерів становили 1,7; 1,4; 1,5 та 1,3 відповідно, а між кластерами – 1,2. Таким чином, наявність однієї супутньої патології підвищувала ризик наявності декількох захворювань у межах усіх кластерів. Закреп був найсильніше пов’язаний з кластером «урогенітальні симптоми та інфекції», тоді як діарея – із кластером «психосоціальні проблеми». Карта коморбідності СПК зображена на рисунку 1.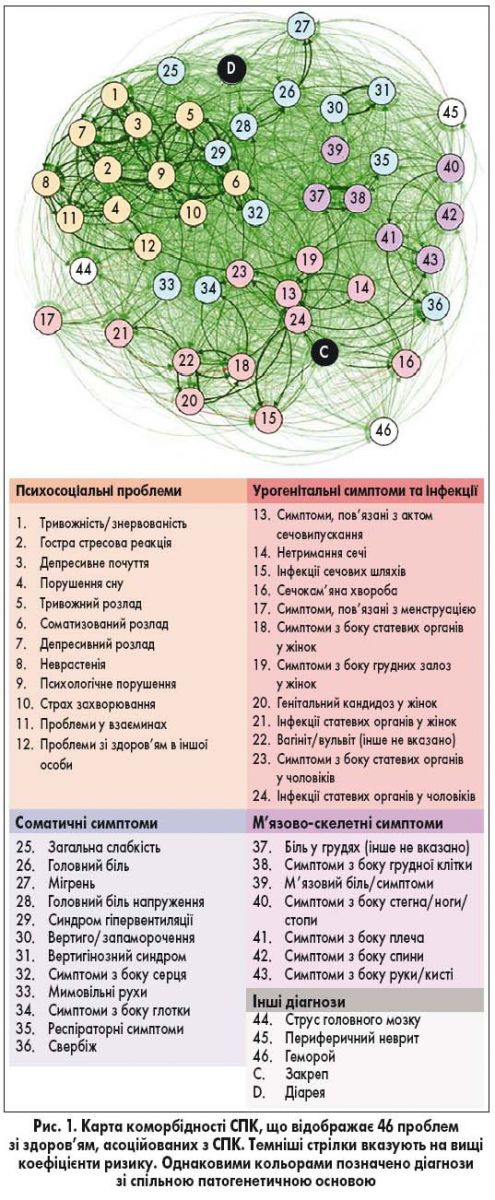
Мета 3. Частота проблем зі здоров’ям у роки перед встановленням діагнозу СПК та після нього
Проблеми зі здоров’ям з 4 кластерів у меті 2 частіше, ніж інші проблеми зі здоров’ям, фіксували в межах 10 років до та після встановлення діагнозу СПК (скоригований показник частоти становив >1,0; рис. 2). Для кластерів «психосоціальні проблеми» та «урогенітальні симптоми та інфекції» скоригований показник частоти був найвищим у рік встановлення діагнозу СПК (1,6 та 1,3). Для кластера «м’язово-скелетні симптоми» він був високим весь час. Скоригований показник частоти проявів з кластера «інші соматичні симптоми» мав тенденцію до деякого зниження після встановлення діагнозу СПК. Пацієнти з СПК мали підвищену частоту розвитку гастроінтестинальних інфекцій як до, так і після встановлення діагнозу СПК (її величина була зіставна з підвищенням частоти урогенітальних інфекцій). Однак підвищення частоти розвитку новоутворень ШКТ не відзначалося (рис. 2).
Обговорення
У цьому дослідженні було продемонстровано, що СПК має спільні тривалі асоціації з багатьма проблемами зі здоров’ям, зокрема:
1) психосоціальними проблемами;
2) урогенітальними симптомами та інфекціями;
3) м’язово-скелетними симптомами;
4) іншими соматичними симптомами, котрі сформували 4 кластери в карті коморбідності СПК.
Більше того, ми показали, що психологічні проблеми й урогенітальні симптоми часто виявляють у той самий рік, що й СПК, вони структурно не передують встановленню діагнозу СПК та не виникають після нього.
Мета 1. Проблеми зі здоров’ям, асоційовані з СПК
Дані про діагностичні категорії, що з більшою частотою виявляли в цьому дослідженні, узгоджуються з даними систематичних оглядів супутніх захворювань при СПК [4, 7, 25-27]. Так, фіброміалгія – стан, клінічна картина якого включає м’язово-скелетний біль, наявна приблизно у третини пацієнтів з СПК та лише у 2% осіб у загальній популяції [28]. Аналогічно цьому дослідженню, Whitehead та співавт. [7] виявили, що багато психіатричних діагнозів та урогенітальних інфекцій частіше фіксують у пацієнтів з СПК, ніж у підібраних контрольних групах осіб без СПК і пацієнтів із ЗЗК. Whitehead та співавт. [7] припускають, що частота урогенітальних інфекцій при СПК може бути вищою, оскільки пацієнти з СПК дуже уважні до виникнення соматичних симптомів і мають низький поріг для звернення за консультацією до лікаря. Наші результати свідчать на користь теорії про посилене сприйняття болю пацієнтами з СПК, оскільки більшість асоційованих з болем станів були представлені у діагностичних категоріях, які частіше зустрічалися у пацієнтів з СПК. Між СПК та урогенітальними інфекціями може існувати патофізіологічний зв’язок. Для того щоб розшифрувати цей зв’язок і його механізми (наприклад, мікробіота [29, 30], імунна система [31], анатомічна близькість [32]), потрібні подальші дослідження, які виходять за рамки даної роботи.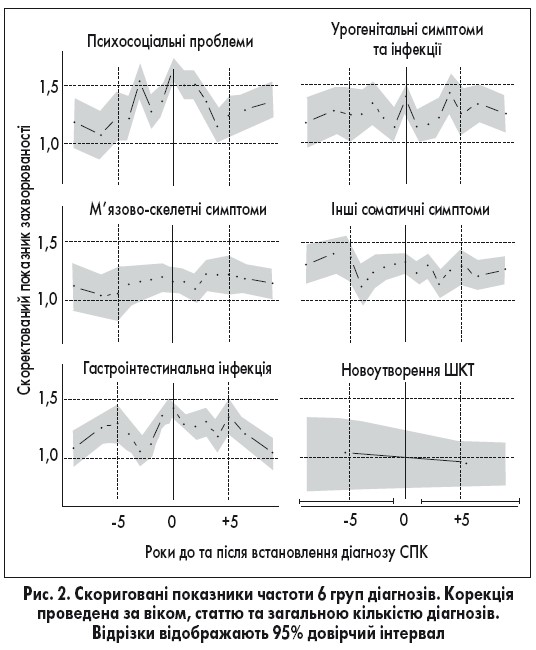
Порівняння пацієнтів з СПК з особами контрольної групи з органічним захворюванням ШКТ надало аналогічні, проте слабші результати, вказуючи на перехрест між профілями коморбідності при СПК та органічному захворюванні ШКТ, при якому психосоціальна, урогенітальна, м’язово-склетна та соматична природа має певну специфічність щодо СПК. Аналогічного висновку дійшли Whitehead та співавт. [7], які виявили, що поширеність соматичних розладів у пацієнтів із ЗЗК була проміжною порівняно з такою при СПК та в осіб контрольної групи без СПК.
Отримані нами результати мають ще кілька аспектів окрім вищевказаних. По-перше, всі діагностичні субкатегорії, що частіше зустрічалися у пацієнтів з СПК, були симптомами, а не новоутвореннями чи інфекціями (за винятком урогенітальних інфекцій), і це підтверджує симптоматичну та доброякісну природу СПК. По-друге, симптоми, що частіше фіксувалися при СПК, охоплювали численні органи та системи, це може свідчити про складну взаємодію між центральними та периферичними процесами. По-третє, профіль коморбідності за наявності органічного захворювання ШКТ був проміжним порівняно з таким в осіб контрольної групи без гастроентерологічного діагнозу та у пацієнтів з СПК. Це свідчить, що більшість супутніх захворювань при СПК первинно не зумовлені таким фактором, як запалення, оскільки саме воно є відмінністю більшості органічних захворювань ШКТ. Таким чином, ми можемо припустити, що центральна сенситизація або інші центральні механізми, які посилюють сприйняття соматичних симптомів, є найбільш сумісними з тим паттерном коморбідності, що спостерігався при СПК.
Мета 2. Взаємодія проблем зі здоров’ям у межах карти коморбідності СПК
Карта коморбідності СПК та її 4 кластери є демонстрацією потенційно пов’язаних супутніх діагнозів, які можуть мати спільні етіологічні фактори або бути важливими з точки зору покращення ведення пацієнтів з СПК. По-перше, якщо пацієнт з СПК повідомляє про біль у зоні сечостатевих органів, то він часто асоційований з інфекціями статевих органів або сечових шляхів, а не з іншими соматичними симптомами. Біль в області сечостатевих органів, таким чином, не повинен одразу ж розцінюватися як частина генералізованої гіперчутливості до болю, зумовленої центральними процесами, а обстеження на наявність урогенітальних інфекцій може виявитися доцільним. По-друге, враховуючи позиціонування закрепу та діареї в карті коморбідності, можуть існувати патофізіологічні асоціації закрепу з урогенітальними інфекціями, а діареї та інфекції ШКТ – з тривожністю, що також спостерігалося у моделях гастроінтестинальних інфекцій у тварин [33]. По-третє, м’язово-скелетні й інші соматичні симптоми не асоціювалися з інфекцією або ураженням і були лише слабко пов’язані з психосоціальними проблемами, що узгоджується з теорією про посилення сприйняття соматичних симптомів як про той первинний фактор, котрий впливає на розвиток супутніх соматичних захворювань при СПК. Хоча окремі компоненти карти коморбідності СПК вже були описані у попередніх дослідженнях [4-7], вона є першим інтегративним зображенням супутніх захворювань при СПК та того, яким чином вони пов’язані один з одним.
Мета 3. Частота проблем зі здоров’ям у роки перед встановленням діагнозу СПК та після нього
Шляхом вивчення показників частоти встановлення певних діагнозів у роки до та після діагностування СПК ми дослідили потенційні механізми розвитку фонової коморбідної патології. Оскільки СПК є розладом цереброінтестинальної взаємодії, деякі дослідження оцінювали часову спрямованість розладів з боку кишечнику та психіки. Було встановлено, що у практиці лікарів первинної ланки охорони здоров’я тривожні розлади часто передують діагностуванню СПК, і ця спрямованість підтримує теорію про те, що тривожність відіграє певну роль у розвитку цього функціонального захворювання (як мінімум, у деяких пацієнтів) [9-10]. Хоча ми також виявили підвищену частоту тривожних розладів у період до встановлення діагнозу СПК, скоригований показник частоти психосоціальних проблем був найвищим саме у рік діагностування СПК. Те ж саме стосується супутніх урогенітальних захворювань, що свідчить про прямий зв’язок між гастроінтестинальними й урогенітальними симптомами або інфекціями. Підвищена частота гастроінтестинальних інфекцій у пацієнтів з СПК порівняно з особами контрольної групи була добре описана (особи з гастроінтестинальними інфекціями більш схильні до розвитку СПК, а пацієнти з попередньою наявністю симптомів з боку ШКТ – до гастроінтестинальних інфекцій [34]; обидва ці явища ми також виявили у цьому дослідженні). Підвищення частоти гастроінтестинальних інфекцій не було більш вираженим, ніж урогенітальних інфекцій.
Paula та співавт. [35] виявили, що некишкові інфекції мають більшу прогностичну значущість щодо розвитку СПК, ніж гастроінтестинальні інфекції. Можливо, некишкові інфекції також можуть виступати тригерами розвитку постінфекційного СПК. Nоrgaard та співавт. [23] проаналізували частоту розвитку колоректального раку у ході дослідження, дизайн якого був дуже схожий на такий нашого дослідження, і встановили відсутність підвищення цього ризику у період між 1-м та 10-м роком після встановлення діагнозу СПК.
Однією з сильних сторін нашого дослідження є його велика вибірка, представлена загальною фламандською популяцією. Крім того, (хоча є багато повідомлень про наявність асоціацій між СПК й окремими супутніми захворюваннями) ми застосували інтегративний підхід – карту коморбідності СПК, що показує підвищення частоти виявлення певних діагностичних категорій при СПК, та безперервну вісь часу для оцінювання спрямованості діагнозів. Основним обмеженням цього дослідження є систематичні помилки у повідомленні інформації ЛЗП. Ми спробували вирішити цю проблему шляхом зіставлення практики різних ЛЗП, виключаючи пацієнтів з коротким періодом даних, та шляхом використання аналізу функціонального збагачення з метою інтерпретації коефіцієнтів ризику. Ми також вирішили, що оптимально буде виключити діагнози ICPC з боку травної системи, інакше це призводитиме до систематичних помилок різних типів (наприклад, збільшення обсягу обстежень ШКТ у пацієнтів з СПК, плутанина у діагнозах) [23, 26]. Друге обмеження полягає у тому, що рік встановлення діагнозу може не збігатися з роком появи симптомів. Тому ми також вибрали інформацію щодо захворюваності протягом 10 років до та після встановлення діагнозу СПК.
Таким чином, СПК має спільні довгострокові асоціації з психологічними проблемами, урогенітальними симптомами й інфекціями, м’язово-скелетними та іншими соматичними симптомами, документально зафіксованими лікарями на рівні первинної ланки охорони здоров’я. Ці асоціації були стійкішими при СПК, ніж при органічних захворюваннях ШКТ, і, ймовірно, можуть бути зумовлені специфічними для СПК факторами (такими як генералізована гіперчутливість до болю), а не зниженням порогу для звернення за консультацією до ЛЗП. Супутні психологічні проблеми й урогенітальні розлади часто діагностували у той самий рік, що й СПК (тобто структурно вони не передували СПК та не виникали за ним). Клініцистам рекомендується обов’язково враховувати супутні захворювання при діагностуванні та лікуванні СПК, оскільки це може мати важливі наслідки для ведення пацієнтів.
Література
1. Mearin F., Lacy B.E., Chang L. et al. Bowel disorders. Gastroenterology. 2016; 150: 1393-1407.
2. Lovell R.M., Ford A.C. Global prevalence of and risk factors for irritable bowel syndrome: a meta-analysis. Clin Gastroenterol Hepatol. 2012; 10: 712-721.
3. van Oudenhove L., Levy R.L., Crowell M.D. et al. Biopsychosocial aspects of functional gastrointestinal disorders: how central and environmental processes contribute to the development and expression of functional gastrointestinal disorders. Gastroenterology. 2016; 150: 1355-1367.
4. Whitehead W.E., Palsson O., Jones K.R. Systematic review of the comorbi-dity of irritable bowel syndrome with other disorders: what are the causes and implications? Gastroenterology. 2002; 122: 1140-1156.
5. Sibelli A., Chalder T., Everitt H., Workman P., Windgassen S., Moss-Morris R. A systematic review with meta-analysis of the role of anxiety and depression in irritable bowel syndrome onset. Psychol Med. 2016; 46: 3065-3080.
6. Walker E.A., Katon W.J., Roy-Byrne P.P., Jemelka R.P., Russo J. Histories of sexual victimization in patients with irritable bowel syndrome or inflammatory bowel disease. Am J Psychiatry. 1993; 150: 1502-1506.
7. Whitehead W.E., Palsson O.S., Levy R.R., Feld A.D., Turner M., Von Korff M. Comorbidity in irritable bowel syndrome. Am J Gastroenterol. 2007; 102: 2767-2776.
8. Koloski N.A., Jones M., Kalantar J., Weltman M., Zaguirre J., Talley N.J. The brain-gut pathway in functional gastrointestinal disorders is bidirectional: a 12-year prospective population-based study. Gut. 2012; 61: 1284-1290.
9. Jones M.P., Tack J., Van Oudenhove L. et al. Mood and anxiety disorders precede development of functional gastrointestinal disorders in patients but not in the population. Clin Gastroenterol Hepatol. 2017; 15: 1014-1020.
10. Sykes M.A., Blanchard E.B., Lackner J., Keefer L., Krasner S. Psycho-pathology in irritable bowel syndrome: support for a psychophysiological model. J Behav Med. 2003; 26: 361-372.
…
36. Spiller R. Is it diverticular disease or is it irritable bowel syndrome? Dig Dis. 2012; 30: 64-69.
Стаття друкується у скороченні.
Повний список літератури знаходиться в редакції.
Clevers E., Vaes B., Henrard S., Goderis G., Tack J., Tornblom H.,
Simren M., van Oudenhove L. Health problems associated with irritable bowel syndrome: analysis of a primary care registry. Aliment Pharmacol Ther. 2018; 47(10): 1349-1357.
Переклала з англ. Олена Терещенко
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3 (49), жовтень 2018 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...




