Палбоцикліб: сучасні можливості в лікуванні гормоночутливого раку грудної залози
 7-8 вересня у м. Кам’янці-Подільському на честь 70-річчя заснування онкологічної служби Хмельницької області відбулася медична наукова конференція «Подільські дні онкології». Лікарі-онкологи з різних регіонів України мали змогу обговорити проблемні питання онкологічної допомоги, сучасні методи діагностики злоякісних новоутворень і найновіші тенденції в розвитку підходів до лікування. Доповідь, присвячену новій стратегії лікування гормоночутливого раку грудної залози (РГЗ), в рамках конференції презентувала лікар-хіміотерапевт, керівник наукового відділу «Клініки Спіженка», кандидат медичних наук, доцент Дінара Есенбенківна Риспаєва.
7-8 вересня у м. Кам’янці-Подільському на честь 70-річчя заснування онкологічної служби Хмельницької області відбулася медична наукова конференція «Подільські дні онкології». Лікарі-онкологи з різних регіонів України мали змогу обговорити проблемні питання онкологічної допомоги, сучасні методи діагностики злоякісних новоутворень і найновіші тенденції в розвитку підходів до лікування. Доповідь, присвячену новій стратегії лікування гормоночутливого раку грудної залози (РГЗ), в рамках конференції презентувала лікар-хіміотерапевт, керівник наукового відділу «Клініки Спіженка», кандидат медичних наук, доцент Дінара Есенбенківна Риспаєва.
Метастатичний РГЗ (мРГЗ) продовжує залишатися невиліковним захворюванням і на цей час розглядається як хронічний процес, що вимагає тривалого лікування з періодичною заміною одних видів терапії на інші. Саме тому найважливішою метою лікування мРГЗ є не тільки збільшення тривалості життя, а й збереження та покращення його якості.
Основою лікування позитивного за рецепторами естрогенів (ER+) HER2-негативного мРГЗ є послідовна гормонотерапія (ГТ). Вона характеризується значно меншою токсичністю, ніж хіміотерапія (ХТ), і забезпечує порівнянні показники виживаності.
Утім, незважаючи на багаторічні дослідження у сфері ГТ мРМЖ, до останнього часу не вдавалося подолати певне плато терапевтичних можливостей: медіана виживаності без прогресування (ВБП) коливалася від 6 міс при терапії тамоксифеном до 12 міс в окремих дослідженнях інгібіторів ароматази, а медіана загальної виживаності (ЗВ) становила близько 3 років. Ситуація дещо змінилася з появою інгібітора mTOR еверолімусу: при додаванні до екземестану він збільшував ВБП, проте істотно не впливав на ЗВ.
Справжнім проривом у лікуванні гормоночутливого РГЗ стало відкриття механізмів регуляції клітинного циклу за участю циклінзалежних кіназ (cyclin-dependent kinase, CDK). CDK – це велике сімейство серин-треонінових кіназ, які діють спільно з білками-партнерами (циклінами). Гіперактивація CDK 4 і 6 типу (CDK4/6) призводить до ініціації проліферації шляхом гіперфосфорилювання білка ретинобластоми (pRb) з подальшим вивільненням раніше блокованих транскрипційних факторів і переходом від фази росту (G1) до фази реплікації (S) ДНК і подальшої клітинної прогресії. При РГЗ з експресією ER втрата контролю над CDK4/6 є ключовим механізмом естрогеннезалежної активації нижчих сигнальних шляхів і, відповідно, розвитком резистентності до ГТ.
Відкриття механізмів регуляції клітинного циклу за участю CDK було удостоєне Нобелівської премії 2001 року в галузі медицини і зрештою привело до створення першого інгібітора CDK4/6 – палбоциклібу (Ібранс, Pfizer). Результати доклінічних досліджень показали, що подвійне інгібування CDK4/6 і сигнального шляху ER створює синергічний ефект, дозволяючи блокувати ріст клітинних ліній ER-позитивного РГЗ у фазі G1 і запобігати розвитку резистентності.
У дослідженні ІI фази PALOMA‑1 було встановлено, що додавання палбоциклібу до летрозолу в 1-й лінії терапії ER+ HER2- мРГЗ у жінок в періоді менопаузи достовірно покращує ВБП, частоту об’єктивної відповіді (ЧОВ), тривалість об’єктивної відповіді і частоту клінічної відповіді. Специфічним і найбільш частим небажаним явищем у комбінованій групі була нейтропенія, пов’язана з впливом інгібітора CDK4/6 на клітини-попередники в кістковому мозку, однак цей побічний ефект був передбачуваним, добре керованим і не призводив до серйозних ускладнень.
У лютому 2015 р. на підставі результатів дослідження PALOMA‑1 Управління з контролю якості харчових продуктів і лікарських препаратів США (FDA) за прискореною процедурою схвалило палбоцикліб для застосування в комбінації з летрозолом у 1-й лінії системної терапії поширеного або метастатичного РГЗ у жінок в постменопаузальному періоді.
У 2016 р. були представлені перші результати аналогічного за дизайном і популяцією пацієнток багатоцентрового рандомізованого плацебо-контрольованого дослідження III фази PALOMA‑2. У дослідження було включено 666 хворих, яких у співвідношенні 2:1 рандомізували на дві групи: палбоцикліб + летрозол і плацебо + летрозол. Первинною кінцевою точкою була ВБП, вторинними точками – ЗВ, ЧОВ, клінічна відповідь і безпека.
Представлені результати відповідали отриманим раніше даним. Медіана ВБП була достовірно більшою при комбінованій терапії і становила 24,8 міс проти 14,5 міс для летрозолу (відносний ризик – ВР – 0,58; р<0,000001). ЧОВ досягла, відповідно, 42,1 проти 34,7% (р=0,031) у всій популяції пацієнток і 55,3 проти 44,4% (р=0,013) у хворих з вимірюваними вогнищами. Клінічна відповідь також реєструвалася частіше в комбінованій групі: 84,9 проти 70,3 (р<0,0001). Аналіз підгруп показав, що палбоцикліб статистично та клінічно значимо збільшував ВБП у всіх підгрупах пацієнток.
Перспективною стратегією 2-ї лінії терапії гормоночутливого мРГЗ є комбінування палбоциклібу з фулвестрантом (антиестрогеном). У багатоцентровому рандомізованому плацебо-контрольованому дослідженні III фази PALOMA‑3 вивчали ефективність і переносимість цієї комбінації у пацієнток з ER+ HER2- мРГЗ з прогресуванням на тлі попередньої ГТ (n=521). Первинною кінцевою точкою була ВБП, вторинними – ЗВ, ЧОВ, клінічна відповідь (об’єктивна відповідь + стабілізація >24 тиж), а також якість життя і безпека. У дослідження включали пацієнток незалежно від менопаузального статусу; жінкам у пременопаузі додатково призначали гозерелін.
У групі з палбоциклібом медіана ВБП сягала 9,5 міс у порівнянні з 4,6 міс при монотерапії фулвестрантом (ВР 0,46; p<0,0001), клінічна відповідь відзначалась у 34 і 19% пацієнток відповідно (р<0,001). У подальшому результати незалежного сліпого центрального контролю ефективності підтвердили статистично і клінічно значиме збільшення ВБП при додаванні палбоциклібу до фулвестранту порівняно з однією ГТ.
Важливо, що вихідний менопаузальний статус не впливав на ефективність лікування палбоциклібом: медіана ВБП була майже однаковою у пацієнток в пре-/перименопаузі та постменопаузі (ВР 0,44 і 0,41 відповідно). Це обґрунтовує застосування зазначеної стратегії в широкій популяції хворих на ER+ мРГЗ. Крім того, підгруповий аналіз продемонстрував перевагу комбінації палбоцикліб + фулвестрант у пацієнток із вісцеральними і невісцеральними метастазами, незалежно від чутливості до попередньої ГТ, статусу рецепторів прогестерону (PR), характеру і кількості ліній попереднього лікування.
Терапевтичні можливості палбоциклібу в лікуванні було продемонстровано на прикладі з клінічної практики.
Під спостереженням перебувала пацієнтка 1980 р.н. з діагнозом раку лівої грудної залози, cT2NxM1 (кістки, печінка), IV стадія. Патологогістологічний висновок (трепан-біоптат) від 14.09.2015 р.: інвазивна протокова карцинома, G2. Імуногістохімічне дослідження від 16.09.2915 р.: ER(+) 80%, PR(+) 70%, HER2/neu (0), Ki67 18%. Мутацій BRCA 1/2 не виявлено.
У вересні 2015 р. у зв’язку з патологічним переломом шийки лівої стегнової кістки була проведена дистанційна променева терапія (ПТ) на лівий кульшовий суглоб (сумарна вогнищева доза – СВД – 30 Гр) з подальшим призначенням ГТ (тореміфен + гозерелін).
У лютому 2016 р. були виявлені нові вогнища в печінці. Призначено ХТ за схемою АТ (доксорубіцин + доцетаксел) 6 циклів, деносумаб, потім тореміфен + гозерелін.
У серпні 2016 р. з’явилися нові вогнища у кістках скелета; наявні множинні метастази в печінці.
У вересні 2016 р. проведена ПТ на кістки таза справа та праву стегнову кістку (СВД 30 Гр), призначено ХТ (бевацизумаб + карбоплатин) 3 цикли, деносумаб, ГТ.
Станом на грудень 2016 р. – позитивна динаміка, солітарне вогнище в печінці (радіохірургічне втручання, сумарна доза 45 Гр), в кістках – початок склерозування.
У березні 2017 р. на тлі ГТ розвинулися нові вогнища в печінці, призначено ХТ за схемою TC (доцетаксел + циклофосфамід) + деносумаб.
Комп’ютерна томографія (травень 2017 р.) показала солітарне вогнище в печінці.
У червні 2017 р. було розпочато ГТ (летрозол + гозерелін) в комбінації з палбоциклібом (Ібранс). Також пацієнтка продовжувала лікування деносумабом.
Позитронно-емісійна томографія з КТ (ПЕТ/КТ), проведена того ж місяця, екстрамамарної метаболічно активної тканини не виявила; у лівій грудній залозі залишався вузол з SUVmax 1,17 (рис.).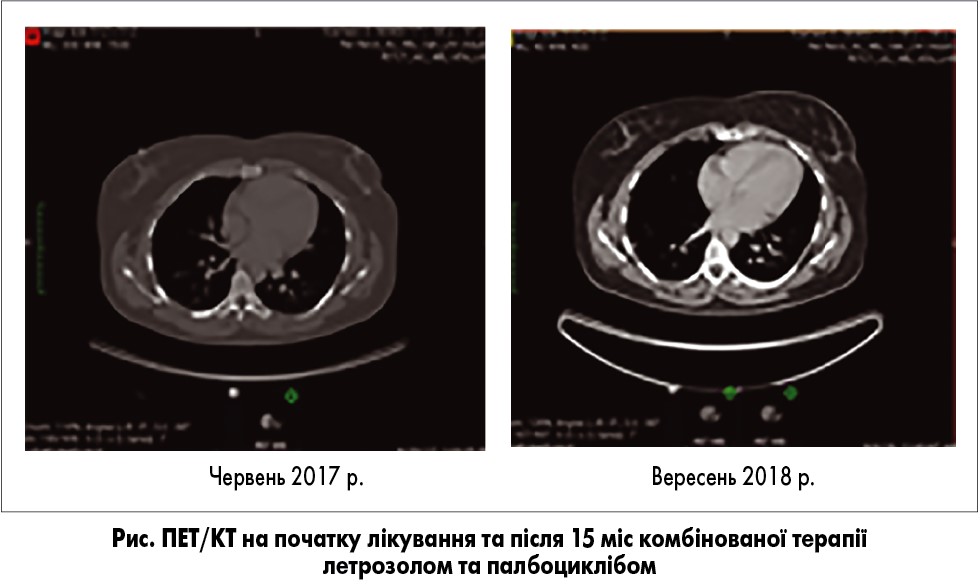
У вересні 2017 р. екстрамамарної метаболічно активної тканини за даними ПЕТ/КТ не виявлено, метаболічна активність вузла в лівій грудній залозі знизилась (SUVmax 0,86), що було розцінено як повна відповідь.
06.10.2017 р. пацієнтці було проведено лампектомію лівої грудної залози та двосторонню аднексектомію з подальшою ПТ на регіонарні лімфатичні вузи та шляхи лімфовідтоку.
З грудня 2017 р. і дотепер пацієнтка продовжує лікування летрозолом, палбоциклібом і деносумабом. Контрольні ПЕТ/КТ-дослідження у березні та вересні 2018 р. метаболічно активної тканини не виявили (рис.).
Таким чином, наведений клінічний випадок демонструє, що при ER/PR-позитивному HER2-негативному мРГЗ комбінація ГТ і палбоциклібу здатна забезпечувати швидку та повну відповідь і її тривале збереження.
Список літератури знаходиться в редакції
Підготував Олександр Гладкий
Надруковано за підтримки
«Пфайзер Експорт Бі. Ві.», що діє через своє Представництво в Україні.
PP-IBR-UKR-0009
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 4 (55), жовтень 2018 р
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




