Антитромбоцитарная терапия и сахарный диабет: как преодолеть барьер истинной резистентности?
По материалам научно-практической конференции «Медико-социальные проблемы артериальной гипертензии в Украине» (30 мая – 1 июня, г. Одесса)
В настоящее время не вызывает сомнения, что высокий уровень смертности у пациентов с сахарным диабетом (СД) в основном обусловлен макрососудистыми осложнениями – инфарктом миокарда (ИМ) и мозговым инсультом. Наличие СД в разы повышает риск возникновения сердечно-сосудистых катастроф, что не в последнюю очередь обусловлено повышенной склонностью к тромбообразованию. Вместе с тем известно, что эффективность основного компонента антитромбоцитарной терапии – ацетилсалициловой кислоты (АСК) – снижена у пациентов с диабетом. Особенностям фармакодинамики антиагрегантов при диабете, а также возможным способам повышения эффективности антитромбоцитарной терапии у таких пациентов посвятил свое выступление член-корреспондент НАМН Украины, руководитель отдела реанимации и интенсивной терапии ГУ «ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины» (г. Киев), доктор медицинских наук, профессор Александр Николаевич Пархоменко.
Профессор А.Н. Пархоменко подробно рассмотрел причины ухудшения тромбогенного статуса пациентов с СД на клеточном уровне, отметив, что тромбоциты – не просто клетки, которые формируют тромб. Тромбоциты выделяют цитокины, влияющие на активность моноцитов и полиморфноядерных нейтрофилов, обусловливая в значительной мере возникновение воспалительного процесса в сосудистой стенке и формирование эндотелиальной дисфункции. При СД происходит увеличение объема и массы тромбоцитов без изменения их количества, а внутри клеток усиливается метаболизм арахидоновой кислоты и синтез тромбоксана А2 (TxA2). Процесс активации тромбоцитов сопровождается также увеличением внутриклеточной концентрации ионов кальция и уменьшением – магния; повышается активность простагландинсинтетазы и протеинкиназы С, снижается синтез и биодоступность оксида азота. Таким образом, активация тромбоцитов является одним из ключевых звеньев в патогенезе прогрессирования сосудистых поражений у пациентов с СД и, заблокировав этот процесс, можно снизить риск многих сердечно-сосудистых осложнений.
Основой антитромбоцитарной терапии в настоящее время остается АСК, эффективность которой в кардиологических дозах убедительно доказана в серии классических исследований и метаанализов, проведенных сообществом исследователей антитромботической терапии (Antithrombotic Trialists’ Collaboration). Если целесообразность назначения АСК в целях первичной профилактики сердечно-сосудистых событий пациентам без установленного атеросклеротического заболевания (ишемической болезни сердца – ИБС, цереброваскулярного заболевания или заболевания периферических артерий) еще обсуждается экспертными обществами и зависит от баланса расчетного индивидуального сердечно-сосудистого риска и риска кровотечений, то роль АСК во вторичной профилактике у лиц, перенесших коронарные события или инсульт, не вызывает сомнений. Рекомендуемые в настоящее время кардиологические дозы АСК для профилактики сосудистых катастроф – 75-162 мг/сут в американских и 75-150 мг/сут в европейских клинических руководствах.
Однако при СД проблема заключается в том, что патофизиологические процессы, происходящие на фоне этого заболевания, препятствуют полной реализации антиагрегантного эффекта АСК, что отражается на клинических исходах. Так, по данным метаанализа Antithrombotic Trialists’ Collaboration, опубликованного в 2002 г., снижение риска сердечно-сосудистых событий при вторичной профилактике в общей популяции пациентов составило 22%, а в подгруппе пациентов с СД – только 7% без статистической достоверности.
Феномен истинной резистентности к терапии АСК у пациентов с СД, безусловно, заслуживает внимания как исследователей, так и клиницистов, ведь именно в этой популяции сердечно-сосудистые риски максимальны и неполноценность антитромбоцитарного действия АСК может оказаться фатальной. В рекомендациях Европейского общества кардиологов (ЕОК) по профилактике сердечно-сосудистых осложнений у пациентов с диабетом и предиабетом в 2013 г. впервые появилось официальное патогенетическое объяснение ослабленного антитромбоцитарного эффекта АСК при СД. Суть объяснения сводится к тому, что прием АСК в низких дозах 1 р/сут может быть ассоциирован с неполным подавлением активности фермента циклооксигеназы-1 (ЦОГ-1) тромбоцитов и сохранением их повышенной активности (обусловленной TxA2). Предполагается, что это происходит вследствие ускоренного обновления популяции тромбоцитов при СД. Другими словами, в 24-часовых интервалах между приемами доз АСК активность ЦОГ-1 может восстанавливаться в достаточной степени, что существенно ослабляет антиагрегантный эффект.
Поддерживающие эту позицию доказательства указывают на потенциально полезные эффекты применения АСК 2 р/сут у пациентов с СД и сердечно-сосудистыми заболеваниями. Проведены исследования, которые показывают, что удвоение дозы и кратности приема АСК у больных диабетом может обеспечить более эффективное ингибирование реактивности тромбоцитов и позволить преодолеть барьер истинной резистентности. Данную гипотезу проверяли в открытом исследовании D. Capodanno и соавт. (2011), в котором изучали эффективность альтернативных режимов дозирования АСК у пациентов с коронарным атеросклерозом и СД, оценивая индуцированную коллагеном агрегацию тромбоцитов. В соответствии с дизайном исследования, пациентов, которые принимали АСК в дозе 81 мг/сут в течение минимум 1 нед, переводили в одну из четырех групп: на прием препарата 81 мг 2 р/сут, 162 мг 1 р/сут, 162 мг 2 р/сут или 325 мг 1 р/сут.
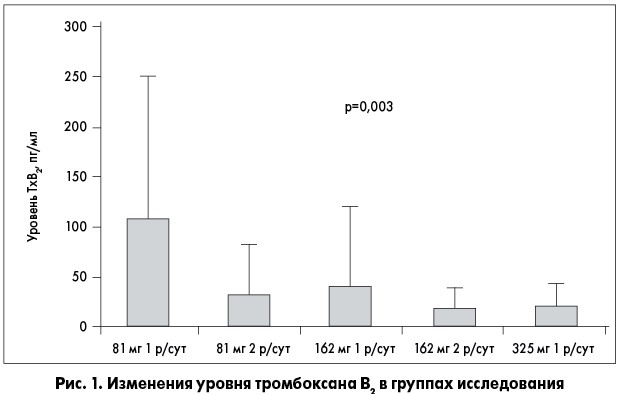 Пациенты контрольной группы продолжали принимать АСК по 81 мг 1 р/сут. Антитромбоцитарный эффект оценивали через 1 нед лечения. Согласно полученным результатам удвоение кратности приема АСК ассоциировалось с достоверной редукцией реактивности тромбоцитов (рис. 1). Стоит отметить, что на сегодня это первое исследование, в котором подтверждено усиление фармакодинамического эффекта АСК при удвоении кратности приема препарата.
Пациенты контрольной группы продолжали принимать АСК по 81 мг 1 р/сут. Антитромбоцитарный эффект оценивали через 1 нед лечения. Согласно полученным результатам удвоение кратности приема АСК ассоциировалось с достоверной редукцией реактивности тромбоцитов (рис. 1). Стоит отметить, что на сегодня это первое исследование, в котором подтверждено усиление фармакодинамического эффекта АСК при удвоении кратности приема препарата.
Целесообразность такого подхода продемонстрирована и в другом исследовании – AVOCADO, в которое включили 304 пациента с СД 2 типа, исходно принимавших стандартную дозу (75 мг) АСК. 90 (35,4%) пациентов с высокой реактивностью тромбоцитов, определенной по коллаген/адреналин-индуцированному времени агрегации (CEPI-CT), рандомизировали к приему двойной дозы АСК (150 мг) или 75 мг клопидогреля. В результате показано, что удвоение дозы АСК привело к достоверной пролонгации времени агрегации и снижению уровня TxB2 в крови (рис. 2).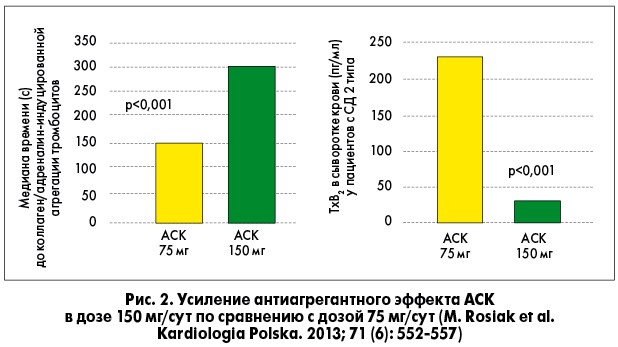
Возможно, результаты этих исследований будут учтены при составлении новых рекомендаций по антитромбоцитарной терапии у пациентов с СД. На сегодняшний же день в инструкциях производителей АСК рекомендован ее прием 1 р/сут в диапазоне от 75 до 150 мг.
В ходе доклада были развенчаны два мифа относительно возможностей преодоления аспиринорезистентности.
Миф 1. Если пациент не чувствителен к АСК, его следует перевести на клопидогрель.
АСК и клопидогрель сопоставимы у пациентов со стабильной ИБС по эффективности, безопасности (в том числе по рискам развития любых кровотечений), а также по частоте развития истинной резистентности к молекуле. Но в соответствии с действующими рекомендациями ЕОК по ведению больных со стабильной ИБС (2013) и Национальным клиническим протоколом (2016) АСК в дозе 75-150 мг показана всем пациентам (класс рекомендации I, уровень доказательств A), а клопидогрель следует использовать в качестве альтернативного средства в случае непереносимости АСК (I, B). Кроме того, АСК является базисным компонентом двойной антитромбоцитарной терапии (ДАТ) у больных с острым коронарным синдромом или после стентирования коронарных артерий, в то время как клопидогрель является дополнительным компонентом.
Миф 2. Лекарственная форма АСК с кишечнорастворимой оболочкой (КРО) уменьшает частоту сердечно-сосудистых осложнений в большей степени из-за пролонгированного действия.
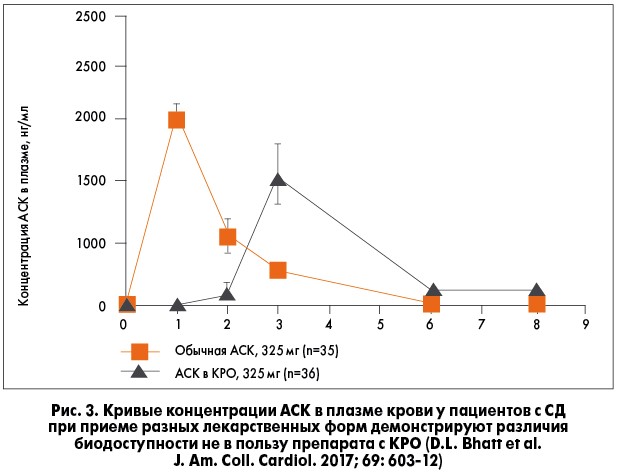 На самом деле замедленное высвобождение АСК и меньшая пиковая концентрация при приеме препарата с КРО препятствуют полной реализации эффекта препарата. Недавно в специальном исследовании было показано, что у пациентов с СД кишечнорастворимая форма АСК недостаточно эффективно подавляет TxB2 из-за сниженной биодоступности (рис. 3). Особенно опасным этот недостаток КРО может быть в острой ситуации – при нестабильной стенокардии, остром ИМ (ОИМ), инсульте, когда необходимо быстро подавить реактивность тромбоцитов.
На самом деле замедленное высвобождение АСК и меньшая пиковая концентрация при приеме препарата с КРО препятствуют полной реализации эффекта препарата. Недавно в специальном исследовании было показано, что у пациентов с СД кишечнорастворимая форма АСК недостаточно эффективно подавляет TxB2 из-за сниженной биодоступности (рис. 3). Особенно опасным этот недостаток КРО может быть в острой ситуации – при нестабильной стенокардии, остром ИМ (ОИМ), инсульте, когда необходимо быстро подавить реактивность тромбоцитов.
Что говорят на этот счет рекомендации? В руководстве ЕОК по ведению пациентов с ОИМ с подъемом сегмента ST (2017) АСК рекомендуется всем пациентам без противопоказаний в первоначальной нагрузочной дозе 150-300 мг/сут и поддерживающей дозе 75-100 мг/сут долгосрочно, независимо от стратегии лечения (высший класс рекомендации и уровень доказательств – I, A).
ДАТ в составе АСК и тикагрелора или прасугреля (или клопидогреля, если тикагрелор или прасугрель недоступны или противопоказаны) рекомендуется в течение 12 мес после чрескожного коронарного вмешательства (ЧКВ), если нет противопоказаний, таких как повышенный риск кровотечения (I, A).
Рекомендации не содержат особых указаний относительно состава и дозировок антитромбоцитарной терапии у пациентов с СД. В руководстве ЕОК по ведению пациентов с ОИМ без подъема сегмента ST (2015) рекомендованы одинаковые подходы к антитромбоцитарной терапии у пациентов как с СД, так и без СД (I, C). Вместе с тем отмечено, что больные СД демонстрируют худший антитромбоцитарный ответ на актуальные режимы применения клопидогреля и АСК и менее благоприятные исходы после ЧКВ и коронарного шунтирования по сравнению с пациентами без СД.
Выводы
- АСК остается основным компонентом антитромбоцитарной терапии кардиологических пациентов, в том числе с СД.
- У пациентов с СД ослабление антитромбоцитарной активности низких доз АСК обусловлено патогенетическими причинами. Эффект АСК у этих больных отличается значительной вариативностью (особенно при использовании лекарственной формы с КРО), что влечет повышение риска тромботических событий.
- На данный момент действующие клинические руководства в целом не предусматривают особых режимов терапии АСК для кардиологических пациентов с СД. Хотя повысить антитромбоцитарную эффективность АСК у этих пациентов возможно ее применением в дозе от 150 мг.
Справка «ЗУ»
Международные и национальные кардиологические общества рекомендуют применять АСК в дозе от 75 мг как для первичной профилактики тромбозов и сердечно-сосудистых заболеваний (например, острого коронарного синдрома) у пациентов с факторами сердечно-сосудистого риска (возраст, пол, артериальная гипертензия, СД, гиперхолестеринемия, ожирение, семейный анамнез сердечно-сосудистых заболеваний), так и для вторичной профилактики с целью снижения частоты тромботических осложнений у пациентов с острой и хронической формами ИБС, заболеваниями периферических артерий и нарушениями мозгового кровообращения в анамнезе. Для достижения максимального антитромбоцитарного эффекта при назначении АСК в низких дозах следует отдавать предпочтение препарату без КРО, обеспечивающему начало всасывания действующего вещества в желудке.
Назначая долгосрочную терапию для профилактики сердечно-сосудистых катастроф, врач должен быть уверен в качестве препаратов.
В Украине представлены препараты АСК европейского производства компании Takeda GmbH (Германия) – Кардиомагнил (таблетки, покрытые пленочной оболочкой; одна таблетка содержит 75 мг АСК) и Кардиомагнил Форте (таблетки, покрытые пленочной оболочкой; одна таблетка содержит 150 мг АСК).
Подготовил Дмитрий Молчанов
Статья печатается при содействии ООО «Такеда Украина».
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (59) вересень-жовтень 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....





