Аспекти вибору між БРА та іАПФ: антигіпертензивна дія, побічні явища, вплив на прогноз
Артеріальна гіпертензія (АГ) – поширена в усьому світі хвороба, ускладнення та наслідки якої супроводжуються високими показниками смертності (NHANES, 2014). Рекомендації Європейського товариства кардіологів та Європейського товариства гіпертензії (ESC/ESH, 2018) стверджують, що метою антигіпертензивної терапії є зниження артеріального тиску (АТ) у більшості пацієнтів до <140/90 мм рт. ст., а за умов хорошої переносимості лікування – до 120-129/80 мм рт. ст.
Основні класи антигіпертензивних засобів включають інгібітори ангіотензинперетворювального ферменту (іАПФ), блокатори рецепторів ангіотензину ІІ (БРА), блокатори кальцієвих каналів (БКК), бета-блокатори (ББ) та діуретики.
Обсерваційне дослідження R. Petrella та P. Michailidis (2011) за участю 170 тис. дорослих пацієнтів з АГ продемонструвало, що цільового АТ досягають 28% хворих групи БРА, 27% – іАПФ, 26% – БКК, 21% – ББ та 19% – діуретиків. Порівняння терапії БРА з лікуванням усіма іншими класами антигіпертензивних засобів довело значущу перевагу БРА. У хворих групи БРА відзначалася менша кількість кардіоваскулярних подій, ніж у тих, які приймали іАПФ чи БКК (4,3 проти 7,0 та 11,0% відповідно; p<0,001).
Наукова спільнота світу активно обговорює питання вибору між іАПФ і БРА. На думку професора F. Messerli, зіставна ефективність іАПФ та БРА на тлі меншої кількості побічних явищ за умов застосування останніх вже є достатньою причиною обирати саме БРА. Крім того, більшість базових досліджень іАПФ проведені багато років тому за умов відсутності сучасних засобів вторинної профілактики, зокрема статинів. Тоді було легко забезпечити переваги для хворого шляхом використання інноваційного препарату. Що ж стосується БРА, вони демонструють пріоритет вже на тлі застосування цих профілактичних засобів.
Свого часу державні та страхові програми відшкодовували лише вартість іАПФ, оскільки перші БРА – оригінальні медикаменти – були значно дорожчими і призначалися лише у разі невдачі терапії іАПФ. На сьогодні, коли на фармацевтичному ринку представлені доступні генеричні препарати, позиція надання переваги іАПФ у зв’язку з меншою вартістю необґрунтована (Messerli F. H. et al., 2018).
 Загалом, ренін-ангіотензин-альдостеронова система (РААС) – важлива мішень дії антигіпертензивних засобів. На РААС впливають такі медикаменти, як іАПФ, БРА (рис. 1), антагоністи альдостерону та прямі інгібітори реніну. Потреба у регуляції роботи РААС зумовлена дією ангіотензину II на судинну систему, виведенням нирками натрію та води, проліферацією клітин (Brenner G. M., Stevens C. W., 2013). На жаль, гальмування дії ангіотензинперетворювального ферменту за допомогою іАПФ лише частково запобігає утворенню ангіотензину II. Останній активує два типи рецепторів, перший з яких наявний у судинах, мозку, серці, нирках, наднирниках, нервах, тоді як другий переважно виявляється у тканинах плода на етапі внутрішньоутробного розвитку, а в постнатальний період кількість таких рецепторів зменшується (Appel G.B., Appel A.S., 2004). Активація рецепторів 1-го типу спричиняє генералізовану вазоконстрикцію внаслідок скорочення непосмугованих м’язів судин, а також підвищує рівень альдостерону, що призводить до збільшеної реабсорбції натрію у нирках і посилення проліферації клітин артерій та серця (Brenner G.M., Stevens C.W., 2013). Серед інших негативних для серцево-судинної системи ефектів ангіотензину II є сприяння вивільненню катехоламінів з надниркових залоз та нервових закінчень на тлі розвитку гіперактивності симпатичної нервової системи (Weir M.R., Dzau V. J., 1999). Отже, блокада рецепторів ангіотензину ІІ 1-го типу веде до зниження і пре-, і постнавантаження (Brenner G.M., Stevens C.W., 2013). В експериментальних дослідженнях на тваринах показано, що ангіотензин ІІ спричиняє гіпертрофію серця навіть за відсутності підвищення АТ (Brunner H.R., 2001).
Загалом, ренін-ангіотензин-альдостеронова система (РААС) – важлива мішень дії антигіпертензивних засобів. На РААС впливають такі медикаменти, як іАПФ, БРА (рис. 1), антагоністи альдостерону та прямі інгібітори реніну. Потреба у регуляції роботи РААС зумовлена дією ангіотензину II на судинну систему, виведенням нирками натрію та води, проліферацією клітин (Brenner G. M., Stevens C. W., 2013). На жаль, гальмування дії ангіотензинперетворювального ферменту за допомогою іАПФ лише частково запобігає утворенню ангіотензину II. Останній активує два типи рецепторів, перший з яких наявний у судинах, мозку, серці, нирках, наднирниках, нервах, тоді як другий переважно виявляється у тканинах плода на етапі внутрішньоутробного розвитку, а в постнатальний період кількість таких рецепторів зменшується (Appel G.B., Appel A.S., 2004). Активація рецепторів 1-го типу спричиняє генералізовану вазоконстрикцію внаслідок скорочення непосмугованих м’язів судин, а також підвищує рівень альдостерону, що призводить до збільшеної реабсорбції натрію у нирках і посилення проліферації клітин артерій та серця (Brenner G.M., Stevens C.W., 2013). Серед інших негативних для серцево-судинної системи ефектів ангіотензину II є сприяння вивільненню катехоламінів з надниркових залоз та нервових закінчень на тлі розвитку гіперактивності симпатичної нервової системи (Weir M.R., Dzau V. J., 1999). Отже, блокада рецепторів ангіотензину ІІ 1-го типу веде до зниження і пре-, і постнавантаження (Brenner G.M., Stevens C.W., 2013). В експериментальних дослідженнях на тваринах показано, що ангіотензин ІІ спричиняє гіпертрофію серця навіть за відсутності підвищення АТ (Brunner H.R., 2001).
БРА характеризуються більшою афінністю до рецепторів ангіотензину ІІ 1-го типу, ніж до таких 2-го типу. Відсутність впливу БРА на рецептори 2-го типу має окреме клінічне значення, оскільки взаємодія ангіотензину ІІ із ними викликає вазодилатацію та забезпечує антипроліферативний ефект (Messerli F.H. et al., 2017). Важливо, що БРА (на відміну від іАПФ) блокують несприятливі впливи ангіотензину ІІ незалежно від способу його утворення: за допомогою ангіотензинперетворювального ферменту чи інших ензимів, наприклад кардіальної хімази (Israili Z.H., 2000; Miura S. et al., 2011).
БРА використовуються у клінічних умовах з 1995 р. і за цей час зарекомендували себе як дієві антигіпертензивні агенти з відмінним профілем переносимості (рис. 2). Сполучення БРА з тіазидними діуретиками та БКК дигідропіридинового ряду забезпечує додаткове зниження АТ без збільшення кількості побічних ефектів. Крім того, БРА продемонстрували сприятливий вплив на захворюваність та смертність за умов серцевої недостатності (СН) та хронічної хвороби нирок (ХХН), особливо при супутньому цукровому діабеті 2-го типу (Sipahi I. et al., 2010; Bangalore S. et al., 2011; Pasternak B. et al., 2011). Антигіпертензивні властивості БРА переважно опосередковані зниженням периферійного опору судин (Israili Z.H., 2000).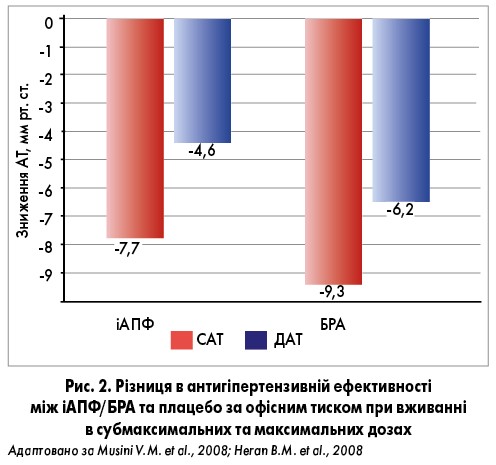
Метааналіз I.L. Vega (2015), до складу якого входило 11 007 осіб з АГ, виявив однакову ефективність іАПФ та БРА у зниженні загальної та кардіоваскулярної смертності, а також сумарної кількості кардіоваскулярних подій. Однак число випадків припинення участі в дослідженні у зв’язку з небажаними ефектами було вищим у групі іАПФ. Найпоширенішим ефектом виявився сухий кашель, що становив 43% усіх побічних дій серед пацієнтів, які приймали іАПФ, та близько 4% у групі БРА. Серед інших побічних явищ іАПФ, які змусили хворих припинити лікування, були тріпотіння передсердь, набряки, висипання, зростання рівня креатиніну.
Монотерапія БРА є більш ефективною та безпечною у контролі АТ та зниженні смертності у пацієнтів із ХХН 5-ї стадії, ніж прийом лише іАПФ чи комбінації цих двох класів препаратів. С.С. Lin et al. (2017) залучили до участі в дослідженні 14 117 пацієнтів із ХХН на стадії предіалізу. Було встановлено, що застосування іАПФ асоціювалося з вищою смертністю, ніж БРА, у всіх хворих на ХХН – відношення ризиків (ВР) 1,17; 95% довірчий інтервал (ДІ) 1,07-1,27; р=0,03) та окремо в підгрупі осіб із цукровим діабетом (ВР 1,32; 95% ДІ 1,18-1,48; р=0,03). Ці результати підтверджують висновки K.E. Chan et al. (2011), які порівнювали вплив БРА, іАПФ та подвійної блокади РААС на кардіоваскулярну смертність у 9300 пацієнтів, що підлягали гемодіалізу. Після стандартизації за факторами ризику в групі іАПФ відзначався на 27% вищий відносний ризик кардіоваскулярної смерті, ніж при прийомі БРА.
Упродовж >20 років використання БРА продемонструвало відмінний профіль безпеки як у вигляді монотерапії, так і в поєднанні з іншими антигіпертензивними засобами. У переважній кількості досліджень переносимість БРА відповідає такій плацебо, тоді як іАПФ асоційовані зі збільшенням імовірності появи кашлю у 2-3 рази порівняно із плацебо (Visser L.E. et al., 1995; Caldeira D. et al., 2012). У метааналізі 11 контрольованих випробувань частота припинення лікування серед пацієнтів, які приймали БРА, відповідала аналогічному показнику в групі плацебо: ВР 0,99; 95% ДІ 0,84-1,17 (Caldeira D. et al., 2012). Отже, БРА є класом антигіпертензивних препаратів із найкращою переносимістю, що веде до збільшення прихильності до лікування. Оскільки БРА являють собою найновіший клас антигіпертензивних засобів, синтезований у 1990-х рр., їм властиві довші періоди напіврозпаду, більша потужність та триваліша дія (Abraham H.M.A. et al., 2015). Результати порівняння ефективності й безпеки БРА та іАПФ відображені на рисунку 3.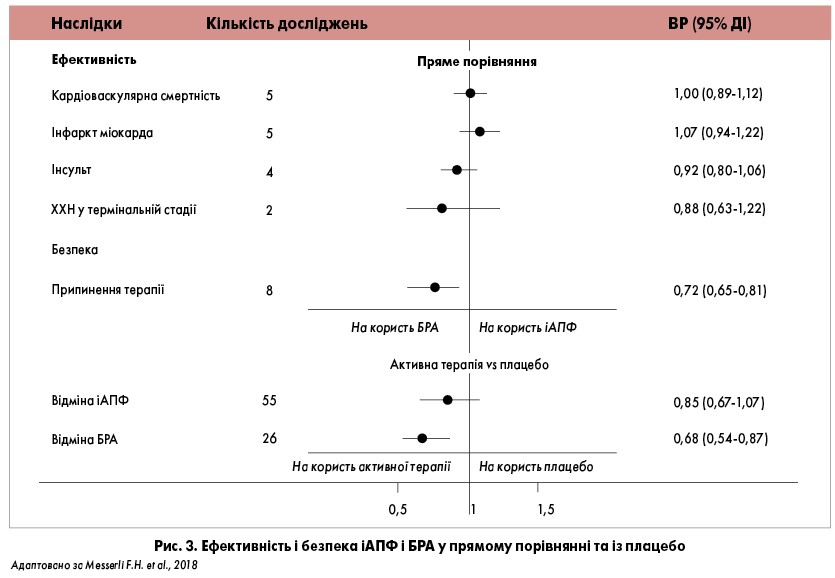
У США та Європі схвалено до використання 8 БРА різної хімічної структури (валсартан, кандесартан, олмесартан, ірбесартан, лосартан, азилсартан, епросартан, телмісартан). Валсартан призначається 1 раз на добу в стартовій дозі 80-160 мг/добу, а максимальна сягає 320 мг/добу. Крім АГ, валсартан показаний у лікуванні СН ІІ-IV функціональних класів (ФК) за NYHA для зниження кардіоваскулярної смертності у клінічно стабільних пацієнтів із лівошлуночковою СН чи дисфункцією після інфаркту міокарда (Abraham H.M.A. et al., 2015).
Серед антигіпертензивних засобів на фармацевтичному ринку України наявні класичний, відмінно вивчений БРА валсартан під назвою Вальсакор (КРКА, Словенія) та комбінації валсартану з амлодипіном (Валодип) і гідрохлортіазидом (Вальсакор Н) – обидва препарати виробництва компанії КРКА (Словенія).
Крім вираженого антигіпертензивного впливу, валсартан здатний зменшувати внутрішньоклубочкову гіпертензію в осіб із діабетичною нефропатією. У дослідженні MARVAL, де порівнювали антипротеїнуричні ефекти валсартану та амлодипіну, встановлено, що рівень екскреції альбуміну з сечею через 24 тижні лікування валсартаном у дозі 80 мг/добу зменшився до 56% вихідного рівня, а у групі амлодипіну по 5 мг/добу становив 92% стартових показників. Нормоальбумінурії вдалося досягти 29,9% хворим групи валсартану і 14,5% – амлодипіну (p<0,001) (Viberti G., Wheeldon N.M., 2002).
Блокада ефектів ангіотензину є важливою терапевтичною стратегією за умов СН. Дослідження Val-HeFT продемонструвало, що в пацієнтів із СН II-IV ФК за NYHA, які приймали валсартан, спостерігалися достовірно менші захворюваність і смертність, оцінені за такими станами, як зупинка серця з успішною реанімацією, госпіталізацією із приводу СН чи потреба у введенні внутрішньовенних інотропних або вазодилатуючих засобів (ВР 0,87; 97,5% ДІ 0,77-0,97; p=0,009), ніж у групі плацебо. Прийом валсартану також асоціювався зі зменшенням ступеня СН за NYHA, зростанням фракції викиду та покращенням якості життя (p<0,01) (Cohn J.N., Tognoni G., 2001).
Нові рекомендації з лікування АГ вказують, що загалом стартова терапія повинна являти собою комбінацію двох засобів. Перевагу слід надавати сполученню іАПФ/БРА з тіазидним діуретиком (Вальсакор Н) або БКК (Валодип). Безсумнівно, доцільно застосовувати фіксовані комбінації, оскільки вони дозволяють полегшити режим прийому медикаментів, покращуючи прихильність до лікування. Призначення діуретиків веде до активації РААС, але БРА протидіють цьому, дозволяючи пацієнту отримати максимальні переваги від індукованого діуретиками зменшення кількості натрію. Ця взаємодоповнююча синергетична дія покращує переносимість, оскільки дозволяє знизити призначувані дози окремих компонентів комбінації (Waebццer B., 2003). БРА також мінімізують несприятливі метаболічні ефекти, асоційовані з прийомом діуретиків, зокрема гіпокаліємію, гіперурикемію, порушення толерантності до глюкози (Sica D. A. et al., 2011).
Високоефективною комбінацією з відмінною переносимістю є також комбінація валсартану з амлодипіном. БКК дигідропіридинового ряду здатні спричиняти периферійні набряки через збільшення капілярного гідростатичного тиску внаслідок артеріальної вазодилатації. БРА нормалізують капілярний гідростатичний тиск шляхом покращення венозного повернення до серця, у такий спосіб протидіючи цьому побічному ефекту, який часто розвивається на тлі прийому амлодипіну (Fogari R. et al., 2007). Рандомізовані контрольовані дослідження довели, що додавання амлодипіну до БРА супроводжується більш вираженим зниженням АТ, ніж прийом монотерапії в аналогічних дозах. Отже, здебільшого пацієнтам вдається досягти цільового АТ на тлі зіставної кількості побічних явищ (Chrysant S.G. et al., 2008; Philipp T. et al., 2007; Flack J.M. et al.,2009; Neutel J.M. et al., 2012).
Профіль безпеки комбінації валсартану з гідрохлортіазидом відповідає показникам монотерапії (Calhoun D.A. et al., 2008), а сумісний прийом валсартану та амлодипіну супроводжується меншою частотою периферійних набряків, ніж монотерапія амлодипіном (Philipp T. et al., 2007).
Отже, для контролю АГ відповідно до сучасних рекомендацій потрібно обирати ефективний та безпечний засіб першої лінії терапії – Вальсакор (КРКА, Словенія) або фіксовану комбінацію БРА з БКК чи гідрохлортіазидом (Валодип, Вальсакор Н, КРКА, Словенія). Поєднання європейської якісті та доступної вартості цих генеричних препаратів дозволяє їм утримувати лідерські позиції серед антигіпертензивних засобів.
Підготувала Лариса Стрільчук
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (60) листопад 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....




