Ревматологія • Дайджест
Влияние хондроитина сульфата на выраженность синовиита у больных остеоартритом коленных суставов
Цель исследования – оценить влияние хондроитина сульфата на ультразвуковые признаки воспаления синовиальной оболочки (синовиита) у пациентов с остеоартритом (ОА) коленных суставов (КС), а также изучить биохимические процессы, происходящие в воспаленной синовиальной оболочке.
Методы. В этом рандомизированном одностороннем слепом контролированном исследовании приняли участие больные первичным ОА КС, которым рекомендовали принимать хондроитина сульфат или ацетаминофен* на протяжении 6 мес. Степень тяжести ОА КС оценивали перед назначением лекарственных средств, а также через 6 нед, 3 и 6 мес терапии, применив метод ультразвукового исследования (используя дефиницию, предложенную экспертной группой OMERACT). Интенсивность болевого синдрома и функцию пораженных суставов определяли посредством визуальной аналоговой шкалы (ВАШ) и индекса Лекена соответственно; активность воспалительных медиаторов в сыворотке крови и синовиальной жидкости – при помощи иммуноферментного исследования.
Результаты. Распространенность синовиита в группе больных, получавших хондроитина сульфат, уменьшилась на 50%, тогда как в группе пациентов, принимавших ацетаминофен, этот показатель возрос до 123%. После завершения курса лечения ацетаминофеном у 85,71% пациентов, не имевших в ходе первичного обследования ультразвуковых признаков воспаления синовиальной оболочки, диагностирован синовиит; в группе хондроитина сульфата этот показатель составил всего 25%. Оба вида терапии улучшали функцию КС, но статистически значимое уменьшение интенсивности болевого синдрома зафиксировано лишь в группе хондроитина сульфата. Более того, только прием хондроитина сульфата сопровождался достоверным изменением сывороточной концентрации хемокина, экспрессируемого и секретируемого Т-клетками при их активации.
Выводы. Включение хондроитина сульфата в схему лечения ОА КС оказывает благоприятное влияние на состояние больных, предупреждая возникновение синовиита или уменьшая степень его выраженности, а также нивелируя клинические проявления ОА КС. Ацетаминофен уменьшает степень выраженности клинических симптомов, но не влияет на активность воспалительного процесса. Противовоспалительное действие хондроитина сульфата может быть связано с уменьшением содержания хемокина, экспрессируемого и секретируемого Т-клетками при их активации.
Tіo L. et al. 2017. Doi: 10.1016/j.medcli.2016.12.045.
* Парацетамол. – Прим. ред.
Эффективность хондроитина сульфата в купировании боли при ОА КС: результаты 12-месячного двойного слепого рандомизированного многоцентрового клинического исследования
Цель данного исследования заключается в выявлении возможных расхождений в эффективности двух различных доз хондроитина сульфата в лечении рентгенологически подтвержденного ОА КС.
Методы. В этом рандомизированном двойном слепом сравнительном исследовании сопоставлялась эффективность различных доз хондроитина сульфата в купировании болевого синдрома при ОА КС. В эксперимент включили больных со II-III стадией ОА КС по рентгенологической классификации Келлгрена-Лоуренса, предъявлявших жалобы на выраженную боль, оцененную по ВАШ ≥30 баллов (n=73). Пациентов рандомизировали для приема низких (260 мг/сут; контрольная группа) или высоких (1560 мг/сут; основная группа) доз хондроитина сульфата перорально на протяжении 12 мес. Интенсивность болевого синдрома оценивали при помощи индекса Лекена и ВАШ. В зависимости от интенсивности болевого синдрома пациентов дополнительно распределили на две подгруппы (индекс Лекена ≥8 баллов или <8 баллов). У всех больных, кроме того, определяли содержание гиалуроновой кислоты и олигомерного матриксного белка хряща в сыворотке крови.
Результаты. На фоне терапии как высокими, так и низкими дозами хондроитина сульфата зафиксировано быстрое уменьшение интенсивности болевого синдрома на протяжении 3 месяцев с более мягким ее снижением в течение последующих 9 мес (рис., а).
Высокие дозы хондроитина сульфата (1560 мг/сут) способствовали быстрому нивелированию болевого синдрома в подгруппе пациентов с выраженной алгией (индекс Лекена ≥8 баллов) (рис., б).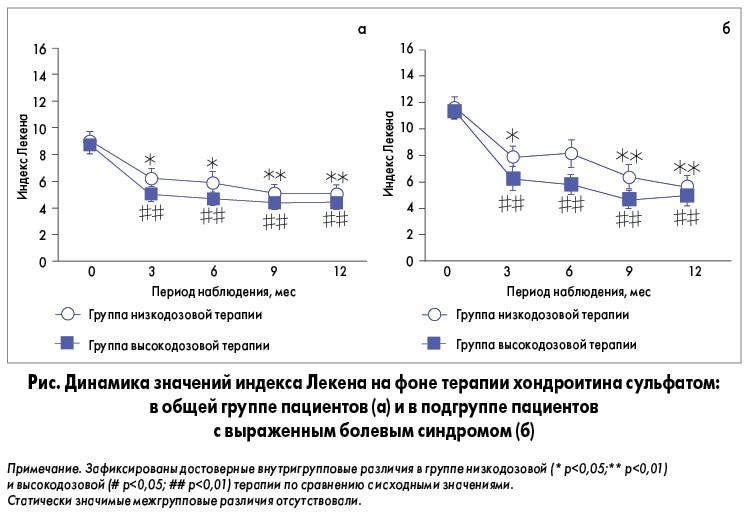
Ни низкие, ни высокие дозы хондроитина сульфата не оказывали значимого влияния на содержание гиалуроновой кислоты и олигомерного матриксного белка хряща в сыворотке крови. Хондроитина сульфат хорошо переносился, его клиническое применение не сопровождалось появлением серьезных нежелательных явлений.
Выводы. Высокие дозы хондроитина сульфата (1560 мг/сут) более эффективны в купировании болевого синдрома при ОА КС, чем низкие (260 мг/сут). Хондроитина сульфат хорошо переносится при пероральном приеме. Пероральная терапия хондроитином сульфатом позволяет достичь значимого контроля над болью у пациентов с ОА КС.
Morita М. еt al. 2018. Doi: 10.1248/bpb.b17-00556.
Хондроитина сульфат при остеоартрите
Цель метаанализа – оценить преимущества и недостатки перорального приема хондроитина сульфата в лечении ОА по сравнению с плацебо или другими препаратами, включая нестероидные противовоспалительные средства (НПВС), аналгетики, опиоиды, глюкозамин, фитопрепараты.
Методы. Поиск проведен в семи электронных базах данных по ноябрь 2013 года, включая Кокрановский регистр контролированных исследований (CENTRAL), Ovid MEDLINE, CINAHL, EMBASE, Web of Science, а также базы данных Управления по контролю за качеством продуктов питания и лекарственных средств США (FDA) и Европейского агентства лекарственных средств (EMA).
Критерии отбора. В метаанализ включали рандомизированные или частично рандомизированные клинические исследования, длившиеся более 2 нед и проведенные с участием взрослых больных ОА любых суставов, в которых эффективность применения хондроитина сопоставлялась с таковой плацебо или других активных препаратов сравнения, например НПВС.
Результаты. Проанализированы результаты 43 рандомизированных контролированных исследований, в которых 4962 пациента получали хондроитин, а 4148 больных принимали плацебо или другой активный препарат сравнения. Большинство исследований проводилось с участием больных ОА КС, в нескольких испытаниях участвовали пациенты с ОА тазобедренных и плечевых суставов. Длительность испытаний варьировала от 1 мес до 3 лет.
В исследованиях, длившихся менее 6 мес, зафиксировано статистически и клинически значимое уменьшение интенсивности болевого синдрома (оцененное при помощи ВАШ) у больных, принимавших хондроитин, по сравнению с пациентами, получавшими плацебо (снижение абсолютного риска на 10% (95% доверительный интервал (ДИ) 15-6; число больных, которых необходимо пролечить для получения одного благоприятного исхода (NNT), 5 (95% ДИ 3-8); данные 8 исследований). В испытаниях, длившихся более 6 мес, снижение абсолютного риска составило 9% (95% ДИ 18-0; данные 6 исследований), но этот показатель имел низкий уровень доказательности. Терапия хондроитином позволила улучшить значения шкалы WOMAC (WOMAC MCII): прием хондроитина сопровождался 20% снижением интенсивности болевого синдрома у 53/100 больных по сравнению с 47/100 пациентов из группы плацебо; снижение абсолютного риска составило 6% (95% ДИ 1-11; данные 2 исследований). В исследованиях, длившихся менее 6 мес, отмечено достоверное улучшение значений индекса Лекена (боль, функция, трудоспособность) на фоне лечения хондроитином по сравнению с плацебо (снижение абсолютного риска 8%; 95% ДИ 12-5). В отличие от плацебо прием хондроитина замедлял сужение внутрисуставной щели (снижение относительного риска -4,7%; 95% ДИ 1,6-7,8). Терапия хондроитином не сопровождалась статистически значимым увеличением количества нежелательных явлений / отменой его приема, обусловленной побочными действиями, по сравнению с плацебо или другими препаратами сравнения.
Выводы. Обзор результатов рандомизированных исследований показал, что хондроитин превосходит плацебо в нивелировании болевого синдрома у больных ОА в кратковременной перспективе. Прием хондроитина позволяет добиться клинически значимого уменьшения интенсивности болевого синдрома на 8 баллов (по 100-балльной шкале) и улучшения значений индекса Лекена на 2 балла (по 24-балльной шкале). Терапия хондроитином ассоциируется с низким риском возникновения серьезных нежелательных явлений по сравнению с контролем.
Singh J. A. et al. 2015. Doi: 10.1002/14651858.CD005614.pub2.
Хондроитина сульфат как фармакологический препарат обладает эффективностью целекоксиба и превосходит плацебо в лечении симптоматического ОА КС: исследование CONCEPT (хондроитин в сравнении с группой целекоксиба и группой плацебо)
Хондроитин сульфат (800 мг/сут) как фармакологический препарат используется в лечении симптоматического ОА КС согласно рекомендациям ЕМА.
Методы. В данном проспективном рандомизированном 6-месячном 3-групповом двойном слепом исследовании сравнивался хондроитин с плацебо и целекоксибом (200 мг/сут) для купирования болевого синдрома (интенсивность последнего оценивалась при помощи ВАШ и индекса Лекена – первичные конечные точки). В качестве вторичных конечных точек рассматривали минимальное клинически значимое улучшение (Minimal-Clinically Important Improvement, MCII) и индекс PASS (Patient-Acceptable Symptoms State).
Результаты. В исследовании приняли участие 604 пациента с ОА КС (диагноз подтверждали согласно критериям Американской коллегии ревматологов) из пяти европейских стран; длительность наблюдения составила 182 дня. Хондроитин и целекоксиб достоверно уменьшали выраженность болевого синдрома, оцененного при помощи индекса Лекена, по сравнению с плацебо. В популяции пациентов, начавших получать лечение, зафиксировано снижение интенсивности болевого синдрома по данным ВАШ к 182-му дню терапии как в группе хондроитина (-42,6 мм; р=0,001), так и в группе целекоксиба (-39,5 мм; р=0,009), что достоверно превосходило аналогичный показатель в группе плацебо (-33,3 мм); точные статистические отличия между группами хондроитина и целекоксиба отсутствовали. Подобная тенденция отмечена в отношении индекса Лекена: прием хондроитина (-4,7; р=0,023) и целекоксиба (-4,6; р=0,015) способствовал достоверному снижению значений этого показателя по сравнению с плацебо (-3,7); статистически значимые отличия между группами сравнения не зафиксированы. В группе хондроитина и целекоксиба обнаружены положительные изменения вторичных конечных точек (MCII и PASS) к 182-му дню терапии. Все виды лечения продемонстрировали высокий профиль безопасности.
Выводы. Хондроитин сульфат (800 мг/сут) как фармакологический препарат превосходит плацебо и аналогичен целекоксибу в нивелировании болевого синдрома, улучшении функции суставов при симптоматическом ОА КС. Следует рассмотреть целесообразность применения этого препарата в качестве терапии первой линии у больных ОА КС.
Reginster J.Y. et al. 2016. Doi: 10.1136/annrheumdis‑2016-210860.
Подготовила Татьяна Можина
Медична газета «Здоров’я України 21 сторіччя» № 22 (443), листопад 2018 р.
СТАТТІ ЗА ТЕМОЮ Ревматологія
Сечова кислота (СК) – кінцевий продукт метаболізму пуринів, який здебільшого синтезується в печінці та виводиться нирками і кишечником [1, 2]. Гіперурикемія – підвищений рівень СК у сироватці крові – є метаболічною основою подагри, одного з найпоширеніших запальних артритів. У середні віки подагра вважалася хворобою надмірності аристократії, нині її поширеність зростає у всьому світі через зміни в харчуванні, переважання в дієті оброблених продуктів, фруктози та збільшення поширеності ожиріння [3]....
Глюкокортикоїди (ГК), які використовуються з початку 1950-х рр., стали невід’ємною частиною лікування ревматоїдного артриту (РА) [1]. Ключовою перевагою ГК є швидке настання ефекту, особливо порівняно з класичними синтетичними хворобомодифікувальними антиревматичними препаратами (ХМАРП) на кшталт метотрексату. Відповідно, ГК мають привабливий профіль для лікування спалахів хвороби або для застосування в ролі засобів для бридж-терапії на ранніх стадіях РА в очікуванні ефекту класичних синтетичних ХМАРП. Ця стратегія широко використовується після публікації результатів дослідження COBRA в 1997 р. [2]. ...
Гостре розтягнення зв’язок гомілковостопного суглоба (ГРЗГС) є поширеним, інвалідизувальним, клінічно значущим захворюванням, щодо якого по медичну допомогу щороку звертається >1 млн пацієнтів [1]; асоціюється зі значним соціально-економічним тягарем [2]. Майже 16-40% випадків ГРЗГС – спортивна травма, а час одужання є дуже важливим для спортсменів, професіоналів та осіб, котрі готуються до великих змагань. Найпоширенішими (85%) є латеральні (бічні) розтягнення зв’язок гомілковостопного суглоба; особливо часто ушкоджується передня таранно-гомілкова зв’язка – зазвичай унаслідок високошвидкісної інверсії та внутрішньої ротаційної травми [3]; ≈40% розтягнень гомілковостопного суглоба мають ризик хронізації. Характерними ознаками ГРЗГС є біль під час навантаження, нестабільність гомілковостопного суглоба та проблеми з рухливістю [4-6]....
Наприкінці жовтня минулого року Всеукраїнська асоціація ревматологів України провела науково-практичну конференцію, до якої було залучено фахівців різних галузей медицини, як-от ревматологія, загальна практика (сімейна медицина), терапія, кардіологія, медицина невідкладних станів, неврологія, функціональна й ультразвукова діагностика. Захід відбувся у змішаному форматі (онлайн / офлайн). До участі в конференції було запрошено не лише вітчизняних спікерів із різних регіонів України, а і закордонних, зокрема з Канади, США та Великої Британії. ...




