Роль амиодарона в лечении нарушений ритма сердца
По материалам ХІХ Национального конгресса кардиологов Украины, 26-28 сентября, г. Киев
В конце сентября внимание отечественного медицинского сообщества было приковано к ХІХ Национальному конгрессу кардиологов Украины. Обширная научная программа мероприятия объединила как основы кардиологии, так и вопросы ультрасовременных методов диагностики и лечения сердечно-сосудистых заболеваний (ССЗ). Особое место в рамках конгресса занимала аритмология, которой были посвящены курс лекций для семейных врачей и несколько тематических заседаний.
 В ходе круглого стола «Роль и место амиодарона в лечении нарушений ритма сердца: когда альтернативы нет» выступил руководитель отдела аритмий сердца ГУ «Национальный научный центр «Институт кардиологии им. Н. Д. Стражеско» НАМН Украины», доктор медицинских наук, профессор Олег Сергеевич Сычев.
В ходе круглого стола «Роль и место амиодарона в лечении нарушений ритма сердца: когда альтернативы нет» выступил руководитель отдела аритмий сердца ГУ «Национальный научный центр «Институт кардиологии им. Н. Д. Стражеско» НАМН Украины», доктор медицинских наук, профессор Олег Сергеевич Сычев.
Докладчик сообщил, что на рубеже 2000-х гг. был опубликован ряд испытаний, авторы которых утверждали, что восстанавливать ритм необязательно, достаточно лишь обеспечить контроль частоты сердечных сокращений (ЧСС). Однако сегодня известно, что это не так, данный факт был подтвержден в нескольких масштабных исследованиях. В одном из них пациенты были разделены на две когорты – контроля ритма и контроля ЧСС. Уже через 1 год смертность от всех причин (наиболее точный показатель эффективности лечения ССЗ) была на 28% ниже в группе контроля ритма, чем в группе контроля желудочковых сокращений.
Несомненно, при назначении антиаритмических препаратов (ААП) следует тщательно взвешивать пользу и риск, а также мониторировать состояние пациента, поскольку все представители данного класса лекарственных средств потенциально проаритмогенны и способны вызвать блокаду или асистолию. Кроме того, все ААП, за исключением амиодарона, снижают сократимость миокарда. Выбор ААП должен основываться на тщательной оценке состояния пациента; также нужно принимать во внимание наличие коморбидностей, уровень сердечно-сосудистого риска и вероятность развития серьезной аритмии (проаритмические состояния) либо экстракардиальных токсических эффектов. При этом важно учитывать предпочтения пациента и степень нагрузки симптомами.
Больных, принимающих ААП, рекомендуется периодически обследовать для подтверждения приемлемости дальнейшей антиаритмической терапии. В начале лечения ААП необходимо оценить электрокардиограмму (ЭКГ) пациента с целью мониторинга ЧСС, выявления удлинения интервалов QRS и QT, а также атриовентрикулярных блокад. Угрожающим ЭКГ‑признаком, требующим прекращения лечения амиодароном, служит удлинение интервала QT >500 мс. Необходимый режим мониторинга ЭКГ при лечении амиодароном предусматривает исходную запись, запись через 1 нед, в дальнейшем – каждые 4 нед.
К сожалению, современные рекомендации касательно выбора пациентов для восстановления ритма не содержат четких формулировок. Вместе с тем в руководствах однозначно указывается, что при наличии у пациента симптомов необходимо восстановить и контролировать ритм. В отсутствие такой возможности акцент смещается на контроль ЧСС. Для принятия решения о лечении следует ответить на вопросы, является ли пациент гемодинамически стабильным и имеет ли структурное заболевание сердца. Далее применяется алгоритм, утвержденный Европейским обществом кардиологов (2016) (рис.). Для фармакологической кардиоверсии в условиях тяжелой сердечной недостаточности (СН) или выраженного аортального стеноза используется амиодарон (Кордарон®) внутривенно. Амиодарон является также одним из нескольких ААП, которые могут назначаться при наличии ишемической болезни сердца (ИБС), умеренной СН или гипертрофии левого желудочка (ЛЖ).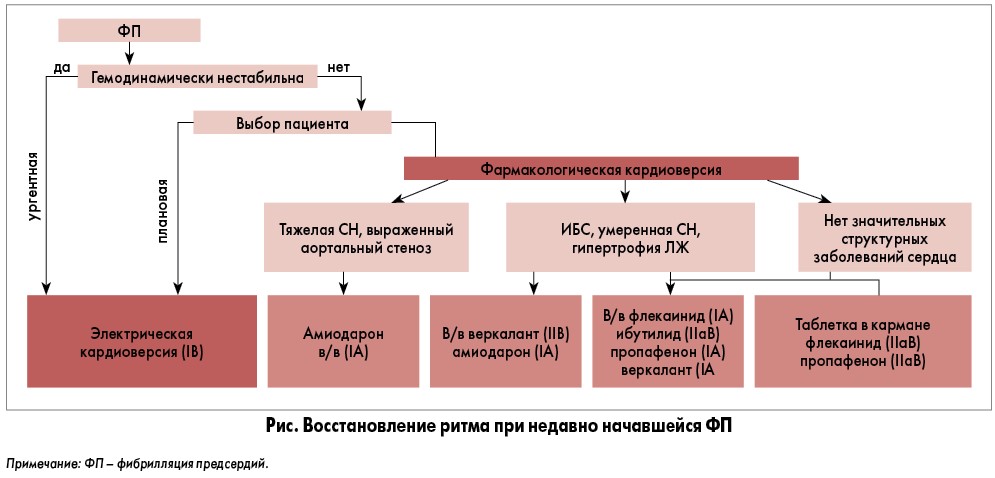
При начале долгосрочного контроля ритма пациенту с ИБС, клинически значимыми клапанными заболеваниями и/или значительной гипертрофией ЛЖ следует выбрать между катетерной абляцией или медикаментозным лечением (амиодарон, дронедарон, соталол). Если же у больного диагностирована СН, единственной альтернативой катетерной абляции выступает Кордарон® (амиодарон).
Рекомендации Европейского общества кардиологов по лечению фибрилляции предсердий (2016) указывают, что амиодарон более эффективен в профилактике рецидивов ФП, чем другие ААП, но при его назначении обычны экстракардиальные токсические эффекты, частота которых со временем увеличивается. По этой причине в первую очередь должны быть рассмотрены другие ААП. Тем не менее у пациентов с СН для профилактики рецидивов симптомной ФП рекомендован именно амиодарон.
Отдельный вопрос – восстановление и контроль ритма при наличии ФП и коморбидных заболеваний (СН, WPW‑синдрома). По данным профессора О. С. Сычева, эффективность радиочастотной абляции в последнем случае составляет 97%, однако пациента необходимо доставить в катетерную лабораторию без осложнений, что обусловливает необходимость в медикаментозном прикрытии. При WPW‑синдроме противопоказаны сердечные гликозиды и бета-адреноблокаторы, что выводит амиодарон на ведущие позиции в контроле данного нарушения ритма.
В прошлом выявление желудочковых экстрасистол неизменно побуждало врача назначить какое-либо лечение. С появлением холтеровского мониторирования было показано, что такие нарушения ритма могут возникать и в молодом возрасте у лиц без кардиоваскулярной патологии. Подобные экстрасистолы зачастую не нуждаются в терапевтическом вмешательстве, вместе с тем у пациентов с частой симптомной желудочковой экстрасистолией или наджелудочковыми тахикардиями следует рассмотреть возможность проведения катетерной абляции либо лечения амиодароном. Терапию последним также необходимо рассмотреть при профилактике желудочковых тахикардий у лиц с дисфункцией ЛЖ и стойкой мономорфной желудочковой тахикардией с имплантированным кардиовертером-дефибриллятором либо без такового.
Что касается вторичной профилактики внезапной сердечной смерти и желудочковых тахикардий, то если пациент с ФП или желудочковой тахикардией, которому показана имплантация кардиовертера-дефибриллятора, отказывается от данного вмешательства, имеет противопоказания, связанные с сопутствующими патологическими состояниями, или по какой-либо причине данная опция для него недоступна, также следует рассмотреть возможность терапии амиодароном. Метаанализ АТМА, включавший данные 6553 пациентов, получавших амиодарон, показал, что применение этого препарата уменьшало вероятность аритмической смерти на 20%.
Еще один актуальный вопрос: ФП и СН – что первично? Исследование данных за 154 тыс. пациенто-лет позволило установить, что в течение жизни ФП развилась у 7,5% пациентов. При наличии ФП риск застойной СН был выше в 3 раза, инсульта – в 2 раза по сравнению с отсутствием ФП. В свою очередь, СН в 8,5 раз увеличивает риск развития ФП, что опосредовано снижением сердечного выброса и ухудшением почечного кровотока, вызывающим активацию ренин-ангиотензиновой системы и рост концентрации предсердного натрийуретического пептида. Регистр, включающий более 63 тыс. пациентов с доказанным атеросклерозом, показал, что наличие ФП достоверно увеличивает вероятность госпитализации, связанной с СН. Трехлетнее наблюдение за 7548 пациентами с ФП без инсульта в анамнезе, начатое в течение 30 дней после пароксизма, продемонстрировало, что риск инсульта был в 1,81 раза выше, если пациент не принимал амиодарон, то есть лечение указанным препаратом сопровождалось снижением риска инсульта. Комбинация амиодарона с дигоксином повышала риск инсульта, в связи с чем ее применение не рекомендуется (Chen W.-C. et al., 2015). Подобные результаты подчеркивают важность лечения ФП и контроля ритма в целом.
Докладчик напомнил три положения Резолюции совета экспертов по аритмологии, состоявшегося 4 ноября 2016 г.
- При лечении ФП при остром коронарном синдроме из ААП должен применяться амиодарон.
- Амиодарон является единственным ААП, используемым для восстановления и удержания синусового ритма у больных с хронической СН.
- При лечении больных без выраженной органической патологии сердца амиодарон должен использоваться при неэффективности других ААП, а также при отказе больного от проведения радиочастотной абляции либо в случае ее неэффективности.
Термин «без органического поражения сердца» предусматривает фракцию выброса ЛЖ >45%; отсутствие в анамнезе инфаркта миокарда с зубцом Q, гипертрофической или дилатационной кардиомиопатии, застойной или прогрессирующей СН, а также стадии СН выше ІІА; врожденных или ревматических пороков сердца, выраженной гипертрофии ЛЖ (толщина одной из стенок ≥14 мм). Артериальная гипертензия, хронические формы ИБС и другие кардиологические заболевания не являются противопоказаниями к назначению ААП І класса, если не ведут к указанным выше изменениям.
При наличии органического поражения сердца и повторных эпизодов ФП амиодарон должен быть назначен для постоянного применения с целью удержания синусового ритма, профилактики осложнений и перехода ФП из персистирующей форму в постоянную. Противопоказанием к назначению амиодарона со стороны щитовидной железы является лишь гипертиреоз. В условиях субклинического гипотиреоза амиодарон можно принимать.
Условия для отмены амиодарона при его длительном использовании включают появление побочных эффектов, переход ФП в постоянную форму и развитие коморбидностей, являющихся противопоказаниями к приему данного препарата. В случае возникновения побочных эффектов или коморбидных состояний решение об отмене амиодарона следует принимать мультидисциплинарно (семейный врач, кардиолог, узкий специалист соответствующего профиля).
Таким образом, несмотря на наличие в арсенале кардиолога/аритмолога многих ААП, существуют ситуации, когда альтернатива амиодарону отсутствует. Назначение препарата Кордарон® (амиодарона) позволяет восстановить и удерживать синусовый ритм, а также уменьшить вероятность развития инсульта и аритмической смерти.
Подготовила Лариса Стрильчук
Медична газета «Здоров’я України 21 сторіччя» № 22 (443), листопад 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....




