Безсимптомна гіперурикемія: практичні поради щодо початку уратзнижувальної терапії
Безсимптомна гіперурикемія (ГУ) – це підвищення сироваткової концентрації сечової кислоти (СК), яке не супроводжується симптомами чи патологічними станами, зумовленими відкладанням кристалів СК (подагра, сечокислий уролітіаз). Хоча в пацієнтів з ГУ ці клінічні симптоми можуть маніфестувати в будь-який момент, у 75% таких осіб тофуси, напади подагри або хронічна подагрична нефропатія ніколи не розвиваються. З іншого боку, безсимптомна ГУ асоціюється з іншими захворюваннями, великою мірою не пов’язаними з кристалізацією уратів, зокрема з артеріальною гіпертензією, атеросклерозом, метаболічним синдромом, цукровим діабетом, хронічною хворобою нирок і псоріазом (Yu K. H., 2018).
Визначення та епідеміологія
Розповсюдженість ГУ залежить від статі, віку, расової приналежності й інших факторів. Протягом останніх 10 років цей показник постійно зростає (як і захворюваність на подагру), що пов’язують зі змінами дієтичних уподобань і способу життя осіб з більш високим економічним статусом. У здорових дорослих частота виявлення ГУ становить 5-8%, але насправді, імовірно, є вищою. За даними відомого дослідження NHANES (США, 2007-2008), безсимптомна ГУ присутня в 47% пацієнтів з артеріальною гіпертензією, 70% пацієнтів з хронічною хворобою нирок ≥2 стадії та 54% осіб з ожирінням (індекс маси тіла ≥30 кг/м2).
Розвитку ГУ можуть сприяти багато факторів, зокрема генетика, інсулінорезистентність, перевантаження залізом, артеріальна гіпертензія, гіпотиреоз, ниркова недостатність, ожиріння, дієта і надмірне вживання алкогольних напоїв. Серед цих факторів вживання алкоголю (особливо пива) є найважливішим. Підвищувати сироваткові рівні СК можуть ацетилсаліцилова кислота в низьких дозах, β-блокатори (пропранолол, атенолол, метопролол, тимолол), діуретики (петльові, тіазидні, спіронолактон, еплеренон).
Верхня межа нормального діапазону СК сироватки становить 6 мг/дл (360 мкмоль/л) у жінок та 6,8 мг/дл (400 мкмоль/л) у чоловіків (референтний показник у лабораторії). Нижній рівень СК у жінок у пременопаузі пов’язаний з естрогенами, які посилюють нирковий кліренс СК. Європейська антиревматична ліга (EULAR) та Американська колегія ревматології (ACR) встановили єдину верхню межу СК сироватки для жінок і чоловіків – 360 мкмоль/л; у рекомендаціях з уролітіазу Європейської асоціації урології (EAU) зазначено дещо вищу межу – 380 мкмоль/л. Щодо нижньої межі, EULAR не рекомендує знижувати СК сироватки <3 мг/дл у довгостроковій перспективі.
На відміну від інших лабораторних показників, норму яких встановлюють на підставі статистичних даних, нормальний сироватковий рівень СК і, відповідно, ГУ є фізико-хімічними визначеннями. Кристалізація уратних кристалів in vitro відбувається за концентрації СК ≥6,8 мг/дл (температура 37 °C) або >6,0 мг/дл (температура 35 °C) при рН 7,0. Цей процес може відбуватись і в разі нижчих концентрацій СК – за умови більш низьких рН та температури (наприклад, у периферичних суглобах).
Патогенез
Високі сироваткові рівні СК утворюються внаслідок недостатньої екскреції (90%) або надмірного синтезу (10%) СК (Borghi C. et al., 2018) (рис.). Причини надмірного синтезу СК можуть бути екзогенними (дієта, багата на фруктозу та пурини) й ендогенними (підвищений розпад пуринових нуклеотидів, генетично зумовлені дефіцит або підвищена активність певних ферментів тощо).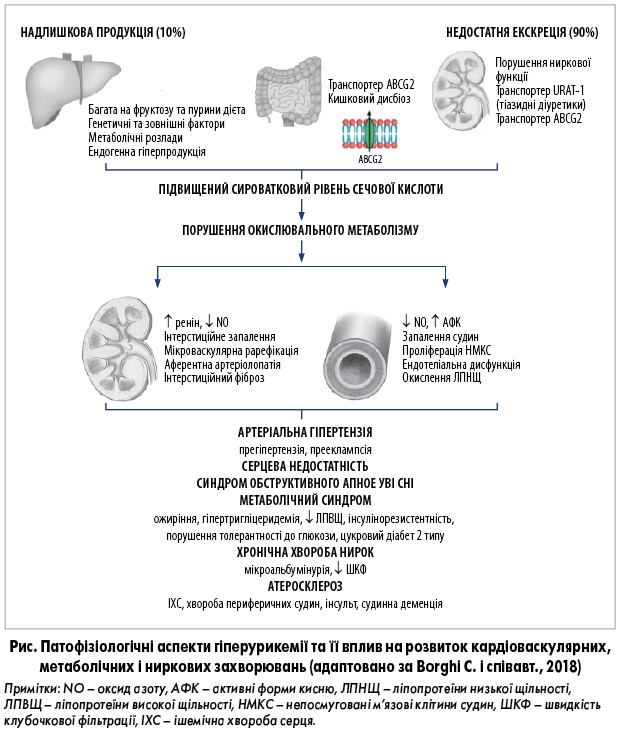
У нирках СК фільтрується в клубочку і потім зазнає реабсорбції, секреції та постсекреторної реабсорбції. Зниження гломерулярної фільтрації (хронічна хвороба нирок), зменшення тубулярної секреції (ацидоз) та посилена тубулярна реабсорбція (цукровий діабет, діуретична терапія) можуть спричинити ГУ. В умовах ацидозу (діабетичний кетоацидоз, кетоз під час голодування, інтоксикація етанолом) в організмі накопичуються органічні кислоти, які конкурують із СК за тубулярну секрецію, що призводить до розвитку ГУ.
Визначити патофізіологію ГУ в пацієнта можна за добовою екскрецією уратів: екскреція >800 мг СК за 24 год на тлі звичайної дієти з великою імовірністю вказує на надмірний синтез пуринів як етіологічний фактор.
Коли розпочинати уратзнижувальну терапію?
Viggiano і співавт. (2018) запропонували алгоритм початку уратзнижувальної терапії в пацієнтів із безсимптомною ГУ.
У разі виявлення ГУ на першому етапі слід провести мікроскопію осаду сечі та/або ультразвукове дослідження (УЗД) суглобів. Наявність уратних кристалів в осаді сечі є свідченням перенасичених рівнів СК у нирках. За даними досліджень за участю пацієнтів з хронічною хворобою нирок, сімейною формою гіперурикозурії-гематурії й ідіопатичною нефропатією, ця ознака з’являється задовго до появи клінічних симптомів подагри; такі хворі добре відповідають на уратзнижувальну терапію.
Безсимптомні відкладення уратів також можна виявити за допомогою УЗД (зазвичай досліджують перший плеснофаланговий, перший п’ясткофаланговий, таранно-човноподібний, колінний, ліктьовий суглоби та зап’ясток). Сонографічними ознаками, які передують суглобовим симптомам подагри, є гіперехогенність поверхні хряща, подвоєння контуру хряща, інтраартикулярні гіперехогенні включення, ерозії кістки, синовіт і періартикулярні сигнали.
Наявність уратних кристалів у сечі та/або суглобах може бути підставою для початку уратзнижувальної терапії. За відсутності ознак уратних кристалів слід оцінити ШКФ, протеїнурію та СК сироватки в динаміці (інтервал між дослідженнями – принаймні 6 міс). Якщо ці показники стабільні, пацієнта можна лише спостерігати і повторювати обстеження з більшим інтервалом. Натомість у разі погіршення ниркової функції доцільно розпочати уратзнижувальну терапію або залужнювання сечі з оцінкою ефективності через 6 міс; стабілізація ШКФ та протеїнурії вказує на потенційну користь лікування і доцільність його продовження.
Уратзнижувальна терапія
Головною метою лікування ГУ є зниження рівня СК. Відповідно до європейського консенсусу (Borghi C. et al., 2018), оптимальним цільовим рівнем СК є <6 мг/дл (360 мкмоль/л). Цільовий рівень <5 мг/дл може бути розглянутий у пацієнтів з високим кардіоваскулярним ризиком, які мають принаймні два стани з наведених далі: артеріальна гіпертензія, цукровий діабет, дисліпідемія, нещодавно перенесений інфаркт міокарда або інсульт. Після досягнення цільового рівня СК уратзнижувальну терапію продовжують невизначено довго, рекомендована періодичність спостереження – двічі на рік.
Інгібітори ксантиоксидази (алопуринол, фебуксостат) є першою лінією уратзнижувальної терапії. Алопуринол, який застосовується з 1966 р., є більш дешевим і представлений великою кількістю генеричних препаратів. Головними недоліками алопуринолу є складний режим дозування і титрації, особливо в пацієнтів зі зниженою нирковою та/або печінковою функцією (важко балансувати між адекватним зниженням СК і побічними ефектами), та значний ризик реакцій гіперчутливості, що потребує пильного спостереження за пацієнтами. Реакції гіперчутливості з ураженням шкіри часто призводять до відміни лікування і в рідкісних випадках можуть бути фатальними. Серед інших клінічно значимих побічних ефектів алопуринолу заслуговують на увагу пригнічення кісткового мозку з розвитком апластичної анемії, депресія, порушення зору, артеріальна гіпертензія, гепатит, у чоловіків – гінекомастія, нічні полюції й еректильна дисфункція. Досить несприятливим також є профіль лікарських взаємодій алопуринолу, зокрема, з такими широко застосовуваними препаратами, як діуретики (підвищення ризику реакцій гіперчутливості), інгібітори АПФ (гематотоксичні реакції), ампіцилін й амоксицилін (алергічні реакції).
Сучасною альтернативною алопуринолу є фебуксостат (Аденурик®) – непуриновий селективний інгібітор ксантиоксидази з подвійним механізмом дії. Порівняно з алопуринолом він забезпечує більш потужний уратзнижувальний ефект і краще переноситься. Фебуксостат має сприятливий профіль лікарських взаємодій та завдяки подвійному шляху елімінації не потребує корекції дози в пацієнтів з помірним порушенням ниркової або печінкової функції. Метааналіз 15 рандомізованих контрольованих досліджень (n=7245) показав, що серед 5 уратзнижувальних препаратів (алопуринол, бензбромарон, фебуксостат, пеглогліказа та пробенецид) фебуксостат має найкращі профілі ефективності та безпеки.
Рекомендації зі зміни способу життя
Пацієнтам з ГУ рекомендовано зменшити вживання червоного м’яса, субпродуктів, морепродуктів, фруктози, солодких газованих напоїв та алкоголю, оскільки ці продукти підвищують рівні СК. Дієтичними факторами, які сприяють зниженню сироваткових рівнів СК, є кава, молочні продукти, вишні й аскорбінова кислота. Підвищене вживання солі (натрію) знижує рівні СК, але збільшує систолічний артеріальний тиск.
Дослідження показали, що зниження маси тіла та регулярні фізичні навантаження є ефективними в зниженні рівнів СК. Отже, всім пацієнтам з ГУ необхідно рекомендувати підтримання здорової ваги та підвищення фізичної активності.
Підготував Андрон Буряк
Медична газета «Здоров’я України 21 сторіччя» № 23 (444), грудень 2018 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Тіамін (вітамін В1) – важливий вітамін, який відіграє вирішальну роль в енергетичному обміні та метаболічних процесах організму загалом. Він необхідний для функціонування нервової системи, серця і м’язів. Дефіцит тіаміну (ДТ) спричиняє різноманітні розлади, зумовлені ураженням нервів периферичної та центральної нервової системи (ЦНС). Для компенсації ДТ розроблено попередники тіаміну з високою біодоступністю, представником яких є бенфотіамін. Пропонуємо до вашої уваги огляд досліджень щодо корисних терапевтичних ефектів тіаміну та бенфотіаміну, продемонстрованих у доклінічних і клінічних дослідженнях....
Актуальність проблеми порушень моторної функції шлунково-кишкового тракту (ШКТ) за останні десятиліття значно зросла, що пов’язано з великою поширеністю в світі та в Україні цієї патології. Удосконалення фармакотерапії порушень моторики ШКТ та широке впровадження сучасних лікарських засобів у клінічну практику є на сьогодні важливим завданням внутрішньої медицини....
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Однією із найвагоміших знахідок із часу відкриття дигіталісу Нобелівський комітет назвав синтез і дослідження β-блокаторів, які зараз мають провідні стабільні позиції у лікуванні більшості серцево-судинних хвороб (ішемічна хвороба серця – стенокардія, гострий коронарний синдром, інфаркт міокарда, артеріальна гіпертензія, серцева недостатність, тахіаритмії) (Радченко О.М., 2010). Це епохальне відкриття зроблено під керівництвом британського фармаколога Джеймса Блека (James Whyte Black), який отримав за нього Нобелівську премію в 1988 році. ...




