Клинический потенциал глимепирида в лечении больных сахарным диабетом 2 типа
 Сахарный диабет (СД) по-прежнему остается одной из наиболее актуальных проблем современной медицины. В рейтинге распространенности хронических неинфекционных заболеваний в большинстве стран мира он прочно удерживает лидирующие позиции, уступая первенство только артериальной гипертензии (АГ). Эксперты Международной диабетической федерации (IDF) прогнозируют дальнейшее увеличение количества больных СД, которое к 2035 году может превысить полмиллиарда, а к 2045 году составить 629 млн человек [1]. СД характеризуется хронической гипергликемией, развивающейся в результате нарушения секреции инсулина, его действия или их сочетания. По этиопатогенетическому принципу СД разделяют на два основных типа – СД 1 и 2 типов. В основе развития СД 1 типа лежит поражение β-клеток поджелудочной железы и их абсолютная неспособность к синтезу инсулина. К основным механизмам развития СД 2 типа относят неадекватную секрецию инсулина при сохраненной жизнеспособности β-клеток поджелудочной железы и инсулинорезистентность (ИР) – нарушение чувствительности инсулиновых рецепторов периферических тканей к собственному инсулину.
Сахарный диабет (СД) по-прежнему остается одной из наиболее актуальных проблем современной медицины. В рейтинге распространенности хронических неинфекционных заболеваний в большинстве стран мира он прочно удерживает лидирующие позиции, уступая первенство только артериальной гипертензии (АГ). Эксперты Международной диабетической федерации (IDF) прогнозируют дальнейшее увеличение количества больных СД, которое к 2035 году может превысить полмиллиарда, а к 2045 году составить 629 млн человек [1]. СД характеризуется хронической гипергликемией, развивающейся в результате нарушения секреции инсулина, его действия или их сочетания. По этиопатогенетическому принципу СД разделяют на два основных типа – СД 1 и 2 типов. В основе развития СД 1 типа лежит поражение β-клеток поджелудочной железы и их абсолютная неспособность к синтезу инсулина. К основным механизмам развития СД 2 типа относят неадекватную секрецию инсулина при сохраненной жизнеспособности β-клеток поджелудочной железы и инсулинорезистентность (ИР) – нарушение чувствительности инсулиновых рецепторов периферических тканей к собственному инсулину.
Этиологию СД нельзя считать изученной в полной мере. Оба типа СД имеют полигенный характер наследования, но «виновником» заболевания пока не признан ни один из изучаемых генов. При СД 1 типа генетическая предрасположенность ассоциирована с патологией иммунной системы, приводящей к развитию аутоиммунного воспаления и гибели β-клеток. Генетические дефекты, ответственные за развитие СД 2 типа, отражаются как на свойствах рецепторных комплексов, активности переносчиков глюкозы в клетки и сигнальных процессах метаболизма глюкозы, так и на процессах запрограммированной репликации и апоптоза β-клеток. Поэтому генетически обусловленная ИР сочетается со снижением синтеза инсулина ввиду наличия генетически детерминированной недостаточности островкового аппарата поджелудочной железы.
Количество больных СД различных типов прогрессивно увеличивается, что связано с потенцированием генетической предрасположенности средовыми факторами: для СД 1 типа таковыми являются факторы, губительно воздействующие на эндокринный аппарат поджелудочной железы, – вирусы (в частности, энтеровирусы, вирусы краснухи, Коксаки В, эпидпаротита), нитраты, тяжелые металлы, а также вещества, к которым снижена толерантность у детей раннего возраста (глютен, коровье молоко, ненасыщенные жиры), и другие, для СД 2 типа – гиподинамия и ожирение.
СД 2 типа не имеет ярко выраженного клинического дебюта и может диагностироваться поздно – в стадии сосудистых осложнений, которые являются следствием поражения сосудов разного калибра, то есть макро- и микроангиопатий. К макроангиопатиям относятся инфаркты, инсульты, облитерирующие заболевания сосудов нижних конечностей, к микроангиопатиям – ретинопатия, нефропатия, полинейропатия, тотальное поражение микрососудов всех органов и систем. Формирование макрососудистых осложнений начинается достаточно рано, на стадии предиабета, тогда как собственно СД 2 типа долгое время протекает латентно, поэтому нередко впервые его выявляют при клиническом обследовании пациентов острых кардиологических и неврологических отделений [2]. Итак, ключевыми звеньями патогенеза СД 2 типа считают ИР, нарушение секреции инсулина, повышение продукции печенью глюкозы, а также наследственную предрасположенность и особенности образа жизни и питания, способствующие ожирению [3].
Роль наследственного фактора в развитии СД 2 типа не вызывает сомнения. Многолетние исследования показали, что у монозиготных близнецов конкордантность для СД 2 типа приближается к 100%. Гиподинамия и нарушения в питании приводят к развитию ожирения, усугубляя тем самым генетически детерминированную ИР и способствуя реализации генетических дефектов, которые непосредственно ответственны за развитие СД 2 типа [3]. ИР – это общий механизм развития и прогрессирования компонентов метаболического синдрома – АГ, СД 2 типа и ожирения [3]. Ожирение, особенно висцеральное (центральное, андроидное, абдоминальное), играет важную роль как в патогенезе ИР и связанных с ней метаболических расстройств, так и в возникновении СД 2 типа. Это обусловлено особенностями висцеральных адипоцитов, которые характеризуются сниженной чувствительностью к антилиполитическому действию инсулина и повышенной чувствительностью к липолитическому действию катехоламинов. В связи с этим в висцеральной жировой ткани активизируется процесс липолиза, что, в свою очередь, приводит к поступлению большого количества свободных жирных кислот (СЖК) в портальную циркуляцию, а затем – в системный кровоток. В печени СЖК препятствуют связыванию инсулина с гепатоцитами, что, с одной стороны, способствует системной гиперинсулинемии, а с другой – усугубляет ИР гепатоцитов и подавляет ингибирующий эффект гормона на печеночный глюконеогенез и гликогенолиз. Последнее обстоятельство обусловливает повышенную продукцию глюкозы печенью. Высокая концентрация СЖК в периферическом кровотоке усугубляет ИР скелетных мышц и препятствует утилизации глюкозы миоцитами, что приводит к гипергликемии и компенсаторной гиперинсулинемии. Так формируется замкнутый круг: увеличение концентрации СЖК ведет к еще большей ИР на уровне жировой, мышечной и печеночной ткани, гиперинсулинемии, активации липолиза и еще большему нарастанию концентрации СЖК. Гиподинамия также усугубляет имеющуюся ИР, поскольку транслокация транспортеров глюкозы 4 типа (ГЛЮТ‑4) в мышечной ткани в состоянии покоя резко снижена [3].
! ИР, обычно имеющая место при СД 2 типа, представляет собой состояние, характеризующееся недостаточным биологическим ответом клеток на инсулин при его достаточной концентрации в крови. В настоящее время ИР в большей степени связывают с нарушением действия инсулина на пострецепторном уровне, в частности со значительным снижением мембранной концентрации специфических ГЛЮТ‑4, ГЛЮТ‑2, ГЛЮТ‑1 [3]. По современным представлениям СД 2 типа манифестирует в ситуации, когда секреторные возможности β-клеток оказываются несостоятельными для преодоления барьера ИР [4].
Гипергликемия и гиперинсулинемия – причина сосудистой эндотелиальной дисфункции, лежащей в основе поражения органов-мишеней (сердца, сосудов, почек, головного мозга, печени), от состояния которых зависит прогноз заболевания [5, 6]. Патофизиология диабетических ангиопатий заключается в повреждении эндотелия, что сопровождается адгезией тромбоцитов к структурам сосудистой стенки. Высвобождающиеся при этом медиаторы воспаления способствуют сужению сосудов и увеличению их проницаемости. Гипергликемия вызывает дисфункцию эндотелия, снижение синтеза вазодилататоров при одновременном повышении выброса вазоконстрикторов и прокоагулянтов, что способствует развитию поздних осложнений СД [7]. Гипергликемия способствует гликозилированию белков, оксидативному стрессу, развитию атеросклероза, нарушению метаболизма фосфоинозитида, ведущих к нарушению клеточных функций. При этом важную роль играют нарушения гемостаза и микроциркуляции. Поэтому оптимальное лечение СД 2 типа включает терапию гипергликемии и дисметаболического синдрома [7].
Сегодня СД 2 типа рассматривают как эквивалент клинически выраженного сердечно-сосудистого заболевания (ССЗ). СД в 2-4 раза увеличивает риск развития ССЗ, а смертность при их сочетании возрастает в 4-5 раз. В структуре смертности больных СД основное место занимают инфаркт миокарда (ИМ) (55%) и инсульт (29%), что в 70 раз превышает частоту смертности от микрососудистых осложнений и диабетической комы (1-4%) [8-13]. Большой интерес представляет зависимость степени сердечно-сосудистого риска от уровней гликемии натощак и после еды. Взаимосвязь между постпрандиальным уровнем глюкозы и кардиоваскулярной смертностью была изучена во многих исследованиях: Honolulu Heart Program (1987), Diabetes Intervention Study (1996), Whitehall, Paris and Helsinki Study (1998), The Rancho-Bernardo Study (1998), DECODE (1999), Pacific and Indian Ocean (1999), Funagata Diabetes Study (1999). Установлена линейная связь между сердечно-сосудистым риском и уровнем гликемии, при этом постпрандиальный уровень глюкозы имеет большее прогностическое значение в отношении сердечно-сосудистого риска, нежели гликемия натощак. Сопоставляя влияние постпрандиальной гипергликемии как самостоятельного фактора риска на уровень смертности от сердечно-сосудистой патологии (СС-патологии), исследователи пришли к выводу, что по своей значимости постпрандиальная гипергликемия сопоставима с такими общепризнанными факторами риска, как гипертриглицеридемия и АГ. Установлено, что даже развитие бессимптомной гипергликемии после приема пищи достоверно увеличивает риск смерти от ишемической болезни сердца. Это дало право некоторым исследователям утверждать, что кратковременные, но повторяющиеся эпизоды повышения уровня глюкозы крови после приема пищи являются более значимым фактором риска развития кардиоваскулярной патологии, чем гипергликемия натощак [14].
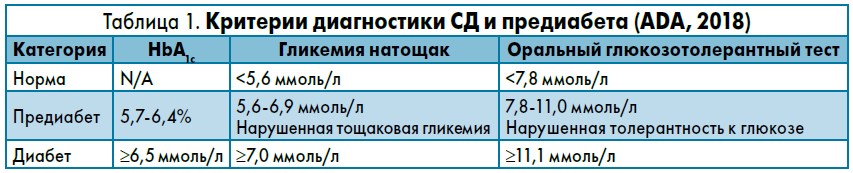
Лечение больных СД 2 типа включает комплекс мероприятий, направленных на коррекцию образа жизни, гликемический контроль, контроль АД и липидного обмена. Комплексный подход к лечению больных СД 2 типа безусловно способствует позитивным результатам. За последние 10 лет увеличилась доля пациентов с диабетом, которые достигли рекомендуемого уровня гликированного гемоглобина (HbA1c), артериального давления (АД) и холестерина (ХС) липопротеидов низкой плотности (ЛПНП). Это сопровождалось улучшением сердечно-сосудистых исходов и привело к существенному сокращению микрососудистых осложнений на конечной стадии. Тем не менее от 33 до 49% пациентов все еще не имеют целевых уровней гликемии, АД или ХС, и только у 14% больных отмечается достижение целевых уровней всех трех показателей [15-17]. Поэтому обоснованы предположения, что прогресс контроля сердечно-сосудистого риска может замедлиться. В связи с этим Американская диабетическая ассоциация (ADA) рекомендует проводить скрининг на диабет и предиабет у двух категорий лиц: 1) у лиц в возрасте старше 45 лет – если факторов риска нет, скрининг СД 2 типа необходимо проводить каждые 3 года; 2) у взрослых любого возраста с избытком веса (ИМТ>25 кг/м2) или другими факторами риска (как минимум одним фактором риска – низкая физическая активность; наличие СД у родственников первой степени родства; гестационный СД у женщин или рождение ребенка с массой тела >4 кг; наличие АГ; гиперхолестеринемия или гипертриглицеридемия; синдром поликистозных яичников у женщин; HbA1c ≥5,7%, повышенный уровень гликемии натощак или нарушение толерантности к глюкозе при предыдущем тестировании; наличие ССЗ в анамнезе и др.) [18].
Критерии диагностики СД и предиабета представлены в таблице 1.
Основными инструментами лечения СД 2 типа являются коррекция образа жизни и медикаментозная терапия. Целевые уровни гликемии, АД, липидов: HbA1c <7,0% (индивидуально), гликемия натощак 3,9-7,2 ммоль/л, постпрандиальная гликемия (ППГ) <10 ммоль/л, АД <140/90 мм рт. ст. для большинства больных и <130/80 мм рт. ст. при высоком сердечно-сосудистом риске, ЛПНП <2,6 ммоль/л или <1,8 ммоль/л (при СС-патологии и очень высоком риске кардиоваскулярных осложнений), липопротеины высокой плотности (ЛПВП) >1,0 ммоль/л (мужчины) и >1,3 ммоль/л (женщины), общие триглицериды <1,7 ммоль/л [19, 21, 22].
Известно, что в основе развития СД 2 типа лежат ряд эндокринных дефектов: нарушение секреции инсулина, ИР жировой и мышечной тканей и ИР печени. Возможности коррекции этих нарушений определяют прогноз. Резистентность к инсулину может уменьшаться в результате снижения веса и/или под влиянием лекарственных средств, однако она редко восстанавливается до нормальной. Секреция инсулина у этих больных неполноценна и недостаточна для того, чтобы компенсировать ИР [22]. Уже в момент установления диагноза СД 2 типа функционирует лишь 50% β-клеток, и в дальнейшем секреция инсулина продолжает ежегодно снижаться на 5-6%. Таким образом, большинство пациентов с СД 2 типа уже на ранних этапах заболевания нуждаются в назначении им препаратов, влияющих на секрецию инсулина. Эксперты АDА в 2018 году предложили алгоритм ведения пациентов с предиабетом и факторами риска СД (табл. 2).
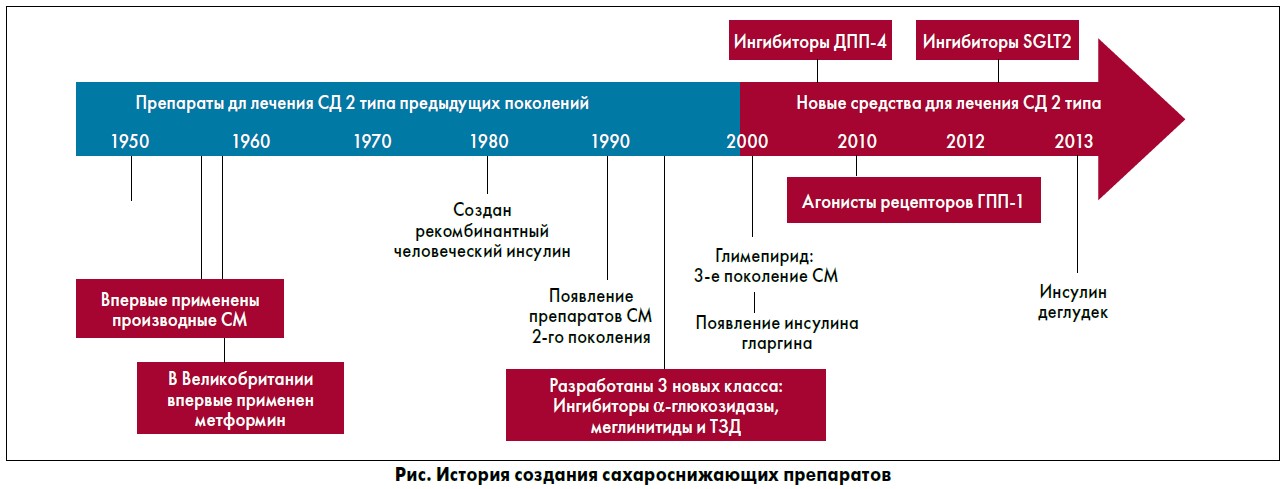
Что касается СД 2 типа, то в большинстве случаев диагноз устанавливается не на самых ранних стадиях, и лечение требует комбинации бигуанида метформина, повышающего чувствительность тканей к инсулину, с другими сахароснижающими препаратами, способными одновременно и активировать синтез инсулина, среди которых производные сульфонилмочевины (СМ), меглитиниды, а также новые классы – инкретиномиметики и ингибиторы дипептидилпептидазы‑4 (ДПП‑4). Однако если в отношении препаратов СМ накоплен более чем 50-летний опыт применения, то долгосрочные эффекты и безопасность новых сахароснижающих средств требуют дальнейшего изучения.
История создания сахароснижающих средств представлена на рисунке.
Препараты СМ с успехом используются для лечения СД 2 типа в течение многих лет. Они оказывают влияние на два звена патогенеза заболевания, а именно увеличивают секрецию инсулина и повышают его утилизацию периферическими тканями (печени, мышечной и жировой тканью). В Европе высокая эффективность препаратов СМ в снижении уровня гликированного гемоглобина (на 1,5-2,0%) позволяет использовать этот класс препаратов в качестве монотерапии почти у 70% больных СД 2 типа.
В зависимости от фармакодинамических характеристик препараты СМ можно условно разделить на три поколения. Представителями первого поколения являются толбутамид, карбутамид, хлорпропамид и некоторые другие лекарственные средства, которые сегодня не используются в клинической практике. К препаратам второго поколения относятся глибенкламид, глипизид, гликлазид и гликвидон. Третье поколение представлено молекулой глимепирида. Очень актуальным является вопрос выбора конкретного лекарственного средства из этой группы препаратов. В этих случаях целесообразно обращать внимание на такие важные характеристики препарата, как его глюкозоснижающая активность, длительность действия, частота и выраженность гипогликемических состояний, безопасность в отношении влияния на сердечно-сосудистую систему и массу тела пациента.
В клинической практике при назначении глимепирида (Амарил®) следует помнить, что он обладает рядом уникальных и полезных свойств. Двойной механизм действия препарата – уменьшение ИР за счет улучшения транспорта глюкозы в клетку и мягкая стимуляция образования инсулина (минимальное соотношение между уровнем секреции инсулина и уровнем снижения гликемии) [23]. Как и традиционные препараты СМ, Амарил® стимулирует секрецию инсулина путем закрытия АТФ-зависимых калиевых каналов (КАТФ-каналов) панкреатических β-клеток. Однако уже на этом, наиболее существенном, этапе действия проявляется отличие Амарила от других препаратов СМ.
! В то время как другие препараты СМ связываются на клеточной мембране β-клетки с рецептором, молекулярная масса которого составляет 140 кДа, Амарил® связывается с субъединицей этого рецептора массой 65 кДа. Благодаря этому Амарил® в 2,5-3 раза быстрее связывается со своим рецептором по сравнению с другими препаратами СМ. Таким образом, Амарил® обладает быстрым началом действия.
Кроме того, препарат способен высвобождаться и диссоциировать с рецепторным аппаратом β-клетки в 8-9 раз быстрее, чем другие препараты СМ, что обусловливает менее выраженное повышение уровня инсулина и, как следствие, более редкое развитие нежелательных эффектов и гипогликемических реакций по сравнению с другими похожими сахароснижающими препаратами [24]. Амарил® обеспечивает оптимальный контроль гликемии в течение суток при однократном утреннем приеме, при этом уровень инсулинемии значительно ниже, чем при использовании других производных СМ. К тому же однократный прием увеличивает приверженность к терапии. Интересным является тот факт, что Амарил® не вызывает прибавки массы тела и даже способствует ее снижению, тогда как увеличение массы тела и частые гипогликемии являются основными побочными эффектами у других препаратов СМ. Подобный эффект объясняется блокированием дифференциации адипоцитов, что делает Амарил® препаратом выбора у больных СД 2 типа, ассоциированным с ожирением [23].
Амарил® обладает экстрапанкреатическим эффектом, то есть он ограничивает утилизацию глюкозы путем перенесения ее молекул сквозь плазматическую мембрану посредством ГЛЮТ‑4. Амарил® усиливает перемещение ГЛЮТ‑4 от микросом низкой плотности к плазматической мембране инсулинорезистентных жировых и мышечных клеток. Также Амарил® усиливает утилизацию глюкозы периферическими тканями, повторяя эффект инсулина [25].
Другие внепанкреатические эффекты Амарила [26]:
Антиагрегантный:
- ингибирует агрегацию тромбоцитов более выраженно, чем гликлазид и глибенкламид;
- восстанавливает фибринолитическую активность сосудистого эндотелия.
Антихолестеринемический:
- уменьшает рост атеросклеротической бляшки;
- повышает уровень адипонектина.
Антиишемический:
- уменьшает частоту желудочковых экстрасистолий после перевода с гликлазида;
- не влияет на ишемическое прекондиционирование миокарда.
Эффективность, безопасность, плейотропность и доступная стоимость позволяют рассматривать препараты СМ в качестве основного варианта лечения СД при непереносимости метформина или дополнительной терапии к лечению метформином. Предпочтения отдаются глимепириду (Амарил®) и гликлазиду благодаря их способности снижать смертность от всех причин, сердечно-сосудистую смертность, исходы сочетания острого ИМ и инсульта, не влиять негативно на почки. Кроме того, они предпочтительны по сравнению с обычными препаратами СМ у пациентов с высоким риском развития гипогликемии, при ожирении, повышенном риске ССЗ или их наличии [27].
В Центральном Южном университете (Китай) изучали влияние глимепирида на метаболические параметры и сердечно-сосудистые факторы риска у пациентов с недавно диагностированным СД 2 типа. Глимепирид быстро и стабильно улучшал гликемический контроль и метаболизм липопротеинов, значительно снижал резистентность к инсулину и усиливал фибринолитическую активность [28].
! Амарил® – это препарат СМ, который может использоваться как в монотерапии, так и в сочетании с другими антигипергликемическими агентами, включая инсулин. Это единственный препарат СМ, рекомендованный для использования одновременно с инсулином.
Амарил® эффективен в снижении уровней глюкозы в плазме крови натощак, ППГ и HbA1c и является полезным, экономически эффективным вариантом лечения СД 2 типа.
Британское широкомасштабное проспективное исследование СД United Kingdom Prospective Diabetes Study (UKPDS), которое осуществлялось в течение 30 лет, показало, что по сравнению с диетой пациенты на интенсивной терапии с помощью препаратов СМ имели значительно более сниженный относительный риск возникновения микрососудистых заболеваний (24%; р=0,001), ИМ (15%; р=0,01), смерти от диабета (17%; р=0,01) или от любой причины (13%; р=0,007) [29, 30].
В Японии наблюдается устойчивый рост числа пациентов с диабетом – наиболее часто используемыми в этой стране являются препараты СМ и пиоглитазон: метаанализ рандомизированных исследований показал, что пиоглитазон увеличивал риск сердечной недостаточности и побочных эффектов в виде увеличения веса, отеков и переломов. Было проведено сравнительное исследование эффективности и безопасности терапии первой линии с глимепиридом и пиоглитазоном у пациентов с СД 2 типа (n=191): в группе глимепирида на 3-м мес терапии было значительно ниже среднее значение HbA1c (6,9±0,7% vs 7,3±1,0%; р=0,022) и достоверно большие снижения уровней общего ХС и его атерогенных фракций; в группе пиоглитазона на 6-м мес наблюдались значительные внутригрупповые увеличения массы тела и уровня натрийуретического пептида типа В (BNP) в крови. Оба эти антидиабетические средства хорошо переносились – единственными побочными эффектами, связанными с лечением, были отеки у четырех пациентов в группе пиоглитазона и запоры у одного пациента в группе глимепирида [31].
Японские ученые исследовали эффективность глимепирида в улучшении артериальной жесткости, оцененной сердечно-сосудистым индексом (CAVI), у пациентов с СД 2 типа. По сравнению с глибенкламидом глимепирид улучшал CAVI, снижал уровень оксидативного стресса и ИР [32].
Проведено сравнительное исследование влияния глимепирида и глибенкламида на ИР, адипоцитокины и развитие атеросклероза. В группе глимепирида по сравнению с группой глибенкламида:
- выраженно снизился индекс ИР HOMA-IR (Homeostasis Model Assessment of Insulin Resistance);
- увеличился уровень в крови адипонектина;
- значительно снизились уровни в плазме фактора некроза опухоли-альфа, интерлейкина‑6 и С-реактивного белка;
- были значительно ниже скорость пульсовой волны и индекс аугментации, свидетельствующие о позитивном влиянии глимепирида на жесткость сосудистой стенки (ее снижение) [33].
В Университете Альберты (г. Эдмонтон, Канада) был выполнен систематический обзор и метаанализ исследований риска смертности среди больных СД 2 типа, получавших препараты СМ. Прием глимепирида был связан с более низким риском смертности от всех причин и вследствие ССЗ по сравнению с глибенкламидом [34].
В Кливлендском государственном университете (г. Кливленд, штат Огайо, США) изучался риск общей смертности у пациентов с СД 2 типа, получавших глипизид, глибенкламид или глимепирид в виде монотерапии. При этом была выявлена тенденция к снижению риска смерти в группе глимепирида [35].
Итак, Амарил®:
- эффективный и быстродействующий гипогликемический препарат, снижающий постпрандиальную гипергликемию и гипергликемию натощак при однократном приеме с минимальным риском гипогликемических состояний;
- препарат выбора в лечении больных СД 2 типа в тех случаях, когда диетотерапия, физические нагрузки и прием бигуанидов не приводят к ожидаемому результату;
- эффективен у больных СД 2 типа с избыточной массой тела или ожирением;
- используется при отсутствии ответа на другие пероральные сахароснижающие препараты;
- рекомендуется применять у больных с СД 2 типа при интенсивных физических нагрузках;
- целесообразно назначать пациентам, имеющим в анамнезе сосудистые катастрофы (инфаркты, инсульты);
- имеет большой диапазон дозировок, что дает возможность индивидуально подбирать дозу для каждого пациента.
Список литературы находится в редакции.
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (44) грудень 2018 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....
Метформін – протидіабетичний препарат першої лінії, який пригнічує глюконеогенез у печінці і в такий спосіб знижує рівні глюкози в крові. Крім того, він знижує ризик кардіоваскулярних подій, чинить нефропротекторний ефект і здатен подовжувати тривалість життя. Завдяки цим властивостям метформін нині розглядають як мультифункціональний препарат і дедалі частіше застосовують для лікування та профілактики різноманітних захворювань....
Сучасне лікування хворих на цукровий діабет (ЦД) 2 типу включає зміну способу життя і медикаментозну терапію для контролю глікемії та профілактики ускладнень. Проте дослідження показують, що на практиці небагато хворих досягають контролю захворювання (частково через погану прихильність до лікування). Частка пацієнтів, які дотримуються протидіабетичної терапії, коливається від 33 до 93% (упродовж 6-24 міс) [1, 2]....