Вірусний гепатит В: експресія дефектних поверхневих антигенів і патогенез

Вірус гепатиту В (HBV) є одним з найважливіших і найпоширеніших патогенів людини. Станом на 2016 р. поверхневий антиген HBV (HBsAg) мали 290 млн осіб, тобто 3,9% світової популяції. HBV уражає переважно гепатоцити та викликає широкий спектр клінічних проявів від безсимптомного носійства до гострого та хронічного гепатиту з подальшим прогресуванням у цироз і гепатоцелюлярну карциному. Для лікування пацієнтів з хронічним гепатитом В сьогодні застосовують інтерферон-α й аналоги нуклеотидів, проте ефективність лікування не така, як мала б бути. Краще розуміння молекулярного патогенезу HBV-інфекції може сприяти розробленню нових методів лікування та профілактики.
Особливості реплікацїї HBV
HBV належить до родини Hepadnaviridae і є невеликим, вкритим оболонкою вірусом із геномом у вигляді частково дволанцюжкової ДНК розміром близько 3,2 кб. Протягом життєвого циклу HBV прегеномна РНК транскрибується з ковалентно замкненої циркулярної ДНК і слугує шаблоном для реплікації ДНК HBV шляхом зворотної транскрипції, опосередкованої полімеразою вірусу. Оскільки остання позбавлена коректувальної функції, геном HBV еволюціонує зі швидкістю від 1×10-3 до 1×10-6 замін нуклеотидів на 1 цикл реплікації. Реплікація HBV включає зворотну транскрипцію, подібну до такої у ретровірусів, проте складна структура геному HBV обмежує спектр і швидкість мутацій. Водночас цей унікальний спосіб реплікації забезпечує велику різноманітність геномів HBV, що в контексті довготривалої еволюції HBV веде до появи різних генотипів, субтипів, мутантів, рекомбінантів і навіть квазівидів вірусу. У низці досліджень продемонстровано, що поява варіантів HBV відіграє важливу роль у прогресуванні HBV-асоційованих хвороб печінки. Одним із типів мутації з великою клінічною значимістю є мутація, яка спричиняє експресію дефектного поверхневого антигену.
Біологія поверхневих антигенів HBV
Три білки оболонки вірусу – великий (LHB, або L-HBsAg), середній (MHB, або M-HBsAg) та малий (SHB, або S-HBsAg) поверхневі антигени – експресуються з єдиної відкритої рамки зчитування (S-ORF), але транслюються з двох різних мРНК. LHB кодується субгеномною РНК довжиною 2,4 кб, MHB та SHB – субгеномною РНК довжиною 2,1 кб. Ці субгеномні РНК керуються промоторами preS1 та preS2/S відповідно, що дозволяє здійснювати варіабельну регуляцію експресії протеїнів. Промотор preS1 розташований у висхідному регіоні S-ORF, тоді як промотор preS2 відповідає домену preS1. Таким чином, транскрипція субгемномної РНК 2,1 кб також регулюється доменом preS1 (рис.).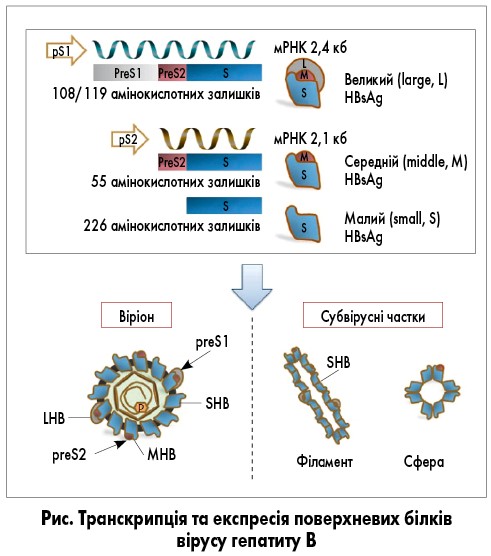
Поверхневі протеїни мають однаковий карбокситермінальний регіон, а їх неоднакова довжина зумовлена різними амінотермінальними регіонами. Через це LHB містить preS1 + preS2 + S (389 або 400 амінокислотних залишків), MHB – preS2 + S (281 амінокислотний залишок), а SHB – лише S-домен (226 амінокислотних залишків). Крім того, існує усічений і мутований preS2/S, що є продуктом інтегрованих вірусних послідовностей, дефектних для реплікації. LHB, MHB та SHB є важливими для структури та життєвого циклу HBV. Шляхом зв’язування preS1 домену (амінокислотної послідовності 2-48) з рецептором HBV на гепатоцитах (таурохолат-котранспортним поліпептидом – NTCP) LHB забезпечує потрапляння вірусу в клітину з подальшим інфікуванням, а також є необхідним для побудови та збірки віріонів. Вважають також, що LHB реаранжує свою структуру протягом дозрівання віріонів HBV і таким чином регулює вивільнення й інфективність віріонів. Точна роль MHB та SHB не встановлена.
Ранні дослідження свідчили, що MHB не є обов’язковим для реплікації HBV і побудови віріона; водночас є дані, які вказують на роль MHB у секреції віріонів. Зокрема, MHB взаємодіє з церулоплазміном і впливає на продукування позаклітинних віріонів. SHB як домінуючий компонент вірусних часток є необхідним для продукування віріонів і субвірусних часток. У зрілих (інфекційних) віріонах співвідношення LHB, MHB та SHB в оболонці становить орієнтовно 1:1:4. Зміна цієї пропорції порушує продукування та вивільнення віріонів. Щодо субвірусних часток, то їх кількість у 10 000-1 000 000 разів перевищує таку віріонів, і ці частки серологічно ідентифікуються як HBsAg. Секреція субвірусних часток може дозозалежно пригнічуватися під дією LHB, що переключає S-білок на побудову віріона.
Домени preS1, preS2 та S містять низку епітопів В- і Т-лімфоцитів, що може мати значення для розвитку імунної відповіді. Великий гідрофільний регіон (MHR) у межах амінокислотної послідовності 100-169 SHB, особливо а-детермінантний регіон у послідовності 124‑147, є найважливішою антигенною детермінантою у поверхневих білках HBV, а також необхідний для ідентифікації HBsAg та розроблення вакцини проти HBV. Отриманий з плазми крові рекомбінантний HBsAg використовувався для створення вакцин і викликав потужну специфічну захисну відповідь. Вважається, що наявність анти-HBs-антитіл забезпечує достатній імунітет проти HBV-інфекції. Натомість велика кількість циркулювального HBsAg у пацієнтів із хронічною HBV-інфекцією, ймовірно, є свідченням порушеної імунної відповіді. Дефектна HBsAg-специфічна відповідь Т-лімфоцитів у хронічно інфікованих осіб корелює з сироватковими титрами HBsAg. Це є свідченням того, що надлишкове продукування HBsAg впливає на імунну систему у спосіб, вигідний для вірусу. In vitro HBsAg може змінювати функцію Toll-подібних рецепторів і стимулювати продукування інтерлейкіну‑10 купферівськими клітинами. Нещодавно було встановлено, що в осіб із хронічною HBV-інфекцією HBsAg може полегшувати індукцію мієлоїдних супресорних клітин. HBsAg також асоціюється з індукцією регуляторних Т-лімфоцитів. Отже, HBsAg є не лише структурним компонентом віріонів і субвірусних часток, а й важливим модулятором імунної відповіді.
Експресія дефектного HBsAg і її наслідки
Мутанти HBsAg уперше виявили в осіб, які були вакциновані проти HBV, але захворіли на HBV-інфекцію попри наявність захисних анти-HBs-антитіл. Ці мутанти характеризуються зниженою здатністю зв’язуватися з анти-HBs-антитілами та нижчою реактивністю у лабораторних тестах. Найбільш відомими мутаціями HBsAg є sG145R та sK122I, за яких порушується нейтралізація і кліренс HBsAg при HBV-інфекції. Інші мутації, наприклад sT123N, можуть впливати на секрецію HBsAg.
На сьогодні відомо, що мутації, які ведуть до появи дефектного HBsAg, можуть виявлятись при гострій HBV-інфекції, хронічному гепатиті В, носійстві HBV та асоційовані з тяжкими хворобами печінки, зокрема цирозом, фульмінантним гепатитом В і гепатоцелюлярною карциномою. Поки не встановлено, чи мутанти за HBsAg виникають внаслідок адаптації вірусу до запалення і зниження функції печінки, чи вони є причиною тяжчого ураження печінки.
З’являються дані про те, що експресія дефектних поверхневих антигенів бере участь у патогенезі фульмінантного гепатиту. Делеції preS і мутації в а-детермінантному регіоні спричиняють секрецію дефектного HBsAg, який може посилювати синтез та ампліфікацію ковалентно замкненої циркулярної ДНК, полегшуючи реплікацію HBV. Накопичення дефектного HBsAg у клітині може викликати стрес ендоплазматичного ретикулуму з подальшою аутофагією, що ще більше посилює реплікацію вірусу. У свою чергу, посилена реплікація HBV призводить до подальшого накопичення дефектного HBsAg, за механізмом позитивного зворотного зв’язку формується хибне коло, збільшується ушкодження гепатоцитів. Цей процес супроводжується швидким розвитком запалення з надмірною реакцією цитотоксичних Т-лімфоцитів, що сприяє прогресуванню фульмінантного гепатиту.
Експресія дефектних антигенів також може брати учаcть у безсимптомному носійстві HBV. Останнє характеризується наявністю дуже низьких рівнів ДНК HBV у плазмі крові та/або печінці в осіб з негативними результатами тесту на HBsAg. Небезпека безсимптомного носійства полягає у можливій передачі вірусу через кров, під час трансплантації органів, гемодіалізу або від матері до дитини, потенційному розвитку цирозу та гепатоцелюлярної карциноми. Реактивація HBV часто спостерігається після хіміотерапії, імуносупресивної терапії, після трансплантації, а також у пацієнтів з коінфекцією вірусом імунодефіциту людини або гепатиту С, що може призводити до розвитку фульмінантного гепатиту та смерті.
Мутації поверхневих антигенів, зокрема делеції preS, можуть порушувати транскрипцію субгеномної РНК HBV (2,4 та 2,1 кб), що веде до зниження рівнів трьох поверхневих білків HBV. Крім того, дефектні поверхневі антигени з делеціями preS і мутаціями в а-детермінантному регіоні відрізняються зниженою секрецією. Одиничні або множинні мутації MHR у межах амінокислотних залишків 99-169 SHB, особливо в а-детермінантному регіоні (124-147), можуть викликати конформаційні зміни HBsAg. Мутований HBsAg погано визначається імуноферментними методами, що в деяких випадках може розцінюватися як безсимптомне носійство HBV.
Висновки
- Поверхневі антигени HBV є корисними маркерами для діагностики HBV-інфекції та клінічного спостереження.
- У разі хронічної інфекції геном HBV може набувати й накопичувати мутації та делеції, які ведуть до експресії дефектних поверхневих антигенів HBV.
- Дефектні поверхневі антигени можуть брати участь у прогресуванні HBV-асоційованих захворювань та ускладнювати визначення HBsAg імуноферментними методами на основі антитіл.
- Сучасні препарати для лікування пацієнтів з HBV-інфекцією, як-от аналоги нуклеотидів, ефективно пригнічують синтез ДНК HBV, але не впливають на експресію генів. Через це білки HBV (включно з поверхневими антигенами) продовжують продукуватися на тлі терапії.
- Перспективним є розроблення специфічних засобів, які блокують патогенний потенціал білків HBV, наприклад шляхом сайленсингу РНК.
Список літератури знаходиться в редакції.
Стаття друкується у скороченні.
Wu C.-C. et al. Hepatitis B virus infection: Defective surface antigen expression and pathogenesis. World J Gastroenterol. 2018 Aug 21; 24(31): 3488-3499.
Переклав з англ. Олексій Терещенко
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (51), лютий 2019 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...




