Функціональні гастроінтестинальні розлади в дітей: що нового?

 Досить швидко пролетіли 10 років з моменту обговорення та публікації так званих Римських критеріїв III діагностики функціональних гастроінтестинальних розладів (ФГІР) (Drossman, 2006), положення яких також дискутувалися й в інших країнах (Пиманов С. І., Силивончик Н. Н., 2006; Майданник В. Г., 2007; 2010). Незважаючи на результати проведених численних досліджень, проблема ФГІР дотепер залишається актуальною (Drossman, Hasler, 2016). Нещодавно в м. Сан-Дієго (США) відбулася довгоочікувана подія: в рамках Американського тижня гастроентерології (Digestive Disease Week), що проводився за підтримки Американської асоціації гастроентерологів (American Gastroenterological Association), було не лише прийнято й озвучено нові критерії діагностики функціональних порушень (Римські критерії IV – Rome IV), а й внесено суттєві зміни та доповнення в документ. У роботі конференції взяли участь 117 дослідників та експертів з 23 країн. Очолював цю досить складну роботу професор Douglas Arnold Drossman (Adjunct Professor of Gastroenterology and Psychiatry, Center for Functional GI and Motility, University of North Carolina at Chapel Hill).
Досить швидко пролетіли 10 років з моменту обговорення та публікації так званих Римських критеріїв III діагностики функціональних гастроінтестинальних розладів (ФГІР) (Drossman, 2006), положення яких також дискутувалися й в інших країнах (Пиманов С. І., Силивончик Н. Н., 2006; Майданник В. Г., 2007; 2010). Незважаючи на результати проведених численних досліджень, проблема ФГІР дотепер залишається актуальною (Drossman, Hasler, 2016). Нещодавно в м. Сан-Дієго (США) відбулася довгоочікувана подія: в рамках Американського тижня гастроентерології (Digestive Disease Week), що проводився за підтримки Американської асоціації гастроентерологів (American Gastroenterological Association), було не лише прийнято й озвучено нові критерії діагностики функціональних порушень (Римські критерії IV – Rome IV), а й внесено суттєві зміни та доповнення в документ. У роботі конференції взяли участь 117 дослідників та експертів з 23 країн. Очолював цю досить складну роботу професор Douglas Arnold Drossman (Adjunct Professor of Gastroenterology and Psychiatry, Center for Functional GI and Motility, University of North Carolina at Chapel Hill).
Мета даної статті – ознайомити широке коло лікарів, зокрема лікарів-педіатрів та лікарів-гастроентерологів, із сучасним станом розуміння такої складної патології, як функціональні розлади шлунково-кишкового тракту (ФР ШКТ).
Як відомо, історія розробки критеріїв для діагностики ФГІР бере свій початок у Римі. Тридцять років тому Aldo Torsoli, професор гастроентерології в Римському університеті, займався створенням робочих груп для міжнародної наради з гастроентерології, що проходила в столиці Італії в 1988 р. В усіх регіонах світу було обрано експертів для співпраці на основі консенсусу, щоб сформулювати єдину думку щодо складних клінічних питань, на які не можна знайти відповідь за допомогою наукових доказів, і представити результати своєї роботи на цій зустрічі (Milholland et al., 1973; Torsoli, Corazziari, 1991). А. Torsoli разом з W. G. Thompson, доктором медицини з Оттави (Канада), авторитетним гастроентерологом, який вивчав нову область ФР ШКТ, сформував робочу групу з розробки критеріїв консенсусу для діагностики синдрому подразненого кишечнику (СПК). У той час Thompson та ін. були одними з небагатьох експертів, які працювали з епідеміологічними, клінічними й психосоціальними дослідженнями СПК. Потім вони опублікували перші діагностичні критерії для СПК на основі консенсусу.
Ця робоча група з СПК продовжила подальший Римський процес шляхом створення критеріїв діагностики на основі консенсусу між експертами в усьому світі. Проте СПК не був єдиним ФР ШКТ. У 1980-х роках були вивчені публікації про інші неструктурні симптоми на основі розладів: некардіальний функціональний біль у грудях (Richter et al., 1986); невиразкову диспепсію (Talley, Piper, 1985); постхолецистектомічний біль (Funch-Jensen et al., 1982); кишкові розлади, пов’язані зі здуттям живота, діареєю, закрепами й аноректальними розладами, включно з нетриманням калу, важкою дефекацією і ректальним болем (Whitehead et al., 1985; Whitehead, Schuster, 1987), – для яких не було загального робочого визначення або класифікації.
У 1989 р. Torsoli і Corazziari з Римського університету приєдналися до Drossman, щоб продовжити роботу в команді. D. A. Drossman запропонував розробити систему класифікації для всіх ФР ШКТ і створити для них критерії діагностики. За підтримки журналу Gastroenterology International був розпочатий процес створення системи класифікації з критеріями діагностики для всіх ФР ШКТ (Drossman, 2016). У 1994 р. статті були зібрані в книгу The Functional Gastrointestinal Disorders: Diagnosis, Pathophysiology, and Treatment («Функціональні шлунково-кишкові розлади: діагностика, патофізіологія та лікування»; Drossman et al., 1994), що назаразі вважається Римськими критеріями I. Згодом були запропоновані Римські критерії II (Drossman et al., 1999) і III (Drossman, 2006), які також обговорювалися в нашій країні (Майданник В. Г., 2007; 2010).
Причиною внесення змін до Римських критеріїв IV стали результати численних досліджень, що проводилися протягом останніх 10 років.
Визначення
Протягом усього періоду вивчення визначення ФР ШКТ змінювалося залежно від соціальних перспектив хвороби, наукових даних, а також підготовки клініцистів та особистої упередженості. Навіть сьогодні ФР ШКТ розглядаються багатьма як менш підтверджений діагноз, ніж діагноз з патологічною основою; також пацієнти з ФР ШКТ можуть бути визначені за симптоми, які вони вважають дуже реальними. Така ситуація виникла після попереднього обговорення питання щодо впливу дуалістичних принципів, які відокремлюють органічні та функціональні розлади, що часто вважаються психіатричними або залишаються без визначення (Drossman, 2005). Однак з плином часу і з кожною новою публікацією визначення мінялося: від відсутнього органічного захворювання до психічного розладу через стрес і до розладу моторики, а з Римськими критеріями III – до розладу шлунково-кишкового функціонування (Drossman et al., 2006).
Але все ще існує необхідність в конструктивному робочому визначенні, щоб підійти до цих розладів з наукової точки зору і без упередженості. Щоб досягти цього в Римських критеріях IV, Радою директорів було створено і поширено між головами і співголовами комітетів Римських критеріїв IV нове визначення з метою отримати відгуки для редагування й остаточного схвалення. Узгоджене визначення є таким: «Функціональні розлади шлунково-кишкового тракту є розладами взаємодії між кишечником і головним мозком» (Drossman, 2016). Ця група захворювань, класифікованих за шлунково-кишковими симптомами, пов’язана з будь-якою комбінацією певних функцій, як-от: моторика, порушення вісцеральної гіперчутливості, змінені слизова оболонка й імунні функції, зміна кишкової мікробіоти, змінена робота центральної нервової системи (ЦНС).
На думку експертів, це визначення найбільш відповідає сучасному розумінню кількох патофізіологічних процесів, які окремо або разом визначають особливості симптомів, що характеризують Римську класифікацію розладів. Як вважає Drossman (2016), наведене визначення легко зрозуміти і прийняти лікарям, науковцям, представникам регуляторних органів та фармацевтичної промисловості, а також пацієнтам.
Для повноти розуміння необхідно навести визначення ФР ШКТ, узгоджене Римськими критеріями III (Drossman, 2006). Відповідно до цього визначення «функціональні гастроінтестинальні розлади – це різноманітна комбінація гастроінтестинальних симптомів без структурних або біохімічних порушень». При цьому раніше Drossman визначив функціональні гастроінтестинальні розлади «як психологічні порушення або просту відсутність органічних хвороб» (Drossman, 2005). Згідно із цією дефініцією до функціональних захворювань відносять стани, коли не вдається виявити морфологічних, генетичних, метаболічних та інших змін, якими можна було б пояснити наявні клінічні симптоми. Відчуваєте різницю між наведеними визначеннями?
Таким чином, нова система класифікації є важливим компонентом для впорядкування цих розладів, але ефективне управління вимагає біопсихосоціального підходу, що враховує мінливість і складність цієї групи пацієнтів.
Етіологія і патогенез
ФР ШКТ визнані самостійною нозологічною формою і розглядаються як психосоціальні захворювання. Однак це визначення, прийняте Римськими критеріями в 1999 р. і 2006 р., є суперечливим з огляду на високу коморбідність, що має місце не тільки в дорослих, а й у дітей (Печкуров Д. В. і співавт., 2014). Наразі сформована нова біопсихосоціальна модель ФР ШКТ, що включає кілька детермінантів: порушення моторики, вісцеральну гіперчутливість, зміну мукозального імунітету і запального потенціалу. Принципово новим у цій концепції є фактор мукозального гомеостазу, під яким розуміють здатність слизової оболонки забезпечувати свою стабільність (Печкуров Д. В. і співавт., 2014). У зв’язку із цим змінюється визначення ФР ШКТ, підходи до їх діагностики та лікування. Біопсихосоціальна модель розглядає деякі інфекційні та неінфекційні фактори як коморбідні ФР ШКТ, тому важливими компонентами терапії розладів є виявлення й усунення цих чинників (Печкуров Д. В. та співавт., 2014). Не викликає сумнівів поліетіологічность ФР ШКТ у дітей. Основними в їх патогенезі вважаються порушення моторної функції і вісцеральної чутливості, проте до них часто приєднуються зміни секреторної, всмоктувальної функцій, мікрофлори ШКТ і запального потенціалу слизової оболонки.
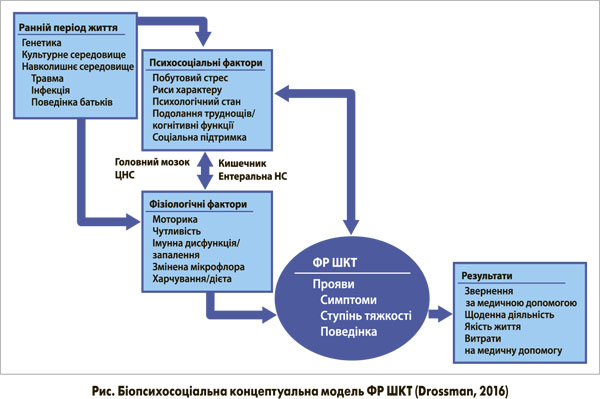
Біопсихосоціальна модель (система) розвитку ФР ШКТ
Що стосується патогенезу ФР ШКТ, то ключова подія, яка об’єднала здоров’я і хворобу в єдине ціле, відбулася 1977 року, коли були опубліковані роботи George Engel (1977). Ці статті вплинули на багатьох дослідників і клініцистів, спрямувавши їхній пошук від конкретних основних біологічних причин до більш інтегрованої біопсихосоціальної моделі розвитку хвороби. G. Engel, терапевт і психоаналітик, запропонував сучасне викладення холістичної теорії (системи), припустивши, що хвороба є результатом біологічних, психологічних і соціальних підсистем, які взаємодіють на різних рівнях; поєднання цих взаємодіючих підсистем визначає хворобу (рис.; Drossman, 2016).
Пізніше, наприкінці 1990-х років, з’явилися новіші клінічні та трансляційні методи, що мали відношення до аферентної сигналізації кишечнику, нервового збудження і реєстрації, оцінки сприйняття болю, зв’язку між нервовими клітинами і функціями імунної системи, а також до візуалізації мозку; покращили наше розуміння про взаємодію головного мозку і кишечнику. Це, свою чергою, привело до виникнення поняття осі «кишечник – головний мозок». Термін «нейрогастроентерологія» на позначення нової галузі досліджень був згаданий у Римських критеріях II в 1999 р. в розділах про фундаментальну науку і фізіологію (Kellow et al., 1999; Wood et al., 1999). По суті, нейрогастроентерологія відображає структурні і фізіологічні компоненти біопсихосоціальної моделі. Використання нейрогастроентерології в проведених дослідженнях забезпечує закономірність вивчення взаємодії кишечнику з головним мозком. За останні два десятиліття цей термін використовувався багатьма науково-дослідними товариствами, а також у спеціалізованих виданнях.
У ранньому віці генетика, соціокультурні чинники і фактори зовнішнього середовища можуть негативно вплинути на психосоціальний розвиток з точки зору особистісних якостей, схильності до життєвих стресів, певного психологічного стану, а також в аспекті пізнання і навичок подолання труднощів. Ці фактори впливають і на сприйнятливість до дисфункції кишечнику (ненормальна моторика або чутливість, змінена імунна дисфункція слизової оболонки або запалення, мікробне середовище, а також вплив їжі і поживних речовин). Крім того, ці змінні зв’язку головного мозку і кишечнику впливають на експресію ЦНС.
Таким чином, вважають, що ФР ШКТ є продуктом взаємодії між психологічними факторами і зміненою кишковою фізіологією через вісь «головний мозок – кишечник» (Mayer et al., 2014). Генетика людини і взаємодії з навколишнім середовищем пізніше впливають на сприйнятливість до захворювань, їх фенотипічну експресію, а також на ставлення і поведінку пацієнта (в тому числі на звернення за медичною допомогою). Дослідження родин і близнюків показали, що генетичний компонент до СПК й інших імовірних ФР ШКТ з декількома поліморфізмами і генами-кандидатами може впливати на фізіологічні функції, включно з моторними функціями, проникністю мембран і вісцеральною чутливістю (Camilleri et al., 2011).
Хоча психосоціальні фактори для діагностики не потрібні, вони впливають на фізіологічне функціонування ШКТ через вісь «головний мозок – кишечник» (моторика, чутливість, бар’єрна функція), є модуляторами болю і симптомів поведінки пацієнта і в кінцевому підсумку впливають на вибір лікування та клінічні результати. При оцінці психосоціальних чинників клініцисти мають розглянути 4 загальні зауваження.
1. Психологічний стрес або емоційна відповідь на стрес підсилює шлунково-кишкові симптоми і може сприяти розвитку ФР ШКТ. Це відбувається в здорових осіб і пацієнтів із структурними діагнозами, що переконливо продемонстровано у хворих з розвитком функціональних шлунково-кишкових розладів, а загальним прикладом є постінфекційний СПК або диспепсія (Collins et al., 2012). Дослідники також бачать високу кореляцію психосоціальних супутніх захворювань, життєвих стресів і зловживань серед пацієнтів з ФР ШКТ, які призводять до гірших результатів.
2. Психосоціальні чинники змінюють перебіг хвороби і поведінку, зокрема звернення за медичною допомогою. Пацієнти з ФР ШКТ показують більш клінічно значимі психологічні розлади. Це пояснюється тим, що психосоціальні травми (наприклад, пережите сексуальне або фізичне насильство) частіше зустрічаються в спеціалізованих медичних центрах, ніж у ланці невідкладної медичної допомоги, що може знизити поріг болю в симптомах, а також асоціюється з гіршими клінічними результатами (Drossman et al., 1996). Зазначені фактори можуть бути ослаблені або пом’якшені адаптивними навичками подолання труднощів і соціальної підтримки. Таким чином, це означає, що психосоціальна реакція сім’ї, суспільства і культури також може мати паліативний ефект на перебіг хвороби.
3. Функціональні шлунково-кишкові розлади можуть мати психосоціальні наслідки. Будь-яке хронічне захворювання має психосоціальні наслідки на самопочуття, щоденний статус функції і відчуття контролю над симптомами, а також наслідки хвороби з точки зору майбутнього функціонування на роботі і вдома. Це зрозуміло з точки зору якості життя, пов’язаного зі здоров’ям.
4. Психосоціальні наслідки хвороби, а саме емоційний стрес і недостатньо адаптовані когнітивні функції, можуть повернутися назад, щоб закріпити і посилити симптоми. У пацієнтів з важкими симптомами можуть розвиватися хворобливий песимізм і безпорадність, а також вибіркова стурбованість і надпильність щодо своїх симптомів, що призводить до вісцеральної тривоги, зниження порогу відчуття і приниження власної гідності. У цих випадках необхідне поведінкове втручання, щоб допомогти відновити психологічний субстрат для покращення стану здоров’я.
Слід також звернути увагу на те, що різноманітні фізіологічні процеси можуть призвести до шлунково-кишкових симптомів, а якщо вони переважатимуть, то й до функціональних шлунково-кишкових розладів.
Патологічна моторика
Порушена шлунково-кишкова моторика може викликати симптоми нудоти, блювання, діареї, гострий абдомінальний біль, нетримання сечі та ін. Крім того, в здорових осіб, тим більше в пацієнтів з ФР ШКТ, сильні емоції або екологічний стрес через вісь «головний мозок – кишечник» можуть призвести до розладу моторики в усьому ШКТ. У пацієнтів з ФР ШКТ в порівнянні зі здоровими людьми реакція моторики на стресові фактори є ще більш вираженою (Camilleri, 2012). Проте ці моторні реакції тільки частково корелюють із симптомами і є недостатніми для того, щоб пояснити скарги на хронічний або рецидивуючий абдомінальний біль.
Вісцеральна гіперчутливість
Слабкий зв’язок болю із шлунково-кишковою моторикою і великою кількістю ФР ШКТ (наприклад, функціональний біль у грудній клітці, функціональна диспепсія – епігастральний больовий синдром, СПК і т. ін.) пояснюється концепцією вісцеральної гіперчутливості (Mayer, Gebhart, 1994). Ці пацієнти мають більш низький поріг больової чутливості через балонне розтягування кишечнику (вісцеральна гіпералгезія) або підвищену чутливість навіть за нормальної функції кишечнику (наприклад, алодинія). Вісцеральна гіперчутливість може бути посилена у пацієнтів з ФР ШКТ: багаторазове повторення балонного здуття в товстій кишці призводить до прогресуючого, хоча й короткочасного підвищення інтенсивності болю в здорових людей і більш тривалого – у хворих з ФР ШКТ. Гіперчутливість і сенсибілізація можуть бути посилені на всіх рівнях осі «головний мозок – кишечник» через фактори, зазначені нижче.
Імунна дерегуляція, запалення і бар’єрна дисфункція. Опрацювання проблематики постінфекційного СПК і диспепсії було пов’язане з підвищеним інтересом до проникності мембрани слизової оболонки через зміни щільних контактів (Piche, 2014), кишкову флору і змінену імунну функцію слизової оболонки. Ці зв’язки розширюють доступ до внутрішньопросвітніх антигенів у підслизовій оболонці, пов’язаних зі слабко вираженою активацією мастоцитів і збільшеним вивільненням запальних цитокінів (Ohman, Simren, 2010). Подібні дії змінють чутливість рецепторів у слизовій оболонці кишечнику та міентеричному сплетінні, забезпечуючи вісцеральну гіперчутливість. Фактори сприяння включають генетику, психологічний стрес через активацію мастоцитів, а також змінену чутливість рецепторів у слизовій оболонці кишечнику та міентеричному сплетінні. Це посилюється за рахунок зміни бактеріального середовища або прямої інфекції.
Мікробіом. Мікробіом – сукупність мікроорганізмів, що утворюється за допомогою таких факторів хазяїна, як генетика і поживні речовини, проте, своєю чергою, може впливати на його здоров’я і хвороби. Мікробіом став одним з основних напрямів досліджень у галузі функціонування кишечнику з ФР ШКТ; крім того, виникає концепція осі «мікробіом – кишечник – головний мозок» (Pigrau et al., 2016). Відмінності серед пацієнтів із СПК у бактеріальній композиції кишечнику (наприклад, збільшення Firmicutes і зменшення Bacteroidetes і Bifidobacter) і в зниженій фекальній мікробній різноманітності в порівнянні з такими в здорових осіб свідчать про причинну роль у виникненні і підтримці СПК. Це підтверджується невеликим ефектом пробіотиків і більш істотною користю періодичного лікування антибіотиками в покращенні симптомів СПК. Проте необхідні подальші дослідження, щоб повністю зрозуміти місце бактеріальної флори в патогенезі ФР ШКТ.
Продукти харчування, раціон і внутрішньопросвітні чинники. Недавнє доповнення щодо розуміння ФР ШКТ стосується продуктів харчування і дієти, а також їх зв’язку з кишковою мікробіотою (Rajilic-Stojanovic et al., 2015). Деякі специфічні зміни в раціоні, такі як оліго-, ди- і моносахариди та поліоли з низьким рівнем ферментації або обмеження клейковини у деяких пацієнтів, можуть принести користь у результаті зниження осмотичних ефектів або змін у слизовій оболонці кишечнику. При цьому жодна дієта не має особливого значення, лікування повинно бути індивідуальним. Крім того, дієта забезпечує субстрати для мікробної ферментації, і, оскільки при СПК склад кишкової мікробіоти змінюється, зв’язок між їжею і раціоном, складом мікробіоти і продуктами ферментації може відігравати важливу роль у патогенезі СПК. Це варте уваги, адже існує невідповідність між думкою пацієнтів і лікарів про вплив їжі на симптоми ФР ШКТ: пацієнти вважають ефект більш актуальним (Halpert et al., 2007).
Вісь «головний мозок – кишечник». Вісь «головний мозок – кишечник» є нервово-анатомічним субстратом, у якому щойно описані психосоціальні чинники впливають на ШКТ і навпаки. Зв’язок між головним мозком і кишечником є складною інтегральною схемою, яка передає інформацію від емоційних і когнітивних центрів (що сприяють думкам, почуттям, спогадам і регуляції болю) головного мозку за допомогою нейромедіаторів (програмне забезпечення) для периферійного функціонування ШКТ і навпаки (Gaman, Kuo, 2008). За структурою існують прямі зв’язки між ЦНС і міентеричним сплетінням та вісцеральними м’язами й іншими структурами кінцевих органів, які впливають на сенсорні, моторні, ендокринні, вегетативні, імунні та запальні функції (Jones et al., 2006). Отже, такі емоції, як страх, гнів, тривога, больові стимули і фізичний стрес, можуть сповільнити спорожнення шлунка і кишковий транзит. Вони також здатні стимулювати ободову моторну функцію через зниження тривалості ободового транзиту, підвищену скоротливу активність, індукцію дефекації і симптоми діареї. Крім того, психологічний стрес може порушити поріг кишкового болю і погіршити секреторні і бар’єрні функції слизової оболонки, що пов’язано з переміщенням продуктів бактеріальних клітин, і тим самим призвести до шлунково-кишкового болю та діареї, як і в разі СПК. З іншого боку, посилена моторика, вісцеральне запалення і ушкодження можуть посилити висхідній вісцеральний шлях і вплинути на ділянки мозку, що зумовлює виникнення більш вираженого болю і зміну психічного функціонування, включно з тривогою і депресією. Власне, взаємовідносини, які називаються віссю «головний мозок – кишечник», є нервово-анатомічним і нейрофізіологічним субстратом для клінічного застосування систем або біопсихосоціальної моделі (Mayer et al., 2015).
Таким чином, у біопсихосоціальній моделі розвитку ФР ШКТ виділяються два тісно взаємодіючі функціональні рівні: ЦНС і психічна сфера, з одного боку, і ШКТ – з іншого, – кожен з яких по-своєму контактує із зовнішнім середовищем (Акопян А.Н. та співавт., 2014). Нервова система через психічну сферу перебуває під впливом соціальних факторів, а ШКТ – аліментарних. На рівні психіки визначається, які саме аліментарні фактори будуть представлені органам травлення, а стан ШКТ формує не тільки характер інформації, що надходить до нервової системи, а й потік нутрієнтів, необхідних для її функціонування, як, утім, і для існування організму в цілому (Акопян А.Н. та співавт., 2014).
Отже, мукозальний гомеостаз є необхідною умовою забезпечення гомеостазу системного, хоча і перебуває під контролем вищих нервових і гуморальних факторів. Водночас порушення регуляторного ланцюжка може призводити до ФР ШКТ, причому ці порушення іноді розвиваються як на центральному, так і на периферичному рівні. Наприклад, їх причиною може бути вісцеральна гіперчутливість, зумовлена дисфункцією кишкової мікробіоти, що призводить до відповідної реакції нервової системи з розвитком гіпермоторики (Акопян А.Н. та співавт., 2014). Можлива також неадекватна реакція нервової системи на інформацію про стан органів травлення, що надходить з периферії, з розвитком такої ж гіпермоторной реакції і неадекватним її відображенням у психоемоційній сфері.
Таким чином, за результатами обговорення біопсихосоціальної моделі з’ясовано, що психосоціальні чинники є сильними факторами, які визначають використання ліків, візити в лікарню, функціональну здатність, втрату робочого часу, а також витрати на медичну допомогу. Усі ці фактори можуть бути розглянуті і потенційно змінені незалежно від діагностичного стану, якщо лікар має ефективні навички спілкування. Представлена модель визначає необхідність комплексного підходу до корекції ФР ШКТ з обов’язковим урахуванням соціальних факторів, характеру харчування, психоемоційної сфери, вегетативного статусу і власне стану органів травлення та порушення мукозального гомеостазу. З даної концепції випливає також очевидність генералізованого характеру патологічного процесу, тобто залучення, хоча і різною мірою, всіх відділів ШКТ.
Класифікація ФР ШКТ та Римські критерії IV
Класифікація ФР ШКТ, розробка якої була ініційована організацією Rome Foundation, ґрунтується головним чином на симптомах, а не на фізіологічних критеріях (Drossman et al., 1990). Цьому сприяла її корисність в медичній допомозі, а обмежені дані про фізіологічні порушення (наприклад, моторики) повною мірою пояснювали симптоми пацієнта; крім того, симптоматика змушувала пацієнтів звертатися за медичною допомогою. Проте фізіологічні критерії, якщо вони підвищують точність діагностики, до сьогодні використовуються, як і у випадку аноректальних розладів. Drossman (2016) вважає, що в майбутньому в критерії будуть включені біомаркери (якщо вони зможуть підвищити прогностичну цінність).
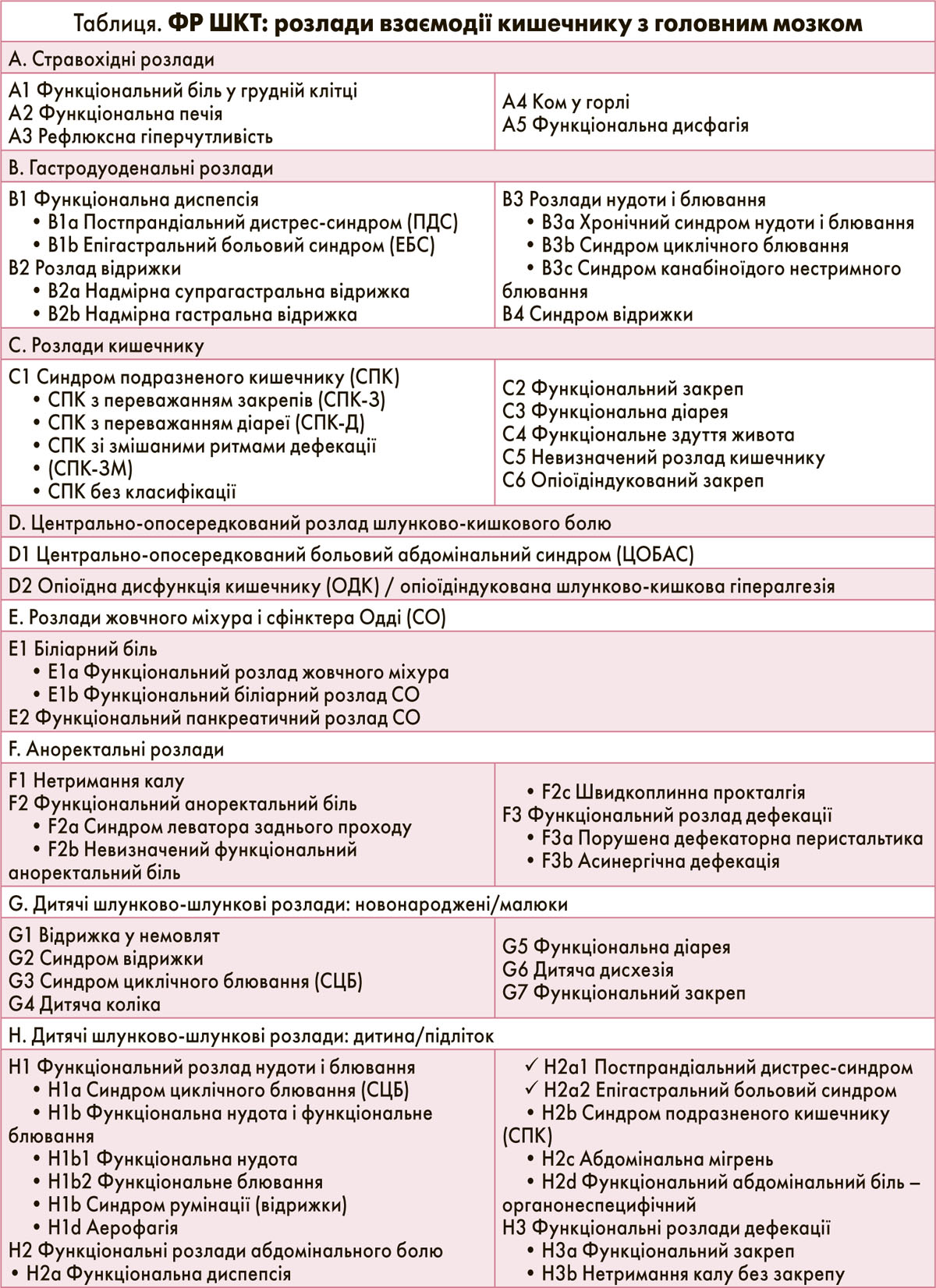
Класифікація розладів за анатомічними областями (стравохідна, гастродуоденальна, кишкова, жовчовивідна й аноректальна) передбачає поєднання функцій, що лежать в основі діагностики і терапії та мають відношення до місцезнаходження цих органів. Таким чином, функціональна печія відноситься до стравоходу, нетримання калу – до аноректальної частини, а розлад сфінктера Одді (РСО) – до біліарної системи. Проте локалізації симптомів недостатньо, особливо нелегко локалізувати ФР ШКТ з болем (наприклад, СПК, функціональну диспепсію і центрально-опосередкований больовий абдомінальний синдром), на які більше впливають загальні ефекти, зумовлені дерегуляцією шляхів контролю ЦНС над симптомами ентеральної нервової системи.
У таблиці зазначені 33 дорослі і 20 дитячих ФР ШКТ для Римських критеріїв IV. У цій статті ми переважно зупинимося на обговоренні діагностичних ознак (включно з Римськими критеріями IV) і деяких аспектів лікування.
Зміни в Римських критеріях IV
Після всебічного обговорення до Римських критеріїв IV було внесено цілу низку доповнень та уточнень.
1. Експерти вважають за необхідне усунення по можливості термінологічного означення «функціональний» у назві патологічних станів (Drossman, 2016). Слід зазначити, що дебати щодо цього питання точилися протягом багатьох десятиліть. Однак це означення настільки вкоренилося в нозології, що його неможливо легко замінити. Проте слово «функціональний» є неспецифічним, тож має обмеження. Таким чином, експерти надали більш точне визначення ФР ШКТ. На їхню думку, надалі коректною буде наступна термінологія: «порушення цереброінтестинальної взаємодії» (disorders of gut-brain interaction), тобто порушення взаємодії кишечнику і головного мозку (Drossman, 2016). І хоча вимовляти це словосполучення складніше, воно більш точно відображає суть патогенезу змін, що виникають в організмі. Крім того, експерти усунули слово «функціональний» із назв порушень (наприклад, «розлади стравоходу», а не «функціональні розлади стравоходу») і з деяких діагнозів (наприклад, «нетримання калу» замість «функціональне нетримання калу»), як це було в Римських критеріях III. Крім того, визначення «функціональний синдром абдомінального болю» було замінено на «центрально-опосередкований синдром абдомінального болю», щоб більш адекватно вирішувати патогенез розладу, мінімізувати таврування терміну «функціональний» і відобразити нову інформацію про взаємодію кишечнику і головного мозку. Разом із тим у назвах деяких клінічних порушень (наприклад, «функціональна діарея», «функціональна печія») термін зберігся, щоб відрізнити їх від порушень, які мають подібні симптоми, але з чіткою структурною етіологією.
2. До класифікації додані нові діагнози з відомою етіологією. Зокрема, було додано опіоїдну дисфункцію кишечнику («опіоїдіндукована шлунково-кишкова гіпералгезія» – opioid-induced gastrointestinal hyperalgesia) до рубрики «Центрально-опосередковані розлади шлунково-кишкового болю», «опіоїдіндукований закреп» був доданий до рубрики «Розлади кишечнику», а «синдром канабіноїдого нестримного блювання» – до рубрики «Гастродуоденальні розлади» (Drossman, 2016). Ці діагнози відрізняються від інших ФР ШКТ наявністю речовин (опіати і канабіноїди), вживання яких сприяє появі симптомів, відповідно, їх уникнення може привести до нормалізації. Оскільки ці діагнози є результатом відомих етіологічних чинників, то вони не є по-справжньому функціональними, проте їх включили в Римські критерії IV, оскільки вони відповідають новому визначенню: розлади взаємодії кишечнику і головного мозку (Drossman, 2016). Ці розлади також характеризуються зміненою функцією ЦНС або ентеральної нервової системи; їх клінічні прояви аналогічні таким ФР ШКТ (Drossman, 2016). Отже, зазначені діагнози слід розрізняти, при цьому вони поки ще не є належним чином охарактеризованими або не досягли рівня розгляду як окремі розлади (такі як непереносимість лактози, мікроскопічний коліт), проте вони також були включені до списку нових термінів, незважаючи на те що функціональність їх походження викликає певні сумніви. З іншого ж боку, новий озвучений підхід «порушення цереброваскулярної взаємодії» набагато ближчий за змістом у випадку застосування наркотичних засобів, ніж «функціональні порушення».
3. Доповнено та внесено поправки до деяких рубрик. Наприклад, нова рубрика «Кишкове мікросередовище і функціональні розлади шлунково-кишкового тракту» (Intestinal Microenvironment and the Functional Gastrointestinal Disorders) об’єднує дані про мікробіом, раціон та способи харчування для покращеного розуміння процесів внутрішньопорожнинного (люмінального) шлунково-кишкового травлення (Drossman, 2016). Стосовно аспектів функціональних шлунково-кишкових розладів з фармакологічних і фармакокінетичних фокус змінено на фармакологічні, фармакокінетичні та фармакогеномні, щоб включити роль генетики в клінічну реакцію на фармацевтичне лікування. Такі чинники з Римських критеріїв III, як стать, вік, соціальне оточення, культура і точка зору пацієнта, були розділені на 2 статті, щоб відобразити швидке зростання обсягу знань у цих областях. Термін «психосоціальні аспекти ФР КШТ» змінено на «біопсихосоціальні аспекти ФР КШТ», щоб відобразити багатозначний характер цих процесів. Назву рубрики «Синдром функціонального абдомінального болю» з Римських критеріїв III у новій редакції змінено на «Центрально-опосередковані розлади шлунково-кишкового болю», щоб відобразити домінуючий внесок ЦНС у розвиток симптомів.
4. Змінено порогові величини для критеріїв діагностики. Через обмежену інформацію про частоту симптомів у здорового кишечнику і недостатні дані літератури щодо частоти шлунково-кишкових симптомів з використанням Римських критеріїв організація дослідила нормативні симптоми, тому комітети з розробки глав змогли включити порогові величини на основі фактичних даних для оцінки симптомів навіть за межами нормального діапазону. Комітет з анкетування організації Rome Foundation провів опитування про фізичні симптоми, включно із симптомами ФР ШКТ, у доклінічній загальнонаціональній вибірці в США. З використанням отриманої в ході опитування інформації було визначено порогові величини частоти для критеріїв діагностики, які відрізнялися від загальних частот вибірки.
5. До класифікації додано новий офіційний діагноз для хворих з порушеннями цереброваскулярної взаємодії – «рефлюксна гіперчутливость», або «гіперчутливий рефлюкс» (Drossman, 2016). У Римських критеріях III функціональна печія визначала симптоми печії за відсутності доказів того, що печія пов’язана з гастроезофагеальною рефлюксною хворобою. Проте у деяких пацієнтів рефлюкс має місце при нормальних рівнях кислоти, але вони чутливі до фізіологічного рефлюксу, і таким чином розвивається печія. У Римських критеріях IV ця ситуація описана в розділі «Рефлюксна гіперчутливість» (A3), її слід відрізняти від функціональної печії (А2). До того ж тепер у медичній практиці можна використовувати такі назви синдромів, як «синдром хронічної нудоти» та «синдром хронічного блювання» (Drossman, 2016).
6. У нових рекомендаціях переглянуто критерії РСО (Drossman, 2016). Дисфункція сфінктера Одді тепер виключає органічну патологію, проте досі враховує вади розвитку та ферментативні порушення як основу патології. Внесено зміни і в терапевтичні підходи. Зокрема, рекомендації щодо проведення біліарної сфінктеротомії на підставі клінічних критеріїв (біліарної дилатації і підвищеної біохімії печінки або підвищених рівнів ферментів підшлункової залози) для передбачуваного болю сфінктера Одді не мали переконливої доказової бази (Geenen et al., 1989). Таким чином, врівноваження переваг полегшення симптомів з потенційними ризиками панкреатиту, кровотечі і перфорації було складним завданням, як належні рекомендації Римські критерії III для цих розладів не були особливо корисні. Тепер на основі доказів, які розвіюють значення сфінктеротомії для РСО III типу (Cotton et al., 2014), комітет з розробки критеріїв розладів жовчного міхура і сфінктера Одді переніс ці порушення в іншу категорію, тим самим забезпечивши більш раціональний алгоритм лікування. Попередня категоризація РСО III типу згідно з Мілуокською класифікацією була видалена, тому пацієнтам без ознак обструкції жовчних проток не слід призначати ендоскопічну ретроградну холангіопанкреатографію з вимірюванням тиску для можливої сфінктеротомії. Замість цього їх потрібно лікувати симптоматично. Крім того, при лікуванні функціонального розладу біліарного сфінктера Одді у пацієнтів тільки з помірними об’єктивними ознаками біліарної обструкції слід розглянути інші варіанти обстеження до прийняття рішення щодо сфінктеротомії (Drossman, 2016).
7. Наразі функціональні розлади кишечнику перебувають в області симптоматичних проявів. Для позначення цих розладів найчастіше використовується діагноз СПК (Irritable bowel syndrome – IBS). Крім того, СПК має підтипи: із переважанням закрепу, діареї, змішаних розладів і без класифікації. В новій класифікації вказані підтипи більше не розглядаються як різні. Тепер вони існують у зв’язку з патофізіологічними функціями, які мінливо проявляються у відмінностях конкретного пацієнта, а саме в кількості, інтенсивності і тяжкості симптомів у клінічному аспекті. Цей перетин клінічних ознак добре спостерігається в разі СПК з переважанням закрепів і хронічних закрепів, при якому категорії можуть перетинатися залежно від ступеня болю і підкласів СПК, пов’язаних зі зміною випорожнень протягом тривалого часу (Drossman et al., 2005; 2008; Wong et al., 2010; Shekhar et al., 2013). Це також може відбуватися при СПК з функціональною диспепсією або функціональними закрепами з диссинергією діафрагми таза. У клінічних випробуваннях специфічні критерії діагностики необхідні для оцінки цільових ефектів препаратів, проте на етапах медичної допомоги пацієнтам можуть змінювати діагноз з одного на інший або на комбінацію діагнозів, за якої необхідне комплексне лікування (наприклад, антидепресанти від болю між декількома діагнозами).
8. Експертним комітетом внесені зміни в ідентифікацію підтипів СПК. Класифікація Римських критеріїв III для підтипів СПК необхідна для того, щоб кількісний показник від загального числа випорожнень з використанням Брістольської шкали форми калу застосовувався для класифікації СПК з переважанням діареї (>25% частий/водянистий, <25% твердий/кусковий), СПК з переважанням закрепів (>25% твердий/кусковий, <25% частий/водянистий), СПК змішаного типу (>25% частий/водянистий, >25% твердий/кусковий) і СПК без класифікації (<25% частий/водянистий, <25% твердий/кусковий). Але в пацієнтів тривалий час може спостерігатися нормальна консистенція випорожнень, тому у великій кількості випадків йдеться про підтип СПК без класифікації по відношенню до інших груп (Dorn et al., 2009; Engsbro et al., 2012). Ґрунтуючись на цьому спостереженні і результатах дослідження з нормативних симптомів, проведеного Rome Foundation, критерії підтипів СПК були змінені і наразі стосуються кількісних показників симптоматичних випорожнень (тобто частий/водянистий і твердий/кусковий), а не всіх випорожнень (в тому числі нормальних). Унаслідок цього група без класифікації помітно зменшилася.
9. Експертна група вилучила термін «дискомфорт» з критеріїв діагнозу СПК. У Римських критеріях III для СПК використовували поняття абдомінального болю або дискомфорту, припускаючи, що ці терміни існують у діапазоні від важкого ступеня (біль) до менш важкого (дискомфорт). Проте більш пізні дані (Spiegel et al., 2010) показали, що пацієнти вважають ці два терміни якісно іншими, і дискомфорт може включати в себе різні симптоми. Крім того, термін «дискомфорт» має різні значення (Shah et al., 2001). Тому, щоб уникнути симптоматичної і культурної гетерогенності, використовується тільки термін «біль» як основний діагностичний критерій для СПК. Таким чином, вилучено поняття дискомфорту, яке, на думку експертів, не має діагностично важливого значення і нерідко дезорієнтує хворих. Тепер дане поняття пояснює конкретно біль у момент дефекації.
10. Експерти також звернули увагу на комбінований розлад нудоти і блювання як новий діагноз B3a у Римських критеріях IV для дорослих. Розділ «Хронічний синдром нудоти і блювання» об’єднує попередні розділи з Римських критеріїв III «Хронічна ідіопатична нудота» і «Функціональне блюванням». Це пояснюється відсутністю доказів розмежування різних діагностичних підходів і лікування нудоти в порівнянні з блюванням. Відповідно з клінічними спостереженнями ці два симптоми зазвичай пов’язані. Хоча експерти визнають, що в пацієнтів може мати місце лише нудота, клінічний підхід до діагностики та лікування залишається таким, як і раніше (Drossman, 2016). У дітей відповідно до класифікації зазначені стани залишилися розмежованими (Hyams et al., 2016).
Що стосується дітей і підлітків, то зміни критеріїв будуть представлені дещо пізніше. Можна лише зазначити, що є дві статті, які охоплюють ФР ШКТ у новонароджених/малюків (Benninga et al., 2016) і дітей/підлітків (Hyams et al., 2016). При цьому Benninga і співавт. (2016) запропонували більше нейробіологічних доказів на підтримку розуміння шлунково-кишкового болю в немовлят і дітей молодшого дошкільного віку та надають систему класифікації для 7 ФР ШКТ. І нарешті, Hyams і співавт. (2016) переглянули чинні діагностичні критерії, які тісніше наближаються до таких для дорослих розладів, включно з підтипами постпрандіального дистрес-синдрому й епігастрального больового синдрому функціональної диспепсії. Автори описали два нових розлади, зокрема функціональну нудоту і функціональне блювання, замінили термін «абдомінальний біль, пов’язаний з функціональними шлунково-кишковими розладами» на «функціональний розлад абдомінального болю» і ввели новий термін «функціональний абдомінальний біль – без додаткових уточнень» для опису розладів у дітей, які не вписуються в рамки конкретного розладу, такого як СПК, функціональна диспепсія або абдомінальний біль. Також незначні зміни були внесені в кілька інших ФР ШКТ.
Зважаючи на масштабність поправок, ми акцентували увагу на найбільш значимих змінах у Римських критеріях IV. Вважаємо, що клінічне використання нових запропонованих критеріїв дозволить суттєво покращити надання медичної допомоги хворим з патологією ШКТ.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України» № 17 (390), вересень 2016 p.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...