Дифференцированное применение ингибиторов протонной помпы при кислотозависимой патологии
Открытие и внедрение в клиническую практику ингибиторов протонной помпы (ИПП) стало одним из наиболее весомых достижений гастроэнтерологии ХХ века,
поскольку их применение совершило революцию в лечении кислотозависимой патологии и прочно вошло в стандартные схемы антихеликобактерной терапии, позволяющие полностью излечивать большинство больных с хроническими гастритами и пептической язвенной болезнью. ИПП начали включать в клиническую практику более 25 лет назад, и на сегодняшний день они являются одними из самых применяемых медикаментов в клинике внутренней медицины. В настоящее время ИПП занимают первое место среди 5 наиболее распространенных препаратов как по количеству потребителей, так и по общей стоимости. Их постоянно или эпизодически принимает приблизительно 5% всего взрослого населения. Ввиду своей высокой доказанной эффективности и безопасности некоторые ИПП уже перешли в разряд безрецептурных препаратов.
Основные показания для назначения ИПП. Классические ИПП отсроченного высвобождения (омепразол, лансопразол, пантопразол, рабепразол и эзомепразол) используют в лечении нарушений, обусловленных действием хлористоводородной кислоты: гастроэзофагеальной рефлюксной болезни (ГЭРБ) и пищевода Барретта, пептической язвенной болезни, функциональной и неисследованной диспепсии, синдрома Золлингера – Эллисона и других более редких кислотозависимых заболеваний. Кроме того, ИПП являются обязательным компонентом эрадикационной терапии инфекции H. pylori и применяются для профилактики и лечения гастропатий, индуцированных приемом нестероидных противовоспалительных препаратов (НПВП), а также для снижения всасывания железа при гемохроматозе и повышения эффективности заместительной ферментной терапии при внешнесекреторной недостаточности поджелудочной железы.
Основные показания к применению ИПП:
- диагностика и лечение ГЭРБ и пищевода Барретта, включая ИПП-тест;
- лечение пептических язв;
- профилактика и лечение НПВП-гастропатий;
- лечение и профилактика язвенных кровотечений, профилактика образования стрессовых язв;
- эрадикация инфекции H. pylori;
- эмпирическое лечение диспепсии;
- синдром Золлингера – Эллисона и другие редкие гиперсекреторные состояния;
- повышение эффективности заместительной ферментной терапии при внешнесекреторной недостаточности поджелудочной железы;
- уменьшение всасывания железа при гемохроматозе.
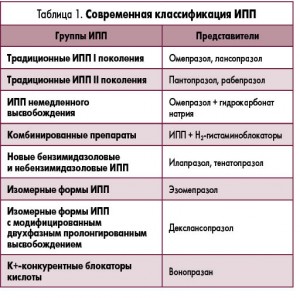
Классификация ИПП. Условно классические ИПП делятся на препараты I и II поколения (табл. 1). К ИПП I поколения относят омепразол и лансопразол, к препаратам II поколения – пантопразол и рабепразол. Кроме того, отдельно выделяют стереоизомеры ИПП – эзомепразол и декслансопразол.
Учитывая такое разнообразие ИПП и то, что в Украине имеются как брендовые препараты, так и множество генериков 6 основных ИПП (омепразола, лансопразола, пантопразола, рабепразола, эзомепразола и декслансопразола), практикующие врачи часто сталкиваются с проблемой их выбора, при этом нередко возникают важные в клиническом отношении вопросы. В частности, какой ИПП является наиболее безопасным? Какой ИПП имеет преимущество в отношении межлекарственных взаимодействий? Какой ИПП обладает наиболее сильным и предсказуемым кислотоснижающим эффектом? Какой ИПП имеет преимущество при проведении эрадикации инфекции H. pylori? Какой ИПП имеет доказанные преимущества при лечении конкретной кислотозависимой патологии (ГЭРБ, язвы желудка, язвы двенадцатиперстной кишки, НПВП-гастропатии и т.д.)?
Преимущества ИПП II поколения. При ответе на первые два вопроса следует вспомнить основные моменты, отличающие ИПП I и II поколения. Хотя по конечному кислотоснижающему эффекту через 4 недели все ИПП примерно одинаковы, относительным недостатком препаратов I поколения является зависимость их эффективности от генетического полиморфизма печеночного изофермента CYP2C19, ответственного за их метаболизм, а также определенный риск нежелательных межлекарственных взаимодействий при одновременном применении с другими лекарственными препаратами, также метаболизирующимися CYP2C19, такими как антиконвульсанты, седативные препараты и миорелаксанты (например, фенитоин, мефенитоин, диазепам, флунитразепам, фенобарбитал, гексобарбитал, мефобарбитал и карисопродол). К еще более важным субстратам CYP2C19 относятся также антидепрессанты (циталопрам, эсциталопрам, флуоксетин, сертралин, венлафаксин, имипрамин, кломипрамин, тримипрамин, амитриптилин, нортриптилин и моклобемид) и некоторые другие часто применяемые лекарства, например пропранолол, варфарин и клопидогрель.
Учитывая перечисленные выше недостатки ИПП I поколения, в середине 1990-х годов в Германии и Бельгии были синтезированы ИПП II поколения (соответственно, пантопразол и рабепразол), которые в меньшей степени зависели от генетического полиморфизма CYP2C19, обладали более выраженным антисекреторным эффектом, оказывали меньшее количество межлекарственных взаимодействий и были более безопасными. Самый изученный в этом отношении ИПП, который к тому же является наиболее рН-селективным и безопасным, – пантопразол (Проксиумтм).
Напомним, что рН-селективность, которая во многом определяет безопасность ИПП, – это значение рН внутри париетальной клетки, при котором ИПП активируется, начинает блокировать протонные помпы и оказывать кислотоснижающий эффект. Чем меньше диапазон и время активации, тем более безопасен ИПП. Установлено, что омепразол и лансопразол активируются в диапазоне 1,0-4,0, а рабепразол быстро активируется в диапазоне рН 1,0-5,0 (наименее рН-селективный) и создает предпосылки для повреждения лизосом иммунных клеток и протонных помп других органов (миокард, почки, костная ткань), тем самым повышая вероятность возникновения нежелательных побочных эффектов. Пантопразол медленно активируется в более узком диапазоне 1,0-3,0, не блокирует протонные помпы в других органах и тканях, является наиболее рН-селективным и поэтому считается самым безопасным ИПП.
В отличие от омепразола, пантопразол не вызывает межлекарственных взаимодействий при одновременном введении с фенитоином, варфарином, диазепамом, R-варфарином, β-блокаторами, теофиллином, диклофенаком, фенацетином, ацетаминофеном, кларитромицином и другими препаратами, метаболизирующимися с участием CYP2C19 и CYP3A4. Поэтому при необходимости длительного сочетанного применения ИПП и этих медикаментов он рассматривается как препарат выбора. Пантопразол также не оказывает клинически значимых перекрестных реакций с НПВП, в первую очередь с диклофенаком, который является одним из наиболее часто применяемых препаратов этой группы. Поэтому при высоком риске возникновения НПВП-гастропатий, когда требуется дополнительное превентивное назначение ИПП или при необходимости продолжения приема диклофенака даже в случае развития НПВП-гастропатии, дополнительным лечебным препаратом выбора также является пантопразол.
В последнее время в центре внимания кардиологов и гастроэнтерологов оказались появившиеся сведения о якобы негативном влиянии некоторых ИПП (в первую очередь омепразола и ланcопразола) на антитромбоцитарное действие клопидогреля, который, как и ИПП, подвергается метаболизму в печени до своей активной формы с участием изофермента CYP2C19 (CYP3A4). Этот феномен, по-видимому, возникает по причине конкуренции между ИПП и клопидогрелем за один и тот же фермент CYP2C19. Как известно, клопидогрель назначается после острого инфаркта миокарда или постановки коронарного стента, при этом очень часто для профилактики гастроинтестинального кровотечения назначаются и ИПП. В нескольких недавних исследованиях сообщалось об ухудшении прогноза среди пациентов, одновременно принимающих клопидогрель и ИПП. Так, в исследовании 8205 ветеранов, госпитализированных по поводу острого коронарного синдрома, смерть вследствие повторной госпитализации была отмечена у 615 (20,8%), получавших клопидогрель без ИПП, и у 1561 (29,8%), получавших клопидогрель в сочетании с ИПП, что повышало риск смерти или повторной госпитализации (добавочный относительный риск – 1,25). Большое ретроспективное исследование стентированных пациентов, в течение 1 года получавших клопидогрель, показало большую частоту развития острого коронарного синдрома у 4521 больного, принимавшего клопидогрель и ИПП, чем у 9862 больных, принимавших клопидогрель как монотерапию (32,5 против 21,2%). В другом ретроспективном исследовании Juurlink и соавт. показали, что среди 13 636 пациентов, которым клопидогрель назначался после выписки из больницы, где они находились по поводу острого инфаркта миокарда, дополнительное назначение ИПП в течение 30 дней ассоциировалось с повторными инфарктами (дополнительный относительный риск – 1,27). Было отмечено также, что назначение только пантопразола, который не ингибирует изофермент CYP2C19, не ассоциировалось с реинфарктами.
Кроме того, пантопразол (Проксиумтм) также является наилучшим ИПП по переносимости. При его приеме незначительные побочные эффекты фиксируются всего у 1,1% больных. Программы контроля за результатами клинического применения показали, что среди 100 000 пациентов с кислотозависимыми расстройствами, получавших пантопразол, какие-либо неблагоприятные эффекты наблюдались только у 0,77%. Очень важно и то, что фармакокинетика пантопразола существенно не отличается у молодых и пожилых людей – основного контингента пациентов, которым назначаются многочисленные препараты по поводу сопутствующей патологии. Кроме того, даже легкая и среднетяжелая дисфункция печени не влияет на фармакокинетику пантопразола, что обеспечивает стабильность его фармакологического эффекта.
Генетические полиморфизмы изофермента CYP2C19 и преимущества стереоизомеров ИПП. Существует такое понятие, как полиморфизм изоферментов CYP450. Его смысл заключается в различном генетическом контроле активности некоторых ферментов цитохрома Р450 в разных популяциях. Этот феномен обусловливает различную ферментативную активность этой системы у разных людей. К полиморфным энзимам относят CYP2C19, 2D6 и 1A2. Феномен полиморфизма указанных изоферментов имеет по крайней мере 2 клинически значимых последствия. Во-первых, он может предопределять генетически обусловленную индивидуальную вариабельность фармакологического эффекта некоторых препаратов, взаимодействующих с указанными энзимами, включая ИПП. Во-вторых, если два препарата или более метаболизируются одним из этих ферментов, то это неизбежно приведет к их взаимодействию и, возможно, к взаимному антагонизму, что может вызвать повышение концентрации препарата в сыворотке крови, увеличить период его полураспада и в худшем случае – привести к побочным действиям.
В настоящее время наиболее изученный пример этого феномена – полиморфизм фермента CYP2C19, определяющий выраженные индивидуальные и межэтнические колебания в фармакокинетических показателях ИПП. Исходя из скорости метаболизма субстратов CYP2C19, выделяют три группы пациентов в зависимости от их генотипа. В целом быстрым метаболизатором (с повышенной ферментативной активностью) называют пациента с комбинацией *1/*1, промежуточным метаболизатором (с умеренной ферментативной активностью) – с *1/*2 и *1/*3 и медленным метаболизатором (со сниженной ферментативной активностью) – с *2/*2, *2/*3 и *3/*3. Кроме того, известен вариантный аллель (аллель CYP2C19*17, –806C>T и –3402C>T), ответственный за ультрабыстрый метаболизм CYP2C19.
По данным исследований, проведенных еще в конце 1990-х годов, во всех изученных популяциях большинство пациентов относилось к группе быстрых метаболизаторов, и только меньшинство принадлежало к медленным. Так, считается, что в европеоидной популяции частота индивидуумов с медленным метаболизмом CYP2C19 находится в пределах 2,5-8,5%, тогда как распространенность медленных метаболизаторов среди китайцев и японцев оценивается на уровне 8-23%. У пациентов, которых принято считать медленными и промежуточными метаболизаторами (характеризуются сниженной активностью гидроксилазы CYP2C19), обычно выявляются повышенные концентрации ИПП в плазме крови и их клиническая эффективность выше, тогда как у ультрабыстрых и быстрых метаболизаторов плазменные концентрации препаратов могут отмечаться на уровне ниже оптимальных, и, соответственно, их антисекреторный эффект и клиническая эффективность как при лечении кислотозависимой патологии, так и при проведении антихеликобактерной терапии существенно ниже. Например, средние показатели рН желудочного содержимого после приема однократной дозы 20 мг омепразола у медленных метаболизаторов (4,1-4,47) выше по сравнению с промежуточными (3,3) и быстрыми метаболизаторами (2,1-2,3). После 8-дневного лечения средние показатели рН желудочного содержимого составляли соответственно 5,9, 4,7 и 4,1. Доля времени с рН>4 у медленных метаболизаторов (92%) была существенно выше по сравнению с промежуточными (72%) или быстрыми метаболизаторами (37%).
К сожалению, ИПП I поколения (омепразол и лансопразол), большей частью метаболизирующиеся при участии CYP2C19, в стандартных рекомендованных дозах не могут обеспечивать необходимый уровень подавления секреции кислоты у быстрых метаболизаторов, составляющих большинство популяции. Поэтому данной группе пациентов при лечении серьезной кислотозависимой патологии, например тяжелых эзофагитов, необходимо по меньшей мере вдвое повышать дозы препаратов либо применять ИПП с другим типом метаболизма, менее зависящим от генетического полиморфизма CYP2C19. Именно с этой целью были синтезированы стереоизомеры ИПП. Синтез, изучение особенностей метаболизма, клинической эффективности и безопасности эзомепразола – первого оптического стереоизомера среди ИПП, а также его последующий выход на фармацевтический рынок ознаменовали новый этап в лечении кислотозависимой патологии. За технологию создания эзомепразола (препарата Нексиум) в 2000 году была присуждена Нобелевская премия по химии.
Установлено, что эзомепразол, являющийся левовращающим стереоизомером омепразола, демонстрирует более высокую метаболическую устойчивость с более высокой биодоступностью по причине самостоятельного ингибирующего действия на CYP2C19. Поскольку меньшее количество S-изомера подвергается клиренсу после воздействия изофермента CYP2C19, возникающий в результате этого рост показателя плазменной концентрации для эзомепразола обеспечивает более эффективный контроль секреции желудочного сока, чем при приеме всех прочих ИПП в стандартных дозах, независимо от генотипа CYP2C19. Предполагается, что эзомепразол преобразует фенотип быстрого метаболизатора в фенотип медленного, в связи с чем контроль кислотности желудка при приеме эзомепразола более предсказуемый, выраженный и стабильный.
Клинические преимущества эзомепразола. По сравнению со своими предшественниками, эзомепразол характеризуется улучшенными свойствами: после приема внутрь он быстрее и лучше усваивается, выделяет большее количество активного вещества, блокирующего выработку кислоты, действует более длительно, при краткосрочном применении практически не вызывает каких-либо существенных побочных эффектов. В отличие от других подобных препаратов этого класса, при использовании эзомепразола кислотоснижающий эффект более предсказуемый и более продолжительный. В связи с этим в настоящее время большинство гастроэнтерологов мира рассматривают эзомепразол как самый эффективный кислотоснижающий препарат. Этот факт подтверждает и то, что оригинальный эзомепразол (Нексиум) является третьим по продажам среди всех применяемых в мире медикаментов.
Эзомепразол в дозе 40 мг в сутки более эффективен в поддержании внутрижелудочного рН на уровне 4 или выше (уровень, необходимый для контроля симптомов ГЭРБ и заживления эзофагитов) по сравнению с другими ИПП, назначаемыми в стандартных дозах. В 4-х слепых рандомизированных перекрестных исследованиях пациентов с ГЭРБ однократный прием эзомепразола в дозе 40 мг сравнивался с приемом других ИПП в стандартных дозах один раз в сутки в отношении их воздействия на интрагастральный рН. Средний процент общего времени с интрагастральным рН>4 в первый день при приеме эзомепразола оказался достоверно выше по сравнению с лансопразолом 30 мг (соответственно, 9,7 и 8 час; р=0,0182), пантопразолом 40 мг (12,1 и 7 час; р<0,001) и рабепразолом 20 мг (9,8 и 7,1 час; р=0,002). Так же и на 5-й день приема эзомепразол сопровождался достоверно более высоким процентом времени интрагастрального рН>4 по сравнению с лансопразолом 30 мг (13,8 и 10,7 час; р<0,001), омепразолом 20 мг (16,8 и 10,5 час; р<0,001), пантопразолом (16,1 и 10,8 час; р<0,001) и рабепразолом 20 мг (14,3 и 10,7 час; р<0,001).
В нескольких клинических испытаниях проводилось сравнение эзомепразола с другими ИПП для заживления ГЭРБ. Всего в эти исследования были включены 13 797 пациентов с эрозивной ГЭРБ, контрольные эндоскопические исследования проводились на 4-й и 8-й неделе лечения. В 5 из 8 исследований было показано, что однократный прием 40 мг эзомепразола приводил к более высокой частоте заживления эрозивного эзофагита после 4-й и 8-й недель терапии по сравнению с однократным приемом 20 мг омепразола, 30 мг лансопразола, 40 мг пантопразола. В одном из исследований было установлено, что уровни заживления у пациентов с исходным умеренным или тяжелым эрозивным эзофагитом (степень С или D по Лос-Анджелесской классификации) при использовании эзомепразола были значительно выше, чем для омепразола на 4-й (60,8 против 47,9%, р=0,02) и 8-й неделях (88,4 против 77,5%, р=0,007), но статистически значимая разница отсутствовала у пациентов с легким (степень А или В по Лос-Анджелесской классификации) эрозивным эзофагитом.
Имеется пять метаанализов по эффективности различных ИПП, три из которых фокусировались на эффектах различных ИПП (включая эзомепразол) на заживление эрозивного эзофагита. В последний метаанализ, сравнивающий эффективность ИПП при кратковременном использовании, были включены два исследования, оценивающие степень заживления рефлюкс-эзофагитов при использовании 40 мг эзомепразола по сравнению с 20 мг омепразола один раз в сутки. Авторы пришли к заключению, что эзомепразол превосходил по эффективности омепразол. Другой метаанализ (S. Edwards et al., 2004) по сравнению эффективности ИПП в лечении ГЭРБ и пептических язв включал три исследования, сравнивающих эзомепразол в дозе 40 мг один раз в сутки с омепразолом в дозе 20 мг один раз в сутки или лансопразолом в дозе 30 мг один раз в сутки. Авторы пришли к заключению, что эзомепразол превосходил по эффективности в заживлении эрозивного эзофагита и скорости исчезновения симптомов оба ИПП, с которыми проводилось сравнение. Еще один метаанализ тех же исследователей, сравнивающий эзомепразол с другими ИПП в заживлении эрозивного эзофагита, включал все рандомизированные исследования, проведенные к 2006 г. (S. Edwards et al., 2009). Авторы пришли к заключению, что применение эзомепразола было связано с более высокой степенью заживления по сравнению со стандартными дозами всех других ИПП на 4-й неделе (относительный риск 0,92; 95% ДИ 0,90-0,94; р<0,00001) и на 8-й неделе (относительный риск 0,95; 95% ДИ 0,94-0,97; р<0,00001).
Кроме того, эзомепразол и другие ИПП обладают самостоятельной антихеликобактерной активностью и всегда входят во все схемы эрадикационного лечения инфекции H. pylori. Совместное применение эзомепразола и основного антихеликобактерного антибиотика кларитромицина повышает концентрацию эзомепразола в плазме крови и продлевает его действие, что в конечном итоге приводит к усилению кислотоснижающего эффекта, более выраженному и продолжительному подъему интрагастрального рН, что, в свою очередь, усиливает антихеликобактерную эффективность кларитромицина. Метаанализ 35 исследований (A.G. McNicholl et al., 2012) показал, что использование схем эрадикационной терапии с эзомепразолом дает более высокий процент эрадикации, чем схемы с ИПП I поколения (эзомепразол в составе эрадикационной терапии был эффективнее эзомепразола в 1,8 раза).
Заключение: преимущественные показания для назначения разных ИПП. Таким образом, ИПП являются основными препаратами для лечения кислотозависимой патологии и инфекции H. pylori. До настоящего времени в качестве золотого стандарта лечения любой кислотозависимой патологии рассматривается омепразол. По своему конечному клиническому эффекту при кислотоснижающей патологии через 4-8 недель применения каких-либо различий между омепразолом и другими ИПП нет, поскольку механизм действия всех этих препаратов одинаков: блокада протонной помпы париетальных клеток и глубокое угнетение желудочной секреции. Тем не менее в определенных клинических ситуациях некоторые ИПП имеют существенные преимущества и должны применяться в первую очередь. Поэтому назначение ИПП следует проводить дифференцированно в зависимости от силы их кислотоснижающего эффекта, особенностей метаболизма, преимущественных показаний и безопасности. Несмотря на то что ИПП в целом являются безопасными препаратами, в определенных случаях (НПВП-гастропатия, риск межлекарственных взаимодействий при лечении коморбидной патологии, прием клопидогреля, пожилые пациенты) предпочтение следует отдавать наиболее безопасному из них – пантопразолу (препарату Проксиумтм). В тех случаях, когда у быстрых метаболизаторов, составляющих не менее 90% всей европеоидной популяции, необходимо предсказуемо достичь быстрого и сильного кислотоснижающего эффекта (при ГЭРБ, пептическиих язвах, эрадикации инфекции H. pylori), предпочтение следует отдавать наиболее сильному ИПП – эзомепразолу (препарату Нексиум).
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...