Антиаритмическая терапия амиодароном: роль и место в современной клинической практике
Амиодарон применяется в кардиологии почти 50 лет и остается одним из самых назначаемых антиаритмических препаратов (ААП) с широким спектром показаний, как в качестве длительной поддерживающей терапии, так и при неотложных вмешательствах у пациентов с жизнеугрожающими нарушениями ритма. Несмотря на то что амиодарон хорошо изучен во множестве контролируемых клинических исследований, возникает необходимость обновления информации о возможностях его применения в связи с публикацией новых рекомендаций международных экспертных ассоциаций. Практические аспекты применения амиодарона в свете последних консенсусных документов по ведению больных с фибрилляцией предсердий (ФП), желудочковыми аритмиями, а также профилактике внезапной кардиальной смерти комментирует сопредседатель Ассоциации аритмологов Украины, модератор рабочей группы по нарушениям ритма и проводимости сердца, руководитель отдела нарушений ритма сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Олег Сергеевич Сычев.
Напомните, какие свойства амиодарона обусловливают столь широкий спектр показаний и практически универсальность этого ААП при различных нарушениях ритма сердца?
Амиодарон относится к ААП III класса. Основной механизм его действия обеспечивается блокадой ионных калиевых каналов клеточных мембран кардиомиоцитов. Но амиодарон также обладает электрофизиологическими свойствами всех четырех основных классов ААП: инактивирует быстрые натриевые и медленные кальциевые каналы; кроме того, подавляет активность α- и β-адренорецепторов, не будучи их блокатором, что предотвращает избыточную симпатическую активацию. Амиодарон влияет на все проводящие структуры сердца: уменьшает автоматизм синоатриального узла, повышает рефрактерность миокарда желудочков, предсердий, атриовентрикулярного узла, в системе Гиса-Пуркинье, а также замедляет проведение импульса по дополнительным путям (пучкам Кента, волокнам Махейма и др.), которые играют важную роль при синдромах преждевременного возбуждения желудочков. Очень важно, что в отличие от других ААП, снижая частоту сердечних сокращений (ЧСС) и увеличивая интервал PQ и ширину комплекса QRS, амиодарон не оказывает отрицательного инотропного действия на миокард. Это позволяет использовать его даже у пациентов с сердечной недостаточностью (СН).
Уникальное сочетание свойств амиодарона делает его препаратом выбора при большинстве форм суправентрикулярных и желудочковых тахиаритмий. Противопоказания включают только выраженные нарушения атриовентрикулярной проводимости, синусовую брадикардию и синдромы с пролонгацией интервала QT.
Каковы позиции амиодарона в последних европейских рекомендациях по ведению больных с желудочковыми аритмиями?
Спектр желудочковых аритмий варьирует от доброкачественных и асимптомных до жизнеугрожающих и связанных с высоким риском внезапной кардиальной смерти. Соответственно роль и способы применения антиаритмической терапии, включая амиодарон, различны.
Тактику лечения пациентов с желудочковыми аритмиями определяют не только характер и прогностическое значение нарушения ритма, но и состояние сердечно-сосудистой системы в целом. Это в полной мере относится и к выбору ААП. В Консенсусе экспертов Европейской ассоциации ритма сердца, Общества ритма сердца и Азиатско-Тихоокеанского общества ритма сердца (EHRA/HRS/APHRS) по желудочковым аритмиям (2014) указано, что по сравнению с другими ААП амиодарон характеризуется наименьшим аритмогенным потенциалом, что делает его предпочтительным у большинства больных со структурными изменениями сердца и СН. При наличии структурных изменений в сердце основными препаратами для лечения пациентов с желудочковыми тахикардиями – ЖТ (помимо базисной терапии ишемической болезни сердца – ИБС, СН и артериальной гипертензии – АГ) по-прежнему являются бета-блокаторы и амиодарон. Применение других ААП в таких ситуациях очень ограничено или не рекомендуется.
Внутривенные инфузии амиодарона показаны для купирования гемодинамически стабильной или нестабильной ЖТ, кратковременной профилактики рецидивов ЖТ и фибрилляции желудочков; амиодарон включен также в алгоритмы реанимации при внезапной смерти. В разделе, посвященном купированию фибрилляции желудочков, приводятся данные о более высокой частоте успешной реанимации у больных, которым после неудачных попыток электрической дефибрилляции внутривенно вводили амиодарон, по сравнению с пациентами, у которых для восстановления ритма использовали лидокаин (P. Dorian et al., 2002).
Пероральная терапия амиодароном рекомендована у больных с симптомными нестойкими желудочковыми аритмиями, если бета-блокаторы или недигидропиридиновые антагонисты кальция не обеспечивают достаточного контроля симптомов.
Пациенты со стойкой мономорфной желудочковой тахикардией (СМЖТ) без структурной патологии сердца (идиопатическая ЖТ), как правило, имеют хороший прогноз. Однако у большинства больных СМЖТ связана с выраженным ремоделированием миокарда (наиболее частая причина – ИБС), и в указанном случае ассоциируется с повышенным риском смерти. Лечение основного заболевания является недостаточным для профилактики рецидивов мономорфной ЖТ. Самый высокий класс рекомендаций и уровень доказательств у пациентов со структурной патологией сердца и СМЖТ имеет имплантация кардиовертера-дефибриллятора (I, A). Специфическая терапия желудочковой аритмии амиодароном, мекселитином или соталолом или выполнение катетерной абляции рекомендуются в дополнение к имплантируемому устройству.
В 2015 г. опубликованы обновленные рекомендации Европейского общества кардиологов (ESC) по ведению больных с желудочковыми аритмиями и профилактике внезапной кардиальной смерти. Какое место занимает в них амиодарон?
В данном руководстве амиодарон также сохраняет позиции оптимального ААП при симптомных желудочковых аритмиях у пациентов с ИБС и структурной патологией сердца, включая СН и кардиомиопатии.
Амиодарон перорально в дозах 200-400 мг/сут одобрен для лечения больных с ЖТ и фибрилляцией желудочков. У пациентов с показаниями к имплантации постоянного кардиовертера-дефибриллятора терапия амиодароном может быть использована как альтернативная стратегия c целью предотвращения внезапной кардиальной смерти, если аппаратный метод контроля ритма недоступен (в основном по причине его высокой стоимости) или больной отказывается от госпитализации.
Отдельный раздел рекомендаций ESC посвящен ведению пациентов с желудочковыми аритмиями, которые вызваны электрической нестабильностью миокарда при остром коронарном синдроме (ОКС) или реперфузионной терапией. Электрическая кардиоверсия или дефибрилляция рекомендуются как метод выбора для прерывания эпизода желудочковой аритмии у больных с ОКС. Антиаритмическая терапия бета-блокаторами или амиодароном может применяться, если эпизоды ЖТ или фибрилляции частые и больше не могут контролироваться электрической кардиоверсией или дефибрилляцией. При этом следует помнить, что применение ААП с целью профилактики желудочковых аритмий у пациентов с ОКС не рекомендуется.
Повторные эпизоды стойкой ЖТ, особенно полиморфной, или рецидивы фибрилляции желудочков могут служить признаками неполной реперфузии миокарда или повторной острой ишемии. Амиодарон в дозе 150-300 мг внутривенно болюсно следует ввести для подавления повторных гемодинамически значимых желудочковых аритмий. Применение других ААП (например, прокаинамида, пропафенона, флекаинида) у больных с ОКС не рекомендуется.
При симптомных, но не жизнеугрожающих аритмиях (синдром предвозбуждения желудочков, нестойкая ЖТ) у пациентов, перенесших инфаркт миокарда с сохраненной функцией левого желудочка (ЛЖ), амиодарон является препаратом выбора, поскольку он способен купировать аритмию без ухудшения прогноза.
Больным, у которых после перенесенного инфаркта миокарда развивается дисфункция ЛЖ, вызывающая синдром предвозбуждения желудочков, также может быть назначена антиаритмическая терапия амиодароном. Синдром предвозбуждения желудочков и эпизоды нестойкой ЖТ могут быть как причиной, так и следствием дисфункции ЛЖ. У пациентов со структурными изменениями сердца указанные формы аритмий повышают риск смерти. Если частые предвозбуждения желудочков и эпизоды нестойкой ЖТ послужили причиной снижения фракции выброса ЛЖ (кардиомиопатия, индуцированная тахикардией), следует назначить амиодарон или рассмотреть возможность выполнения катетерной абляции.
У больных с аритмогенной кардиомиопатией правого желудочка терапия амиодароном показана для контроля симптомов при частых предвозбуждениях желудочков или эпизодах нестойкой ЖТ, если бета-блокаторы противопоказаны или плохо переносятся.
Получен ли в исследованиях последних лет ответ на главный вопрос – о возможности влияния антиаритмической терапии на долгосрочную выживаемость пациентов?
В некоторых исследованиях были получены положительные результаты улучшения выживаемости больных с желудочковыми аритмиями на фоне поддерживающей терапии амиодароном после перенесенного инфаркта миокарда и при наличии СН (метаанализ данных рандомизированного клинического исследования – РКИ с участием 6500 пациентов, Amiodarone Trials Meta Analysis Investigators, 1997).
Еще один метаанализ, в который включили данные 8522 больных с систолической СН или перенесших инфаркт миокарда, показал, что назначение амиодарона у каждой тысячи пациентов предотвращало 5 смертей от всех причин, 24 кардиоваскулярные смерти и 26 внезапных смертей, хотя абсолютное снижение риска общей смертности на 1,5% не достигло уровня статистической достоверности (J.P. Piccini et al., 2009). Это объясняется тем, что риск смерти зависит не только от наличия аритмии и ее формы, но и от многих других причин, на которые антиаритмическая терапия не влияет. Тем не менее результаты этих исследований указывают на то, что амиодарон является единственным представителем ААП, который может улучшать выживаемость больных с кардиальной патологией или, по крайней мере, позволяет безопасно контролировать аритмии без повышения смертности у пациентов с СН.
Какова роль терапии амиодароном при ФП?
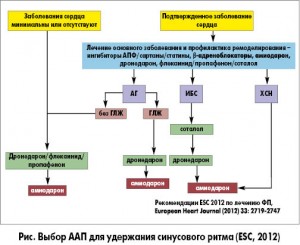
Фибрилляция предсердий – самая распространенная наджелудочковая аритмия, которая ассоциируется с 3-5-кратным повышением риска тромбоэмболических событий, двукратным повышением риска кардиальной смерти, приводит к развитию СН, снижает качество жизни пациентов. Рекомендации по выбору антиаритмической терапии у больных с ФП, так же, как и при желудочковых аритмиях, базируются на оценке состояния сердечно-сосудистой системы. В последних рекомендациях ESC по ведению пациентов с ФП (2012) амиодарон занимает позиции резервного ААП у больных без органической патологии сердца, с ИБС, АГ, а также препарата первого выбора при наличии СН (рис.). Из всех ААП только амиодарон является достаточно безопасным для применения у пациентов с ФП и СН, поскольку он не оказывает отрицательного инотропного эффекта на миокард.
Особым показанием для назначения амиодарона (при невозможности проведения радиочастотной абляции или перед ее проведением) является ФП на фоне синдрома Вольфа-Паркинсона-Уайта, при котором нельзя назначать ни бета-блокаторы, ни сердечные гликозиды, ни антагонисты кальция, поскольку указанные препараты могут усиливать антеградную проводимость по дополнительным путям за счет удлинения рефрактерного периода атриовентрикулярного узла.
На каких этапах ведения пациентов с ФП может применяться амиодарон?
Амиодарон можно назначать как для восстановления, так и для удержания синусового ритма после проведения медикаментозной или электрической кардиоверсии у пациентов с ФП.
Вопрос о том, в каких конкретно случаях целесообразно добиваться восстановления ритма, сегодня до конца не решен. В рекомендациях ESC отсутствуют четкие критерии для выбора стратегии восстановления или удержания ритма у больных с ФП. Выбор остается за врачом и осуществляется в основном на основании доступности методов восстановления ритма, анамнеза и результативности предыдущей терапии. Длительность ФП не является определяющим фактором, хотя особенно эффективным медикаментозное восстановление ритма может быть у пациентов с недавно развившимся пароксизмом. Амиодарон остается наиболее доступным средством для купирования пароксизма ФП у больных с выраженной структурной патологией сердца. С этой целью он вводится внутривенно капельно в дозе 300-450 мг, возможны повторные введения в течение 1-2 суток. Если пациент уже находится на терапии амиодароном, ритм может быть восстановлен путем повышения дозы препарата. Если пароксизм ФП привел к гемодинамической нестабильности, рекомендуется проведение электрической кардиоверсии. У больных с персистирующей ФП предварительная терапия амиодароном может быть полезной для усиления эффекта плановой электрической кардиоверсии: за 2-3 нед до процедуры проводится насыщение амиодароном. В любом случае после восстановления синусового ритма необходимо продолжить прием амиодарона перорально в поддерживающей дозе для профилактики рецидивов.
Известно, что при кардиоверсии возрастает риск тромбоэмболий. Как проводится профилактика данных осложнений?
Пациенты, у которых планируется проведение кардиоверсии, должны получать антикоагулянтную терапию с целью профилактики тромбоэмболий. У больных с ФП длительностью ≥48 ч, или если ее длительность неизвестна, при плановой кардиоверсии рекомендуется проведение антикоагулянтной терапии варфарином с целевыми значениями МНО 2,0-3,0 (или новыми пероральными антикоагулянтами, при приеме которых контроль МНО не требуется) в течение минимум 3 нед перед кардиоверсией и в течение 4 нед после нее, независимо от метода, используемого для восстановления синусового ритма. Не следует забывать о возможностях, связанных с проведением чреспищеводной эхокардиографии, которая в сомнительных случаях, например, при плохой приверженности пациента к лечению, позволяет осуществить дополнительную оценку риска развития тромбоэмболических осложнений перед кардиоверсией: выявить тромб в ушке левого предсердия или другие признаки тромбообразования (наличие феномена спонтанного контрастирования, снижение средней скорости изгнания из ушка левого предсердия).
Больным с ФП длительностью ≥48 ч, которым необходимо немедленное проведение кардиоверсии в связи с нестабильной гемодинамикой, следует ввести внутривенно болюсно гепарин (предпочтительно низкомолекулярный) до увеличения активированного частичного тромбопластинового времени в 1,5-2,0 раза по сравнению с контрольным значением. После этого необходимо проводить терапию пероральными антикоагулянтами (МНО 2,0-3,0) в течение минимум 4 нед, так же, как и при плановой кардиоверсии.
В нашем отделении накоплен положительный опыт применения перед кардиоверсией подкожного введения низкомолекулярного гепарина – эноксапарина.
Какова эффективность противорецидивной поддерживающей терапии амиодароном после восстановления синусового ритма?
Из всех классов ААП амиодарон – наиболее эффективный препарат для предотвращения рецидивов ФП. В ряде зарубежных многоцентровых исследований (CTAF, SAFE-T) продемонстрирована высокая частота удержания синусового ритма на поддерживающей терапии амиодароном (преимущественно в дозе 200 мг/сут) в течение года и более. При этом частота рецидивов ФП была почти в 2 раза ниже, чем при приеме соталола и/или пропафенона.
Возможности терапии ФП амиодароном также хорошо изучены в украинской популяции. При участии специалистов ННЦ «Институт кардиологии им. Н.Д. Стражеско» с 2001 по 2006 г. проводилось многоцентровое исследование, в котором оценивали эффекты оригинального амиодарона (Кордарон, «Sanofi-Aventis», Франция) у пациентов с персистирующей ФП и СН при его назначении для восстановления и последующего сохранения синусового ритма. Амбулаторная фаза исследования продемонстрировала, как и с какими результатами продолжается терапия больных после выписки из стационара в условиях реальной практики. Ретроспективный анализ данных наблюдений в течение последующих 2 лет позволил установить, что прием Кордарона продолжили только 44% пациентов, у остальных врачи либо отменяли антиаритмическую терапию, либо необоснованно заменяли Кордарон на другие ААП. У больных, продолживших терапию Кордароном, не было зафиксировано ни одного случая срыва ритма за первый год, а в течение 2 лет эпизоды тахиаритмии возникали всего у 18% пациентов. Ни в одном случае на фоне приема Кордарона не развилась постоянная форма ФП. Для сравнения – в когорте больных, которым назначали другие ААП, срывы ритма и переход из персистирующей формы ФП в постоянную отмечены у 68% пациентов.
Не стоит забывать, что длительное поддержание синусового ритма обеспечивает регресс симптомов СН и улучшение качества жизни больных, что также было показано в данном исследовании.
Сегодня в клиническую практику все шире внедряются электрофизиологические и инвазивные методы лечения ФП. Какова роль антиаритмической терапии у пациентов с ФП, которым выполняется катетерная абляция?
Несмотря на успехи электрофизиологических методов и малоинвазивной хирургии, полная изоляция эктопических очагов возбуждения миокарда достигается не всегда, и вероятность рецидивирования аритмии остается высокой, особенно у больных с увеличенным левым предсердием и длительно персистирующей ФП. Результаты двойного слепого рандомизированного плацебо-контролируемого исследования AMIO-CAT, опубликованные в 2014 г., демонстрируют, что терапия амиодароном после выполнения катетерной абляции может предотвращать рецидивы ФП и связанные с ними повторные госпитализации (S. Darkner et al., 2014). В исследовании приняли участие 212 пациентов (средний возраст – 61 год) с пароксизмальной ФП или персистирующей ФП, 29% больных – с попытками интервенционного лечения в анамнезе. После выполнения абляции пациенты принимали амиодарон или плацебо в течение 8 нед, а общий период наблюдения составлял 6 мес. У больных, которые получали амиодарон, после 3 мес наблюдения отмечена достоверно боле низкая частота госпитализаций, связанных с повторными эпизодами ФП (снижение риска на 57%) и выполнения кардиоверсии (снижение риска на 64%). Интерпретация результатов данного исследования затрудняется гетерогенностью популяции и методологическими различиями электрофизиологических процедур, которые выполнялись в двух клинических центрах Дании. По мнению некоторых экспертов (K.H. Kuck, E. Wissner, 2014), наибольшую пользу от применения амиодарона могут получить пациенты с персистирующей ФП и более выраженными структурными изменениями левого предсердия.
С какими антиаритмическими препаратами и в каком случае можно комбинировать амиодарон?
В большинстве клинических ситуаций, описанных в международных рекомендациях по ведению пациентов с ФП и желудочковыми аритмиями, амиодарон позиционируется как альтернатива другим ААП, а не как препарат для комбинированной терапии. Следует стремиться к эффективной монотерапии, поскольку взаимодействия даже двух ААП трудно спрогнозировать.
При ЖТ синергичный эффект урежения ЧСС и профилактики фибрилляции желудочков может обеспечивать комбинация амиодарона с бета-блокаторами. Также эта комбинация может применяться для урежения ритма у пациентов с постоянной формой ФП в сочетании с ЖТ или экстрасистолией. Назначение амиодарона в сочетании с ААП IА, IB и IС классов допускается при нарушениях ритма, резистентных к монотерапии, однако при этом повышается риск развития нарушений проводимости. Так, комбинация с хинидином опасна из-за значительного удлинения интервала QT.
Что является критерием эффективности амиодарона? Как врачу определить минимальную дозу препарата?
По рекомендациям ESC (2015), поддерживающая доза препарата для перорального приема при желудочковых аритмиях составляет 200-400 мг/сут. Четкие схемы назначения и контроля приема ААП, в том числе амиодарона, у больных с ФП не разработаны. Критериями эффективности пероральной терапии амиодароном являются исчезновение или урежение эпизодов нарушений ритма по данным повторных записей электрокардиографии, холтеровского суточного мониторинга. В связи с эффектом медленного насыщения начинать оценку эффективности лечения амиодароном можно не раньше, чем с третьей недели.
Как длительно необходимо принимать амиодарон? Зависит ли длительность терапии амиодароном от клинической ситуации и морфофункционального состояния сердечно-сосудистой системы пациента?
В настоящее время доказано значение длительности и непрерывности приема амиодарона у больных с ФП. По данным многоцентрового РКИ со средним сроком наблюдения 2,1 года, у пациентов, получавших эпизодическое лечение амиодароном, была значительно выше частота рецидивов ФП и значительно выше летальность вследствие всех причин, а также выше частота госпитализаций от сердечно-сосудистых причин, по сравнению с больными, получавшими в течение всего этого времени непрерывную терапию амиодароном (S. Ahmed et al., 2008). При персистирующей форме ФП отмена амиодарона в течение первых 1-2 мес на основании регистрации устойчивого синусового ритма является ошибкой, что было также показано в ранее упомянутом украинском исследовании.
Консенсусы по ведению пациентов с желудочковыми аритмиями не содержат рекомендаций по срокам антиаритмической терапии. Влияние ААП на долгосрочный прогноз считается не доказанным, поэтому длительность терапии амиодароном определяется переносимостью препарата и клинической необходимостью, например, частотой эпизодов и выраженностью симптомов аритмии, частотой срабатывания имплантированного кардиовертера-дефибриллятора.
Можно ли применять амиодарон при патологии щитовидной железы?
Из-за структурной схожести молекулы амиодарона с тиреоидными гормонами и большим содержанием йода (75 мг в одной таблетке) бытует мнение, что длительное лечение аритмий вызывает нарушения функции щитовидной железы (ЩЖ), а у пациентов с заболеваниями этого органа прием амиодарона противопоказан. Однако в действительности нарушения синтеза тиреоидных гормонов у пациентов с исходно нормальной функцией ЩЖ развиваются редко: тиреотоксикоз в 0,003-0,9% случаев, гипотиреоз – в 6%, субклинический гипотиреоз – у 3% больных при длительном (1-2 года) приеме амиодарона (С. Зубкова, 2006). В любом случае при планировании длительной терапии амиодароном необходимо определить уровень тиреотропного гормона в плазме крови, и при выявлении отклонений – назначить консультацию эндокринолога. Терапия амиодароном противопоказана только при клинически манифестном тиреотоксикозе, однако и в данном случае решение зависит от того, с какой целью и в какой ситуации был назначен амиодарон. Например, у пациентов с высоким риском фатальных желудочковых аритмий или при неэффективности других ААП польза от продолжения приема амиодарона может превышать риск от влияния на функцию ЩЖ. У больных с гипотиреозом можно продолжать прием амиодарона на фоне заместительной терапии тиреоидными гормонами.
Есть ли разница между брендовым препаратом и генериками амиодарона?
Для определения наличия или отсутствия различий между брендовым препаратом и генериком должны проводиться исследования биоэквивалентности препарата.
Следует также учитывать, что все крупные многоцентровые исследования, на основании которых были одобрены показания к назначению амиодарона и даны вышеперечисленные рекомендации экспертных ассоциаций, проводились с оригинальным препаратом – Кордароном («Санофи»). Применяя генерик, нельзя быть уверенным, что его эффекты будут соответствовать доказательной базе по амиодарону. Ситуация усугубляется тем, что для регистрации генерика в Украине не требуются доказательства биоэквивалентности оригинальному препарату. В назначении амиодарона часто нуждаются сложные пациенты, имеющие сопутствующие кардиологические заболевания и высокий риск смерти. Использовать у таких больных генерический препарат, не обладающий доказанной биоэквивалентностью, – значит, дополнительно увеличивать риски и угрозу для их жизни.
Подготовил Дмитрий Молчанов
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...