Надання допомоги пацієнтам з фібриляцією передсердь бригадами екстреної (швидкої) медичної допомоги за даними Центру екстреної медичної допомоги та медицини катастроф м. Києва
А.В. Вершигора, В.А. Несукай, М.М. Островська, Центр екстреної медичної допомоги та медицини катастроф м. Києва; М.М. Долженко, д.м.н., професор, Національна медична академія післядипломної освіти ім. П.Л. Шупика МОЗ України, м. Київ
Порушення ритму серця та провідності трапляються у практиці кожного лікаря. Немає пацієнта, у якого б ніколи не спостерігалася екстрасистолія. Однак слід зауважити, що поширеність порушень ритму серця та провідності в популяції залежить від методів виявлення, затверджених статистичних показників та інших чинників.
Так, за даними дослідження С.А. Бикової, у разі однократної реєстрації електрокардіограми (ЕКГ) порушення ритму виявлено в популяції у 16,7% чоловіків та 14,7% жінок, а при холтерівському моніторуванні – у 77,2 та 64,7% відповідно.
У структурі гострих порушень ритму серця найбільшу частку становить фібриляція передсердь (ФП). У той же час існуючий у статистичній звітності показник ураження дорослого населення пароксизмальною тахікардією та миготливою аритмією не дає змоги оцінити реальну поширеність ФП. Так, за статистичними даними, поширеність ФП у 2012 р. становила в Україні 162,7 випадку на 100 тис. населення, у тому числі в м. Києві – 129,4 випадку на 100 тис. населення.
Тобто за офіційними даними поширеність ФП дорівнює <0,2%. Однак при цілеспрямованому виявленні пацієнтів з ФП стандартизований за віком показник поширеності ФП серед населення Солом’янського району м. Києва становив для чоловіків 2,7% та для жінок 2,1%.
У зв’язку зі старінням населення збільшується кількість пацієнтів з ФП. У період з 1990 до 2010 р. поширеність ФП у світі зросла з 569,5 до 596,2 випадку на 100 тис. населення для чоловіків та з 359,9 до 373,1 випадку на 100 тис. населення для жінок. При цьому скорегований за віком рівень смертності, пов’язаний з ФП, за 20 років збільшився удвічі і станом на 2010 р. становив 1,6 та 1,7 на 100 тис. населення для чоловіків і жінок відповідно.
Характерно, що рівень смертності не залежить від типу ФП (персистуюча чи постійна). Так, за результатами дослідження Atrial Fibrillation and Congestive Heart Failure, яке проводилося упродовж 2001-2007 рр. у 123 центрах Канади, США, Бразилії, Аргентини, Європи та Ізраїлю, не виявлено різниці стосовно досягнення первинної кінцевої точки (смерть від серцево-судинних причин) у групах контролю ритму та контролю частоти скорочень шлуночків (ЧСШ) у пацієнтів з ФП та серцевою недостатністю.
Не виключено, що на кінцеву точку значною мірою вплинула негативна дія антиаритмічних препаратів, що нівелювало користь від відновлення та збереження синусового ритму.
У той же час дослідження AFFIRM виявило, що ризик тромбоемболічних ускладнень у вигляді гострого порушення мозкового кровообігу за ішемічним типом зростає як у групі пацієнтів, яким проводили відновлення синусового ритму, так і у групі осіб, до яких застосовувалася тактика контролю ЧСШ.
Ось чому в рекомендаціях Європейського товариства кардіологів (ESC, 2010) по веденню пацієнтів з ФП значну увагу приділено профілактиці тромбоемболічних ускладнень.
Спираючись на дані доказової медицини, американських та європейських рекомендацій (зі змінами, внесеними у 2012 р.) по веденню пацієнтів з ФП, робоча група з порушень ритму серця Асоціації кардіологів України видала у 2014 р. рекомендації з діагностики та лікування ФП, в яких наголошується на необхідності визначення класу проявів аритмії за шкалою EHRA, оцінки ризику розвитку інсульту та діагностичного пошуку станів, що призводять до розвитку ФП та ускладнень аритмії.
У рекомендаціях зазначається, що всі пацієнти, які за шкалою CHA2DS2-Vasc мають ризик тромбоемболічних ускладнень ≥2, повинні постійно отримувати оральні антикоагулянти (ОАК) будь-якої групи.
У випадках, коли ухвалюється рішення про відновлення синусового ритму, незалежно від того, чи приймає пацієнт постійно ОАК, а також від методу відновлення (електрична чи фармакологічна кардіоверсія), з метою попередження тромбоемболічних ускладнень хворий має отримати внутрішньовенно нефракціонований гепарин. Після відновлення синусового ритму пацієнтам із факторами ризику розвитку інсульту призначають ОАК, який надалі слід застосовувати пожиттєво.
Враховуючи особливості профілактики тромбоемболічних ускладнень, переваги електричної кардіоверсії порівняно з фармакологічною та можливість у стаціонарних умовах у низці випадків виконати черезстравохідну ехокардіографію з метою виявлення тромбів у вушку лівого передсердя, відновлення синусового ритму рекомендується проводити в стаціонарних умовах.
За даними Центру екстреної медичної допомоги та медицини катастроф м. Києва, значна кількість пацієнтів із персистуючою ФП викликають бригади екстреної (швидкої) медичної допомоги (бригади ЕМД) для відновлення синусового ритму на місці випадку.
За нашими даними, бригади ЕМД щомісяця отримують 500-800 викликів із приводу пароксизмів ФП/тріпотіння передсердь (ТП) або понад 7000 викликів за рік.
Кількість викликів збільшується в зимовий період і зменшується в літній. При цьому далеко не завжди виклик бригади ЕМД пов’язаний із наявністю симптомів III або IV класу EHRA. Нерідко пацієнти, прийнявши самостійно антиаритмічні препарати, рекомендовані в стаціонарі або лікарями первинної ланки медико-санітарної допомоги, не дочекавшись ефекту, через 2-3 год викликають бригаду ЕМД. Зрозуміло, що остання, враховуючи бажання пацієнтів відновити синусовий ритм та відмову від стаціонарного лікування, намагається відновити синусовий ритм і запобігти повторному виклику. А відсутність уніфікованого клінічного протоколу щодо ведення пацієнтів з ФП та наявність у рекомендаціях низки лікарських засобів, які недоступні в Україні, змушують лікарів всупереч рекомендаціям застосовувати інші схеми відновлення синусового ритму, що може збільшувати ризик ускладнень.
З метою аналізу ефективності та безпечності тактики бригад ЕМД нами проаналізовано 389 карт виїздів швидкої медичної допомоги (форма 110/о) до пацієнтів із приводу ФП/ТП упродовж 20 днів (з 1 по 20 березня 2014 р.). У дослідженні взяли участь 134 чоловіки і 255 жінок, вік хворих коливався від 28 до 94 років і в середньому становив 69,4±10,5 року (середній вік чоловіків – 66,1±11,1 року, жінок – 71,1±9,8 року).
Пароксизм ФП мав місце у 351 пацієнта. Розподіл хворих за типом ФП/ТП представлено у таблиці 1.
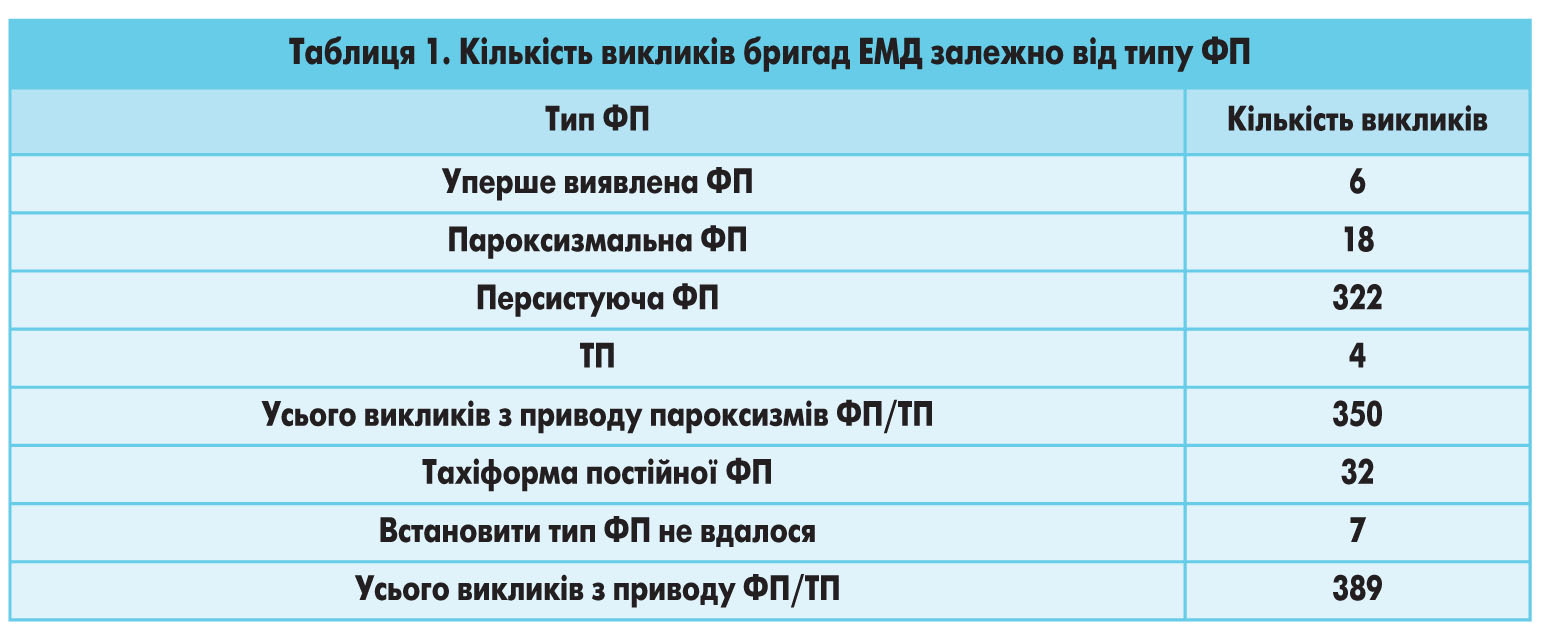
У разі вперше виявленої ФП на догоспітальному етапі призначали лікарські засоби для сповільнення частоти скорочення шлуночків (табл. 2).
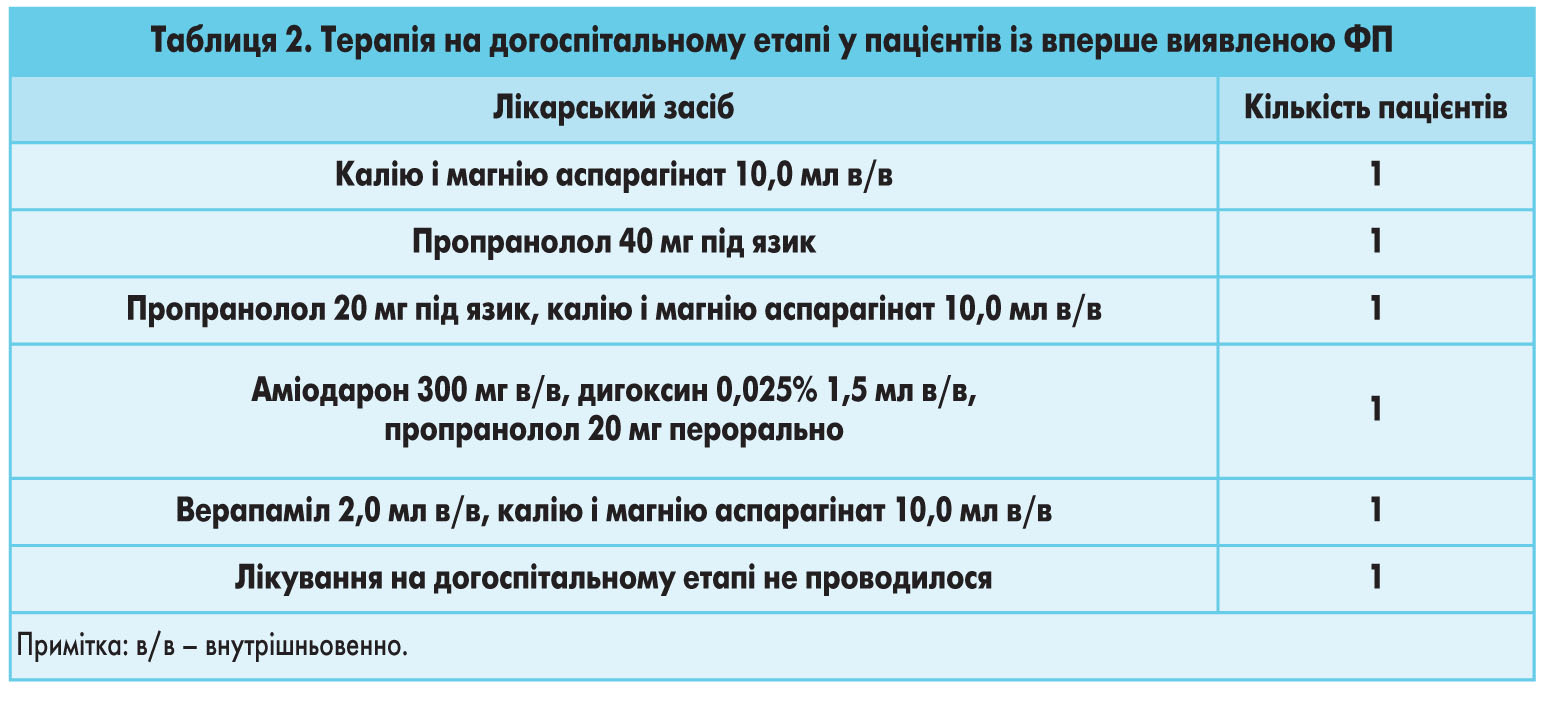 Таким чином, за наявності вперше виявленої ФП терапія на догоспітальному етапі була спрямована на оптимізацію частоти серцевих скорочень, що відповідає рекомендаціям Асоціації кардіологів України.
Таким чином, за наявності вперше виявленої ФП терапія на догоспітальному етапі була спрямована на оптимізацію частоти серцевих скорочень, що відповідає рекомендаціям Асоціації кардіологів України.
У випадках персистуючої ФП для відновлення синусового ритму бригади ЕМД можуть застосовувати внутрішньовенне введення прокаїнаміду або аміодарону, а за нестабільної гемодинаміки – провести електроімпульсну терапію.
На сьогоднішній день рекомендації стосовно комбінування чи послідовного призначення двох антиаритмічних засобів з метою відновлення синусового ритму відсутні або не акцентують увагу на дозах препаратів та проміжках часу між їх призначенням.
Відповідно, не проводиться належна робота з пацієнтами, які самостійно приймають антиаритмічні засоби, а через 2-3 год у зв’язку зі збереженням ФП викликають бригаду ЕМД. Так, із 326 випадків персистуючої ФП/ТП 39 хворих до прибуття бригади ЕМД прийняли аміодарон у дозі 200-400 мг, а 1 пацієнт протягом 1 год – у дозі 800 мг; 14 пацієнтів – пропафенон по 1-3 таблетки; 29 осіб – β-адреноблокатори (18 – пропранолол у дозі 10-80 мг, 4 – метопролол у дозі 25-100 мг, 7 – інші β-адреноблокатори); 2 пацієнти – верапаміл у дозі 40 мг. Ще 10 хворих комбінували різні препарати (здебільшого аміодарон із пропранололом). Викликаючи після цього бригаду ЕМД, пацієнти нерідко вимагають вводити додатково антиаритмічні препарати з метою відновлення синусового ритму, посилаючись на те, що це не перший пароксизм і така тактика застосовувалася раніше.
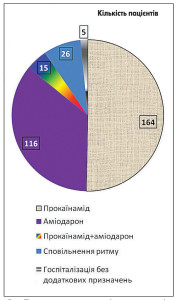
Проведений аналіз цих 326 випадків персистуючої ФП/ТП засвідчив, що для відновлення синусового ритму бригади ЕМД 164 пацієнтам призначали внутрішньовенно прокаїнамід (у більшості випадків у комбінації з фенiлефрином, калiю i магнiю аспарагiнатом та дигоксином), 116 хворим – внутрішньовенно аміодарон (переважно в комбінації з калiю i магнiю аспарагiнатом або з калiю i магнiю аспарагiнатом та дигоксином).
26 пацієнтам призначали лікарські засоби для сповільнення ЧСШ із наступною госпіталізацією: 8 хворим – внутрішньовенно дигоксин, 8 – внутрішньовенно верапаміл, 4 – внутрішньовенно дигоксин та перорально пропранолол, 5 – внутрішньовенно дигоксин із верапамілом і 1 пацієнту – внутрішньовенно верапаміл та перорально пропранолол (останню комбінацію слід вважати не тільки недоречною, а й шкідливою).
Ще 5 осіб, враховуючи прийняті ними антиаритмічні препарати та стабільну гемодинаміку, було госпіталізовано без додаткових призначень на догоспітальному етапі.
Проведений аналіз карт виїздів бригад ЕМД виявив ще одну комбінацію лікарських засобів, яка є нераціональною і може викликати тяжкі ускладнення. 15 пацієнтам, зважаючи на початкову ЧСШ (112±27 за 1 хв), спочатку призначали аміодарон внутрішньовенно в дозі 150-300 мг, а після зменшення ЧСШ – додатково 10% розчин прокаїнаміду в дозі 10,0 мл або 5,0 мл відповідно. Такі призначення траплялись у лікарів, які намагалися будь-що відновити синусовий ритм і попередити можливість повторного виклику бригади ЕМД (рис.).
Таким чином, 50,3% пацієнтів отримали прокаїнамід, 35,6% – аміодарон і 4,6% – комбінацію прокаїнаміду з аміодароном. Остання комбінація антиаритмічних препаратів може призвести до виникнення ускладнень. У нашому випадку при застосуванні цієї комбінації антиаритмічних засобів у 3 пацієнтів із 15 (20,0%) спостерігалося сповільнення AV-провідності з появою AV-блокади I-II ст.
16 хворим перед фармакологічною кардіоверсією призначали прямі антикоагулянти: 10 – нефракціонований гепарин, 4 – еноксапарин, 2 – фондапаринукс, 21 пацієнту – ацетилсаліцилову кислоту, ще 3 особам – клопідогрель у дозі 75 мг.
Призначення нефракціонованого гепарину (а за його тимчасової відсутності – еноксапарину та фондапаринуксу) узгоджується з прийнятими рекомендаціями. Однак відсоток призначень (5,0%) залишається дуже малим, на що у подальшому слід звернути увагу.
За наявності больового синдрому, який бригади ЕМД розцінювали як прояв стенокардії напруги, у більшості випадків призначали ацетилсаліцилову кислоту (а за її непереносимості – клопідогрель).
Аналізуючи проведену на догоспітальному етапі терапію у пацієнтів з персистуючою ФП/ТП, слід зазначити, що у разі застосування прокаїнаміду ускладнення зафіксовано в 23 (13,6%) випадках: крім згаданих вище 3 випадків появи AV-блокади I-II ст. при використанні комбінації прокаїнаміду з аміодароном, AV-блокада I-II ст. виникла у 16 хворих, розширення комплексу QRS – у 2 і гіпотензія – у 2 пацієнтів. Ці ускладнення були минущими і не вимагали додаткової медикаментозної корекції.
Ускладнень на тлі призначення аміодарону не зафіксовано.
Аналізуючи причини сповільнення AV-провідності, не слід забувати і про постійну підтримуючу терапію з метою збереження синусового ритму, на яку бригади ЕМД не завжди звертають належну увагу.
Так, із 326 пацієнтів з персистуючою ФП/ТП аміодарон постійно приймають 39 осіб, β-блокатори – 36, комбінацію β-блокаторів з аміодароном – 11, етацизин – 3 (у тому числі 1 хворий – етацизин разом із β-блокатором), пропафенон – 1 пацієнт. Тобто 90 (27,6%) хворих постійно застосовували антиаритмічні препарати з метою підтримання синусового ритму. У той же час пацієнти з ФП/ТП практично не приймають лікарські засоби для попередження тромбоемболічних ускладнень. Зокрема, лише в 5 картах виїзду бригад ЕМД зазначено, що пацієнти постійно приймають варфарин, не зареєстровано жодного випадку прийому з цією метою ривароксабану чи дабігатрану.
Зафіксовано повторні виїзди бригад ЕМД до 35 пацієнтів, у тому числі 11 після застосування аміодарону, 19 – прокаїнаміду і 5 – комбінації прокаїнаміду з аміодароном.
Після проведеного лікування бригадами ЕМД у зв’язку зі збереженням ФП госпіталізовано 52 пацієнти, з них 6 пацієнтів із вперше виявленою ФП. У однієї пацієнтки із вперше виявленою ФП синусовий ритм відновився приблизно через півгодини на тлі сповільнення ЧСШ після прийому пропранололу (20 мг під язик), корвалолу та внутрішньовенної ін’єкції калiю i магнiю аспарагiнату 10,0 мл. Незважаючи на відновлення синусового ритму, цю пацієнтку також було госпіталізовано для подальшого обстеження в стаціонарних умовах, що узгоджується з чинними рекомендаціями.
У разі постійної ФП для сповільнення ритму бригадами ЕМД застосовувалися аміодарон, прокаїнамід, дигоксин, пропранолол, метопролол, верапаміл (табл. 3).
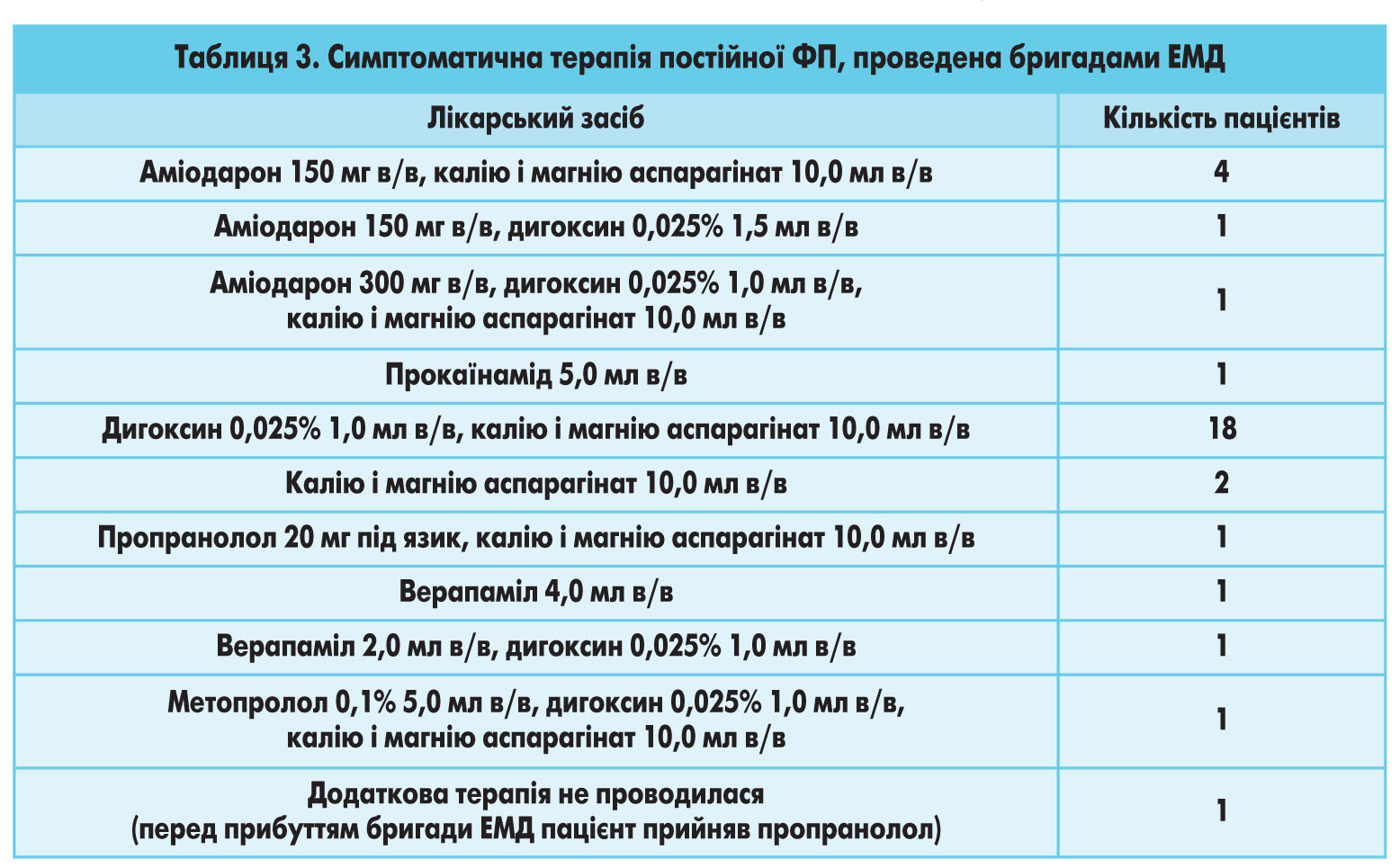
Таким чином, для сповільнення ЧСШ при постійній ФП β-блокатори були призначені 2 пацієнтам, дигоксин – 22, верапаміл – 2, аміодарон – 3, прокаїнамід – 1. Більшість хворих (90,6%) отримали комбіноване лікування. Бригади ЕМД у більшості випадків надають перевагу дигоксину, тому що не завжди можуть оцінити ступінь декомпенсації пацієнта і обирають лікарський засіб, який не пригнічує скоротливість міокарда. Застосування в одному випадку прокаїнаміду, який не є препаратом вибору, свідчить про необхідність подальшої роботи з медичним персоналом стосовно інформування про ведення таких пацієнтів відповідно до прийнятих рекомендацій.
Отже, за даними проведеного аналізу карт виїздів з приводу ФП/ТП, на догоспітальному етапі призначення аміодарону є більш безпечним порівняно з прокаїнамідом, що сприяє зменшенню кількості повторних викликів бригад ЕМД з приводу ФП/ТП.
Чому ж, незважаючи на кращий ефект і відсутність ускладнень після застосування аміодарону, бригади ЕМД продовжують використовувати прокаїнамід? Чому стало можливим призначення внутрішньовенно верапамілу з пероральним пропранололом або внутрішньовенно аміодарону з прокаїнамідом?
Ні в Європейських рекомендаціях з ведення пацієнтів з ФП 2010 р., ні в рекомендаціях Робочої групи з порушень ритму серця Асоціації кардіологів України 2011 р. та 2014 р., ні в рекомендаціях з ведення пацієнтів з фібриляцією передсердь AHA/ACC/HRS 2014 р. такі комбінації не згадуються. Але треба взяти до уваги, що на сьогоднішній день застосування прокаїнаміду також відсутнє в цих рекомендаціях. У той же час на оснащенні бригад ЕМД немає перелічених у цих рекомендаціях для фармакологічної кардіоверсії лікарських засобів, за винятком аміодарону, а також залишається можливість закупівлі прокаїнаміду, який у 2-3 рази дешевший за аміодарон. Тому практикуючі лікарі продовжують застосовувати прокаїнамід, спираючись лише на власний досвід та інструкцію щодо призначення цього препарату, у якій зазначено: «Купірування гострого нападу аритмії. Вводять 100 мг препарату у вигляді повільної внутрішньовенної ін’єкції (зі швидкістю не більше 50 мг/хв), за необхідності ін’єкцію повторюють кожні 5 хв. Для досягнення бажаного клінічного ефекту допустимо застосовувати сумарну дозу до 1 г, при цьому перед кожним наступним введенням обов’язково слід виміряти пульс, артеріальний тиск та оцінити показники ЕКГ».
А що ж робити, якщо виникнуть ускладнення? У тій же інструкції знаходимо далі: «З обережністю застосовують при гострій ішемічній хворобі, кардіоміопатіях, міастенії, інфаркті міокарда через можливість пригнічення скоротливої здатності міокарда. При введенні препарату необхідно постійно слідкувати за пульсом, артеріальним тиском та електрокардіограмою. При виникненні блокади І ступеня необхідно зменшити дозу або припинити введення препарату. Надмірне розширення комплексу QRS чи подовження інтервалу PR свідчить про необхідність зупинити введення препарату. При виникненні артеріальної гіпотензії необхідно зменшити дозу або тимчасово зупинити введення препарату, за необхідності – з обережністю призначити вазопресори».
А чи можна комбінувати прокаїнамід з аміодароном? Читаємо інструкцію далі: «Аміодарон: внаслідок адитивної дії збільшується інтервал QT, можливий розвиток шлуночкової аритмії, а також підвищення концентрації у плазмі крові прокаїнаміду та його метаболіту N-ацетилпрокаїнаміду, що призводить до посилення побічних реакцій».
Тобто формально існує наявне застереження, а не заборона. І лише вдумливий лікар розуміє, що така адитивна дія може викликати серйозне ускладнення.
Те ж саме маємо із застосуванням комбінації верапамілу та пропранололу. Відомо, що одночасне внутрішньовенне призначення верапамілу та пропранололу може призвести до летальних наслідків. А не внутрішньовенне? У довіднику з лікарських засобів написано, що поєднання пропранололу із верапамілом не рекомендовано через ризик різкого знижения кров’яного тиску і скорочувальної здатності серця.
Звернемося до інструкцій. В інструкції для медичного застосування верапамілу гідрохлориду зазначено: «Одночасне застосування верапамілу гідрохлориду з бета-адреноблокаторами збільшує взаємну пригнічувальну дію на автоматизм синоатріального вузла, АV-провідність і скоротливість міокарда, внаслідок цього підвищується ризик розвитку вираженої артеріальної гіпотензії, АV- та SА-блокад, брадикардії, серцевої недостатності, особливо при застосуванні високих доз бета-адреноблокаторів або при їх внутрішньовенному введенні».
В інструкції для медичного застосування пропранололу зазначається: «Одночасне застосування β-блокаторів з блокаторами кальцієвих каналів з негативною інотропною дією (верапаміл, дилтіазем) може призвести до посилення цих ефектів, зокрема, у пацієнтів із порушеною функцією серця та/або синоатріальної або атріовентрикулярної провідності. Це може призвести до тяжкої гіпотензії, брадикардії та серцевої недостатності. β-Блокатор або блокатор кальцієвих каналів не можна вводити внутрішньовенно протягом 48 год після припинення застосування іншого».
Недостатні знання взаємодії лікарських засобів призводять до неправильного трактування рекомендацій та механічного перенесення застосування комбінацій одних груп антиаритмічних препаратів на інші групи. Тому частина лікарів вказівки з рекомендації на кшталт «у пацієнтів із пароксизмальною, персистуючою або постійною ФП рекомендується здійснювати контроль частоти серцевих скорочень за допомогою фармакологічних засобів (β-блокаторів, недигідропіридинових блокаторів кальцієвих каналів, препаратів наперстянки або комбінацій цих засобів); вибір препарату має ґрунтуватися на індивідуальних особливостях пацієнта, а його доза повинна коригуватися таким чином, щоб уникнути брадикардії» сприймають як дозвіл до одночасного обережного застосування згаданих антиаритмічних препаратів, навіть якщо один із них призначено внутрішньовенно.
Те ж саме стосується інтерпретації рекомендацій поєднувати в амбулаторних умовах пропафенон або флекаїнід із недигідропіридиновим блокатором кальцієвих каналів для відновлення синусового ритму не в стаціонарних умовах (тактика «пігулка в кишені», клас IIa, рівень доказів В).
І лише в інструкції до медичного застосування препарату Верапаміл-Дарниця читаємо категоричне застереження: «Протипоказано застосовувати внутрішньовенно пацієнтам, які приймають β-адреноблокатори (крім реанімаційних заходів)».
Це пов’язано з тим, що в дозах, які є нижчими за оптимальні, поєднання недигідропіридинових антагоністів кальцію та β-адреноблокаторів при пероральному прийомі може викликати серйозні ускладнення. І лікарі, які раніше призначали такі комбінації, спираючись на власний досвід, на жаль, інколи продовжують їх призначати.
Таким чином, необхідне проведення подальшої роботи з медичним персоналом бригад ЕМД щодо вибору тактики при наданні допомоги пацієнтам з ФП/ТП. Відсутність низки антиаритмічних препаратів, які вказані в рекомендаціях, та відмова пацієнтів від госпіталізації змушують шукати компромісні рішення. Але при цьому слід особливо ретельно збирати анамнез та при виборі подальшої тактики в кожному випадку враховувати співвідношення ризик/користь.
Затвердження протоколів надання медичної допомоги (локальний протокол «Фібриляція і тріпотіння передсердь» було затверджено в Центрі екстреної медичної допомоги та медицини катастроф м. Києва у травні 2014 р.) є лише частиною постійної кропіткої роботи стосовно підвищення кваліфікації медичних працівників.
Список літератури знаходиться в редакції.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....