Деякі шляхи удосконалення методів діагностики уражень серця у дітей з ревматичними хворобами
О.А. Ошлянська, д.м.н., ДУ «ІПАГ НАМН України», І.А. Чайковський, Ю.О. Фролов, Інститут кібернетики ім. В.М. Глушкова НАН України, Г.В. Мясников, д.м.н., А.П. Казмірчук, Головний військово-медичний клінічний центр «Головний військовий клінічний госпіталь», м. Київ
Ревматичні хвороби (РХ) належать до найважчих форм хронічної патології людини і є найчастішою причиною інвалідизації серед соматичних захворювань у дітей [1, 2]. Значний вплив на її збільшення мають ураження серцево-судинної системи (ССС), які суттєво погіршують клінічну картину, перебіг та прогноз захворювання.
За даними наших попередніх досліджень, прояви уражень ССС у дітей з РХ відзначаються високою частотою. Так, за даними клінічного реєстру, серед 327 пацієнтів з РХ, що перебували на спостереженні у відділенні хвороб сполучної тканини у дітей упродовж останніх 15 років, частота залучення органів ССС у патологічний процес при різних нозологічних одиницях коливалась від 50% у дітей з ювенільним артритом до 81% у хворих на системний червоний вовчак [3]. Причому в останні десятиріччя реєструються більш рідкісні ураження серця запального характеру (4,9% хворих). Однак протягом спостереження у 19,3% дітей з РХ було діагностовано вторинну кардіоміопатію, ще у 3,9% виявили порушення ритму серця, що свідчить про прихований, субклінічних характер міокардіальних уражень, які залишаються своєчасно нерозпізнаними на тлі інших системних проявів захворювання.
Виявлені зміни з боку ССС при РХ у дітей зазвичай поліетіологічні, їх важко трактувати клініцисту, адже вони можуть бути проявом або наслідком перенесеного кардиту, результатом токсичної дії лікарських засобів, бути зумовленими порушенням метаболічних процесів в організмі тощо. В дослідженнях останніх років показано, що збільшення частоти вторинних захворювань ССС при РХ пов’язане з імунозапальними механізмами, які подібні до провідних патогенетичних ланок розвитку атеросклерозу [4].
За даними досліджень, проведених в ДУ «ІПАГ НАМН України», діти з РХ внаслідок проведення тривалої медикаментозної терапії, особливо лікування глюкокортикоїдними гормонами (ГК), мають підвищену вірогідність формування артеріальної гіпертензії [5]. Першим органом-мішенню при підвищенні артеріального тиску у дітей з РХ є серце.
Розвиток аритмій, вторинних кардіоміопатій, артеріальної гіпертензії у дітей з РХ незалежно від їх причини є предиктором розвитку фатальних серцево-судинних подій (інфаркту, інсульту) в майбутньому.
Вищезазначене обумовлює необхідність широкого впровадження в повсякденну ревматологічну практику сучасних діагностичних методів.
Як відомо, електрокардіографія (ЕКГ) у 12 стандартних відведеннях є рутинним методом оцінки стану ССС у дітей, який доступний всім дитячим кардіоревматологам. Однак початкові ознаки кардіологічних уражень при застосуванні традиційних методів обстеження (ЕКГ, ехокардіографії – ЕхоКГ) у хворих на РХ можуть не виявлятися. Потреба удосконалення клінічного та інструментального обстеження хворих дітей зумовлює необхідність постійного пошуку нових інформативних і зручних у застосуванні методів функціональної діагностики, зокрема удосконалення методів оцінки ЕКГ.
Так, доведено, що безумовні клініко-прогностичні переваги порівняно з традиційною ЕКГ має сучасний метод холтерівського моніторування. У попередніх дослідженнях, проведених у нашій клініці, показано, що добове моніторування ЕКГ є одним з найінформативніших засобів оцінки функціонального стану ССС для виявлення предикторів порушень ритму серця завдяки підвищенню точності оцінки дійсного рівня частоти серцевих скорочень, можливості здійснення впливу на гемодинаміку, уточненню часу виникнення порушень, тривалості та характеру добових змін [3].
У цьому аспекті значний інтерес лікарів обумовлений можливістю застосування в дитячому віці дослідження сучасних методів оцінки ЕКГ IV покоління (вважається, що до ЕКГ І покоління належить «ручне» вимірювання амплітудно-часових показників, до ІІ – автоматичне вимірювання при візуальному аналізі кривих, до ІІІ – автоматична електрокардіографічна діагностика з формуванням синдромального діагнозу). Принципова відмінність ЕКГ IV покоління полягає в тому, що інформація обробляється з використанням програмного забезпечення. Для аналізу використовується так звана сигнал-усереднена ЕКГ, отримана шляхом усереднення кількох електрокардіографічних комплексів, за винятком атипових [6].
Представником першої групи дослідження ЕКГ IV покоління є її оцінка в фазовому просторі, зокрема із застосуванням мобільного пристрою «Фазаграф», запропонованого українськими розробниками. Цей метод за рахунок комп’ютерного аналізу симетрії зубця Т та сегмента R(S)-T на ЕКГ дає можливість виявити ранні прояви метаболічних порушень в міокарді. За даними попередніх досліджень, проведених в нашій клініці, оцінка ЕКГ в фазовому просторі є найбільш оптимальною на амбулаторному етапі як скринінговий метод виявлення органічних міокардіальних порушень завдяки простоті виконання дослідження, мобільності пристрою, миттєвому отриманню результатів. Доведено, що її використання у дітей з РХ дозволяє на 20% частіше, ніж за оцінкою стандартної ЕКГ, діагностувати порушення процесів реполяризації міокарда, диференціювати органічні й функціональні ураження міокарда і вирішити питання щодо можливості виконання вправ лікувальної фізкультури [7]. Однак для оптимальної комплексної оцінки функції серцевого м’яза необхідно визначити й проаналізувати значно більше параметрів.
У цьому аспекті варто згадати сучасні методи дослідження серця як електричного генератора, інноваційність яких полягає в розвинених математичних підходах до аналізу даних і удосконалених технічних засобах, що використовуються для реєстрації сигналу. Найбільш відомим та перспективним засобом цієї групи є магнітокардіографія (МКГ) – метод реєстрації і аналізу магнітної компоненти електромагнітного поля, що генерується джерелами електричної активності серця. До його переваг відносять можливість реконструювати всі джерела, що утворюють магнітне поле серця у просторі. Вимірювання надслабких магнітних полів, що виникають під час роботи людського серця, вимагає дуже чутливої апаратури. Значного підвищення чутливості біомагнітних вимірювань було досягнуто з впровадженням так званих СКВІД-магнітометрів, які працюють на основі стаціонарного ефекту Джозефсона при температурі рідкого гелію (4,2 K). Під час реєстрації МКГ лікарю для аналізу надаються карти розподілу густини струму в певний момент кардіоциклу. Попередніми дослідниками розроблено принципи аналізу цих карт, які полягають в оцінці їх однорідності, що дозволяє проводити топічну діагностику уражень міокарда завдяки виявленню вогнищ неоднорідності його магнітного поля [8].
Вищезазначене обумовлює доцільність впровадження таких методик аналізу ЕКГ в практику дитячої кардіоревматології.
Мета роботи – удосконалення ранньої діагностики уражень ССС при РХ у дітей на підставі дослідження показників ЕКГ IV покоління.
Матеріали та методи
Проведено аналіз даних клінічного реєстру відділення хвороб сполучної тканини у дітей ДУ «ІПАГ НАМН України» за 10 останні років, серед всіх хворих на РХ дітей обрано для поглибленого вивчення медичну документацію 21 пацієнта, в якого загалом мали місце системні прояви хвороби, але на момент обстеження не виявлено клінічних і лабораторних ознак кардиту або гемодинамічно значущої вторинної кардіоміопатії. У дослідження включені винятково діти середнього шкільного віку та виключені пацієнти з високою активністю запального процесу, коморбідною ендокринною патологією, ожирінням, наявністю артеріальної гіпертензії.
У цій групі дітей проводилось комплексне клініко-лабораторне обстеження, що окрім загальноклінічних досліджень включало визначення біохімічних маркерів ураження ССС (активності креатинфосфокінази (КФК), лактатдегідрогенази (ЛДГ), кардіоінтервалографію (КІГ), ЕхоКГ, оцінку МКГ. Здійснювався аналіз отриманих показників залежно від активності запального процесу, призначеного лікування (у тому числі терапії ГК), наявності супутньої патології та у порівнянні з окремими лабораторними показниками.
На момент проведення дослідження серед обраної групи хворих на РХ ГК отримували 10 пацієнтів (з них 7 в середньотерапевтичних дозах 1-2 мг/кг за преднізолоном), цитостатичні засоби – 5 (азатіоприн, метотрексат, циклофосфамід), нестероїдні протизапальні препарати (НПЗП) – 13 дітей, кардіотрофічні – 6 пацієнтів, вазоактивні – 2, ренопротектор еналаприл у низькій дозі – 1 дитина, курантил – 5 пацієнтів, препарати кальцію – 11, калію – 1 дитина.
Контрольна група складалася з 18 здорових учасників.
МКГ-дослідження у дітей із РХ та здорових добровольців проводили за наступною методикою [9, 10]. Під час запису МКГ точками спостереження були 36 (6×6) вузлів з кроком 4 см квадратної решітки, що мали прив’язку до анатомічних орієнтирів грудної клітки обстежуваного. Тривалість запису сигналу в одній точці становила 30-90 с (інтервал, необхідний для реєстрації достатньої кількості кардіоциклів, щоб за рахунок усереднення досягти максимального відношення сигнал/шум). Перехід від однієї точки до іншої виконувався завдяки переміщенню ліжка вздовж двох осей. Водночас реєструвалася референтна ЕКГ у ІІ стандартному відведенні, що було необхідним для подальшої процедури усереднення МКГ-сигналу, суть якого полягала в автоматичному зіставленні та накопиченні синхронних комплексів МКГ у різних кардіоциклах (з виключенням артефактів та атипових комплексів) в режимі off-line.
У результаті такої обробки отримали 36 МКГ-кривих, на основі яких за допомогою методу двовимірної інтерполяції створювалися миттєві карти розподілу магнітного поля (рис. 1).
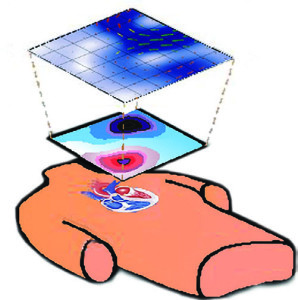 Рис. 1. Модельне відображення карти розподілу
Рис. 1. Модельне відображення карти розподілумагнітного поля та розрахованих векторів густини струмів
Далі за алгоритмом вирішення «зворотного завдання» ці карти перебудовувалися в миттєві карти розподілу векторів густини струмів (ВГC) (рис. 2).
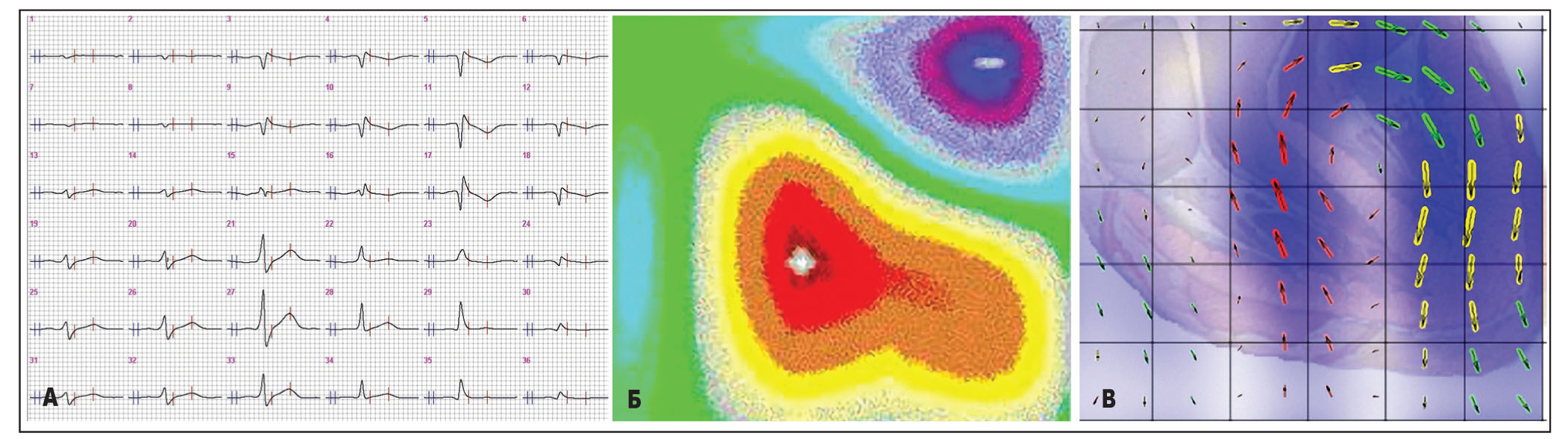 Рис. 2. Різні способи відображення магнітної активності серця: усереднені МКГ-криві (А), карта магнітного поля (Б) та розподілу ВГС (В)
Рис. 2. Різні способи відображення магнітної активності серця: усереднені МКГ-криві (А), карта магнітного поля (Б) та розподілу ВГС (В)Такий підхід дав можливість виділити низку нових МКГ-показників, які дозволяють виключити вплив на результати досліджень технічних особливостей МКГ-системи.
Аналіз динаміки виділених параметрів ВГС в обраних часових інтервалах кардіоциклу (QRS, ST-T, Ta-e) проводився з кроком у 4-10 мс. Для кожного обраного інтервалу досліджувалися часові та/або просторові показники збудження міокарда з кольоровим маркуванням періодів із аномальним напрямком вектора збудження.
СТАТТІ ЗА ТЕМОЮ Педіатрія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....
Зв’язок між рівнем сироваткової сечової кислоти (ССК) і ризиком серцево-судинних захворювань (ССЗ) упродовж багатьох років є предметом вивчення дослідників. Установлено, що рівень ССК – незалежний предиктор смерті від усіх причин і серцево-судинної смерті, зокрема від гострого коронарного синдрому, інсульту та серцевої недостатності (СН). Також опубліковано багато робіт про зв’язок між ССК і функцією нирок. Попри значну кількість публікацій, деякі моменти, а саме: яким є оптимальний поріг ССК для визначення ризику ССЗ, чи необхідна корекція значень ССК для функції нирок, чи є ССК ключовим патологічним елементом метаболічної дисрегуляції, потребують прояснення....




