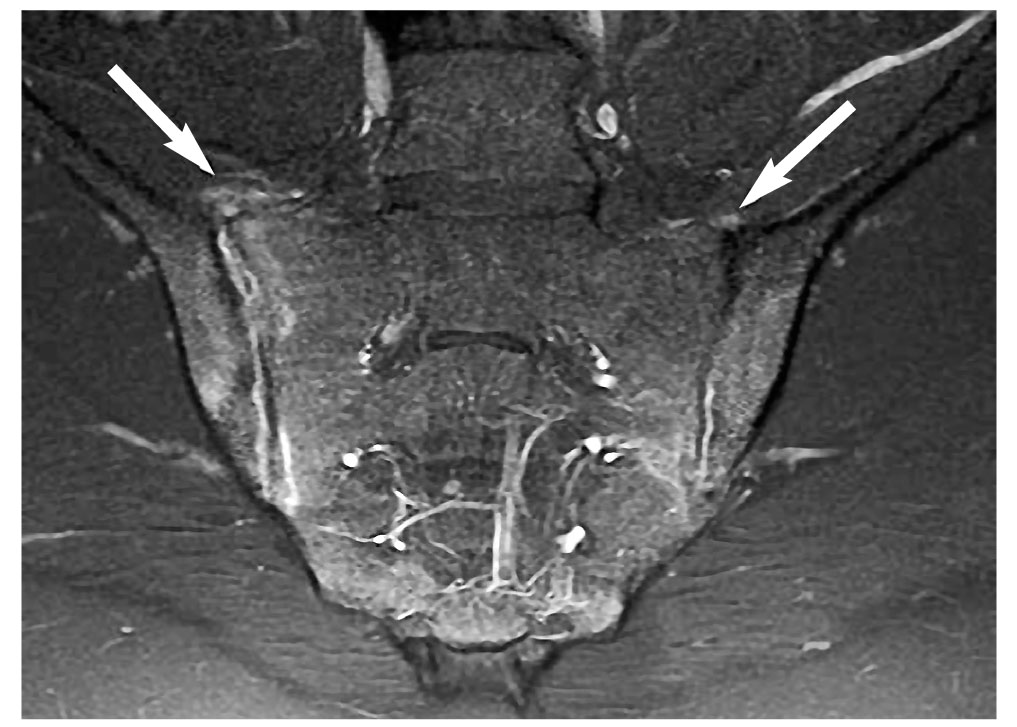
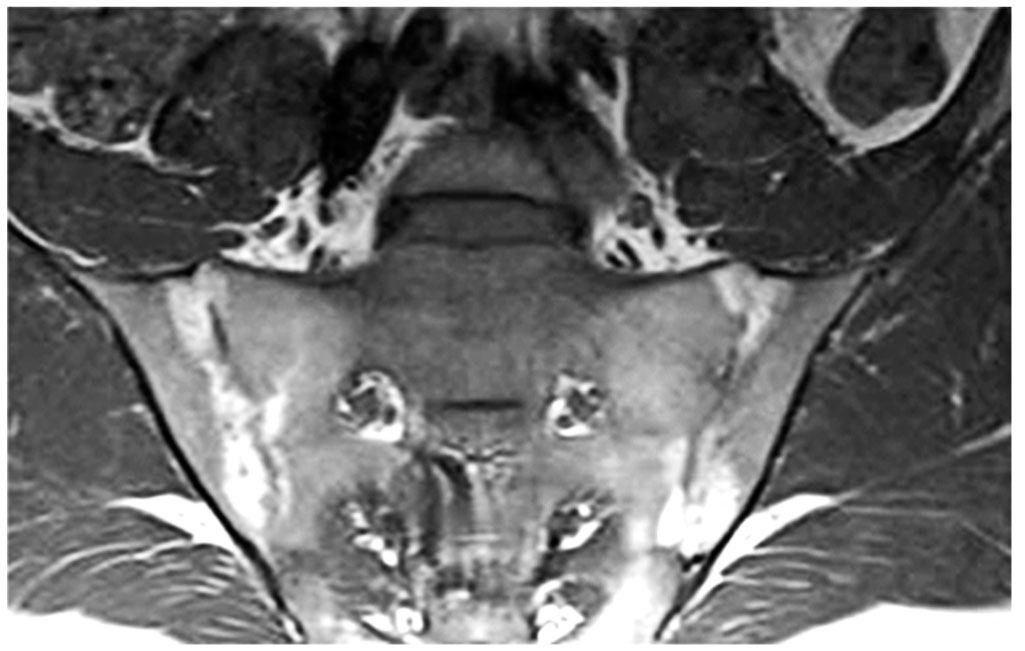
МРТ крестцово-подвздошных сочленений: стандарты диагностики
 Е.А. Гармиш, к.м.н., отдел некоронарогенных болезней сердца и клинической ревматологии, ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, И.Н. Тютюнник, диагностический центр «Медэкс», г. Киев
Е.А. Гармиш, к.м.н., отдел некоронарогенных болезней сердца и клинической ревматологии, ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, И.Н. Тютюнник, диагностический центр «Медэкс», г. Киев
Несмотря на то что симптомокомплекс анкилозирующего спондилита (АС) описан более 100 лет назад, до настоящего времени наблюдается поздняя диагностика этого заболевания – с опозданием на 7-10 лет. Постановка диагноза вызывает затруднения не только у врачей общей практики, но и у ревматологов. На ранней стадии заболевания пациентов зачастую ошибочно наблюдают с диагнозом остеохондроз позвоночника, корешковый синдром, подагрический артрит, острый (или обострение хронического) пиелонефрит, пяточная шпора, коксартроз, гонартроз, реактивный артрит.
В последнее десятилетие, по результатам фундаментальных исследований в области эпидемиологии, генетики и патогенеза, концепция спондилоартрита (СпА) претерпела значительные изменения. Различные заболевания, такие как псориатический артрит, артриты, ассоциированные с поражением кишечника и АС, на дорентгенологической стадии были объединены в одну группу под названием «спондилоартриты». Основанием для классификации того или иного заболевания в группу СпА служит определенный симптомокомплекс с преимущественным поражением позвоночника и крестцово-подвздошных сочленений (КПС). В 2009 г. Международным обществом по оценке спондилоартритов (ASAS) были внедрены новые классификационные критерии СпА, которые включают определения «аксиальный спондилоартрит» (акСпА) и «периферический спондилоартрит» согласно преимущественному поражению в клинической картине аксиального или периферического скелета. С учетом новых критериев группа акСпА включает в себя как пациентов, которые удовлетворяют модифицированным Нью-Йоркским критериям АС 1984 г., так и лиц, которые не удовлетворяют этим критериям. Для таких больных был введен термин «дорентгенологический акСпА». Диагноз дорентгенологический акСпА устанавливают на основании совокупности клинических симптомов и наличия активного сакроилиита по данным магнитно-резонансной томографии (МРТ) или позитивности по антигену HLA-B27. Распространенность акСпА в США составляет 0,9-1,4% населения. Актуальной является достоверная диагностика сакроилиита у пациентов с дорентгенологическим акСпА. Единственным на сегодняшний день высокоспецифичным методом исследования КПС является МРТ.
В 2009 г. были опубликованы рекомендации ASAS/ OMERACT по магнитно-резонансной (МР-) диагностике сакроилиита для постановки диагноза акСпА (M. Rudwaleit, A.R. Dis, 2009).
Согласно этим рекомендациям патологические МР-изменения в КПС разделяют на воспалительные и структурные. К первым относятся отек костного мозга (ОКМ, или остеит), синовит, энтезит и капсулит. Наличие ОКМ, по данным МРТ, достаточно для постановки диагноза сакроилиита. К структурным изменениям относятся склероз, эрозии, жировая инфильтрация и анкилоз.
Воспалительные изменения. Технические аспекты
Для выявления активного воспалительного процесса используются следующие МР-режимы: Т1 взвешенное изображение (ВИ) без или с подавлением сигнала от жировой ткани (FS), усиленное введением контрастного агента; STIR-режим – разновидность режима Т2 градиент эхо с подавлением сигнала от жировой ткани.
В режиме Т1 ВИ жировая ткань дает светлый (гиперинтенсивный) сигнал, а вода – темный (гипоинтенсивный) сигнал. Таким образом, в режиме Т1 активные воспалительные изменения имеют гипоинтенсивный (темный) МР-сигнал, так же как ликвор и межпозвоночный диск, а жировая ткань (как подкожная, так и патологическая жировая инфильтрация костного мозга) – гиперинтенсивный (светлый) МР-сигнал (рис. 1).
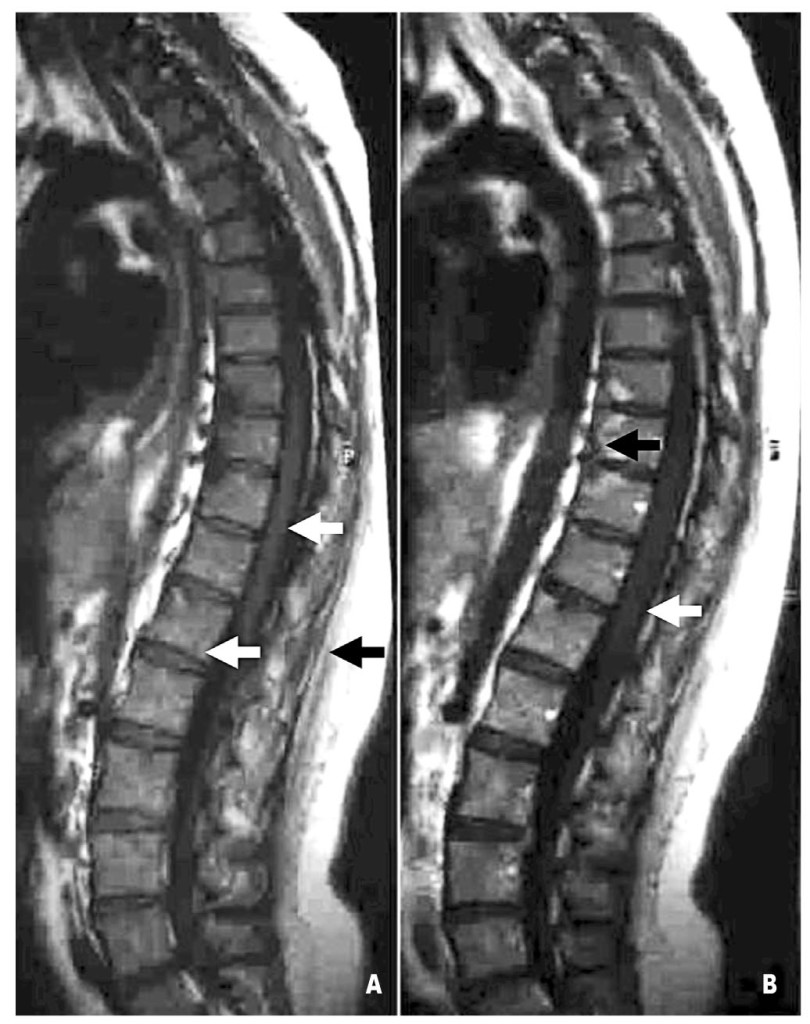 Рис. 1. Стандартное Т1 ВИ (А) и усиленное КА (В) изображение позвоночника. Гипоинтенсивный (темный) сигнал от ликвора и межпозвоночного диска, а также активных воспалительных изменений (белые стрелки). Гиперинтенсивный (светлый) сигнал от подкожного жира. Гиперинтенсивный сигнал от активных воспалительных изменений после введения КА (черные стрелки)
Рис. 1. Стандартное Т1 ВИ (А) и усиленное КА (В) изображение позвоночника. Гипоинтенсивный (темный) сигнал от ликвора и межпозвоночного диска, а также активных воспалительных изменений (белые стрелки). Гиперинтенсивный (светлый) сигнал от подкожного жира. Гиперинтенсивный сигнал от активных воспалительных изменений после введения КА (черные стрелки)Введение контрастного агента (КА) в режиме Т1 изменяет МР-сигнал в области воспалительных изменений с темного на светлый (рис. 1), что позволяет достоверно диагностировать сакроилиит. Введение КА имеет безупречные диагностические преимущества, но имеет и ряд ограничений у пациентов с нарушением функции почек, а также, по данным некоторых авторов, вызывает развитие гадолинийиндуцированного почечного фиброза.
Альтернативой является использование режима STIR (рис. 10). В этом режиме вода имеет светлый (гиперинтенсивный) МР-сигнал, а жировая ткань – темный (нормо- или гипоинтенсивный сигнал в сравнении с таковым показателем в случае нормальной кости в качестве референтного значения).
Исследование необходимо проводить с использованием магнитной катушки мощностью 1-1,5 Тесла в семикорональной проекции (параллель к линии соединения верхних дорзальных углов тел позвонков S1-S3). Технические параметры для режима Т1: TR/TE: 500/10 ms; T1 FS: TR/TE: 660/16 ms; STIR TR/TE/TI: 4000/60/150 ms. Толщина среза 3 или 4 мм.
Костный отек или остеит
ОКМ выглядит как гиперинтенсивный сигнал в режиме STIR или гипоинтенсивный сигнал в режиме Т1. Для диагностики сакроилиита в режиме STIR достаточно наличия нескольких областей гиперинтенсивного сигнала на одном срезе или одной области гиперинтенсивного сигнала на двух и более последовательных срезах. Чем выше интенсивность сигнала, тем больше соответствие выявленных изменений активному сакроилииту. Наибольшая интенсивность сигнала при ОКМ сопоставима с интенсивностью сигнала от кровеносных сосудов и ликвора. Гиперинтенсивный сигнал на Т1 FS изображении с введением КА соответствует избыточной васкуляризации и расценивается как активный сакроилиит (рис. 2) ОКМ, как правило, локализуется периартикулярно – субхондральный отек костного мозга.
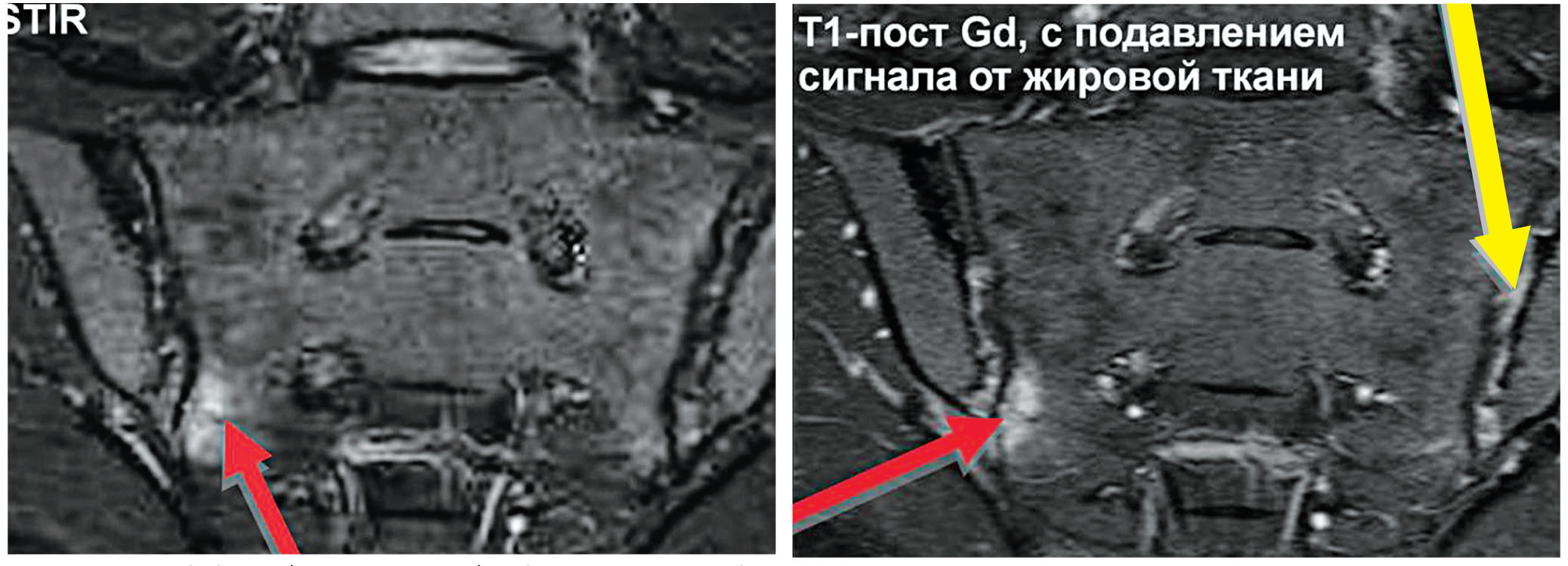 Рис. 2. Остеит (красные стрелки) КПС на МРТ в режиме STIR, Т1 постконтраст с подавлением сигнала от жировой ткани. Введение гадолиния позволяет обнаружить внутрисуставные измения – синовит (желтая стрелка)
Рис. 2. Остеит (красные стрелки) КПС на МРТ в режиме STIR, Т1 постконтраст с подавлением сигнала от жировой ткани. Введение гадолиния позволяет обнаружить внутрисуставные измения – синовит (желтая стрелка)Сигнал от костной ткани в области крестца между фораминальными отверстиями рассматривается в качестве эталона как вариант нормы.
ОКМ как индикатор активного сакроилиита может выявляться при сакроилиите любого происхождения, в том числе инфекционного. ОКМ может ассоциироваться со структурными изменениями, такими как эрозии.
Синовит
В режиме STIR невозможно дифференцировать синовит и физиологическое наличие суставной жидкости. Для диагностики синовита используется режим Т1 FS-постконтраст, при котором синовит определяется как гиперинтенсивный сигнал в синовиальной части КПС (интенсивность подобна сигналу от кровеносных сосудов, рис. 3).
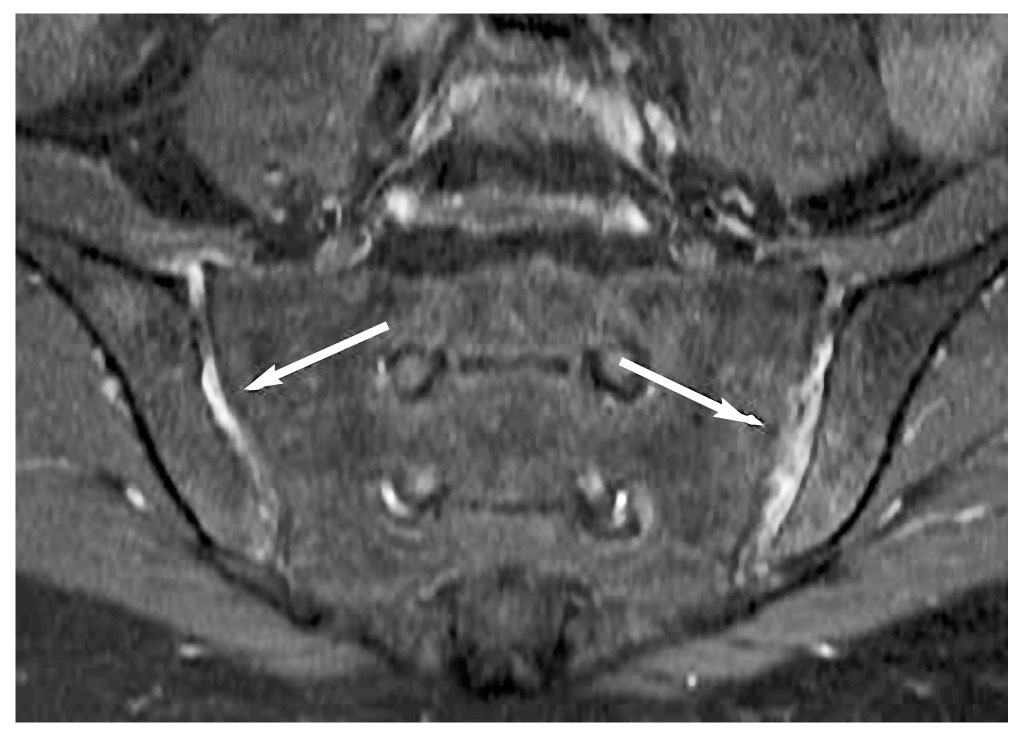 Рис. 3. Синовит. Гиперинтенсивный сигнал (белые стрелки) в режиме Т1 FS постконтраст в синовиальной части КПС (аналогичный сигналу от кровеносных сосудов и ликвора)
Рис. 3. Синовит. Гиперинтенсивный сигнал (белые стрелки) в режиме Т1 FS постконтраст в синовиальной части КПС (аналогичный сигналу от кровеносных сосудов и ликвора)Выявления только синовита без ОКМ недостаточно для постановки диагноза сакроилиита по данным рекомендациям.
Энтезит
Энтезит выглядит как гиперинтенсивный сигнал в режиме STIR и/или постконтрастном Т1 FS изображении в области прикрепления связок и сухожилий к кости, включая ретроартикулярное пространство (рис. 4). Область сигнала может распространяться до костного мозга и мягких тканей.
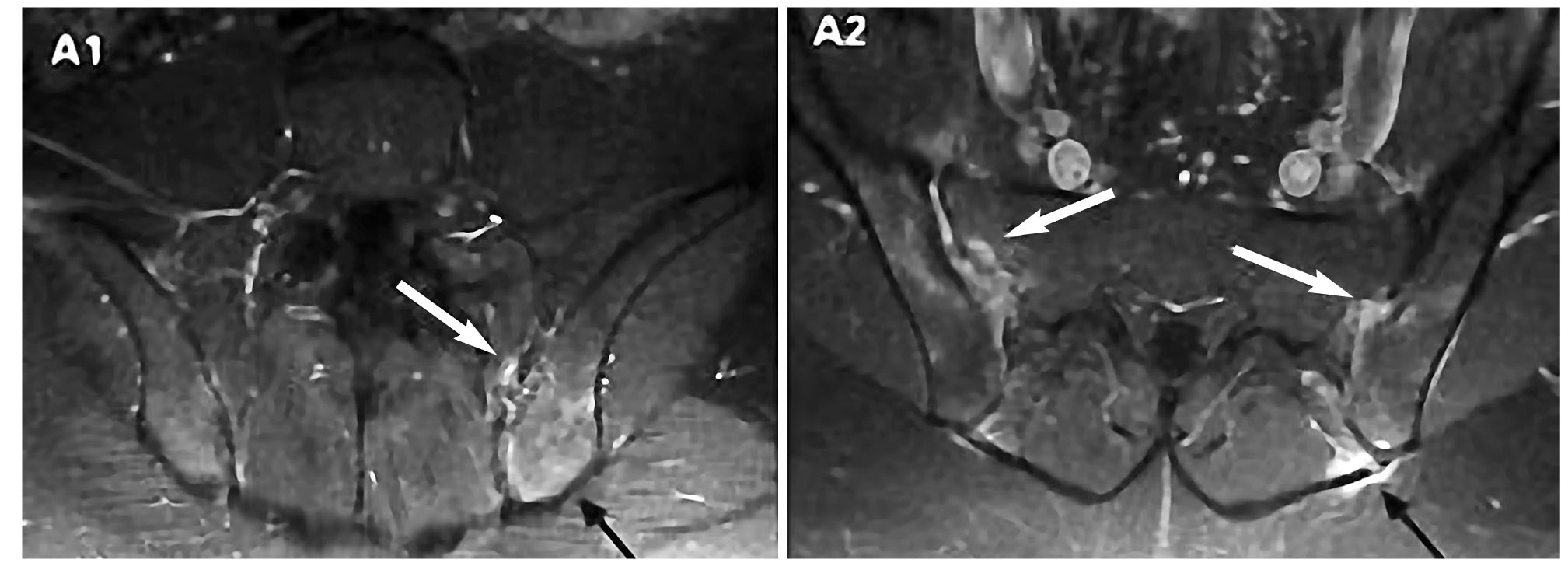 Рис. 4. Энтезит межостистых связок (белые стрелки) в режиме Т1 FS постконтраст + остеит подвздошной кости слева (черные стрелки). А1 – корональный срез, А2 – аксиальный срез
Рис. 4. Энтезит межостистых связок (белые стрелки) в режиме Т1 FS постконтраст + остеит подвздошной кости слева (черные стрелки). А1 – корональный срез, А2 – аксиальный срезЗа пределами КПС локализация энтезитов может быть различной: в связочном аппарате межпозвоночных дисков, сочленении рукоятки с телом грудины, области прикрепления связок к остистым отросткам позвонков, вертеле бедренной кости, надколенниках, ключице; пяточных костях.
Капсулит
Характеристики МР-сигнала при капсулите аналогичны показателям при синовите. Отличия в локализации. Изменения сосредоточены в области передней и задней части капсулы сустава. В передней части суставная капсула постепенно переходит в надкостницу подвздошной кости и крестца и соответствует энтезису. МР-сигнал при капсулите может распространяться медиально и латерально в область периоста (рис. 5).
Дифференциальная диагностика воспалительных
изменений
В основном дифференциальную диагностику воспалительных изменений необходимо осуществлять с инфекционными процессами и реактивными изменениями.
При проведении дифференциальной диагностики следует учитывать, что активные воспалительные изменения при СпА обычно ограничены анатомическими структурами КПС и не выходят за анатомические границы. При инфекционном сакроилиите основными отличиями являются преимущественная односторонность поражения и распространение гиперинтенсивного МР-сигнала вне анатомических границ сустава на область мягких тканей (рис. 6).
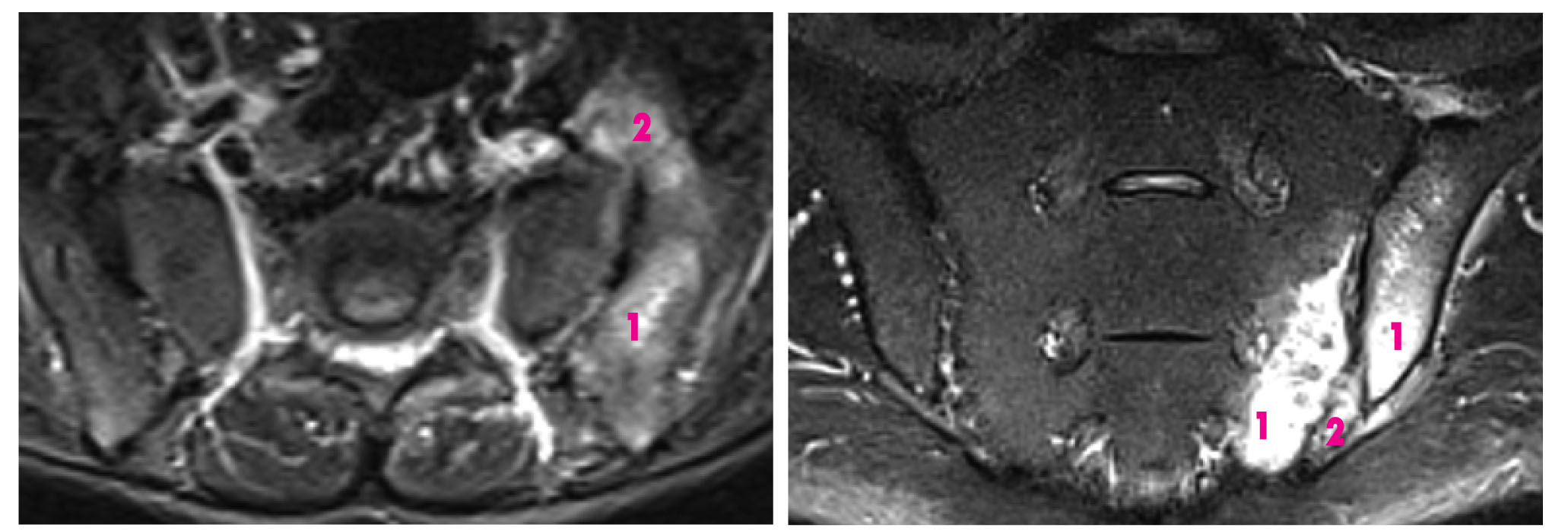 Рис. 6. Туберкулезный сакроилиит в режиме STIR (диагноз подтвержден интраоперационно). Поражение костей (1) и мягких тканей (2)
Рис. 6. Туберкулезный сакроилиит в режиме STIR (диагноз подтвержден интраоперационно). Поражение костей (1) и мягких тканей (2)В случае переломов костей таза или при опухолевых процессах (например, при остеосаркоме) может возникать реактивный сакроилиит (рис. 7).
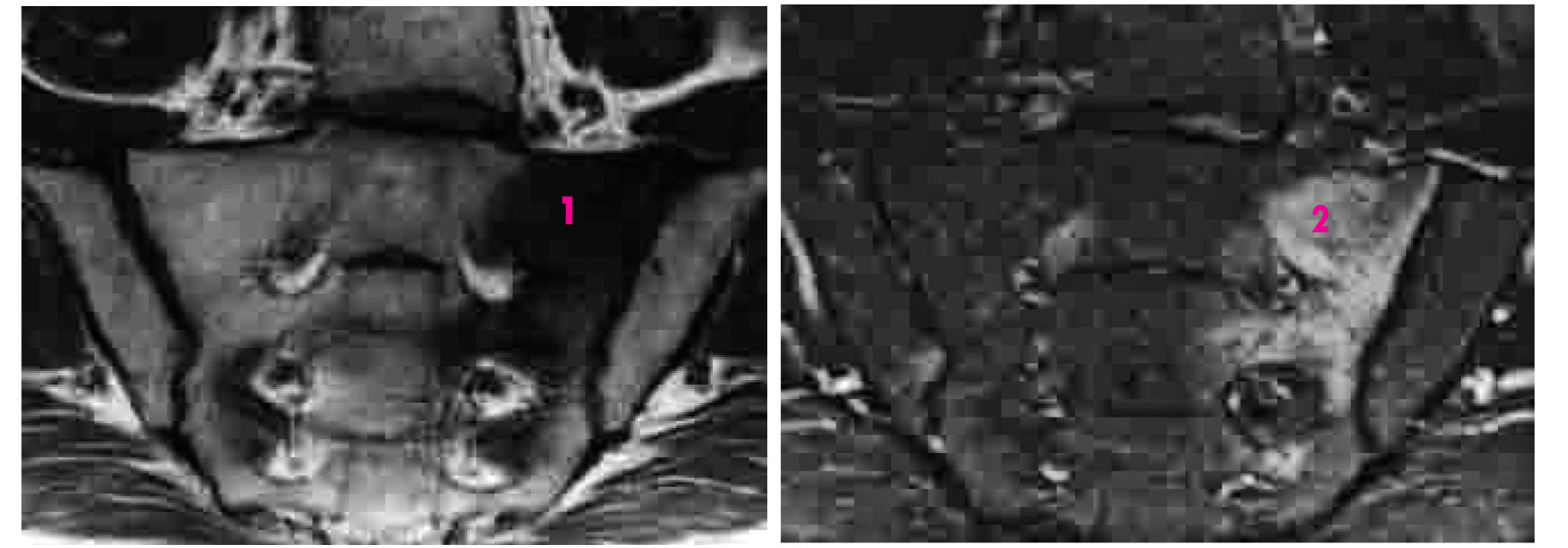 Рис. 7. Остеопоротический перелом крестца. Реактивный сакроилиит в режиме Т1 (1 – темный сигнал) и STIR (2 – светлый сигнал)
Рис. 7. Остеопоротический перелом крестца. Реактивный сакроилиит в режиме Т1 (1 – темный сигнал) и STIR (2 – светлый сигнал)При остеоартрозе КПС у пожилых пациентов иногда могут определяться небольшие очаги ОКМ слабой интенсивности вдоль суставной щели.
Ошибки при анализе МР-изображений
Связки, окруженные сосудами, могут быть ошибочно интерпретированы как воспаленные. В некоторых случаях могут возникать артефакты, так называемый «эффект катушки», когда сигнал от нормальных структур может быть гиперинтенсивным. При использовании семикорональной проекции «эффект катушки» чаще наблюдается в нижней части крестца и иногда подвздошной кости. Также он распространяется на мягкие ткани.
Структурные изменения
В целом все структурные изменения не являются специфическими при СпА, они указывают на очаги предшествующего воспаления.
Субхондральный склероз
Область склероза визуализируется как область низкоинтенсивного или изоинтенсивного сигнала при использовании всех режимов (Т1, STIR, Т1-постконтраст). Интенсивность сигнала не изменяется после введения КА. Субхондральный склероз, являющийся атрибутом СпА, должен распространяться, как минимум, на 5 мм вглубь от суставной щели (рис. 8). Небольшие области периартикулярного склероза могут наблюдаться и у здоровых пациентов (физиологический склероз).
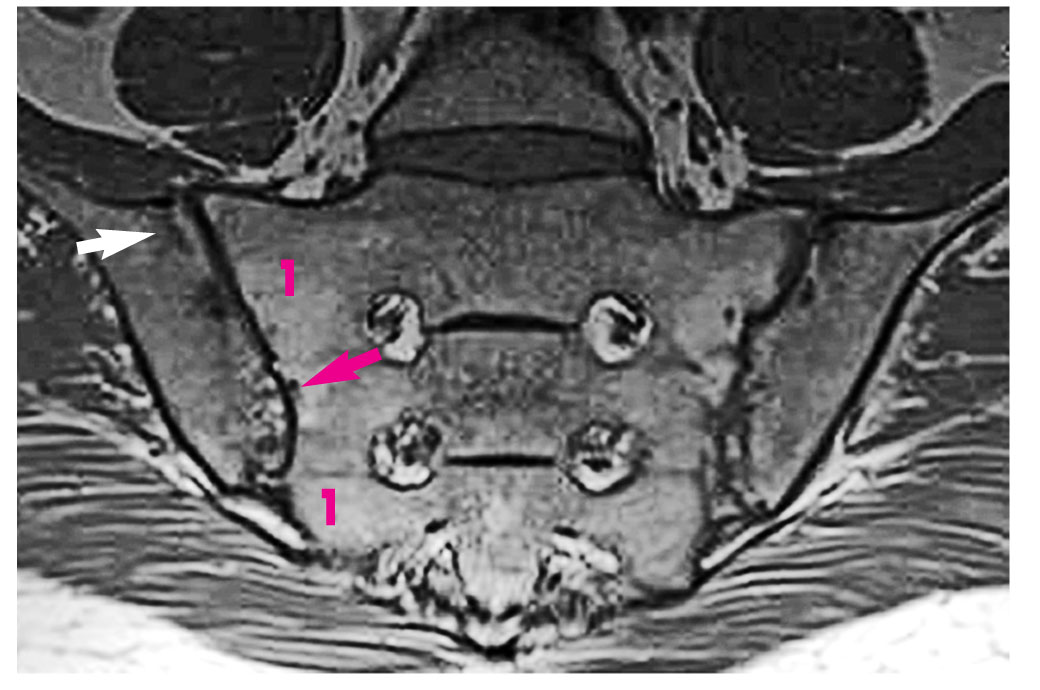 Рис. 8. В режиме Т1 жировая инфильтрация (1 – светлый сигнал), эрозия (красная стрелка – темный сигнал) и субхондральный склероз (белая стрелка) у пациента с АС продолжительностью 10 лет
Рис. 8. В режиме Т1 жировая инфильтрация (1 – светлый сигнал), эрозия (красная стрелка – темный сигнал) и субхондральный склероз (белая стрелка) у пациента с АС продолжительностью 10 летЖировая инфильтрация
Отложения жировой ткани характеризуются повышением интенсивности МР-сигнала (светлый сигнал) в режиме Т1 (рис. 8). Жировые отложения образуются в результате этерификации жирных кислот в очаге воспаления. Это неспецифичный симптом, указывающий на очаги предшествующего воспаления.
Эрозии
Эрозией называется любой краевой дефект кости. Эрозии могут наблюдаться и в хрящевой части. Первично возникают как единичные изменения. При слиянии эрозий может отмечаться «псевдорасширение» суставной щели. МР-признак эрозий: низкоинтенсивный (темный) сигнал в режиме Т1 ВИ и высокоинтенсивный – в режиме STIR, если есть активный воспалительный процесс (рис. 8). Режимы Т2 GE и Т1 FS могут быть более информативными для идентификации эрозий.
Костный анкилоз
Костные мостики или анкилоз выглядят как зона низкоинтенсивного сигнала во всех МР-режимах, иногда окруженная областью высокоинтенсивного сигнала в режиме Т1 (вследствие жировой инфильтрации костного мозга) (рис. 9).
Костные выросты, расположенные друг напротив друга в просвете суставной щели, могут консолидироваться, образуя костные мостики. При наличии нескольких близко расположенных костных мостиков нарушается четкость контура суставной щели.
Заключение
При МРТ КПС наиболее информативным в диагностике сакроилиита является использование режима Т1 ВИ c или без контрастирования и режима STIR. Наличие ОКМ в типичных анатомических областях (субхондрально или периартикулярно) при использовании режима STIR или остеита в режиме Т1 постконтраст достаточно для постановки диагноза сакроилиита. Для диагностики сакроилиита в режиме STIR достаточно нескольких областей гиперинтенсивного сигнала на одном срезе или одной области гиперинтенсивного сигнала на двух и более последовательных срезах (рис. 10).
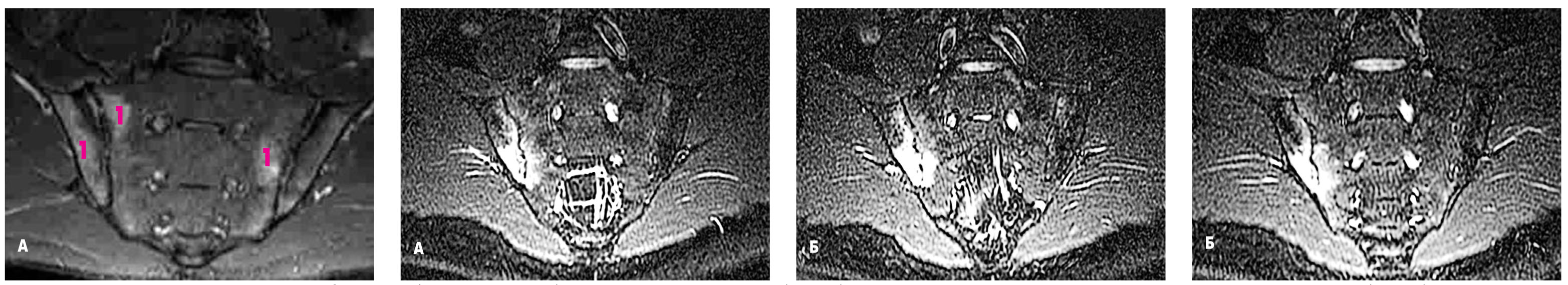 Рис. 10. Множественные области ОКМ (светлый сигнал – 1) в режиме STIR на одном срезе (часть А) и односторонняя локализация изменений на последовательных срезах (часть Б)
Рис. 10. Множественные области ОКМ (светлый сигнал – 1) в режиме STIR на одном срезе (часть А) и односторонняя локализация изменений на последовательных срезах (часть Б)Присутствия других воспалительных изменений (энтезита, синовита, капсулита) без наличия ОКМ не достаточно для постановки диагноза сакроилиит. Для диагностики энтезита, синовита, капсулита более информативно использовать режим Т1 с подавлением жира и обязательным введением контрастного агента. Структурные изменения являются следствием предшествующего воспаления.
СТАТТІ ЗА ТЕМОЮ Ревматологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....
Зв’язок між рівнем сироваткової сечової кислоти (ССК) і ризиком серцево-судинних захворювань (ССЗ) упродовж багатьох років є предметом вивчення дослідників. Установлено, що рівень ССК – незалежний предиктор смерті від усіх причин і серцево-судинної смерті, зокрема від гострого коронарного синдрому, інсульту та серцевої недостатності (СН). Також опубліковано багато робіт про зв’язок між ССК і функцією нирок. Попри значну кількість публікацій, деякі моменти, а саме: яким є оптимальний поріг ССК для визначення ризику ССЗ, чи необхідна корекція значень ССК для функції нирок, чи є ССК ключовим патологічним елементом метаболічної дисрегуляції, потребують прояснення....