Особливості клінічного застосування посаконазолу та каспофунгіну: від теорії до практики
Практично щороку на фармакологічному ринку з’являються нові антифунгальні препарати, здатні подолати збудників опортуністичних інфекцій в осіб з ослабленим імунітетом. Сьогодні ця група лікарських засобів включає десятки препаратів. Здавалося б, не так давно клініцисти дізналися про такі інноваційні антимікотики, як каспофунгін, посаконазол, а нині вони вже мають об’ємне доказове досьє, що підтверджує їхню ефективність у лікуванні різних форм грибкових інфекцій у ВІЛ-інфікованих осіб. Розглянемо докладніше базу ефективності цих препаратів, а також їхнє місце в авторитетних зарубіжних рекомендаціях із лікування опортуністичних інфекцій в осіб із ВІЛ.
Посаконазол: ключові теоретичні відомості
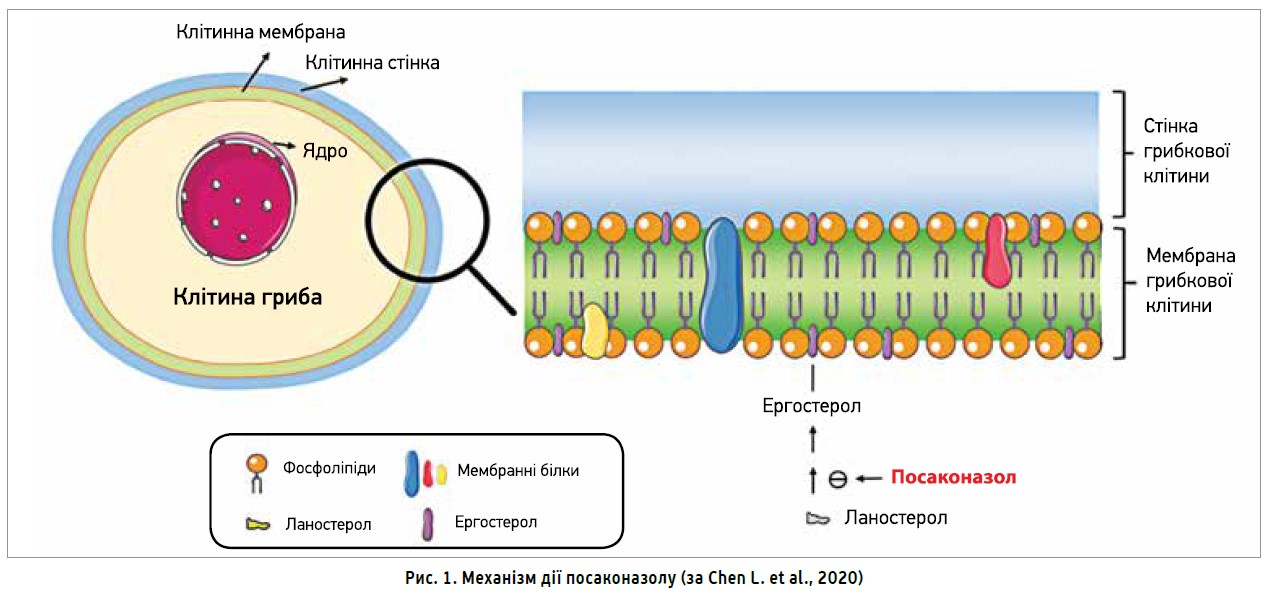
Серед нових похідних азолу найпопулярнішим є посаконазол – системний протигрибковий препарат, який інгібує фермент ланостерол 14α-деметілазу (рис. 1), що каталізує біосинтез ергостеролу (основного компонента клітинної стінки грибів). Посаконазол має широкий спектр антимікотичної активності щодо дріжджових і пліснявих грибів (Chen L. et al., 2020).
Висока активність посаконазолу щодо штамів Candida й Aspergillus зумовлює можливість його застосування не тільки з метою первинного лікування/профілактики інвазивних грибкових інфекцій (ІГІ), а також за умов інфікування патогенами, стійкими до дії інших антимікотиків. Саме ця особливість надала змогу А. Schauwvlieghe та співавт. (2020) успішно використовувати високі дози посаконазолу в лікуванні вориконазол-резистентного аспергільозу.
Серед інших переваг слід підкреслити хорошу переносимість цього азольного антимікотика, низьку ймовірність розвитку гепатотоксичного та кардіотоксичного ефекту (Chen L. et al., 2020). Згідно з чинними рекомендаціями, посаконазол не може бути призначений дітям віком менш ніж 13 років. Однак деякі дослідники вважають, що аналіз клінічних, фармакокінетичних особливостей дії цього препарату дасть змогу розширити вікові межі застосування посаконазолу та рекомендувати його дітям віком від 5 міс (Boonsathorn S. et al., 2018).
Доказова база посаконазолу
Дані рандомізованих клінічних досліджень (РКД)
Серед серії РКД, присвячених вивченню ефективності посаконазолу, слід виокремити Posifi. У рамках цього випробування J. Fortun і співавт. (2019) використовували посаконазол як терапію порятунку (97% випадків) із метою лікування аспергільозу (68,6%) та інших захворювань, зумовлених пліснявими та дріжджовими грибами (10,5%). Середня тривалість терапії зазначеним азольним антимікотиком становила 75 днів. За цей час удалося досягти клінічної відповіді в лікуванні аспергільозу через 3 та 12 міс лікування в 47,8% і 41,3% випадків відповідно, в терапії зигомікозу – в 55,5% в обох випадках, при мікозах іншої етіології – в 69,2% в обох випадках. Дослідники констатували, що пероральна терапія посаконазолом є ефективним методом лікування ІГІ в пацієнтів, які не відповіли на призначення інших антимікотиків / не переносять прийом інших протифунгальних засобів.
В інших роботах, де порівнюють результативність різних антимікотиків, підкреслюється перевага посаконазолу над ітраконазолом, флуконазолом у лікуванні мікозів. Останнім часом зазначений перелік перемог цього похідного азолу поповнився ще одним досягненням: L. Tang і співавт. (2018) констатували кращу переносимість посаконазолу порівняно з вориконазолом в онкогематологічних хворих. Схожі дані отримали К. Phillips і співавт. (2019), які зафіксували частіше виникнення побічних дій у групі вориконазолу на відміну від групи посаконазолу.
В унісон із вищенаведеними результатами звучать дані, отримані L. Le Clech і співавт. (2020): профілактичне призначення посаконазолу в поєднанні з використанням НЕРА‑фільтрів при будівництві гематологічних відділень асоційоване зі зниженням захворюваності на інвазивний аспергільоз (ІА) пацієнтів із гострою мієлоїдною лейкемією, котрі перебували на лікуванні в таких відділеннях.
A. Vazquez і співавт. провели багатоцентрове рандомізоване дослідження, в якому порівняли ефективність посаконазолу та флуконазолу в лікуванні кандидозу ротоглотки в пацієнтів із ВІЛ/СНІД. Ефективність 13-денного курсу лікування виявилася зіставною: клінічного успіху досягли понад 90% пацієнтів в обох групах, а мікологічного успіху (ерадикація збудника) – 68% пацієнтів в обох групах. Однак до 42-го дня значно більша кількість пацієнтів групи посаконазолу зберегла мікологічний успіх (40,6% проти 26,4% відповідно; р=0,038). Частота клінічного рецидиву захворювання становила 31,5% проти 38,2% у групах посаконазолу та флуконазолу відповідно. Отже, посаконазол виявився ефективнішим у підтриманні клінічного успіху після припинення лікування.
Результати систематичних оглядів і метааналізів
Посаконазол став основним діючим компонентом низки систематичних оглядів і метааналізів. В одній із таких робіт, заснованій на вивченні результатів 54 РКД, посаконазол названо найефективнішим антимікотиком для проведення первинної антифунгальної профілактики (Lee С. et al., 2018). Цей висновок зроблено на підставі здатності посаконазолу зменшувати ймовірність розвитку ІГІ (відносний ризик (ВР) 0,19; 95% довірчий інтервал (ДІ) 0,11-0,36). С. Lee та співавт. (2018) довели ефективність посаконазолу у профілактиці ІА (ВР 0,13; 95% ДІ 0,03-0,65) та доведеної грибкової інфекції (ВР 0,14; 95% ДІ 0,05-0,38).
На думку авторів метааналізу 28 досліджень (n=1930), підтримання оптимальної концентрації посаконазолу в крові (0,5 мг/л) удвічі частіше дає змогу досягти позитивних результатів у лікуванні ІГІ порівняно з низькими дозами цього препарату, а також зменшити добову дозу посаконазолу та запобігти таким чином появі дозозалежних побічних дій (Chen L. et al., 2018).
Згідно з результатами метааналізу 5 РКД (n=1617), профілактичне призначення посаконазолу дорослим імуноскомпрометованим пацієнтам асоційоване з мінімальним ризиком розвитку ІГІ (ВР 0,43; 95% ДІ 0,28-0,66; р=0,0001) порівняно з іншими антимікотиками (Wong Т. et al., 2020). Превентивний прийом посаконазолу супроводжується значним зниженням ризику розвитку ІА, інвазивного кандидозу (ІК), зменшенням частоти клінічної невдачі та небажаних подій. Автори підтвердили перевагу посаконазолу над флуконазолом у профілактиці ІГІ (ВР 0,44; 95% ДІ 0,28-0,70; р=0,0004) в онкогематологічних хворих (Wong Т. et al., 2020).
Доведено, що призначення посаконазолу хворим, які перенесли алогенну трансплантацію стовбурових клітин / солідних органів, дає змогу зменшити дозу імуносупресантів: сиролімусу/такролімусу на 60-70%, циклоспорину – на 30-40% (Fu С. et al., 2018).
Положення міжнародних практичних настанов
Вищенаведена доказова база стала підставою для включення посаконазолу в міжнародні рекомендації з лікування опортуністичних інфекцій у пацієнтів із ВІЛ.
Рекомендації з лікування опортуністичних інфекцій в осіб із ВІЛ – 2019 (British HIV Association / British Infection Association guidelines on the management of opportunistic infection in people living with HIV)
Лікування флуконазол-резистентного кандидозу ротоглотки чи стравоходу
Препаратом першої лінії в лікуванні кандидозу ротоглотки чи стравоходу є флуконазол. Якщо симптоматичну відповідь не вдається отримати, рекомендується після консультації з інфекціоністом призначити один із трьох препаратів резерву – посаконазол, ітраконазол або вориконазол.
Посаконазол продемонстрував ефективність у лікуванні резистентного до флуконазолу/ітраконазолу кандидозу ротоглотки та стравоходу. Із цією метою посаконазол рекомендують призначати у вигляді пероральної суспензії в дозі 400 мг 2 р/добу в перший день лікування з подальшим переходом на дозу 400 мг 1 р/день.
У разі резистентності до азолів, їх непереносимості чи гепатотоксичності можна застосувати препарат для внутрішньовенного введення, що не належить до групи азолів. Це може бути каспофунгін, мікафунгін й анідулафунгін або внутрішньовенний ліпосомний амфотерицин В.
Рекомендації з профілактики та лікування опортуністичних інфекцій у дорослих і підлітків із ВІЛ – 2020 (Centers for Disease Control and Prevention, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America)
Орофарингеальний кандидоз
Пероральна суспензія посаконазолу є такою самою ефективною, як і флуконазол. Проте посаконазол ефективніший за флуконазол у підтриманні клінічного успіху після припинення протигрибкової терапії. Посаконазол краще переноситься порівняно з розчином ітраконазолу. Капсули ітраконазолу менш ефективні, ніж флуконазол, у зв’язку з високою варіабельністю всмоктування та більшою кількістю взаємодій з іншими лікарськими засобами.
Посаконазол рекомендують призначати в разі неефективного протигрибкового лікування кандидозу ротоглотки чи стравоходу, якщо ознаки/симптоми захворювання зберігаються через 7-14 днів протигрибкової терапії. Резистентний кандидоз частіше трапляється в пацієнтів, які раніше отримали кілька курсів азольних протигрибкових препаратів.
Посаконазол показаний для лікування орофарингеального кандидозу як терапія першої лінії в дорослих пацієнтів зі зниженим імунітетом, із можливою низькою ефективністю препаратів місцевої дії.
Пероральна суспензія посаконазолу (400 мг 2 р/добу протягом 28 днів) є ефективною в 75% пацієнтів із резистентним до інших азолів кандидозом ротоглотки чи стравоходу.
Кокцидіоїдомікоз
Кокцидіоїдомікоз є грибковою інфекцією, котру зумовлюють ендемічні штами гриба Coccidioides. Більшість випадків цього захворювання припадає на ВІЛ‑інфікованих осіб.
Для пацієнтів, які мають клінічно легкий перебіг інфекції (вогнищева пневмонія), рекомендується початкова терапія триазольним протигрибковим засобом для перорального застосування. Зазвичай це флуконазол або ітраконазол. Пацієнтам, які не реагують на терапію тим чи іншим препаратом, можна призначити посаконазол або вориконазол. Слід ураховувати, що посаконазол характеризується меншою взаємодією з препаратами для антиретровірусної терапії, ніж вориконазол.
Пацієнтам із дифузним ураженням легень як стартову терапію слід призначати амфотерицин В. Терапію амфотерицином В необхідно продовжувати доти, доки не спостерігатиметься клінічне поліпшення, після чого пацієнта переводять на лікування флуконазолом. У разі резистентності до останнього можна призначити посаконазол.
Згідно з висновками представників різних авторитетних міжнародних товариств, сформульованими під час Європейської конференції з інфекцій при лейкемії, посаконазол є препаратом вибору для проведення антифунгальної профілактики в дорослих гематологічних хворих (Maerten J. et al., 2018).
Представники Європейського товариства клінічної мікробіології та інфекційних захворювань, Європейської конфедерації медичної мікології, Європейського респіраторного товариства опублікували спільні настанови з лікування аспергільозу (Ullmann А. et al., 2018). Положення цього погоджувального документа містять наполегливі рекомендації щодо застосування посаконазолу як засобу первинної профілактики мікозів у хворих на гостру мієлогенну лейкемію / мієлодиспластичний синдром при проведенні хіміотерапії. Експерти вищезазначених товариств припускають прийом цього препарату для проведення вторинної профілактики в гематологічних хворих із групи високого ризику.
Також посаконазол призначають для профілактики грибкових інфекцій реципієнтам трансплантатів кровотворних стовбурових клітин, які отримують високі дози імунодепресантів для запобігання реакції «трансплантат проти хазяїна» та в яких високий ризик розвитку інвазивних грибкових інфекцій.
Експерти Американського товариства інфекціоністів (2020) рекомендують використовувати пероральну суспензію посаконазолу для лікування орофарингеального кандидозу в підлітків/дорослих, хворих на ВІЛ. Представники цієї організації радять призначати посаконазол (400 мг 2 р/добу протягом 28 днів) при азолорефрактерному кокцидіоїдомікозі.
Каспофунгін: теоретичні дані
Каспофунгін є одним із найвідоміших ехінокандинів, протигрибкових препаратів, які пригнічують синтез клітинної стінки гриба за рахунок неконкурентного інгібування низки ферментних систем Candida. Встановлено, що каспофунгін сприяє некрозу й апоптозу Candida glabrata (Aryamloo Р. et al., 2019); цей препарат активний щодо Aspergillus fumigatus (Vargas-Muñiz J. et al., 2017).
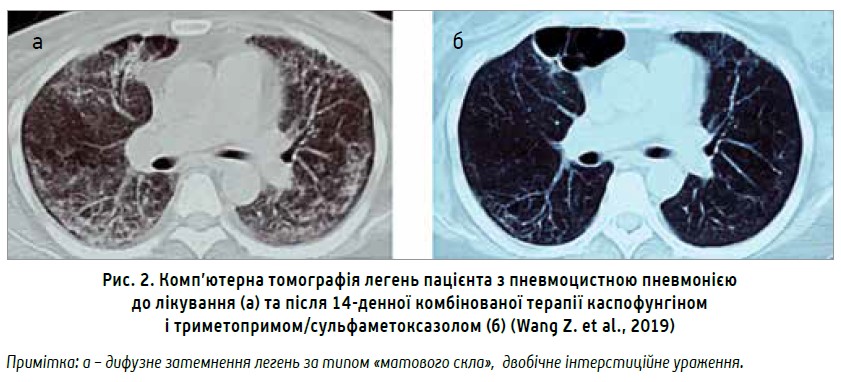
Нещодавно було опубліковано дані, що підтверджують ефективність каспофунгіну в лікуванні пневмоцистної пневмонії; їх отримано під час невеликого ретроспективного дослідження, в якому взяли участь хворі на системний червоний вовчак і пневмоцистну пневмонію, зумовлену P. jiroveci. Усі пацієнти приймали каспофунгін у комбінації з триметопримом/сульфаметоксазолом на тлі терапії глюкокортикоїдами й імуносупресантом. Незважаючи на те що 88,9% пацієнтів мали супутню патологію нирок, дослідники не зафіксували жодного летального випадку: перебіг пневмонії завершився повним одужанням усіх хворих (рис. 2). Отримані результати потребують проведення додаткових РКД і, в разі підтвердження, перегляду та внесення відповідних змін до практичних настанов лікування пневмоцистної пневмонії.
До переваг каспофунгіну належить і хороша переносимість; він може призначатися дітям раннього віку, підліткам, дорослим, літнім хворим.
Зростання експозиції каспофунгіну спостерігалося в дорослих пацієнтів із порушеннями функції печінки легкого ступеня тяжкості, в жінок і в пацієнтів літнього віку. При порушенні функції печінки легкого ступеня зазвичай зростання експозиції було помірним і не таким вираженим, щоб виникала необхідність у корегуванні дози препарату. Для дорослих пацієнтів із порушенням функції печінки помірного ступеня тяжкості чи для пацієнтів із більшою масою тіла може бути необхідним корегування дози препарату.
При порушенні функції нирок помірного ступеня тяжкості (кліренс креатиніну – від 31 до 49 мл/хв), прогресивному порушенні (кліренс креатиніну – від 5 до 30 мл/хв) і в термінальній стадії (кліренс креатиніну <10 мл/хв і проведення діалізу) концентрації каспофунгіну в плазмі крові помірно зростали після застосування разової дози (AUC – у діапазоні від 30 до 49%). Однак у пацієнтів з ІК, кандидозом стравоходу або ІА, яким уводили багатократно Кансидаз® у дозах 50 мг/добу, не спостерігали значущого впливу на концентрації каспофунгіну при легких і прогресивних порушеннях функції нирок. Отже, немає необхідності в корегуванні дози пацієнтам із порушеннями функції нирок. Каспофунгін не виводиться при проведенні діалізу, тому немає потреби в уведенні додаткових доз після гемодіалізу.
Доказова база каспофунгіну
У рамках нещодавно завершеного багатоцентрового РКД каспофунгін призначали дітям (від 3 міс), підліткам і дорослим віком до 30 років з уперше виявленою, рецидивною чи вторинною гострою мієлоїдною лейкемією, котрі мали високий ризик розвитку життєзагрозливої грибкової інфекції, спричиненої дріжджовими та пліснявими грибами (Fisher В. et al., 2019). Пацієнтів рандомізували для прийому каспофунгіну (n=257) чи флуконазолу (n=260). Серед 517 учасників, які пройшли рандомізацію, дослідження завершили 508 осіб. Протягом 5 міс зафіксували 23 доведені/ймовірні випадки ІГІ, з яких у групі каспофунгіну – 6, флуконазолу – 17 (виділено 14 видів цвілевих грибів, 7 видів дріжджових і 2 види грибів не ідентифіковано). Сумарний показник захворюваності доведеним/імовірним грибковим захворюванням при 5-місячному прийомі каспофунгіну становив 3,1% (95% ДІ 1,3-7,0%), при використанні флуконазолу – 7,2% (95% ДІ 4,4-11,8%; достовірні міжгрупові відмінності: р=0,03). Кумулятивна захворюваність доведеним/імовірним ІА в групі флуконазолу (3,1%; 95% ДІ 1,4-6,9%) достовірно (р=0,046) перевищувала таку в групі каспофунгіну (0,5%; 95% ДІ 0,1-3,5%). Ефективність емпіричної протигрибкової терапії каспофунгіном дещо перевищувала таку при застосуванні флуконазолу. Дослідники підкреслили хорошу переносимість каспофунгіну.
Автори іншого РКД (ACTIVE trial) не змогли довести порівняної ефективності ізавуконазолу з ехінокандином у лікуванні кандидемії або інших ІГІ: каспофунгін упевнено перевершив препарат порівняння (Kullberg В. et al., 2019). Сумарна ефективність терапії каспофунгіном після закінчення періоду внутрішньовенного введення становила 71,1%, ізавуконазолом – 60,3% (міжгрупові відмінності: 10,8; 95% ДІ 19,9-1,8) (Kullberg В. et al., 2019).
J. Osei Sekyere та співавт. (2018) зафіксували мінімальну стійкість Candida auris до каспофунгіну (3,48%), тоді як несприйнятливість цього патогену до флуконазолу (44,29%), амфотерицину В (15,46%), вориконазолу (12,67%) достовірно перевищувала таку каспофунгіну.
Думаємо: посаконазол і каспофунгін, говоримо: Ноксафіл®* і Кансидаз®**
Пошук на вітчизняному фармакологічному ринку торгових назв препаратів, які містять посаконазол і каспофунгін, не буде надзвичайно тривалим. Нині на ринку України зареєстровані та доступні лише оригінальні лікарські засоби із зазначеними діючими речовинами – Ноксафіл® і Кансидаз® (пошук здійснювався на сайті http://www.drlz.com.ua станом на 21.10.2020). Обидва препарати представляють виробники – Schering-Plough і Merck Sharp & Dohme B. V.
Ноксафіл® являє собою пероральну суспензію, котра містить мікронізований посаконазол (40 мг/мл). Цей препарат успішно застосовують для лікування ІА, хромобластомікозу та міцетоми, фузаріозу, кокцидіоїдомікозу, а також орофарингеального кандидозу. Ноксафіл® також призначають із метою профілактики ІГІ в пацієнтів, які отримують хіміотерапію для індукції ремісії при лікуванні гострого мієлогенного лейкозу чи мієлодиспластичного синдрому, що може спричинити тривалу нейтропенію, та в яких високий ризик розвитку інвазивних грибкових інфекцій; а також у реципієнтів трансплантатів кровотворних стовбурових клітин, які отримують високі дози імунодепресантів для запобігання реакції «трансплантат проти хазяїна» та в яких високий ризик розвитку інвазивних грибкових інфекцій. Звичайна разова доза препарату Ноксафіл® становить 200 мг (5 мл), але, залежно від типу захворювання, кратність прийому може змінюватися від 1 до 4 р/добу, тривалість терапії також залежить від клінічної ситуації та передбачає прийом препарату протягом 14 діб або декількох місяців. Клініцисти вже мають значний досвід застосування препарату Ноксафіл®: Н. Н. Климко (2008), І. С. Долгополов (2010) констатують його значну ефективність, а І. С. Крисанов (2019), окрім високої результативності, підтверджує економічну обґрунтованість призначення препарату.
Кансидаз® призначений для парентерального введення, його флакони містять 50 мг каспофунгіну. Кансидаз® добре зарекомендував себе в лікуванні ІК, ІА, за підозри на ІГІ за умови фебрильної нейтропенії. Схеми призначення Кансидазу також значно варіюють залежно від клінічної ситуації: зазвичай уводиться навантажувальна доза (70 мг/добу), котра змінюється на терапевтичну (50 мг/добу). Лікування Кансидазом триває щонайменше 14 діб і може бути продовжено ще протягом 7-14 діб після отримання останнього позитивного культурального аналізу. Ефективність терапії цим препаратом демонструють роботи Н. Н. Климко (2006), А. С. Колбіна (2008) та ін.
Отже, теоретичні знання та практичні результати свідчать про високу ефективність посаконазолу (Ноксафіл®) і каспофунгіну (Кансидаз®) у лікуванні/профілактиці різноманітних ІГІ.
Список літератури знаходиться в редакції.
1. Інструкція для медичного застосування лікарського засобу КАНСИДАЗ® (РП UA/2841/01/01, РП UA/2841/01/02).
2. Інструкція для медичного застосування лікарського засобу НОКСАФІЛ® (РП UA/9269/01/01).
* Зареєстрована торгова марка Merck Sharp & Dohme Corp.
** Зареєстрована торгова марка «МСД Інтернешенал Холдінгс ГмбХ».
Медична газета «Здоров’я України 21 сторіччя» № 18 (487), 2020 р.
СТАТТІ ЗА ТЕМОЮ Інфекційні захворювання
Світ не бачив нового класу диво-ліків уже 40 років...
Рекомендації щодо антибіотиків першого і другого вибору для емпіричної терапії негоспітальної пневмонії, середнього отиту та загострення ХОЗЛ...
SARS-CoV‑2 виявився непересічним респіраторним вірусом і спричинив пандемію, яка тривала із 2019 по 2023 рік. Проте вплив цієї інфекції на імунну систему (ІС) людини не обмежується активацією фізіологічних механізмів противірусного захисту. Вірус здатний надмірно активувати ІС, зумовлюючи загрозливе ускладнення – т. зв. цитокіновий шторм, спричинити тяжку вірусну пневмонію, розвиток автоімунного синдрому, впливати на систему коагуляції тощо....
Риносинусит (РС) є одним із найчастіших захворювань у первинній медичній практиці. Трьома найбільш чутливими й специфічними симптомами гострого РС є виділення з носа, закладеність носа, лицевий і головний біль. Неконтрольований гострий біль значно погіршує якість життя пацієнтів із РС: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування. Отже, полегшення болю при РС є найпершим завданням лікаря....