Застосування прокінетиків при гастроезофагеальній рефлюксній хворобі та порушеннях моторики травного тракту
Під час науково-практичної конференції з міжнародною участю «ХІІ Український гастроентерологічний тиждень», яка відбулася 24-25 вересня, значну увагу було приділено гастроезофагеальній рефлюксній хворобі (ГЕРХ) і розладам моторики шлунково-кишкового тракту (ШКТ).
 Начальник кафедри військової терапії Української військово-медичної академії Міністерства оборони України (м. Київ), доктор медичних наук, професор Галина Василівна Осьодло у своєму виступі охарактеризувала клініко-інструментальні паралелі в лікуванні та діагностиці ГЕРХ.
Начальник кафедри військової терапії Української військово-медичної академії Міністерства оборони України (м. Київ), доктор медичних наук, професор Галина Василівна Осьодло у своєму виступі охарактеризувала клініко-інструментальні паралелі в лікуванні та діагностиці ГЕРХ.
У ХХІ ст. ГЕРХ – одна з провідних гастроентерологічних хвороб. У власному дослідженні Галиною Василівною було виявлено вплив стресу як на частоту, так і на структуру ГЕРХ. Зокрема, серед учасників АТО переважає ерозивна форма ГЕРХ (94,2%). Іншим чинником, який спричиняє збільшення ймовірності ерозивних форм ГЕРХ, є підвищення симпатикотонічної активності.
Відповідно до Монреальської класифікації (2005), прояви ГЕРХ розподіляють на стравохідні (симптоматичні синдроми, типовий рефлюксний синдром) і позастравохідні (кашель, рефлюкс-ларингіт, бронхіальна астма, ураження емалі зубів). При оцінці ГЕРХ не можна орієнтуватися виключно на ендоскопічну картину, адже необхідно також ураховувати анамнез, клінічні дані та результати додаткових досліджень. До останніх, зокрема, належать рН‑моніторинг і моніторинг рН‑імпедансу, що дають змогу визначити часовий зв’язок між епізодами рефлюксу та клінічними симптомами ГЕРХ (болем у грудях, кашлем). Це особливо важливо за наявності респіраторних масок ГЕРХ. Часове вікно, що використовується для аналізу асоціації «рефлюкс – симптом», становить 2 хв. Під індексом симптому розуміють відсоток симптомів, які з’явилися після епізодів рефлюксу.
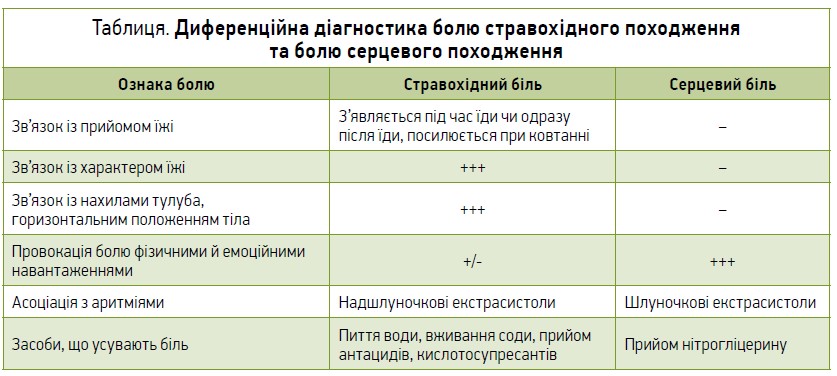
Нерідко спостерігаються й кардіальні маски ГЕРХ, при яких надзвичайно важливо відрізнити біль стравохідного походження від болю серцевого походження (табл.).
Лікування позастравохідних масок ГЕРХ нерідко має бути навіть тривалішим, аніж лікування ерозивної форми цієї хвороби. За власними дослідженнями, при кашлі, асоційованому з неерозивною рефлюксною хворобою (НЕРХ), рівень оксиду азоту в тромбоцитах перевищував контрольні показники в 4,6 раза. Своєю чергою, при кардіалгіях, асоційованих із НЕРХ, рівень оксиду азоту в нейтрофілах перевищував контрольні показники в 4,9 раза. Це може свідчити про більший вплив конститутивної NO‑синтази у хворих із респіраторними масками ГЕРХ та індуцибельної NO‑синтази – у хворих із кардіологічними масками цього захворювання.
Відповідно до рекомендацій Ліонського консенсусу, при діагностиці ГЕРХ, окрім ендоскопії, велике значення надається рН, рН‑імпедансу та манометрії нижнього стравохідного сфінктера.
Для характеризації ГЕРХ та асоційованого з нею езофагіту використовується Лос-Анджелеська класифікація (1999), яка передбачає поділ на ступінь А (один або більше дефектів слизової оболонки завдовжки не більш ніж 5 мм, що не поширюються між верхівками двох складок слизової оболонки); ступінь В (один або більше дефектів слизової оболонки завдовжки >5 мм, які не поширюються між верхівками двох складок слизової оболонки); ступінь С (один або більше дефектів слизової оболонки, котрі поширюються між верхівками двох складок слизової оболонки, але уражають <75% обводу стравоходу); ступінь D (один або більше дефектів слизової оболонки з ураженням >75% обводу стравоходу). Ураження ступеня D підлягають обов’язковій біопсії та повторній оцінці через 6-8 тиж після прийому інгібіторів протонної помпи (ІПП) з метою виключення малігнізації та стравоходу Барретта. Відповідно до рекомендацій Європейського товариства гастроінтестинальної ендоскопії, при стравоході Барретта без дисплазії за розміру ураження («язика») ≥3 см повторну ендоскопію слід виконувати через 2-3 роки, а при ураженні розміром <3 см – через 3-5 років. Якщо стравохід Барретта в пацієнта характеризується низьким ступенем дисплазії, повторне ендоскопічне дослідження проводиться через 6 міс (бажано мати іншу експертну думку та морфологічне підтвердження діагнозу). При невизначеній дисплазії повторну ендоскопію також слід виконувати через 6 міс.
Основним методом лікування ГЕРХ є призначення ІПП. Тривалість кислотосупресивної терапії залежить від форми захворювання. Зокрема, при стравоході Барретта ІПП необхідно приймати практично постійно, оскільки вплив кислоти провокує непухлинні епітеліальні лінії Барретта продукувати активні форми кисню, здатні ушкоджувати ДНК. Якщо дисплазія відсутня, призначають стандартні дози ІПП, якщо ж наявна дисплазія будь-якого ступеня, – подвійні дози.
На жаль, для повноцінного лікування ГЕРХ не завжди достатньо кислотосупресивної терапії, тому (особливо за умов асоціації клінічних симптомів із біліарним рефлюксом) доцільне призначення прокінетиків.
Сьогодні дедалі частіше постає питання безпеки застосування прокінетичних засобів, адже досвід їх використання продемонстрував низку серйозних побічних ефектів із боку серцево-судинної системи (цизаприд, тегасерод, домперидон), екстрапірамідних розладів і гормональних порушень (метоклопрамід). Так, у декількох дослідженнях було зафіксовано домперидон-асоційоване подовження інтервалу QT у дітей. У разі призначення цих препаратів необхідно зіставляти їхню клінічну гастрокінетичну ефективність із несприятливим профілем безпеки й імовірністю розвитку медикаментозно-індукованих аритмій.
Перевага ітоприду (Ітомед®, «ПРО.МЕД.ЦС Прага», Чехія) насамперед у тому, що за умови призначення терапевтичних доз йому не властиві проаритмічна дія та подовження інтервалу QT (Kakiuchi et al., 1997). Окрім того, він не проходить крізь гематоенцефалічний бар’єр (Yamada et al., 1994). Ітоприд може бути безпечною та доступною альтернативою іншим прокінетичним середникам у зв’язку з відсутністю впливу на CYP3A4.
У дослідженні B. J. Chun і D. S. Lee (2013) додавання ітоприду (50 мг 3 р/добу) до ІПП протягом 12 тиж лікування зумовлювало достовірно більше зниження загального індексу симптомів рефлюксу та відчуття клубка в горлі порівняно з групою монотерапії ІПП.
Випробування із застосуванням манометрії високої роздільної здатності показали, що ітоприд сприятливо впливає на перистальтику стравоходу й тиск у трьох сегментах стравоходу та нижньому стравохідному сфінктері, що може бути сприятливим для лікування ГЕРХ (Koshino et al., 2011).
Ітомед® – європейський препарат ітоприду, котрий працює на всій протяжності ШКТ, що особливо важливо при дуоденогастроезофагеальному рефлюксі. Причинами останнього можуть бути функціональні й органічні захворювання жовчного міхура (хронічний холецистит, жовчнокам’яна хвороба), операції на жовчному міхурі, стани після оперативних втручань на шлунку (резекція шлунка, гастректомія, формування обхідного шлункового анастомозу з метою схуднення), пептичні виразки та їх наслідки (пілороспазм, пілоростеноз). Показано, що асоціація кислотного та біліарного рефлюксу особливо небезпечна, оскільки в такому випадку до патологічного процесу включаються такі додаткові складники рефлюктату, як жовчні кислоти, лізолецитин і трипсин. Доведено зв’язок рефлюксу жовчі з розвитком стравоходу Барретта та раку стравоходу.
Лікар-гастроентеролог, сертифікований консультант із питань харчування, професор Дорота Васько-Чопник (Клініка гастроентерології та гепатології, м. Вроцлав, Польща) присвятила свою доповідь застосуванню прокінетиків при розладах моторики ШКТ, докладно зупинившись на ефективності та безпеці ітоприду.
При функціональних розладах травної системи широко застосовуються різноманітні прокінетики та спазмолітики. Серед найчастіше призначуваних препаратів – ітоприд (показання: функціональна диспепсія, ГЕРХ, порушене випорожнення шлунка, гастропарез, дисфагія, порушення моторики стравоходу, закрепи), альверин (показання: синдром подразненого кишечнику, спастичні розлади роботи жовчних протоків, дискінезія жовчних протоків і жовчного міхура, закрепи, здуття живота, синдром надмірного бактерійного росту), мебеверин (показання: синдром подразненого кишечнику з діареєю та змішаного типу, здуття живота), тримебутин (показання: синдром подразненого кишечнику із закрепом, ГЕРХ, функціональна диспепсія, здуття живота, синдром надмірного бактерійного росту), гіосцин (скополамін) + метамізол (показання: функціональний біль у животі, ГЕРХ, синдром подразненого кишечнику, функціональна диспепсія, розлади моторики стравоходу, некоронарогенний біль за грудиною), цизаприд, метоклопрамід (наразі у зв’язку з вираженими побічними ефектами застосовуються рідко).
Професор Васько-Чопник зауважила, що найчастіше до лікаря-гастроентеролога звертаються пацієнти з ГЕРХ, а також хворі з т. зв. синдромом перехресту – сполучення ГЕРХ і функціональної диспепсії чи синдрому подразненого кишечнику. Такі перехресні синдроми спостерігаються в >40% пацієнтів із ГЕРХ (Chang W. C. et al., 2018). За умови сполучення ГЕРХ з іншими патологічними станами перебіг обох хвороб погіршується, зростає кількість супутніх депресивних розладів і порушень сну. Немає сумнівів, що ГЕРХ і НЕРХ негативно впливають на якість життя, а саме на такі її домени, як фізичне, психічне й емоційне благополуччя, соціальне функціонування, відчуття болю.
До етіопатогенетичних чинників ГЕРХ належать порушений кліренс стравоходу (розлади моторики стравоходу та тіла шлунка), слабка нейтралізаційна здатність слини у зв’язку з низькою концентрацією бікарбонатів, знижена секреція бікарбонатів і слизу залозами стравоходу, ураження слизової оболонки стравоходу, порушення роботи кардіального відділу шлунка (дисфункція чи минущі розслаблення нижнього стравохідного сфінктера, дисфункція зовнішнього стравохідного сфінктера, кила стравохідного отвору діафрагми), особливості секрету шлунка (наявність гелікобактерної інфекції, активність пепсину) та наявність інших складових рефлюктату.
Ідеальна схема лікування ГЕРХ має впливати на весь спектр етіопатогенетичних факторів: зокрема, для покращення моторики стравоходу, шлунка та дванадцятипалої кишки доцільно призначати прокінетики, для зменшення виділення шлункової кислоти – ІПП і Н2-гістаміноблокатори, для захисту слизової оболонки стравоходу – альгінати тощо.
На жаль, деяким прокінетикам властивий тягар серйозних побічних ефектів. Наприклад, щодо метоклопраміду 2013 року було отримано застереження від Європейської служби фармакологічного нагляду, адже його недоліками є можливість використання тільки за показаннями (нудота, блювання), невелика максимальна тривалість лікування (5 днів), значна кількість побічних ефектів (галакторея внаслідок гіпертрофії та гіперплазії пролактинопродукувальних клітин гіпофіза, розлади менструального циклу, гінекомастія), великий перелік препаратів, з якими з’являється міжлікарська взаємодія (кетоконазол, кларитроміцин). Щодо ще одного відомого прокінетика (домперидон; не зареєстрований у Польщі) було отримано застереження від Європейської служби фармакологічного нагляду 2014 року через аритмогенну дію та здатність подовжувати інтервал QT. Домперидону властивий обмежений перелік показань до застосування (нудота та блювання); цей препарат не рекомендовано використовувати при ГЕРХ або диспепсії. Максимальна тривалість лікування домперидоном часто є недостатньою для повного вилікування, оскільки становить лише 7 днів. Свого часу великі надії покладалися на прокінетик цизаприд, який, як виявилося, впливає на водія ритму та є аритмогенним, у зв’язку з чим щодо нього було отримано перше застереження від Європейської агенції з оцінки лікарських засобів іще 2003 року.
Своєю чергою, ітоприд є представником нового покоління прокінетиків; йому властивий подвійний механізм дії: цей препарат блокує вивільнення дофаміну, водночас інгібуючи секрецію холінестерази, що дає змогу підтримувати достатній для адекватного функціонування непосмугованих м’язів травного тракту рівень ацетилхоліну. Показанням до застосування ітоприду є зняття симптоматики ГЕРХ і функціональної диспепсії (здуття, відчуття переповнення шлунка після їжі, біль в епігастрії, печія, нудота, блювання). Важливо, що препарат є безпечним; у нього відсутня будь-яка аритмогенна дія (Scarpellini E. et al., 2011), він не проходить крізь гематоенцефалічний бар’єр, тому не чинить жодного негативного впливу на центральну нервову систему. Максимальна концентрація ітоприду в крові досягається через 30 хв після застосування, тобто він працює дуже швидко (така висока швидкість дії дає змогу успішно застосовувати препарат у лікуванні «на вимогу»). Важливим також є те, що ітоприд метаболізується монооксигеназою, а не цитохромом Р450, оскільки внаслідок цього він не взаємодіє з іншими лікарськими засобами та може використовуватись як складова багатокомпонентної терапії. Ітоприд добре переноситься й не має серйозних побічних дій; рекомендований режим дозування передбачає застосування 50 мг 3 р/добу. На рівень всмоктування й ефективність дії не впливає рН шлунка та вживання їжі, тобто препарат не обов’язково застосовувати натщесерце. Зазначені характеристики вигідно відрізняють ітоприд від описаних вище інших прокінетиків.
Слід зауважити, що ітоприд не лише діє на кінетику верхньої частини ШКТ, а й регулює моторні функції нижніх відділів травної системи (за даними досліджень in vitro й in vivo); стимулює перистальтичну та сегментарну активність через викликання тиску на просвіт шлунка та скоротливу активність ШКТ від шлунка до товстого кишечнику. У зв’язку з таким стимулювальним впливом на товстий кишечник ітоприд може застосовуватися для лікування функціональних розладів нижніх відділів ШКТ (функціональний закреп, синдром подразненого кишечнику із закрепом, перехресний синдром ГЕРХ / функціональна диспепсія / синдром подразненого кишечнику). Первинні обсерваційні клінічні дослідження продемонстрували сприятливі ефекти ітоприду в лікуванні та профілактиці післяопіоїдних закрепів, але для підтвердження цих результатів необхідні масштабні рандомізовані контрольовані дослідження (Dzierzanowski et al., 2019).
Додавання ітоприду до ІПП при комплексному лікуванні ГЕРХ покращує ефективність останніх, пришвидшує усунення симптоматики ГЕРХ, зменшує кількість рецидивів. В одному з досліджень, присвячених цьому питанню, комбінація ІПП з ітопридом забезпечувала повне усунення ларингеальних симптомів ГЕРХ у 48% учасників, а сполучення ІПП із плацебо – лише у 20%. Рецидиви після лікування спостерігалися в 5% пацієнтів групи ІПП + ітоприд і у 24% хворих групи ІПП + плацебо. Схожі результати було отримано для різних ІПП (пантопразол, езомепразол, рабепразол, оанзопразол). Комбінація ітоприд + рабепразол ефективніше усувала симптоматику ГЕРХ і сприяла загоєнню виявлених ендоскопічно дефектів стравоходу, ніж комбінація домперидон + рабепразол. Загалом ітоприд покращує ефективність лікування ГЕРХ незалежно від призначеного ІПП.
У метааналізі Huang і співавт. (2012) було проаналізовано 10 рандомізованих контрольованих досліджень за участю 2620 пацієнтів. Порівняно з контрольною групою, в якій застосовувалися домперидон або плацебо, ітоприд помітніше зменшував вираженість переповнення шлунка після прийому їжі та відчуття раннього насичення.
Ітоприд також продемонстрував кращий ефект (аніж домперидон) у пацієнтів із невиразковою диспепсією. Через 2 тиж терапії полегшення симптомів до повного їх зникнення відзначалося у 81% учасників групи ітоприду та в 70% пацієнтів групи домперидону (p<0,05; Sawant et al., 2004).
У 2019 році Польська асоціація сімейної медицини видала рекомендації з лікування ГЕРХ для сімейних лікарів, відповідно до яких алгоритм лікування ГЕРХ передбачає застосування стандартних доз ІПП протягом 4-8 тиж, а в разі неуспішного стартового лікування – призначення подвійних доз ІПП або заміну ІПП на інший кислотознижувальний препарат у поєднанні з альгінатами та/або препаратами гіалуронової кислоти з хондроїтином, а також додавання прокінетиків (тривалість лікування – 8-12 тиж). За відсутності ефекту через 12 тиж необхідно скерувати пацієнта до вузького спеціаліста.
Загалом, щоби досягти терапевтичного ефекту при ГЕРХ, необхідно:
1) призначати адекватну кислотосупресію за допомогою ІПП;
2) за потреби додавати прокінетик, який впливатиме на розлади моторики травного тракту;
3) за неефективності вищезазначених способів додавати до лікування захисні та кислотонейтралізувальні засоби місцевої дії (Gasiorowska et al., 2019).
Професор Васько-Чопник підсумувала свій виступ такими висновками:
1) ітоприд – новітній безпечний та ефективний препарат;
2) показаннями до застосування ітоприду є ГЕРХ, функціональна диспепсія та різноманітні синдроми перехресту хвороб травної системи. Крім того, ітоприд має сприятливий вплив на моторику товстого кишечнику;
3) застосування ітоприду як складової частини комплексної терапії ГЕРХ дає змогу зменшити чи припинити використання інших лікарських засобів, що важливо для зниження медикаментозного навантаження під час пандемії коронавірусної хвороби;
4) ітоприд добре переноситься та не має серйозних побічних ефектів (насамперед аритмогенної дії);
5) у Польщі ітоприд представлено препаратом виробництва чеської компанії «ПРО.МЕД.ЦС Прага», який є і в Україні під торговою назвою Ітомед®.
На завершення доповідачка представила клінічний випадок із власної практики. Чоловік, 57 років, бізнесмен (робота пов’язана з частими стресами); страждає на метаболічний синдром, ішемічну хворобу серця, артеріальну гіпертензію, хворіє на ГЕРХ кілька років, протягом яких відчував біль за грудиною, але при обстеженні виявилося, що цей біль мав стравохідне, а не ішемічне походження. За допомогою фіброгастроскопії було виявлено езофагіт ступеня А за Лос-Анджелеською класифікацією, а також гелікобактер-негативний гастрит. Протягом кількох останніх тижнів хворий скаржився на непродуктивний виснажувальний кашель (переважно вночі), біль у горлі, слабкість, а також біль у загрудинній ділянці, не пов’язаний зі стресом, регургітацію, печію й печіння в горлі, незважаючи на прийом ІПП. Приймає всі призначені кардіологічні препарати; параметри артеріального тиску й електрокардіограми в нормі.
Що ж можна порекомендувати в цьому випадку? Насамперед потрібно заспокоїти пацієнта та запевнити його в необхідності продовження кардіологічного лікування (для виключення коронарогенної причини болю за грудиною може знадобитися консультація кардіолога). Крім того, доцільно збільшити дозу ІПП удвічі та додати до лікування прокінетик (наприклад, ітоприд дозою 50 мг 3 р/добу за 20 хв до прийому їжі), а також змінити спосіб життя й (особливо) харчування.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 22 (491), 2020 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...