Противоаллергические свойства пробиотиков: исследования необходимо продолжить

С.В. Зайков, д.м.н., профессор, А.Е. Богомолов, к.м.н., Винницкий национальный медицинский университет им. Н.И. Пирогова
В последние годы публикуется все больше исследований, посвященных роли микрофлоры в развитии аллергических заболеваний (АЗ), однако эффективность применения пробиотиков с целью профилактики и лечения аллергопатологии остается дискутабельной, поскольку полученные результаты довольно противоречивы, что, возможно, связано с различиями в составе микрофлоры пациентов разных возрастных групп и особенностями влияния различных пробиотических препаратов на иммунную систему. Например, у детей первых 3-6 мес жизни в кишечной микрофлоре преобладают бифидобактерии, а у взрослых доминирующей флорой в кишечнике являются лакто- и бифидобактерии, непатогенные штаммы кишечной палочки. При этом установлено, что виды бифидо- и лактофлоры у детей первых месяцев жизни отличаются от таковых у детей старшего возраста, подростков и взрослых. Так, у детей первого месяца жизни среди бифидобактерий доминируют Bifidobacterium bifidum, Bifidobacterium infantis, Bifidobacterium longum, у детей 8-11 мес преобладают Bifido-bacterium longum, Bifidobacterium bifidum, Bifidobacterium breve, у подростков и взрослых чаще выявляются Bifidobacterium adolescentis, Bifidobacterium catenulatum, Bifidobacterium longum. Как указывалось выше, у детей первого месяца жизни в структуре нормальной кишечной микрофлоры частота обнаружения лактобактерий уступает этому показателю для бифидобактерий. Так, по данным Л.И. Кафарской и соавт., лактобактерии обнаруживались только у 30% здоровых новорожденных. Также установлено, что у детей первых месяцев жизни в кишечной микрофлоре встречаются лишь представители 1-2 видов лактобактерий, преимущественно Lactobacillus salivarius, Lactobacillus gasseri. При изучении влияния лактобактерий на продукцию дендритными клетками провоспалительного цитокина ИЛ-12 обнаружено, что Lactobacillus casei в наибольшей, а Lactobacillus reuteri в наименьшей степени способны к стимуляции ИЛ-12, а инкубация клеток кишечного эпителия с лакто- и бифидобактериями, столь характерными для раннего детского возраста, снижает продукцию провоспалительного цитокина ИЛ-8. Следовательно, бифидо- и лактобактерии, типичные для раннего детского возраста, в меньшей степени способны к продукции провоспалительных цитокинов, чем бифидо- и лактобактерии, характерные для детей старшего возраста, что, вероятно, и формирует механизмы иммунологической толерантности, являющиеся одной из важнейших функций нормальной микрофлоры детей раннего возраста. Таким образом, согласно данным ряда экспериментальных и клинических исследований, именно микрофлора оказывает влияние на дифференцировку Т-лимфоцитов-хелперов (Th), регулируя соотношение Тh-1/Th-2, Тh-17/Treg-лимфоцитов. Взаимодействие между антигенпрезентирующими клетками и микрофлорой обеспечивает баланс про- и антивоспалительных цитокинов на слизистых оболочках. При этом избыточный рост условно-патогенных микроорганизмов может приводить к дисбалансу Тh, усилению синтеза провоспалительных цитокинов и персистенции воспалительного процесса, что характерно для пациентов, страдающих АЗ.
В целом ряде работ изучение кишечной микрофлоры детей с АЗ и без них продемонстрировало существенные отличия в ее видовом составе. Сравнительный анализ состава бифидобактерий новорожденных из стран с высокой и низкой распространенностью АЗ также был различен. Так, у новорожденных детей из Ганы, где АЗ диагностируются редко, в структуре бифидобактерий доминировала Bifidobacterium infantis, которая не входила в состав микрофлоры новорожденных из стран с высокой частотой аллергопатологии. Следует отметить, что у мышей именно Bifidobacterium infantis способна оказывать ингибирующее действие на продукцию спленоцитами мощного провоспалительного цитокина ИЛ-17, а бифидобактерии, встречающиеся в раннем детском возрасте, в значительно меньшей степени способны к стимуляции продукции провоспалительных цитокинов макрофагами, а также ключевого противовоспалительного цитокина ИЛ-10, чем виды бифидобактерий (в частности, Bifidobacterium adolescentis), более характерных для взрослых. Особенно показательны различия в составе микрофлоры у детей с атопическим дерматитом (АД) и без него. Так, у детей с АД отмечались преобладание в микрофлоре эшерихий, лактобацилл, бактероидов, снижение уровня бифидобактерий и их адгезионных свойств, а в структуре бифидобактерий у детей раннего возраста с АД преобладали виды, характерные для детей старших возрастных групп. В работах японских авторов показано, что у детей раннего возраста с АД преобладали Bifidobacterium adolescentis, Bifidobacterium рseudocatenulatum, но в подобной ситуации остался нерешенным вопрос о времени изменения видового состава микрофлоры у детей, поскольку это могло произойти как до начала заболевания, так и после его развития. Ответ на этот вопрос был получен после публикации результатов проспективного исследования, включившего 957 детей, которых наблюдали от момента рождения до двух лет. Авторами было установлено, что изменения микрофлоры кишечника предшествовали клиническим проявлениям аллергопатологии. Эти изменения характеризовались в основном снижением количества бифидобактерий и увеличением уровня клостридий и бактероидов. Аналогичные результаты были получены и другими авторами. Вероятно, бифидобактерии, достигая определенного количественного уровня, оказывают регуляторное действие на параметры иммунитета слизистых оболочек. При снижении их уровня вследствие различных причин (генетическая предрасположенность, незрелость иммунной системы, прием антибиотиков и др.) регуляторные процессы в организме нарушаются, что приводит к дисбалансу дифференцировки Т-лимфоцитов в сторону увеличения доли Тh 2 типа и развитию персистирующего аллергического воспаления, что позволяет предположить целесообразность профилактического назначения пробиотиков с целью благоприятного воздействия на состояние местного иммунитета слизистых и снижения вероятности развития АЗ.
Количество двойных слепых рандомизированных плацебо контролируемых клинических исследований (РКИ), посвященных изучению эффективности пробиотиков для профилактики и лечения АЗ, в последние годы существенно возросло, однако эти работы также продемонстрировали достаточно противоречивые результаты. Так, в исследовании A.L. Taylor и соавт. показано, что использование Lactobacillus acidophilus у детей в возрасте до 6 мес приводило даже к негативным результатам, поскольку в группе, получавшей пробиотик, число пациентов с АЗ оказалось выше, чем в контрольной группе. Вместе с тем при применении лактобактерий с бифидобактериями были получены положительные результаты. В других исследованиях, в которых в комплексе с Lactobacillus rhamnosus использовались Bifidobacterium longum, при оценке результатов не отмечено заметных положительных эффектов пробиотической терапии. В экспериментальном исследовании также были получены данные о том, что у мышей назначение Lactobacillus casei в раннем постнатальном периоде усиливало воспалительные процессы в легких. Вместе с тем применение лактобактерий (Lactobacillus rhamnosus, Lactobacillus reuteri, Lactobacillus сasei) с лечебной целью у детей с АЗ (АД, аллергический ринит) старше одного года приводило к положительным результатам терапии.
Значительное количество РКИ посвящено оценке результатов эффективности использования пробиотиков для профилактики развития АД у детей. Так, в РКИ, включившем 132 ребенка с отягощенным семейным анамнезом по АД, Lactobacillus rhamnosus или плацебо назначали сначала матерям на срок 2-4 нед до родов, а потом новорожденным в течение последующих 6 мес. По достижении детьми 2-летнего возраста частота диагностированного АД снизилась в 2 раза (23% в группе детей, получавших пробиотики, по сравнению с 46% в группе принимавших плацебо; ОР 0,51; 95% ДИ 0,32-0,84). При повторных осмотрах детей в возрасте 4 и 7 лет не было выявлено снижения частоты случаев возникновения бронхиальной астмы, пищевой аллергии, аллергического ринита. Это позволило предположить, что профилактический прием пробиотиков, к сожалению, не предотвратил развитие других проявлений атопии. В более крупном исследовании, включившем 925 детей, использовали Lactobacillus rhamnosus GG в сочетании с Lactobacillus rhamnosus LC 705, Bifidobacterium breve Bb99, Propionibacterium freudenreichii, подвид shermanii JS, и 0,8 г галактоолигосахаридов (только у новорожденных). К моменту достижения детьми 2-летнего возраста авторами получены сходные с предыдущим исследованием результаты в отношении профилактики АД.
Данные одного из последних исследований (PANDA) подтвердили снижение риска развития этого заболевания на 58% у младенцев 3-месячного возраста. Остальные исследования продемонстрировали перспективные, хотя и неоднородные результаты, что можно объяснить различиями в применяющихся пробиотических препаратах, отличиями в их дозировке, а также в планировании и дизайне исследований. Так, группой исследователей из Американской коллегии аллергии, астмы и иммунологии (ACAAI) было установлено, что назначение лактобактерий матерям или детям в раннем возрасте предотвращает последующее развитие АД. Однако в другом РКИ у 232 новорожденных с высоким риском развития АД применение Lactobacillus acidophilus LAVRI-A1 не привело к положительным результатам, что, вероятно, было связано с применением другого штамма или другой дозы пробиотика. По мнению авторов работы, пробиотики при профилактическом применении способны предотвращать развитие АД на трех различных уровнях: с помощью микробиотической модуляции в результате микробного взаимодействия; путем укрепления функции эпителиального барьера; за счет модулирования иммунной системы, основанной на способности пробиотиков снижать реактивность Th 2 типа при одновременном повышении реактивности Th 1 типа и Т-супрессоров.
Поскольку эффект применения пробиотиков традиционно является штамм-специфическим, то, естественно, не все пробиотические штаммы могут быть эффективны для профилактики АД. В частности, получены данные о различной эффективности не только видов, но и отдельных штаммов одного и того же вида пробиотического микроорганизма. Важное значение имеет и период назначения пробиотических препаратов, поскольку профилактический эффект от их применения был получен в ходе тех исследований, которые предусматривали прием пробиотиков в период беременности. В этом случае пробиотики способны влиять на развитие кишечного микробиоценоза ребенка, а также оказывать модулирующее воздействие на иммунологические факторы грудного молока и пуповинной крови, хотя данные выводы пока что детально не исследованы.
Таким образом, следует констатировать, что концепция, согласно которой ранняя профилактика АД, являющегося первым этапом формирования атопического марша, с помощью пробиотиков может предотвратить развитие других АЗ (бронхиальной астмы, аллергического ринита), нуждается в серьезной доказательной базе. К сожалению, практически ни в одном исследовании не показано благоприятное воздействие пробиотиков на уровень чувствительности к причиннозначимым аллергенам при проведении кожного тестирования. Лишь в недавнем исследовании M. Kuitunen и соавт. был показан протекторный эффект смеси пробиотика и пребиотика на развитие IgE-ассоциированных АЗ у детей 5-летнего возраста, родившихся в результате кесарева сечения.
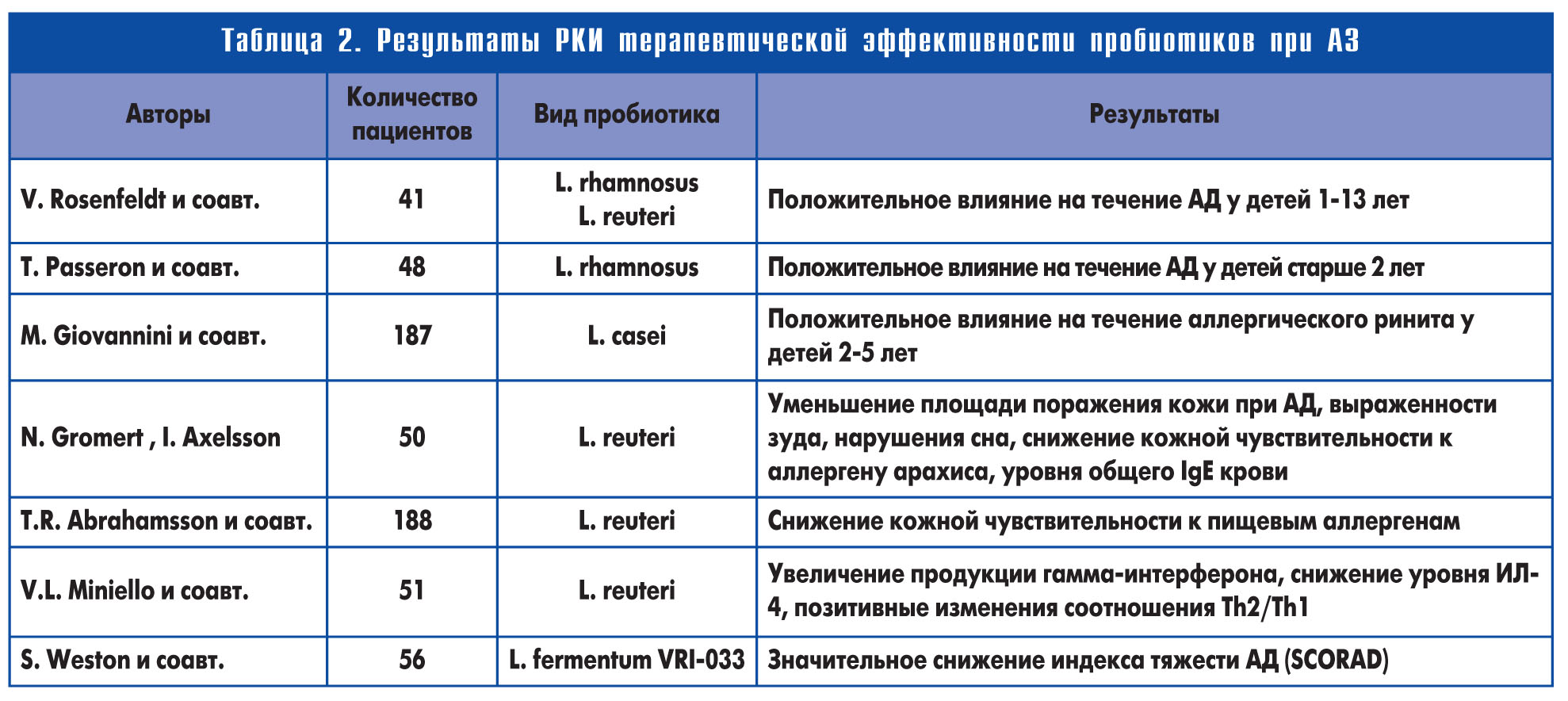
В нескольких менее масштабных РКИ у детей с АД был показан положительный терапевтический эффект применения пробиотиков. S. Weston и соавт. включили в РКИ 56 детей в возрасте 6-18 мес со среднетяжелым или тяжелым течением АД. Дети получали пробиотик Lactobacillus fermentum VRI-033 или равный объем плацебо дважды в день на протяжении 8 нед. По истечении 16 нед авторами было установлено значительное снижение индекса тяжести АД (SCORAD) у детей, получавших пробиотик (p=0,03), в отличие от группы плацебо. Улучшение индекса SCORAD по прошествии 16 нед по сравнению с исходным было зарегистрировано у существенно большего числа детей, принимавших пробиотики (92%), нежели в группе плацебо (63%; p=0,01).
Однако не все попытки применения пробиотиков для лечения пациентов с АЗ были такими успешными. Так, отрицательный вывод о целесообразности применения пробиотиков для лечения АД сделали авторы Кокрановского сотрудничества. В систематический обзор было включено 12 РКИ, охвативших 781 ребенка с АД. По оценке результатов их лечения было отмечено, что пробиотики не уменьшали выраженность проявлений заболевания (в частности, зуда кожи) и не снижали степень его тяжести как по мнению пациентов, так и по суждениям врачей. При анализе отдельных подгрупп детей, сформированных в зависимости от возраста, тяжести заболевания, наличия атопии или пищевой аллергии, не удалось выделить какую-либо популяцию больных, результаты лечения в которой отличались бы от результатов лечения во всей популяции. Однако, поскольку результаты отдельных исследований различались между собой, это указывает на целесообразность продолжения работы в данной области, так как другие виды пробиотиков могут быть более эффективными в терапии АД, чем уже изученные. Авторы Кокрановского сотрудничества также отметили, что лечение пробиотиками ассоциировалось с низким риском развития нежелательных побочных явлений, что указывает на безопасность пробиотической терапии.
Авторы другого Кокрановского обзора, проанализировав результаты 12 РКИ, предположили, что в настоящее время нет достаточных оснований, чтобы рекомендовать применение пробиотиков у детей раннего возраста для профилактики АЗ и пищевой аллергии. Однако сформулировали они это заключение с существенной оговоркой: к результатам анализа следует относиться с осторожностью из-за большого количества пациентов, не завершивших исследования (17-61%). Кроме того, в метаанализе 5 РКИ, в которых были представлены данные об исходах применения пробиотиков у 1477 детей, было установлено статистически значимое снижение заболеваемости АД у обследованных (ОР 0,82; 95% ДИ 0,70-0,95). Однако в случае ограничения анализа исследованиями, изучавшими АД, при котором гиперчувствительность к аллергенам была подтверждена результатами кожного прик-теста или определения специфического иммуноглобулина Е, различия утрачивали статистическую значимость. Во всех испытаниях с положительными результатами применения пробиотиков использовали Lactobacillus rhamnosus, а в исследования включали детей с высоким риском АЗ. При этом польза применения пробиотиков для предупреждения других АЗ или пищевой аллергии не была установлена.
Особый интерес в настоящее время для клиницистов представляет пробиотик Lactobacillus reuteri, впервые описанный G. Reuter в 1980 г. В Украине зарегистрированы пробиотики, содержащие Lactobacillus reuteri, в частности штамм АТСС 55730, который относится к типичным представителям нормальной кишечной флоры. Данный штамм был обнаружен у здоровых лиц в ротовой полости, желудке, тонком, толстом кишечнике, влагалище, грудном молоке. Эффективные колонизационные, иммунотропные и противоаллергические свойства препаратов, содержащих Lactobacillus reuteri, подтверждены результатами многочисленных клинико-лабораторных исследований в странах Европы, в США и Японии, в которых приняли участие свыше 4 тыс. человек, в том числе беременные и новорожденные. Так, было доказано, что применение препаратов Lactobacillus reuteri привело к снижению заболеваемости IgE-ассоциированным АД, положительно влияло на его течение у детей 1-13 лет, что выразилось в уменьшении площади поражения кожи при АД, выраженности зуда, нарушения сна, снижении кожной чувствительности к аллергену арахиса и уровня общего IgE крови, а также, по другим данным, ассоциировалось со снижением кожной чувствительности пациентов к пищевым аллергенам, увеличением продукции гамма-интерферона, уменьшением уровня ИЛ-4, позитивным изменением соотношения Th2/Th1.
В обобщенном виде доступные результаты относительно эффективности применения пробиотиков, в том числе содержащих Lactobacillus reuteri, для профилактики развития АД, а также относительно их терапевтической пользы при АЗ приведены в таблицах 1, 2.

Как уже указывалось выше, факторами, объясняющими такие неоднородные результаты применения пробиотиков с целью профилактики и лечения АЗ, являются видовые и штаммовые различия между пробиотическими бактериями. К благоприятным штамм-специфическим факторам пробиотических штаммов, влияющих на предупреждение развития АЗ, относятся модуляция микробиоценоза, укрепление эпителиального барьера, увеличение Т-супрессоров и угнетение активации Тh 2 типа. Вероятно, наиболее эффективными как для профилактики, так и для лечения АЗ могут стать те пробиотики, которые в меньшей степени способны стимулировать продукцию провоспалительных цитокинов. К таким пробиотическим культурам относятся Lactobacillus reuteri, Bifidobacterium bifidum, Bifidobacterium infantis, Bifidobacterium longum. Возможно также, что бифидобактерии, характерные для раннего детского возраста, способны подавлять продукцию гистамина и экспрессию H1-рецепторов к гистамину, как это было показано в экспериментальной работе японских исследователей. Другими факторами, способствующими успешности клинических результатов применения пробиотиков с профилактической и терапевтической целью, являются высокие уровни колонизации пробиотических бактерий и начало назначения пробиотических препаратов на последнем этапе беременности.
Резюмируя результаты приведенных исследований, посвященных анализу профилактической и терапевтической эффективности пробиотиков при АЗ, можно прийти к выводу, что использование указанных препаратов с целью профилактики и лечения аллергопатологии требует дальнейших исследований. Кроме того, очевидно, что при выборе пробиотика предпочтение следует отдавать препаратам, содержащим те виды бактерий, которые соответствуют нормальной флоре в данной возрастной группе, что особенно актуально для детей. Сроки назначения пробиотиков также достаточно дискутабельны, поскольку длительность их применения требует дальнейшего уточнения и обоснования. При этом лучший профилактический эффект от применения пробиотиков у детей был получен в ходе тех исследований, которые предусматривали их прием матерями в дородовом, а новорожденными в послеродовом периоде. Таким образом, необходимо проведение дополнительных испытаний для формирования достаточной доказательной базы и оформления рекомендаций для более широкого использования пробиотиков при АЗ. В целом же данное направление в аллергологии следует считать перспективным.
Список литературы находится в редакции.
СТАТТІ ЗА ТЕМОЮ Алергія та імунологія
Хронічна кропив’янка (ХК) – це патологія, яка характеризується рецидивними нестійкими висипаннями з/без ангіоневротичного набряку, які виникають мало не щодня впродовж більш як 6 тиж [1]. Розрізняють два варіанти ХК – хронічна індукована кропив’янка (ХІК), або фізична кропив’янка, зумовлена певними фізичними подразниками, такими як тиск, тепло або холод, і більш поширена хронічна спонтанна кропив’янка (ХСК), яка розвивається у 80-90% випадків і характеризується відсутністю відомих екзогенних чинників і причин [2]. На це захворювання страждає від 0,5 до 1% населення світу, переважно особи жіночої статі [3]. Повторні симптоми часто призводять до порушень сну та чинять виражений негативний вплив на якість життя (QoL) [4]. ...
Алергічний риніт (АР) є поширеним запальним захворюванням верхніх дихальних шляхів (ВДШ), особливо серед педіатричних пацієнтів. Ця патологія може знижувати якість життя, погіршувати сон та щоденну продуктивність. Метою наведеного огляду є надання оновленої інформації щодо епідеміології АР та його діагностики, з урахуванням зв’язку з бронхіальною астмою (БА). ...
Поширеність і вплив алергічних захворювань часто недооцінюють [1]. Ключовим фактором алергічної відповіді є імуноглобулін (Ig) Е, присутній на поверхні тучних клітин і базофілів. Взаємодія алергену з IgЕ та його рецепторним комплексом призводить до активації цих клітин і вивільнення речовин, у тому числі гістаміну, які викликають симптоми алергії [2]. Враховуючи ключову роль гістаміну в розвитку алергічних реакцій, при багатьох алергічних станах, включаючи алергічний риніт і кропив’янку, пацієнту призначають антигістамінні препарати [3, 4]....
Алергічний риніт (АР) – дуже поширений патологічний стан, що часто зумовлюється пилком трав і дерев, шерстю тварин, кліщами домашнього пилу та цвіллю. Оцінки його поширеності в різних регіонах Європи та світу дуже різняться [1, 2], але результати епідеміологічних досліджень демонструють, що на нього страждають до 30% дорослих людей і до 40% дітей. Симптоми можуть чинити значний негативний вплив на якість життя пацієнтів, часто заважати сну і сприяти поганій успішності на роботі та в школі. Крім того, АР є відомим фактором ризику розвитку бронхіальної астми; і, навпаки, ця коморбідність значно підвищується [2, 5-7]....




