Погляд на залізодефіцитні анемії у жінок протягом усього життя
За матеріалами конференції
1‑2 жовтня 2020 року за підтримки Асоціації акушерів та гінекологів України пройшла науково-практична онлайн-конференція «Акушерство, гінекологія, репродуктологія: від науки до клінічної практики». У рамках заходу було представлено доповідь президента Італійського товариства психосоматики в акушерстві та гінекології, члена ради директорів Асоціації гінекологів італійського університету, завідувача кафедри акушерства та гінекології Туринського університету (Італія), професора Chiara Benedetto, яка детально висвітлила актуальність проблеми залізодефіцитної анемії у жінок впродовж життя й надала рекомендації щодо лікування даного патологічного стану.
Ключові слова: залізодефіцитна анемія, Сантеферра, сукросомальне (ліпосомальне) залізо.
Анемія – це стан, коли концентрація гемоглобіну (Hb) і/або кількість еритроцитів є нижчою від норми та недостатньою для задоволення фізіологічних потреб організму. Найчастіше анемія діагностується шляхом оцінки концентрації гемоглобіну.
Наразі два мільярди людей (понад 30% світової популяції) страждають від анемії, що визначає дане захворювання як одне з найпоширеніших у світі. Розглядаючи гендерний поділ, слід зазначити, що жінки майже в усіх географічних регіонах мають більший ризик розвитку анемії, ніж чоловіки (у 39% жінок репродуктивного віку та у 46% вагітних жінок було діагностовано анемію у 2016 р.). Саме залізодефіцитна анемія (ЗДА) становить 50% усіх анемій серед невагітних та вагітних жінок.
Нестача заліза – найпоширеніший харчовий розлад та єдиний дефіцит поживних речовин, що суттєво поширений у промислово розвинутих країнах. Глобальна мета Всесвітньої організації охорони здоров’я (ВООЗ) до 2025 р. у харчовій сфері спрямована на зменшення частоти анемії у жінок репродуктивного віку до 50%.
Етіологія залізодефіцитної анемії
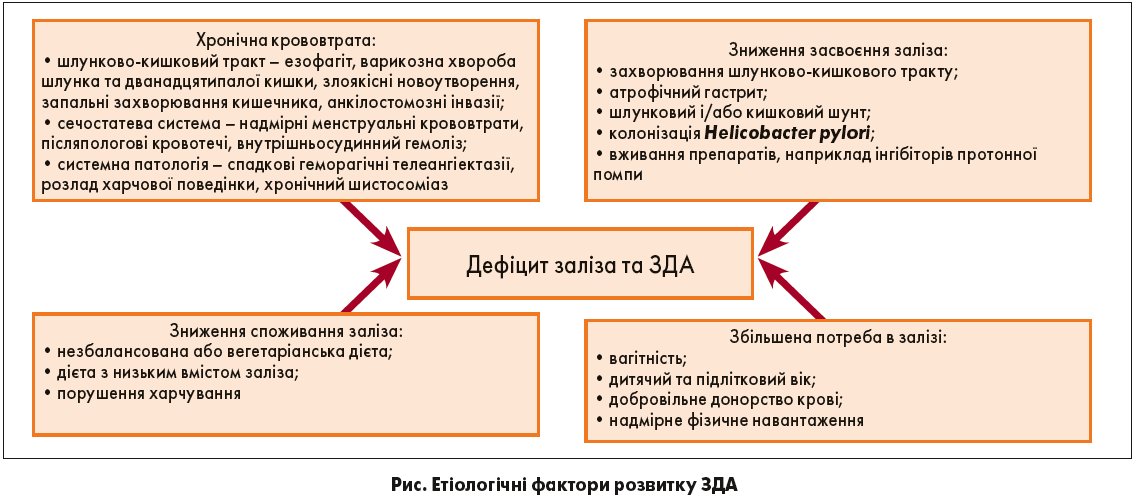
Розглядаючи причини розвитку ЗДА, спікер навела наступні основні фактори (рисунок):
- хронічна втрата крові (рясні менструації, післяпологові кровотечі);
- зменшення абсорбції заліза;
- гемоліз еритроцитів;
- підвищене споживання заліза організмом (вагітність).
Жінки репродуктивного віку мають підвищений ризик розвитку абсолютного залізодефіцитного стану в тому випадку, коли кількість заліза в їхньому раціоні не в змозі задовольнити додаткову потребу в ньому, викликану менструальною крововтратою.
Професор Ch. Benedetto звернула увагу на той факт, що одна із 10 жінок відзначає надмірну менструальну крововтрату, яка становить >80 мл та є основною причиною розвитку зменшення вмісту заліза та ЗДА у жінок репродуктивного віку. Нещодавні дослідження продемонстрували, що у 50‑63% жінок із надмірною менструальною крововтратою діагностовано зменшення кількості заліза або ЗДА.
Під час вагітності, через збільшення об’єму плазми та маси еритроцитів, жінкам необхідно призначати підвищену кількість заліза для забезпечення потреби зростаючого плода та захисту вагітної від несприятливих наслідків крововтрати у пологах. Щоденна потреба матері в залізі змінюється протягом усієї вагітності, збільшуючись приблизно в 10 разів (0,8 мг/день у І триместрі, 4‑5 мг/день у ІІ триместрі та >6 мг/день у ІІІ триместрі вагітності).
Залізодефіцит та ЗДА асоціюються з підвищеним ризиком розвитку таких станів матері та плода:
- прееклампсія;
- післяпологова кровотеча;
- перинатальна смертність;
- низька вага плода при народженні;
- передчасні пологи;
- зниження кількості заліза у новонародженого;
- погіршення фізичного та когнітивного розвитку;
- підвищена захворюваність у дітей.
У післяпологовому періоді анемія пов’язана зі зниженням фізичної працездатності та когнітивних здібностей, із порушенням лактації.
Найчастіша причина крововтрати у жінок у постменопаузальному періоді – кровотечі зі шлунково-кишкового тракту (ШКТ). Крім того, аномальні маткові кровотечі є потенційними факторами дефіциту заліза та розвитку ЗДА. Кровотеча, що призводить до щоденних втрат заліза ≥5 мг, є основною причиною абсолютного його дефіциту, що не може бути компенсований підвищеним всмоктуванням із кишечника й призводить до зменшення запасів заліза в організмі.
Патофізіологія залізодефіцитної анемії
Системний метаболізм заліза забезпечує досить сталий показник загального вмісту заліза в організмі (3‑4 г) завдяки постійному вилученню його із застарілих еритроцитів макрофагами селезінки, що забезпечує 20‑25 мг заліза, необхідного для гемопоезу в кістковому мозку. Підтримання нормальних показників заліза в організмі реалізується за рахунок врівноваження фізіологічних втрат та всмоктування його клітинами ШКТ, що становить 1‑2 мг/день.
Основним регулятором проведення заліза в клітину є гепсидин, що реалізує свою функцію за допомогою макрофагів та базолатеральної мембрани клітин ШКТ. Крім того, гепсидин нейтралізує феропортин, тим самим перешкоджаючи виведенню заліза із клітин-мішеней та знижуючи рівень сироваткового заліза.
Утворення гепсидину стимулюється прозапальними цитокінами, високою концентрацію заліза у тканинах (за допомогою кісткового морфогенетичного білка 6 – ВМР-6) та судинному руслі (за участю насиченого трансферину – TSAT). Недостатність гепсидину призводить до розвитку залізодефіциту, зниження еритропоезу та гіпоксії.
Критерії для встановлення діагнозу «анемія»
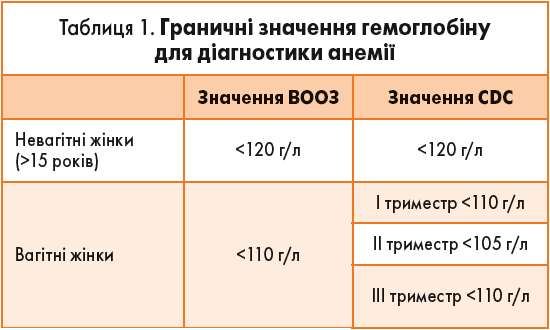
Порогові значення рівня гемоглобіну, що визначені ВООЗ та Центрами контролю і профілактики захворювань США (Centers for Disease Control and Prevention, CDC) для встановлення діагнозу «анемія», наведені у табл. 1.
Профілактика залізодефіциту
Говорячи про профілактичні заходи, доповідач порадила дотримуватися рекомендацій ВООЗ щодо запобігання розвитку ЗДА та визначила основні підходи:
- удосконалення продуктів харчування (покращення техніки їх виготовлення, консервування, переробки, маркетингу, приготування та забезпечення наявності й доступності їжі, багатої на залізо);
- збагачення харчових продуктів (підвищення вмісту заліза в їжі з урахуванням харчових звичок, що передбачає вибір відповідного широко доступного та споживаного продукту, наприклад пшеничне борошно, макарони, рис, цукор, сіль, бульйонні кубики та соєвий соус);
- профілактичне вживання препаратів, що містять залізо, групами населення з найбільшим ризиком (діти, жінки репродуктивного віку);
- усунення побічних ефектів перорального заліза з боку ШКТ.
Лікування залізодефіцитних станів
У терапевтичній стратегії професор Ch. Benedetto серед основних методів відновлення заліза зазначила пероральне або інфузійне введення препаратів та гемотрансфузію, порівняльну характеристику яких наведено у табл. 2.
Розглядаючи фармакокінетику традиційних пероральних препаратів заліза, необхідно зазначити, що їх застосування можливе за цілісності слизової оболонки шлунка (кислотність необхідна для солюбілізації заліза) та дванадцятипалої кишки/проксимальної частини тонкої кишки (де поглинається більша частина заліза), оскільки її ушкодження призведе до порушення мальабсорбції. Крім того, максимальна абсорбційна здатність перорального заліза становить близько 25‑30 мг/день, що в 10‑20 разів перевищує необхідну добову дозу абсорбції заліза (1‑2 мг). Неабсорбоване залізо викликає розвиток побічних ефектів із боку ШКТ.
При внутрішньовенному введенні препаратів залізо-карбогідратні комплекси швидко поглинаються макрофагами й за необхідності повільно вивільняються у судинне русло за допомогою феропортину.
Ліпосомальне залізо (Сантеферра) як шлях до мінімізації побічних ефектів пероральних препаратів заліза
Оскільки пероральні препарати заліза мають численну кількість побічних ефектів, професор Ch. Benedetto рекомендувала призначати залізовмісний комплекс Сантеферра. Він має у своєму складі ліпосомальне (сукросомальне) залізо – фосфоліпідну сполуку, де пірофосфат заліза захищений фосфоліпідною двошаровою мембраною, переважно від лецитину соняшнику. Дана запатентована технологія забезпечує максимальну переносимість, гастрорезистентність, відсутність негативних смакових якостей та побічних ефектів, що зазвичай асоціюються з дотацією заліза.
Крім того, абсорбція комплексу Сантеферра відбувається без застосування звичних механізмів кишкового всмоктування. Це дозволяє отримувати більш високі його концентрації у плазмі порівняно з іншими сполуками перорального заліза. Традиційне пероральне залізо всмоктується за допомогою опосередкованих білкових транспортних шляхів, натомість як Сантеферра повністю абсорбується слизовою оболонкою кишечника як везикулярна структура без допомоги специфічних транспортних клітин. Кишкова абсорбція сукросомального заліза забезпечується мікроскладчастими клітинами Пайєра (М-клітини) та ендоцитозом макрофагами з подальшим надходженням по лімфатичних судинах у незміненому вигляді до гепатоцитів (Baomiao D. et al., 2017).
Клінічні дослідження ефективності ліпосомального заліза (Сантеферра)
Дослідження, що включало пацієнтів з анемією середнього та тяжкого ступеня, спричиненою крововтратою, демонструє більш високу ефективність залізовмісного комплексу Сантеферра порівняно з іншими сполуками перорального заліза. Більше того, Сантеферра ефективний в анемічних пацієнтів із високим рівнем С-реактивного білка, що вказує на абсорбцію засобу незалежно від гепсидину та пов’язаних із ним механізмів.
Інше рандомізоване дослідження впливу різного дозування Сантеферра порівняно із сульфатом заліза оцінювало показники 80 вагітних жінок без анемії у терміні гестації від 12 до 14 тиж. Пацієнти входили до чотирьох груп, що включали по 20 жінок:
- І група – прийом Сантеферра у дозі 14 мг/день;
- ІІ група – прийом Сантеферра у дозі 28 мг/день;
- ІІІ група – прийом сульфату заліза у дозі 30 мг/день;
- ІV група – контрольна.
Порівняно з контрольною та сульфатною групами, група з використанням Сантеферра у дозі 28 мг/день показала статистично значущо вищий рівень гемоглобіну через 28 тиж та у післяпологовому періоді. Крім того, відзначено вищий рівень феритину у терміні 20, 28 тиж вагітності та через 6 тиж після пологів (р<0,01), а також меншу кількість жінок, у яких розвивалась анемія (10% проти 25%) (Parisi F. et al., 2017).
Також було досліджено вплив Сантеферра на 30 жінок у постменопаузальному періоді (45‑65 років) із ЗДА (рівень гемоглобіну <115 г/л), які попередньо проходили лікування іншими препаратами заліза, що мали побічні ефекти (крім алергії). Дана група пацієнтів отримувала 14 мг Сантеферра двічі на день протягом 8 тиж. Результати дослідження вказують на підвищення концентрації гемоглобіну у крові до 127 г/л після проходження курсу лікування ліпосомальним залізом.
Залізовмісний комплекс Сантеферра статистично достовірно знижував кількість побічних ефектів із боку ШКТ (р<0,05). Найбільш частим побічним ефектом, зафіксованим при застосуванні ліпосомального заліза, було забарвлення вмісту кишечника й оцінено у 5 балів за шкалою Лікерта.
Доповідач зазначила, що комплекс Сантеферра – варіант № 1 для багатьох груп пацієнтів. Сантеферра рекомендовано призначати першочергово для наступних груп пацієнтів:
- особи, що мають підвищену потребу в залізі або не споживають його в достатній кількості разом із їжею;
- жінки під час вагітності та годування грудьми;
- підлітки від 12 років у період активного росту;
- вегетаріанці;
- пацієнти з порушенням мальабсорбції;
- пацієнти із целіакією в анамнезі (без глютену);
- хвороби в анамнезі, що викликають хронічну анемію (кровотечі, запальні захворювання кишечника, рак, ниркова недостатність, рясні менструальні кровотечі тощо).
Висновки
На завершення Ch. Benedetto зазначила, що профілактика дефіциту заліза має базуватися на підходах, орієнтованих на збагачення їжі залізом і/або призначення заліза у вигляді препаратів. Особливо важливим є запобігання дефіциту заліза у вагітних, оскільки це впливає на розвиток ускладнень вагітності.
Відновлення рівня заліза можна досягти пероральним призначенням заліза, внутрішньовенним введенням або за допомогою переливання крові. Дані варіанти мають обмеження, що знижують їх ефективність, утім інноваційна розробка сукросомального заліза (Сантеферра) забезпечує більшу доступність, зменшує побічні ефекти з боку ШКТ і запобігає нестабільності рівня заліза.
Клінічні дослідження підтверджують безпечність та ефективність використання залізовмісного комплексу Сантеферра у пацієнтів з анемією, у вагітних жінок та у постменопаузальному періоді, тому його слід розглядати у якості препарату вибору для профілактики та лікування ЗДА. Саме тому Сантеферра є варіантом № 1 при виборі препарату заліза.
Підготувала Вероніка Яремчук
Тематичний номер «Акушерство, Гінекологія, Репродуктологія» № 1 (42) 2021 р.
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Чи варто змінювати свої харчові звички під час вагітності? Довкола цієї теми є багато суперечностей і рекомендацій, у яких легко заплутатися. Команда платформи доказової інформації про здоров’я «Бережи себе» спільно з лікарем-дієтологом Тетяною Лакустою з’ясували, чим раціон жінки в цей період особливий та на що слід звернути увагу. ...
Хронічний тазовий біль (ХТБ) є поширеним патологічним станом, який відзначається у жінок будь-якого віку і супроводжується сексуальною дисфункцією, емоційною лабільністю, аномальними матковими кровотечами, порушенням сечовипускання, розладами з боку кишечника тощо. Пацієнтки, які страждають на ХТБ, часто скаржаться на симптоми тривоги та депресії, що негативно позначається на їхній повсякденній активності, включаючи зниження працездатності та погіршення якості життя [1]. Сьогодні проблема ХТБ є економічним тягарем, пов’язаним із прямими або непрямими медичними витратами, які в середньому в різних країнах світу оцінюються у 4,9 млрд доларів на рік [2]. Раціональна фармакотерапія,спрямована на полегшення та контроль симптомів болю, є ключовою стратегією боротьби із ХТБ...
Дефіцит заліза є найпоширенішим патологічним станом у світі та однією з п’яти основних причин інвалідності. У той час як низький показник феритину у сироватці крові є діагностичною ознакою залізодефіциту, підвищений його рівень визначається як гострофазовий маркер, що може реєструватися при запальних станах уже в І триместрі вагітності. Відповідно до сучасних настанов, проведення рутинного скринінгу на залізодефіцит у невагітних та вагітних жінок за відсутності ознак анемії не рекомендоване. З огляду на останні літературні дані ця рекомендація має бути переглянута...
Наказ Міністерства охорони здоров’я України від 25.08.2023 № 1533 ...