Аналіз ефективності та безпеки оральних антикоагулянтів для тривалого лікування фібриляції передсердь у пацієнтів похилого віку
На фібриляцію передсердь (ФП), що є найчастішою формою серцевої аритмії, страждає близько 2% загальної популяції. ФП, поширеність якої за останні роки зросла, являє собою одну з найактуальніших проблем охорони здоров’я через ризик розвитку таких серйозних клінічних ефектів, як інсульт та деменція. Показано, що застосування пероральної антикоагулянтної терапії у літніх осіб із ФП є вкрай важливим для зменшення імовірності тромбоемболічного інсульту. Європейські експерти F. Pazanet et al. виконали огляд рандомізованих контрольованих клінічних досліджень та коротких інструкцій для медичного застосування деяких оральних антикоагулянтів (ОАК) із метою оновлення даних стосовно їх ефективності та безпеки у пацієнтів похилого віку із ФП. Отримані результати опубліковані у виданні Drugs & Aging (2020; 37: 539‑548).
Частота розвитку ФП із віком зростає: з <0,2% в осіб до 49 років до ~4% у 60‑70 років, а після 80 років сягає 10‑17%. Ризик інсульту в пацієнтів із ФП з віком також підвищується (Zathar et al., 2019). Було показано, що ОАК зменшують імовірність емболічного інсульту більш ніж на 50% у цій когорті хворих (Mitrousi et al., 2013). Однак, як і стосовно багатьох інших ліків, існує недостатньо доказів щодо ефективності та безпеки певних ОАК для тривалого лікування ФП у літньому віці (Wehling et al., 2013; Fialovа et al., 2018).
У 2008 р. було розроблено класифікаційну систему FORTA (Fit fOR The Aged), щоб допомогти лікарям визначити пріоритет у застосуванні медикаментів у пацієнтів віком >65 років. Препарати отримують рейтинг А (незамінний), В (корисний), С (сумнівний) або D (уникати призначення) з огляду на їх ефективність, ризик та доцільність для щоденного використання у літніх хворих (Pazan et al., 2019).
На основі цієї класифікації був розроблений спеціальний перелік FORTA, що включає близько 300 оцінок для 30 діагнозів, які відповідають віковій категорії (Wehling, 2011). У рандомізованому контрольованому дослідженні VALFORTA якість ліків, яку оцінювали з урахуванням побічних реакцій на тлі терапії, та деякі інші клінічні кінцеві точки (щоденна активність) значно поліпшилися завдяки FORTA (Wehling et al., 2016).
У 2016 р. міждисциплінарна група європейських експертів після детальної оцінки переваг традиційних ОАК для тривалого лікування ФП у літніх осіб розробила перелік OAC-FORTA 2016 (Wehling et al., 2017). F. Pazanet et al. (2020) виконали структурований огляд літератури на предмет нових доказів згідно з міжнародним консенсусом Delphi щодо створення переліку OAC-FORTA 2019 (Mitrousi et al., 2013).
Матеріали й методи дослідження
Критерії включення та вибір експертів
Структурований пошук літератури був проведений у базах даних PubMed/MEDLINE з 2016 р. по 2019 р. із використанням критеріїв, як-то ФП та назва препарату: варфарин, дабігатран, едоксабан, ривароксабан, аценокумарол, флуіндіон, фенпрокумон, апіксабан. Загалом було виявлено 202 публікації, після аналізу яких відібрано 11 досліджень, що повністю відповідали критеріям включення.
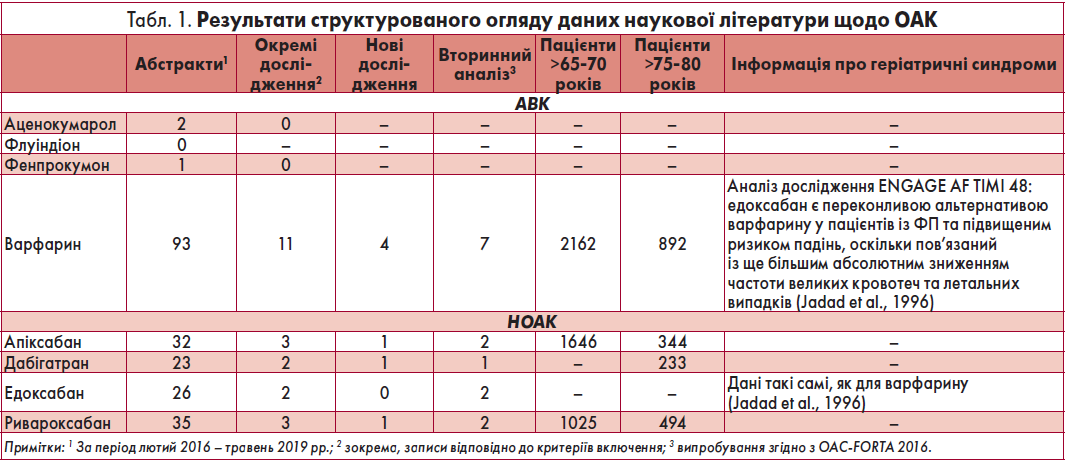
Враховувалися лише рандомізовані контрольовані дослідження за участю принаймні 100 пацієнтів, які отримували лікування одним із медикаментів протягом щонайменше шести місяців. Також міждисциплінарна група провела аналіз оновлених коротких інструкцій для медичного застосування обраних препаратів (n=8). Дані проаналізованих досліджень наведені у таблиці 1.
Статистичний аналіз
Експертна група оцінювала OAК згідно з класифікацією FORTA на основі наданих доказів та власних знань/досвіду. Для кожного препарату був розрахований відсоток експертів, які погодили запропоновані класи FORTA (A, B, C або D). Отримані показники зважували для обчислення скорегованого коефіцієнта консенсусу для кожного препарату, що відображав ступінь варіації між індивідуальними оцінками (0 – одностайність, відсутність відхилень; 1 – сусідні класи FORTA, половинна значущість оцінки; 2 – від А до С або від В до D, третинна значущість оцінки; 3 – від А до D, повна розбіжність оцінки). Для визначення підсумкових класів FORTA оцінки експертів щодо кожного препарату переводили у числові значення A=1, B=2, C=3 і D=4. Далі для окремих ліків розраховували середнє арифметичне m та знову перетворювали значення на попередні класи: 1≤m<1,5: FORTA A; 1,5≤m<2,5: FORTA B; 2,5≤m<3,5: FORTA C; m≥3,5: FORTA D (Wehling et al., 2017).
Критерій Шапіро – Уїлка використовували для перевірки адекватності даних, t-критерій – для порівняння середніх показників двох груп. Статистичний аналіз проводили за допомогою програмного забезпечення SAS версії 9.4 для Windows (SAS Institute Inc., Кері, Північна Кароліна, США).
Результати дослідження
У проаналізованих дослідженнях не виявлено даних щодо використання антагоністів вітаміну К (АВК) аценокумаролу, флуіндіону та фенпрокумону в літніх пацієнтів. Тому оцінку проводили на основі результатів із застосування варфарину. Оскільки варфарин використовували як контроль для ОАК, які не є антагоністами вітаміну К (НОАК), 10 із них розглядали двічі щодо НОАК і варфарину окремо.
З-поміж 11 було виявлено чотири випробування щодо ефективності та безпеки варфарину, апіксабану, дабігатрану чи ривароксабану в літніх хворих (табл. 1). У трьох із них аналізували ефект антикоагулянтної терапії після черезшкірного коронарного втручання в осіб із ФП. Ще в одному проводили вторинний аналіз випробування ENGAGE AF-TIMI 48 (2013), де було показано перевагу едоксабану над варфарином у пацієнтів із ризиком падінь щодо нижчої частоти тяжких кровотеч та летальних випадків (Steffel et al., 2016). Усі 11 досліджень були високої якості за шкалою Джадада (≥3 балів). Найбільші можливі 5 балів мали шість випробувань, що свідчить про їх найвищу методологічну якість.
Загалом в усіх дослідженнях, присвячених порівнянню варфарину та НОАК, останні перевершували варфарин щодо принаймні однієї клінічної кінцевої точки. Апіксабан виявився ефективнішим за варфарин у хворих будь-якого віку (зокрема >75 років) щодо внутрішньочерепних крововиливів, дабігатран – у літніх пацієнтів (у віці 80‑84 або <75 років) стосовно ризику внутрішньочерепних крововиливів. У межах подвійної терапії інгібітором P2Y12 дабігатран перевершував потрійну, яка включала варфарин, щодо основних або клінічно значущих невеликих кровотеч. Окрім того, едоксабан мав переваги перед варфарином стосовно ризику великих кровотеч та внутрішньочерепних крововиливів.
У дослідженні J. Steffel et al. (2016) едоксабан був менш дієвим за варфарин щодо комбінованої кінцевої точки, яка включала смерть, інсульт, системну емболію та велику кровотечу, в пацієнтів із високим ризиком падінь порівняно з такими із низьким. Проте загалом едоксабан перевершував варфарин із точки зору ефективності, безпеки та інших комбінованих кінцевих точок у хворих, що мали підвищену ймовірність падінь.
Оновлення за результатами аналізу коротких інструкцій для медичного застосування препаратів, які стосувалися геріатричних пацієнтів, були щодо: корекції дози, впливу на ниркову недостатність для варфарину, рекомендацій із приводу загальної обережності та застосування менших доз для флуіндіону, даних про фармакокінетику для апіксабану та необхідності оцінки функції нирок за формулою Кокрофта – Голта для дабігатрану.
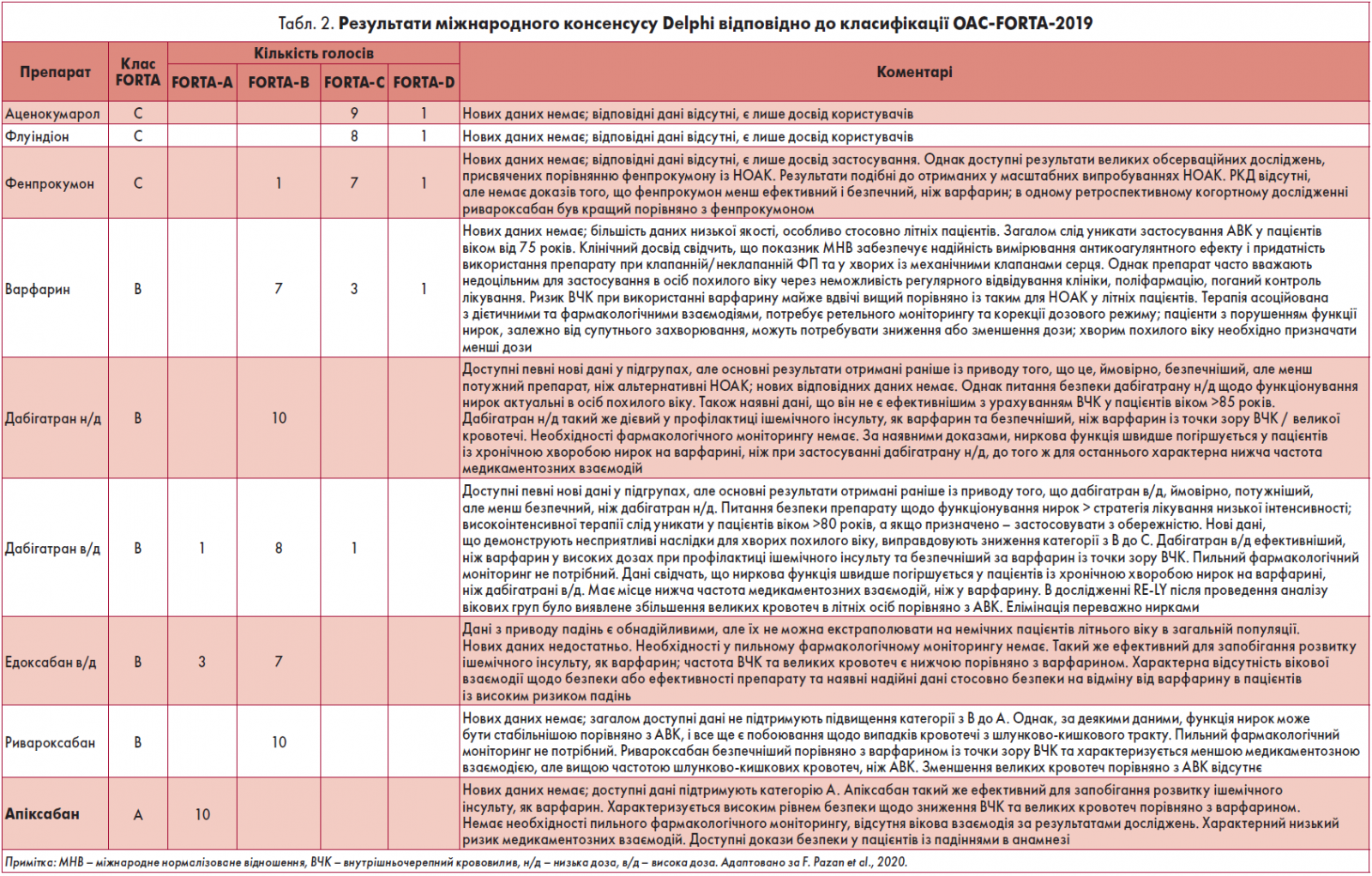
За підсумками експертних оцінок, половині препаратів був присвоєний клас FORTA B (як-то варфарин, дабігатран, едоксабан, ривароксабан), трьом ОАК – FORTA C (аценокумаролу, флуіндіону та фенпрокумону) через відсутність відповідних даних, і лише апіксабан був оцінений як FORTA A. Запропоновані класи FORTA для апіксабану, ривароксабану та дабігатрану були одноголосно підтверджені усіма експертами.
Результати міжнародного консенсусу Delphi відповідно до класифікації OAC-FORTA 2019 представлені в таблиці 2.
Обговорення
Науковий прогрес не стоїть на місці, та оновлення кожні три роки найбільш застосовуваних ОАК у геріатричній популяції з ФП є необхідним та доречним. Як показав поточний огляд наукової літератури, більшість (67%) вторинних аналізів рандомізованих контрольованих досліджень не містять оцінок підгруп літніх осіб, тому важливих доказів щодо ефективності та безпеки ОАК у когорті пацієнтів, які мають найвищий ризик розвитку інсульту та кровотечі, бракує. Наприклад, у нещодавньому вторинному аналізі дослідження ARISTOTLE, присвяченому вивченню використання ОАК у хворих на ФП із падіннями в анамнезі, не оцінювали осіб старечого віку (Granger et al., 2011; Rao et al., 2018). Таким чином, невідомо, чи стосуються отримані перспективні результати щодо переваги апіксабану над варфарином пацієнтів >80 років.
Дослідження F. Pazan et al. (2020) являє собою оновлену версію OAC-FORTA, що містить нові дані клінічних випробувань, інформацію про ліки, сучасні знання та досвід міжнародних експертів. Ця класифікація підтверджує оптимальні терапевтичні рішення щодо призначення антикоагулянтів, зокрема НОАК і АВК, у літніх пацієнтів із ФП у більшості європейських країн.
Також слід зауважити, що результати більшості реєстрів та інших джерел даних щодо застосування ОАК у геріатричних хворих зазвичай відповідають OAC-FORTA і підтримують переваги НОАК над АВК для лікування ФП у літніх осіб (Monelli et al., 2019; Haas et al., 2019; Mazurek et al., 2020). Вони не завжди містять детальний аналіз окремих OАК, але включають дані про недостатньо вивчені АВК, наприклад фенпрокумон (Hohnloser et al., 2018). Так, наразі стали доступними дані про переваги апіксабану та дабігатрану, проте не ривароксабану, над фенпрокумоном щодо ризику кровотечі.
Висновки
Антикоагулянтна терапія ОАК при ФП у геріатричній популяції знаходиться у фокусі уваги науковців. Результати огляду F. Pazanet et al. (2020) підкреслюють можливості антикоагулянтного лікування у літніх пацієнтів із ФП та підтверджують переваги використання НОАК над АВК у цій когорті хворих, зокрема із ризиком падінь, на основі даних клінічних випробувань, сучасних знань та досвіду міжнародних експертів.
Апіксабан залишається найкращим НОАК у цій віковій групі (FORTA A) завдяки одностайній оцінці всіх експертів щодо його ефективності та безпеки. Однак більшість (67%) вторинних аналізів досліджень не містять оцінок підгруп літніх осіб. Тому важливих даних стосовно ефективності й безпеки ОАК у цій віковій категорії, що має найвищий ризик розвитку інсульту та кровотеч, на жаль, досі бракує. Необхідні додаткові дослідження ОАК для застосування у межах терапії хворих похилого віку.
Статтю надруковано за підтримки компанії «Пфайзер» PP-ELI-UKR-0131
Підготувала Олена Коробка
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 2 (75) 2021 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....