Хирургические аспекты лечения обструктивных заболеваний панкреатодуоденальной зоны
Периоперационные осложнения
Основным оперативным вмешательством при лечении обструктивных заболеваний панкреатодуоденальной зоны (ПДЗ) является панкреатодуоденальная резекция (ПДР), которая относится к разряду наиболее сложных оперативных вмешательств, сопровождающихся большим числом периоперационных осложнений. Вопросы профилактики, своевременной диагностики и лечения периоперационных осложнений при ПДР остаются актуальными [2, 4, 6].
Проведена систематизация периоперационных осложнений у больных с обструктивными процессами ПДЗ и вызвавших их причин. Выделены 5 основных групп.
І. Осложнения, связанные с состоянием гепатобилиарной системы.
ІІ. Осложнения, связанные с состоянием поджелудочной железы (ПЖ).
ІІІ. Осложнения, связанные с состоянием желудочно-кишечного тракта (ЖКТ).
IV. Осложнения, связанные с нарушениями других органов и систем.
V. Осложнения, связанные с оперативным вмешательством [1].
Осложнения, связанные с состоянием гепатобилиарной системы
Данные осложнения развиваются из-за наличия следующих дооперационных факторов:
1) длительная (свыше 14 сут) и/или высокая желтуха (свыше 200 мкмоль/л);
2) холангит;
3) патология печени: холестатический гепатит, цирроз печени, печеночная недостаточность, нарушения свертывающей системы.
Перечисленные факторы вызывают развитие как интраоперационных, так и послеоперационных осложнений.
Интраоперационные осложнения: повышенная кровоточивость, которая приводит к обильным операционным кровопотерям и образованию гематом в зоне операции.
Послеоперационные осложнения:
♦ печеночная, печеночно-почечная недостаточность;
♦ нарушение свертывающей системы, которое нередко приводит к развитию тромбогеморрагического синдрома;
♦ диспротеинемия с последующим иммунодефицитом – одна из наиболее частых причин развития недостаточности билиодигестивных и других анастомозов;
♦ холангит с последующим развитием сепсиса и полиорганной недостаточности (ПОН).
Осложнения, связанные с состоянием поджелудочной железы
Факторы риска развития послеоперационных осложнений, связанные с состоянием ПЖ, разделяются на дооперационные, интраоперационные и послеоперационные.
Дооперационные факторы:
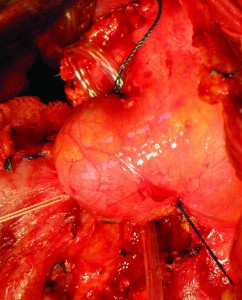
♦ панкреатит: острый без деструкции (рис. 1), с высоким риском деструкции, деструктивный, хронический (фиброзно-кистозный);
♦ отсутствие фиброза при мягкой, «сочной» ткани ПЖ;
♦ узкий диаметр вирсунгова протока.
Интраоперационные факторы:
♦ технические: множественные швы через ткань ПЖ, гематомы в области панкреатоеюноанастомоза (ПЕА);
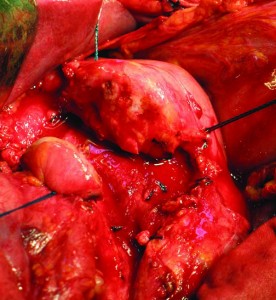
♦ мягкая, «сочная» ткань ПЖ (рис. 2);
♦ расширенная мобилизация головки и тела ПЖ;
♦ просачивание ферментов через проколы и нити швов;
♦ наложение погружающих швов на культю ПЖ;
♦ сдавление панкреатического протока;
♦ удаление большой части ПЖ.
По материалам нашей клиники, изучено состояние паренхимы ПЖ у 146 больных, при этом наличие фиброза в ПЖ выявлено у 104 (73,2%), мягкая, «сочная» ПЖ – у 42 (26,8%) пациентов. Неблагоприятными факторами являлась мягкая, «сочная», жирная ПЖ, более благоприятными – фиброзно измененная, плотная, бугристая ПЖ. При оценке просвета главного панкреатического протока неблагоприятным фактором считалось наличие узкого, тонкостенного вирсунгова протока диаметром до 1-2 мм, как более благоприятный фактор рассматривался средний (2-3 мм) и широкий панкреатический проток диаметром >3 мм с утолщенной стенкой. У 18 (12,3%) больных выявлен узкий, у 71 (48,6%) – средний, у 57 (39,0%) – широкий вирсунгов проток [1].
Послеоперационные факторы, связанные с состоянием ПЖ, в зависимости от вызвавших их причин, а также сроков их развития можно разделить на ранние и поздние.
Ранние осложнения:
♦ панкреатит без деструкции;
♦ панкреатит с деструкцией;
♦ панкреатический свищ;
♦ недостаточность ПЕА;
♦ перитонит;
♦ полиорганная недостаточность;
♦ внутрибрюшное кровотечение из зоны ПЕА;
♦ абсцессы брюшной полости.
Поздние осложнения (в основном связаны с такими факторами, как наличие хронического панкреатита, удаление большой части ПЖ, активность фиброгенеза в ткани ПЖ, которые приводят к нарушению экзо- и эндокринной функций ПЖ):
♦ мальдигестия;
♦ мальабсорбция;
♦ сахарный диабет.
Осложнения, связанные с заболеваниями и нарушениями функции желудочно‑кишечного тракта
Дооперационные осложнения: гастродуоденит, папиллит, язвенная болезнь желудка и двенадцатиперстной кишки, гастродуоденостаз, хронический энтероколит.
Послеоперационные осложнения: эрозивный гастродуоденит с развитием острых язв желудка и двенадцатиперстной кишки и кровотечением из них, гастродуоденостаз, парез кишечника, дисбактериоз.
Осложнения, связанные с нарушениями других органов и систем
Факторы, вызывающие эти осложнения: ишемическая болезнь сердца, гипертоническая болезнь, бронхит, плеврит, венозная недостаточность нижних конечностей, пиелонефрит и др. (в анамнезе в том числе).
Послеоперационные осложнения, вызванные этими факторами: инфаркт миокарда, плевропневмония, тромбоэмболия, уремия, тромбофлебит.
Осложнения, связанные с оперативным вмешательством
Факторы, вызывающие эти осложнения: длительность операции и наркоза, травматичность и инвазивность оперативного вмешательства, бактериальная контаминация.
Осложнения, вызванные этими факторами: печеночно-почечная недостаточность, ПОН, внутрибрюшные кровотечения, желчеистечение, билома брюшной полости, лимфорея, абсцессы брюшной полости, сепсис [1].
При систематизации периоперационных осложнений учитывалась их структура, отличающаяся определенным характером и объемом патологического поражения, в результате чего было выделено 3 основные группы осложнений [1].
I группа – осложнения воспалительного характера:
Іа – с локальным поражением органов ПДЗ в зоне обструкции;
Іб – с системными воспалительными проявлениями.
II группа – осложнения деструктивного характера:
IIа – с локальным поражением органов ПДЗ в зоне обструкции;
ІІб – с системными воспалительными проявлениями.
III группа – осложнения полиорганного характера.
По материалам нашей клиники, среди 223 больных, перенесших ПДР, у 186 (83,4%) наблюдалась механическая желтуха, у 37 (16,6%) – отсутствие желтухи. У 41 (22,0%) пациента отмечалось повышение билирубина с 30 до 100 мкмоль/л, у 66 (35,5%) пациентов – со 101 до 200 мкмоль/л, у 55 (29,6%) – с 201 до 300 мкмоль/л, у 20 (10,8%) – с 301 до 400 мкмоль/л, у 4 (2,2%) – выше 400 мкмоль/л. Тридцати четырем (15,2%) больным с механической желтухой и показателями билирубина выше 250 мкмоль/л выполнена предварительная билиарная декомпрессия.
В послеоперационном периоде после ПДР наиболее частым осложнением являлся острый панкреатит культи ПЖ, а также, как следствие острого панкреатита, частичная или полная несостоятельность ПЕА. Наиболее тяжелым и труднокорригируемым осложнением является несостоятельность панкреатодигестивного анастомоза, так как она в некоторых случаях влечет за собой цепь патологических событий, приводящих к летальному исходу. Основным патогенетическим механизмом развития несостоятельности является местнодеструктивное действие активированных ферментов ПЖ в зоне линии шва. Просачивание панкреатического секрета и скопление в зоне культи ПЖ приводят к образованию очагов воспаления с последующим развитием зон некроза в ПЖ и окружающих тканях [1].
По материалам нашей клиники, в послеоперационном периоде послеоперационный панкреатит развился у 35 (15,7%) пациентов.
Послеоперационный панкреатит культи ПЖ послужил причиной несостоятельности ПЕА у 24 (68,6%) больных, в том числе частичной несостоятельности (панкреатического свища) у 16 (45,7%).
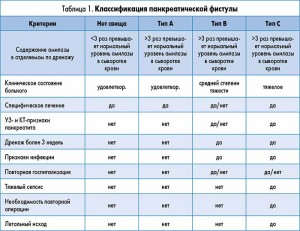
Классификация панкреатической фистулы ISGPF (2005) согласно рекомендациям международной группы экспертов [3, 5] приведена в таблице 1.
В нашей клинике панкреатическая фистула наблюдалась у 16 (7,2%) больных: тип А – у 8 (50%), тип В – у 7 (43,8%), тип С – у 1 (6,2%).
Диагностика послеоперационного панкреатита:
♦ клинико-биохимические исследования (клинические, определение сахара крови, липазы (>200 Ед/мл) и амилазы крови, трипсиногена-2 в моче (тест Actimтм Pancreatitis);
♦ определение маркеров тяжести течения острого послеоперационного панкреатита (определение уровня кальция крови (<2 ммоль/л,) уровня эластазы (>3,5 нг/мл), уровня СРБ (>150 мг/л), прокальцитонина крови (>2 нг/мл);
♦ инструментальные методы диагностики (УЗИ органов брюшной полости, спиральная компьютерная томография, магнитно-резонансная томография, позволяющие определить степень поражения паренхимы культи ПЖ, наличие парапанкреатических жидкостных скоплений).
Современная медикаментозная терапия в периоперационном периоде:
♦ антисекреторная терапия: ингибиторы панкреатической секреции (воздействующие на ацинарную клетку) – сандостатин, октрестатин, октреотид, октрайд; ингибиторы протеолитической секреции (инактивирующие ферменты в крови) – контрикал, гордокс, контривен и др.;
♦ ингибиторы желудочной секреции – пантопразол, рабепразол, эзомепразол;
♦ рациональная антибактериальная терапия (карбапенемы – синерпен, инванз, тиенам; фторхинолоны – левофлоксацин, гатифлоксацин, моксифлоксацин; цефалоспорины III-IV поколения – цефоперазон, цефепим);
♦ противовоспалительная терапия – лорноксикам, кетанов, олфен;
♦ адекватная заместительная терапия (объем инфузии, коррекция гипоксемии);
♦ профилактика и лечение пареза кишечника (предотвращение механизма транслокации), нутриционная поддержка.
Показания к повторным оперативным вмешательствам при несостоятельности ПЕА и развитии панкреатического свища:
♦ перитонит, абсцессы брюшной полости;
♦ ограниченные скопления панкреатического сока;
♦ аррозивное кровотечение.
Обязательным элементом в предотвращении повторных оперативных вмешательств при несостоятельности ПЕА и панкреатической фистуле является адекватное полноценное дренирование области анастомоза двумя наружными силиконовыми дренажами по верхнему и нижнему краю анастомоза и установкой третьего улавливающего дренажа ниже и латеральнее ПЕА.
Одно из наиболее частых осложнений ПДР – послеоперационный гастростаз, особенно после пилоросохраняющих ПДР. Его причинами являются:
♦ «веретенообразная» деформация мобилизованного выходного отдела желудка при наложении гастроеюноанастомоза;
♦ перифокальный инфильтрат вследствие просачивания панкреатических ферментов в окружности ПЕА;
♦ затянувшийся выраженный парез культи желудка, особенно при одновременной ваготомии.
В нашей клинике чаще применяется резекция 1/2 желудка или экономная резекция желудка в виде антрумэктомии (ге‑миантрумэктомии) с селективной ваготомией. Послеоперационный гастростаз наблюдался у 16 (7,2%) больных: у 5 (31,25%) – после резекции 1/2 желудка, у 9 (56,25%) – после антрумэктомии с ваготомией, у 2 (12,5%) – после пилоросохраняющей ПДР.
Для профилактики гастростаза и нарушения пассажа по приводящей петле гастроэнтероанастомоз в последние годы преимущественно располагался нами впередиободочно. Такое расположение гастроэнтероанастомоза позволяет максимально удалить его от влияния возможного панкреатического инфильтрата, который развивается из-за послеоперационного панкреатита культи ПЖ, и уменьшить частоту послеоперационного гастростаза.
При пилоросохраняющей ПДР, перевязывая кровеносные сосуды, хирург всегда должен помнить о многочисленных вариантах кровоснабжения двенадцатиперстной кишки, для того чтобы сохранить адекватное кровоснабжение ее культи и, таким образом, успешно сформировать анастомоз.
На реконструктивном этапе через культю желудка трансназально проводится в отводящую петлю тонкий дуоденальный зонд, который используется для зондового питания в ближайшем послеоперационном периоде и сохраняется до восстановления пассажа пищи через анастомозы. Если зонд был преждевременно удален и не отмечалось эффективного пассажа пищи, то повторно эндоскопически заводится дуоденальный зонд за зону гастроэнтероанастомоза в отводящую кишечную петлю. Девяти (56,3%) пациентам зонд заводился повторно, и в течение 7-10 суток осуществлялось зондовое питание.
Несостоятельность билиодигестивного анастомоза после ПДР встречается реже. При выполнении гепатикоеюноанастомоза чаще возникает несостоятельность, чем при выполнении холедохо- или холецистоеюноанастомоза. Использование желчного пузыря для наложения билиодигестивного соустья считаем нецелесообразной и в ряде случаев порочной методикой, которая может приводить к развитию поздних осложнений. Длительно существующий при такой методике замедленный желчеотток через пузырный проток и желчный пузырь приводит к формированию сладжей и конкрементов в желчном пузыре и печеночных протоках, приступам холангита, что может потребовать повторных операций с выполнением холецистэктомии, гепатиколитотомии, наложения гепатикоеюноанастомоза.
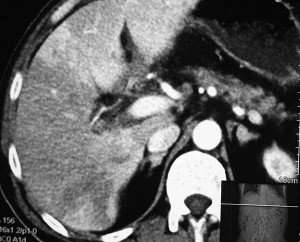
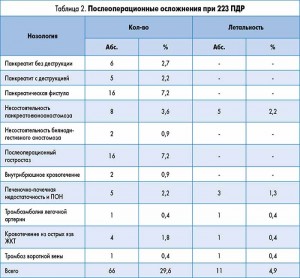
Среди других осложнений наблюдались внутрибрюшное кровотечение – у 2 пациентов (0,9%), печеночно-почечная недостаточность и ПОН – у 5 (2,2%), кровотечение из острых язв ЖКТ – у 4 (1,8%), тромбоэмболия легочной артерии – у 1 (0,4%), тромбоз воротной вены (рис. 3) – у 1 (0,4%).
Структура и частота послеоперационных осложнений показаны в таблице 2.
Поздние осложнения были связаны с такими факторами, как наличие хронического панкреатита, удаление большой части ПЖ, активность фиброгенеза в ткани ПЖ, приводящими к нарушению экзо- и эндокринной функций ПЖ. Мальдигестия наблюдалась у 8 (3,8%), мальабсорбция – у 7 (3,3%), сахарный диабет – у 15 (7,1%) больных. Для купирования поздних осложнений применялись:
♦ нормализация обмена жирных и желчных кислот, устранение проявлений дисбактериоза – дуфалак, лактувит per os;
♦ профилактика и лечение синдрома мальабсорбции (заместительная ферментотерапия) – креон, мезим форте, панзинорм;
♦ устранение синдрома раздраженной кишки (спазмолитическая терапия без угнетения тонуса кишечной стенки) – дуспаталин, метеоспазмил.
Профилактика и лечение периоперационных осложнений
На основании данной систематизации и структуризации периоперационных осложнений у наблюдаемых больных с обструктивными процессами ПДЗ была разработана программа профилактики данных осложнений. Для этого были проведены дополнительные лабораторные исследования, которые позволили выделить группы больных с различной степенью риска развития послеоперационных осложнений. Это дало возможность прогнозировать их развитие еще на дооперационном этапе и в соответствии с данным прогнозом определять хирургическую тактику в каждой из выделенных групп риска развития послеоперационных осложнений у больных с обструктивными заболеваниями ПДЗ.
С учетом проведенных дополнительных лабораторных исследований и выделенных критериев риска развития послеоперационных осложнений, а также сходных лабораторных и клинико-анамнестических данных на основании шкал APACHE II, Glasgow, Ranson, Child выделены 4 подгруппы больных с различным риском послеоперационных осложнений:
І подгруппа – с низким риском послеоперационных осложнений без исходных воспалительных изменений в ПДЗ;
ІІ подгруппа – со средним риском послеоперационных осложнений на фоне воспалительных процессов в ПДЗ (панкреатит, холангит и т.д.) без деструкции;
ІІІ подгруппа – с высоким риском послеоперационных осложнений на фоне высокого риска развития деструктивных процессов в ПДЗ (гнойный холангит, очаговый панкреонекроз, постнекротическая киста ПЖ и т.д.);
IV подгруппа – с максимальным риском послеоперационных осложнений системного характера на фоне высокого риска развития ПОН.
При анализе состояния пациентов с учетом традиционных и предложенных лабораторных критериев риска послеоперационных осложнений проводилась комплексная программа периоперационной профилактики послеоперационных осложнений.
Предоперационный период
І группа (без воспаления) – симптоматическая терапия:
♦ инфузионная терапия – реосорбилакт, гекодез;
♦ лечение болевого синдрома – но-шпа, кетанов, династат, дуспаталин (спазмолитик, не угнетающий перистальтику и тонус желчных протоков);
♦ лечение диспептического синдрома (церукал, мотилиум, смекта).
ІІ группа (воспаление без деструкции):
♦ препараты, применяемые для І группы (без воспаления);
♦ блокаторы желудочной секреции (пантопразол, рабепразол, эзомепразол);
♦ при преимущественном воспалительном поражении ПЖ (панкреатит) – левофлоксацин 500 мг в/в 1-2 раза в сут;
♦ при преимущественном воспалительном поражении билиарного тракта (холангит) – фторхинолоны, цефалоспорины III поколения;
♦ антиферментная терапия:
– ингибиторы панкреатической секреции (воздействующие на ацинарную клетку) – октра (октрайд, октреотид, октрестатин, сандостатин) – 0,1 мг п/к 2-3 раза в сут, соматулин – однократно), позволяющие достичь ингибиции как протеолитической, так и липолитической активности ПЖ на ацинарно-клеточном уровне. Наибольшая потребность в применении ингибиторов панкреатической секреции возникала во время операции и в первые 3-5 сут после нее, когда имела место наивысшая активация ферментов ПЖ, просачивание ферментов через наложенные швы и «уклонение» их в кровеносное русло, при этом эффективно подавлялась базальная и стимулированная секреция ПЖ, предотвращая или значительно снижая вероятность развития послеоперационного деструктивного панкреатита и несостоятельности швов ПЕА;
– ингибиторы протеолитической секреции (инактивирующие ферменты в крови) – контрикал, гордокс, контривен. Эти препараты оказались менее эффективными, так как действуют только в кровяном русле, не влияя на секрецию ПЖ, и не обладают универсальными ингибирующими свойствами, особенно в отношении активной эластазы, липазы и фосфолипазы А;
♦ дезинтоксикационная инфузионная терапия (реосорбилакт, гекотон, волютенз, рефортан, йоностерил);
♦ при наличии механической желтухи – викасол 1,0 п/к в течение 3 сут перед операцией, инфузия свежезамороженной плазмы;
♦ при явлениях гепатита – гепатопротекторы: гептрал, ларнамин, глутаргин (не усиливают внутрипеченочный холестаз в отличие от фосфолипидов, в том числе эссенциале);
ІІІ группа (высокий риск деструкции):
♦ терапия, применяемая для ІІ группы (воспаление без деструкции);
♦ усиление антиферментной терапии с улучшением микроциркуляции и противоотечной терапии ПЖ (миакальцик 100 ед в/в 2 раза в сут, обладающий также выраженным анальгезирующим эффектом);
♦ деэскалационная антибиотикотерапия: левофлоксацин (лефлоцин, локсоф) – 500 мг 1 раз в сут; моксифлоксацин (авелокс); гатифлоксацин (бигафлон) и ротация: имипенем, максипим, фортум;
♦ антицитокиновая терапия – пентоксифиллин в/в 2 раза в сут;
♦ антиадгезивная терапия – лонгидаза. Антиоксидантный эффект лонгидазы реализовался за счет способности активного вещества связывать ионы железа, стимулировать синтез коллагена и ингибиторов гиалуронидазы. Лонгидаза оказывала выраженный противофиброзный эффект, регулировала синтез медиаторов воспаления, стимулировала гуморальный иммунитет, а также ослабляла выраженность течения острой фазы воспалительного процесса, тем самым способствуя профилактике грубого рубцевания и спаечного процесса. С антиадгезивной целью применялись дефенсаль, девискор;
♦ энтеросорбция (энтеросгель, элиминаль гель, мультисорб, дуфалак в зонд и per os);
♦ иммунокоррекция – полиоксидоний, применялся для коррекции как первичных, так и вторичных иммунодефицитных состояний.
ІV группа (высокий риск ПОН):
♦ терапия, применяемая для ІІІ группы;
♦ билиарная декомпрессия – этапная (трехэтапная) хирургическая тактика.
Интраоперационная профилактика
Антиферментная терапия (все группы) – октра (октреотид, октрайд) 0,1 мг в/в (учитывая, что длительность периода полувыведения составляет 90 мин, рекомендуем повторное введение через 1,5-2 ч от начала операции; как правило, это время совпадает с моментом пересечения ПЖ при ПДР, наложением на культю гемостатических швов и последующим наложением ПЕА).
Ранний послеоперационный период
Наряду с проведением инфузионной, антикоагулянтной, антибактериальной терапии, применением гепатопротекторов, белковых препаратов (альбумин, плазма), препаратов, улучшающих микроциркуляцию, применялись следующие схемы антиферментной терапии:
І группа – сандостатин 0,1 мг п/к 2 раза;
ІІ группа – сандостатин 0,1 мг п/к 2 раза, даларгин по 1 мг 2 раза в день в/м;
ІІІ и ІV группы – сандостатин 0,1 мг п/к 3 раза, даларгин по 1 мг 2 раза в день в/м.
Таким образом, ранний прогноз и соответствующая профилактика послеоперационных осложнений на дооперационном этапе с выбором хирургической тактики в зависимости от предложенных групп риска развития прогнозируемых послеоперационных осложнений позволили снизить количество послеоперационных осложнений, значительно уменьшив их тяжесть, сократив койко-день и улучшив качество жизни больных.
Проведенный анализ периоперационных осложнений при ПДР позволил обобщить данные осложнения, детализировать причины их развития и определить основные направления их профилактики и лечения в дооперационном и послеоперационном периодах.
Литература
1. Велигоцкий Н.Н. Обструктивные заболевания органов панкреатодуоденальной зоны / Н.Н. Велигоцкий, А.Н. Велигоцкий // Харьков: Планета-Принт, 2015. – 136 с.
2. Гальперин Э.И. Лекции по гепатопанкреатобилиарной хирургии / Э.И. Гальперин, Т.Г. Дюжева. – М.: Видар, 2011. – 536 с.
3. Осложнения панкреатодуоденальной резекции и возможные пути их предупреждения / А.Б. Кутовой, А.В. Снисарь, В.А. Пелех и др. / Харківська хірургічна школа. – 2016. – № 2 (77). – С. 38-42.
4. Послеоперационный панкреатит при хирургических вмешательствах на поджелудочной железе / А.Г. Кригер, В.А. Кубышкин, Г.Г. Кармазановский и др. // Хирургия. – 2012. – № 4. – С. 14-19.
5. Профілактика ускладнень після панкреатодуоденальної резекції / В.М. Копчак, К.В. Копчак, І.В. Хомяк та ін. // Клінічна хірургія. – 2014. – № 5. – С. 29-31.
6. Haigh P.I. Early postoperative outcomes after pancreaticoduodenectomy in the elderly / P.I. Haigh, K.Y. Bilimoria, L.A. DiFronzo // Arch Surg 2011. – V. 146, № 6. – P. 715-723.
7. Perioperative and long-term outcomes after pancreaticoduodenectomy in elderly patients 80 years of age and older / S. Oguro, K. Shimada, Y. Kishi et al. // Langenbecks Arch. Surg. – 2013. – V. 398 (4). – P. 531-538.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...