Якість життя, пов’язана зі здоров’ям, у пацієнтів із рецидивуючою або рефрактерною множинною мієломою: лікування даратумумабом, леналідомідом і дексаметазоном у дослідженні III фази POLLUX
Множинна мієлома (ММ) може асоціюватися з тяжкими симптомами, які часто негативно впливають на якість життя пацієнтів (health-related quality of life, HRQoL). Пацієнти з рецидивуючою/рефрактерною ММ (ррMM), можливо, неодноразово лікувались, що може бути пов’язане з проблемами, які впливають на якість життя, включаючи соціальне функціонування, емоційний і фізичний комфорт та фінансове навантаження. Результати, про які повідомляють пацієнти, дають більш повне розуміння якості життя, і їх слід розглядати разом з ефективністю та безпекою при оцінюванні здатності нових схем лікування полегшувати стан пацієнтів з ррMM.
Пацієнти з нещодавно діагностованою ММ, як правило, мають виражену симптоматику і низький рівень якості життя; покращення якості життя у цій популяції є важливою метою лікування. У цих хворих оптимальним є лікування, яке сприятиме досягненню нової ремісії без негативного впливу на якість життя.
Даратумумаб – моноклональне антитіло, спрямоване на IgGj CD38 людини, із прямими протипухлинними та імуномодулюючими механізмами дії. У дослідженні III фази POLLUX даратумумаб у комбінації з леналідомідом і дексаметазоном (D-Rd) забезпечував вищу виживаність без прогресування (ВБП) порівняно з тільки леналідомідом і дексаметазоном (Rd). Комбінація D-Rd продовжувала демонструвати тривалу ВБП, вищий загальний коефіцієнт відповіді, вищу повну відповідь або кращі, а також вищі негативні показники мінімальної залишкової хвороби порівняно з Rd після більш ніж 3 років спостереження. У цій статті ми оцінюємо вплив тривалого лікування D-Rd проти Rd на повідомлені пацієнтами результати (Patient-reported outcomes, PRO) у дослідженні POLLUX.
Матеріали і методи
Пацієнти та дизайн дослідження. Подробиці дослідження POLLUX були описані раніше. POLLUX – це рандомізоване відкрите активно контрольоване паралельно-групове багатоцентрове дослідження III фази за участю пацієнтів з ррMM. Дорослих пацієнтів з ррMM рандомізували у співвідношенні 1:1 для призначення тривалих циклів лікування (один цикл 28 днів) D-Rd або Rd до прогресування захворювання, відкликання згоди пацієнта, неприпустимої токсичності або смерті. Даратумумаб вводили внутрішньовенно у дозі 16 мг/кг маси тіла 1 раз на тиждень протягом 8 тижнів (цикли 1-2), потім через тиждень протягом 16 тижнів (цикли 3-6) та через кожні 4 тижні після цього. Пацієнти в групах D-Rd і Rd отримували леналідомід у дозі 25 мг перорально у 1-21-й дні кожного циклу та дексаметазон у дозі 40 мг перорально 1 раз на тиждень.
Повідомлені пацієнтами результати. PRO були оцінені як вторинні кінцеві точки в дослідженні POLLUX і зібрані за допомогою затвердженої Європейською організацією з вивчення і лікування онкологічних захворювань анкети якості життя (EORTC QLQ-C30) та анкети EuroQol (EQ‑5D‑5L).
EORTC QLQ-C30 – це специфічний для онкологічних пацієнтів інструмент оцінки якості життя, який складається із 30 пунктів, що включають 5 функціональних шкал (фізичну, рольову, емоційну, когнітивну та соціальну), 1 шкалу загального стану здоров’я (GHS), 3 шкали симптомів (втома, нудота, блювання та біль) і 6 окремих характеристик (задишка, безсоння, втрата апетиту, запор, діарея та фінансові труднощі). Пацієнти згадували про свій досвід попереднього тижня, і оцінки відображалися на шкалі від 0 до 100.
EQ‑5D‑5L – це оцінка стану здоров’я за 5 вимірами, також включає візуальну аналогову шкалу (VAS).
Пацієнти заповнювали анкети на базовому етапі та в 1-й день кожного циклу лікування.
Результати
Базові характеристики та показники відповідності PRO. Всього 569 пацієнтів було рандомізовано на лікування комбінацією D-Rd (n=286) або Rd (n=283). Базові характеристики двох груп були добре збалансовані. Середній вік учасників становив 65 років (діапазон 34-89 років), вік 11,2% учасників ≥75 років; 59,2% пацієнтів були чоловіками, а 44,6% осіб мали вихідний рівень ECOG 1. Базові значення для EORTC QLQC30 GHS, функціональної шкали, шкали симптомів та EQ‑5D‑5L VAS у групах D-Rd та Rd були зіставними. Відповідність оцінкам PRO була однаковою в обох групах лікування: показники >88% на початковому етапі та >75% протягом 40-го циклу (156-й тиждень). Серед пацієнтів групи D-Rd базові показники GHS, фізикального стану, болю та втоми були кращими у пацієнтів з однією попередньою лінією терапії, ніж в осіб з принаймні двома попередніми лініями терапії.
Вплив лікування на оцінку за шкалою EORTC QLQ-C30
Популяція PRO ITT (аналіз результатів щодо наміру початкового лікування, Intention-to-treat). Медіана часу до значущого поліпшення бала GHS при терапії D-Rd становила 6,6 міс, а при Rd – 6,5 міс (відношення ризиків – ВР – 1,02; 95% довірчий інтервал – ДІ – 0,81-1,29; P=0,8376). Медіана часу до значущого зниження бала GHS становила 4,7 міс в обох групах (ВР 0,92; 95% ДІ 0,74-1,14; P=0,4250).
Зміна середнього значення, обчислена за методом найменших квадратів (Least squares, LS, 95% ДІ), порівняно з вихідним рівнем оцінок EORTC QLQ-C30 GHS дещо знизилася у циклах 2, 3 та 6 для групи Rd і циклах 2, 3 та 4 для групи D-Rd з тенденцією до покращення GHS у групі D-Rd та стабілізацією у групі Rd (рис. А) після циклу 6. Різниця між групами лікування становила від 3,4 до 4,8 і була істотною на користь D-Rd у циклах 11, 13, 14, 18, 31, 36 та 37 (Р<0,05 для всіх). Зміни середнього значення LS від вихідного рівня для оцінки болю EORTC QLQ-C30 були більшими при використанні D-Rd, ніж Rd у більшість моментів оцінки (рис. Б). Різниця оцінки болю між групами була значною на користь D-Rd у багатьох часових точках між циклами 13 та 40, але більшість змін порівняно з вихідним рівнем становили менше 5 балів (рис. Б). Крім того, середні значення LS у функціональних показниках і показниках симптомів неістотно відрізнялись між групами лікування.
Частка пацієнтів, які зазнали значних змін GHS порівняно з початковим рівнем, була більшою при лікуванні D-Rd, ніж Rd в усі моменти оцінки; різниця між групами була статистично значущою у циклах 10 (34,8 проти 23,3%), 11 (33,8 проти 21,8%) та 13 (38,3 проти 24,0%; P<0,05 для всіх). У циклі 5 більша частина пацієнтів у групі D-Rd, ніж у групі Rd, зазнала істотних змін в оцінці когнітивної функції (29,4 проти 16,6%; Р=0,0016); в іншому випадку відмінності між групами не були значними для будь-якої з функціональних шкал. Частка пацієнтів з істотним поліпшенням статусу щодо болю у циклі 3 та діареї у циклах 3-6 та 11 була більшою у групі D-Rd, ніж Rd. Інші відмінності між групами у частці пацієнтів, які зазнали істотних змін в оцінках симптомів, не були статистично значущими. Частка пацієнтів з істотним поліпшенням оцінки болю була найбільшою: 32,6-43,1% пацієнтів у групі D-Rd та 26,8-38,7% хворих у групі Rd спостерігали поліпшення ≥10 балів.
Підгрупи. LS означає середні зміни порівняно з вихідним рівнем GHS, функціональної активності й оцінки симптомів у підгрупах за віком (<65 проти ≥65 років), ECOG (0 або 1 проти 2) та ступенем відповіді (≥VGPR – дуже добра часткова відповідь або краща проти ≥PR – часткова відповідь або краща); зазначені показники були подібні до таких у загальній когорті пацієнтів. В обох групах лікування зміни в порівнянні з вихідними величинами, як правило, були на користь пацієнтів молодшого віку щодо GHS, емоційних, когнітивних і соціальних показників функціонування, а також оцінки болю та втоми. Пацієнти з ефективністю лікування ≥VGPR, як правило, мали більш значне покращення (або менше погіршення), ніж пацієнти з ≥PR, за показниками GHS та болю, незалежно від групи лікування. Це також стосувалося показників фізичного, рольового й соціального функціонування та втоми в групі D-Rd, але не в групі Rd.
Вплив лікування на показники EQ‑5D‑5L VAS
Популяція PRO ITT. Середній час до значущого покращення показника EQ‑5D‑5L VAS при лікуванні D-Rd становив 6,9 проти 9,3 міс при використанні Rd (ВР 1,16; 95% ДІ 0,91-1,47; P=0,2349), а медіана часу до значущого зменшення становила 4,9 проти 4,7 міс (ВР 0,94; 95% ДІ 0,76-1,17; Р=0,5849). Середні показники EQ‑5D‑5L VAS підтримувались при лікуванні як у групі D-Rd, так і Rd (рис. В). Величина змін від базового рівня не тільки не перевищувала MID ≥10 балів, а й 5 балів. Точкові оцінки свідчили про перевагу D-Rd у всі моменти оцінки з циклу 4 по цикл 40. Зміни в балах VAS були істотними на користь групи D-Rd порівняно з групою Rd у циклах 11 (2,4 проти 1,7), 13 (2,2 проти 1,6), 14 (2,1 проти 1,5), 15 (2,4 проти 1,4), 34 (1,0 проти 3,1) та 40 (2,6 проти 2,9; Р<0,05 для всіх).
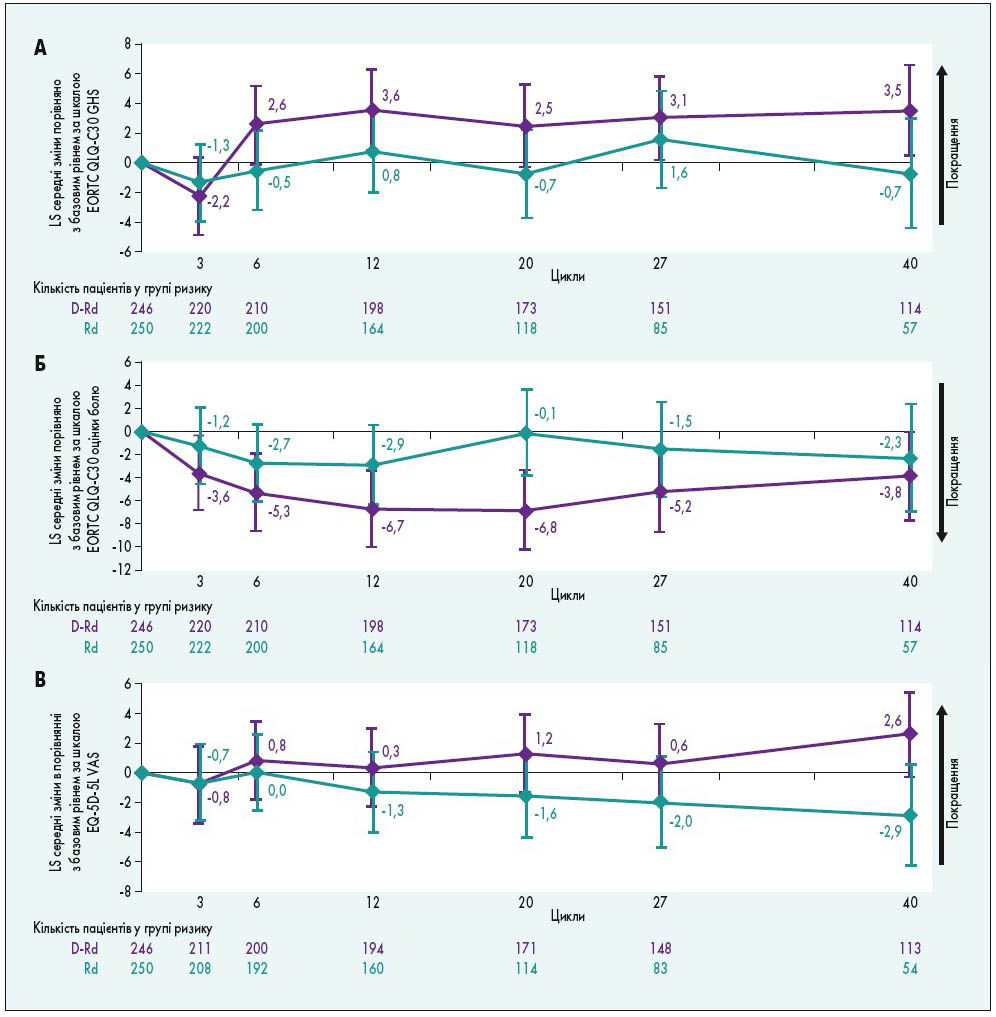 Рис. Зміна показників від базового рівня: A – оцінка за EORTC QLQ-C30 GHS; Б – оцінка болю за EORTC QLQ-C30; В – оцінка за EQ-5D-5L VAS у циклі 40
Рис. Зміна показників від базового рівня: A – оцінка за EORTC QLQ-C30 GHS; Б – оцінка болю за EORTC QLQ-C30; В – оцінка за EQ-5D-5L VAS у циклі 40
Підгрупи. Незалежно від групи лікування, зміни показника VAS порівняно з вихідними значеннями, як правило, переважали у молодих пацієнтів, пацієнтів з 0 або 1 за ECOG та пацієнтів з ≥VGPR. Ми досліджували взаємозв’язок суми балів за шкалою ECOG та відношення до вікової підгрупи з групою лікування у своїй моделі змішаних ефектів, що оцінює вплив лікування на якість життя. Значна взаємодія (р<0,05) спостерігалася для підгруп ECOG та EQ‑5D‑5L VAS, а також когнітивних функцій, емоційної оцінки, втоми та нудоти/блювання за EORTC QLQ-C30. Вік пацієнтів істотно асоціювався лише з показниками EQ‑5D‑5L VAS.
Обговорення
Загалом істотних поліпшень показника HRO при ррMM не спостерігалось. Були значні відмінності між групами базових показників за EORTC QLQ-C30 GHS, функціональних показників, оцінок симптомів та EQ‑5D‑5L VAS протягом декількох періодів під час лікування. Для пацієнтів, які продовжували лікуватися, відсутність негативного впливу упродовж тривалого часу (45 циклів, 176 тижнів) ілюструє, що клінічні переваги, отримані при застосуванні D-Rd, не досягнуті за рахунок якості життя, а також підтримує тривале використання цього режиму у хворих на ррMM. Загалом результати аналізу підгруп відповідали таким загальної когорти пацієнтів для більшості шкал EORTC QLQ-C30 із тенденцією до більших покращень або меншого погіршення серед молодих пацієнтів порівняно зі старшими. Пацієнти з ≥VGPR, особливо у групі D-Rd, також, як правило, мали кращі показники, ніж хворі з ≥PR, що узгоджується з даними попередніх досліджень, у яких виявлено кращу якість життя у пацієнтів з більшою відповіддю.
Загалом базові показники EORTC QLQ-C30 для GHS, фізичного, рольового та соціального функціонування, а також болю і втоми були гіршими в дослідженні POLLUX, ніж в осіб без пухлин, що відповідає порушенню якості життя, пов’язаному з ММ. Однак інші вихідні показники були зіставними в учасників дослідження POLLUX та пацієнтів без пухлин, була вищою й оцінка емоційного функціонування. Крім того, вихідні показники EORTC QLQ-C30 були кращими у пацієнтів з POLLUX, ніж у референтної популяції пацієнтів з ММ, і можуть відображати їх рецидивний/рефрактерний статус.
Виявлено відносну відсутність істотних розбіжностей між групами щодо PRO, на відміну від клінічних результатів, які були значно кращими при використанні D-Rd, ніж Rd у дослідженні POLLUX. Можливою причиною відсутності додаткової переваги щодо якості життя при застосуванні D-Rd порівняно з Rd може бути те, що це був аналіз під час лікування. Пацієнти, які продовжували лікування, досягли відповіді та, ймовірно, мали однаковий рівень якості життя, незалежно від режиму терапії.
Поліпшення показників GHS, фізичного функціонування та болю було більш значним у групі D-Rd у різний час, однак у кожній групі лікування величина цих змін не перевищувала середньопорогового значення ≥10 балів. Можна припустити, що ці зміни мали мінімальний вплив на якість життя як у групі D-Rd, так і у групі Rd. Навіть якби до результатів POLLUX застосовували нижчий поріг середнього значення у 5 балів, зміни балів GHS від вихідного рівня все одно не вважатимуться значущими в будь-який момент часу для будь-якої групи лікування. Зміни показників фізичного функціонування вважалися б значущими у групі Rd у циклах 35 та 37, тоді як зміни в оцінці болю вважалися б значущими в більшості моментів із циклів 5-39 у групі D-Rd.
PRO є важливими для оцінки якості життя, але часто не враховують відсутність даних з аналізів, потенційне зміщування вимірювання та пропущені критерії звітування, які можуть потенційно покращити результати майбутніх досліджень PRO. Вплив лікування за схемами на основі Rd на PRO при ррMM вивчався раніше; загалом подібні до POLLUX, ці дослідження продемонстрували підтримку даних щодо якості життя та незначну різницю в них між експериментальними та контрольними групами під час лікування. У дослідженні ASPIRE порівнювали застосування карфілзомібу + Rd лише з Rd. Час до погіршення показника GHS був довшим при застосуванні карфілзомібу + Rd, ніж при Rd (10,3 проти 4,8 міс; ВР 0,80; 95% ДІ 0,65-0,98; Р=0,03). Міжгрупові відмінності для інших шкал EORTC QLQ-C30 не були істотними. Серед хворих, які отримували карфілзоміб + Rd, пацієнти з більш глибокою відповіддю мали кращі показники GHS; цього не спостерігалося в групі Rd. Leleu та співавт. повідомляли про показники якості життя у дослідженні TOURMALINE-MM1, в якому пацієнти отримували лише іксазоміб + Rd або плацебо + Rd. Результати GHS зберігались протягом курсу лікування без істотних відмінностей між групами лікування. Загалом бали за функціональною шкалою та шкалою симптомів також зберігались, за винятком когнітивних функцій, які в обох групах відхилялись від вихідних значень. Якість життя у пацієнтів з прогресуючим захворюванням була гіршою, ніж в осіб із клінічною відповіддю.
У дослідженні ELOQUENT‑2 порівнювали використання елотузумабу + Rd лише з Rd. Показники GHS, втоми, фізичного функціонування та болю залишались відносно незмінними порівняно з вихідними в обох групах, значних відмінностей між групами в будь-який момент не було. До циклу 30 змін на >10 балів не було.
Це дослідження мало кілька обмежень. РRО в дослідженні POLLUX оцінювались як вторинні кінцеві точки, і можливості виявляти відмінності між групами лікування не було. Аналіз підгруп за віком, ECOG та відповіддю на лікування проводився post hoc. РRО оцінювали лише у пацієнтів, які перебували на лікуванні (пацієнти були піддані цензурі з аналізу РRО після припинення досліджуваного лікування); тому РRО не враховували прогресування захворювання, що частіше траплялось у хворих, які отримували Rd. Крім того, пацієнти були обізнані щодо призначення свого лікування, і обидві групи застосовували активне лікування, що могло вплинути на оцінювання якості життя; однак є обмежені докази щодо РRО в онкологічних дослідженнях.
Базові показники якості життя зберігались у пацієнтів з ррMM протягом тривалого періоду після лікування D-Rd та Rd. Наші результати демонструють, що тривале лікування (>3 роки) D-Rd або Rd не призвело до будь-якого зменшення показника якості життя, ілюструючи значення цих схем лікування у пацієнтів з ррMM. Однак важливо, що більша кількість хворих групи Rd, ніж групи D-Rd, перенесли прогресуюче захворювання і, отже, перейшли на наступну лінію терапії. Ці PRO доповнюють стійке і значне покращення результатів виживання протягом 3 років спостереження у дослідженні POLLUX, включаючи ВБП, вищу та тривалішу відповідь на лікування.
За матеріалами Plesner T. et al. Health-related quality of life in patients with relapsed or refractory multiple myeloma: treatment with daratumumab, lenalidomide, and dexamethasone in the phase 3 POLLUX trial. British Society for Haematology and John Wiley & Sons Ltd. 2021. doi: 10.1111/bjh.17435.
Підготував Назар Лукавецький
CP-228753
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 2 (69) 2021 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




