Роль імунотерапії у лікуванні меланоми шкіри
12-14 березня на міжнародній медичній науково-освітній платформі Medical Knowledge Hub відбулася друга Школа дерматоонкології. Онлайн-захід був орієнтований на лікарів, які займаються діагностикою та лікуванням пухлин шкіри, а саме дерматологів, онкологів, онкохірургів, патоморфологів, суміжних спеціалістів. Особливою подією школи став сателітний симпозіум компанії MSD, у рамках якого провідні фахівці висвітлили сучасні погляди на діагностику та лікування меланоми.
 Дерматоонколог, асистент кафедри дерматовенерології, клінічної, лабораторної імунології та алергології Національного університету охорони здоров’я України імені П.Л. Шупика, директор клініки персоналізованої медицини EuroDerm (м. Київ) Богдан Вікторович Литвиненко виступив із доповіддю «Імунотерапія метастатичної меланоми: від теорії до практичних кроків».
Дерматоонколог, асистент кафедри дерматовенерології, клінічної, лабораторної імунології та алергології Національного університету охорони здоров’я України імені П.Л. Шупика, директор клініки персоналізованої медицини EuroDerm (м. Київ) Богдан Вікторович Литвиненко виступив із доповіддю «Імунотерапія метастатичної меланоми: від теорії до практичних кроків».
– Відповідно до наявних фахових рекомендацій, імунотерапія посідає провідне місце в лікуванні хворих із неоперабельною формою меланоми шкіри ІІІ-IV стадії. Ефективність застосування інгібітора імунних контрольних точок (білка програмованої клітинної смерті 1, PD‑1) пембролізумабу (Кітруда® компанії MSD) у пацієнтів із вказаною патологією підтверджена у дослідженнях KEYNOTE‑001, -002 та -006. Зокрема, 5-річна загальна виживаність (ЗВ) у дослідженні ІB фази KEYNOTE‑001 склала 34% у всіх хворих і 41% – у раніше не лікованих пацієнтів (рис. 1). Застосування пембролізумабу дозволило досягти об’єктивної відповіді (ОВ; кількість випадків повної відповіді, тобто зникнення всіх вогнищ ураження, підтверджене за допомогою комп’ютерної томографії, проведеної з інтервалом понад 4 тижні + кількість випадків часткової відповіді, тобто зменшення вогнищ не менше ніж на 30%) у 41% пацієнтів і контролю захворювання (кількість випадків повної відповіді + кількість випадків часткової відповіді + кількість випадків стабілізації захворювання, яка полягає у відсутності прогресування) – у 65%, а при його використанні як першої лінії лікування – у 52 та 72% відповідно. Частота повної відповіді у разі призначення пембролізумабу в першій лінії терапії становила 17%.
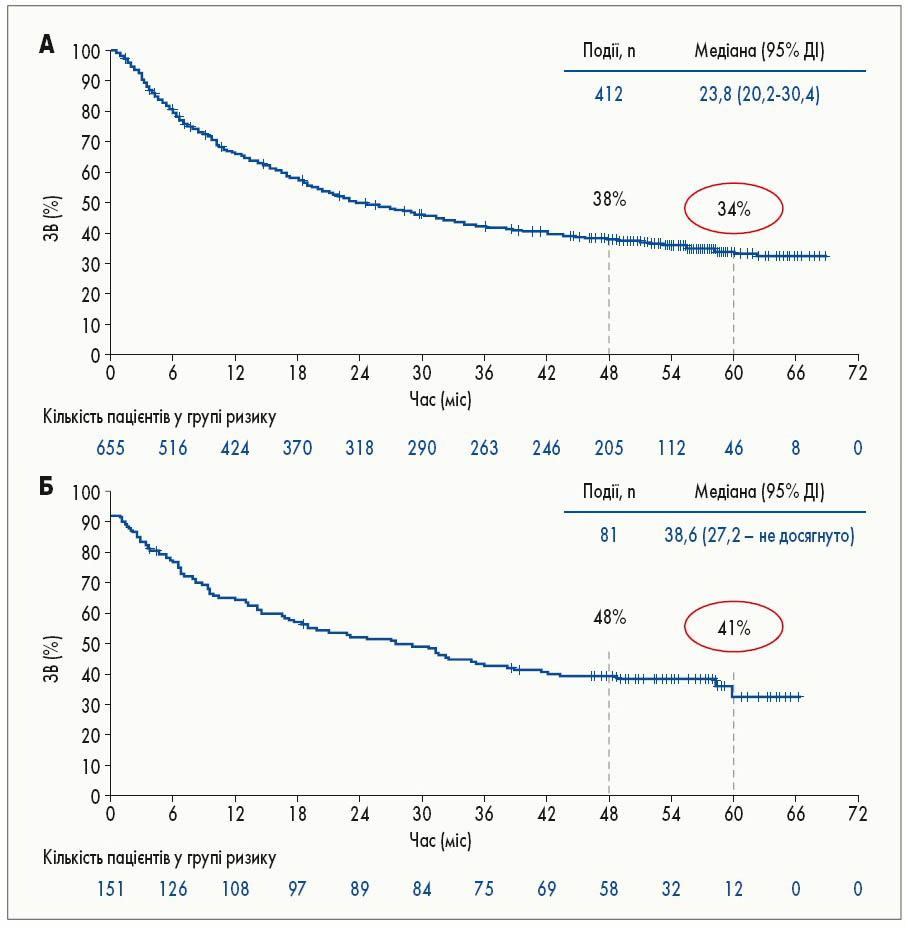 Рис. 1. П’ятирічна ЗВ у дослідженні KEYNOTE‑001: А – у загальній популяції учасників (n=655); Б – у раніше не лікованих пацієнтів (n=151)
Рис. 1. П’ятирічна ЗВ у дослідженні KEYNOTE‑001: А – у загальній популяції учасників (n=655); Б – у раніше не лікованих пацієнтів (n=151)
П’ятирічна виживаність без прогресування (ВБП) сягала 21% у загальній популяції та 29% у раніше не лікованих осіб. При застосуванні пембролізумабу доволі швидко вдалося досягти відповіді на лікування. Так, медіана часу до отримання відповіді на терапію пембролізумабом становила 2,8 міс, а медіана тривалості відповіді досягнута не була. Відповідь на лікування зберігалась у 73% раніше лікованих пацієнтів та у 82% осіб, у яких пембролізумаб застосовували у першій лінії. У пацієнтів, які досягли повної відповіді на лікування, вона зберігалась у 89% осіб. При цьому 19% осіб продовжують використання пембролізумабу, 17% – припинили лікування через появу побічних реакцій, прогресування або з іншої причини, а 64% припинили лікування та перебувають під спостереженням. Незважаючи на те що частота небажаних явищ, пов’язаних із лікуванням, склала 86%, 3-4 ступінь токсичності відзначено лише у 17% хворих і тільки 7,8% з них потребували відміни лікування (O. Hamid et al., 2019).
Рандомізоване дослідження II фази KEYNOTE‑002 включало пацієнтів із поширеною меланомою та позитивним статусом за BRAF V600, у яких зафіксовано прогресування захворювання на тлі застосування іпілімумабу та комбінованої анти-BRAF терапії. У цьому дослідженні порівнювали ефективність терапії пембролізумабом у дозі 2 мг/кг маси тіла, пембролізумабом 10 мг/кг і хіміотерапії. Дизайн допускав перехід пацієнтів із прогресуванням захворювання на тлі хіміотерапії на прийом пембролізумабу. На момент оцінювання результатів (30 травня 2018 р.) загальна відповідь була досягнута у 22,7% пацієнтів групи пембролізумабу. ВБП склала 16,9% через 36 міс та 15% через 48 міс, а ЗВ сягала 30,3 та 27,2% через 36 та 48 міс відповідно (A. Ribas et al., 2018).
У дослідженні III фази KEYNOTE‑006, у якому порівнювали терапію пембролізумабом (10 мг/кг через кожні 2 тижні або 10 мг/кг через кожні 3 тижні) й іпілімумабом (3 мг/кг через кожні 3 тижні, всього 4 введення), у групі пембролізумабу вдалося досягти 5-річної ЗВ 32,7 міс порівняно з 15,9 міс у групі іпілімумабу (рис. 2). При цьому у пацієнтів, які отримували першу лінію лікування, медіана ЗВ становила 38,7 міс у групі пембролізумабу та 17,1 міс – іпілімумабу, а у раніше лікованих осіб – 23,5 та 13,6 міс відповідно.
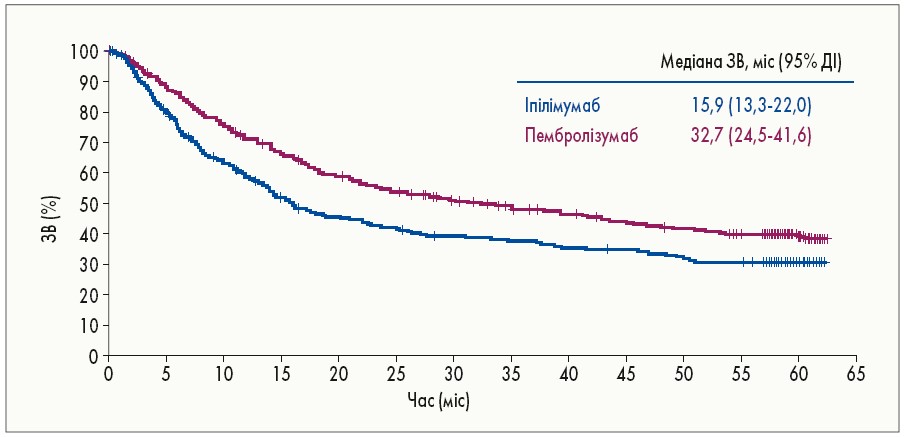 Рис. 2. П’ятирічна ЗВ у дослідженні KEYNOTE‑006
Рис. 2. П’ятирічна ЗВ у дослідженні KEYNOTE‑006
ОВ на лікування досягла 42% у групі пембролізумабу та лише 17% у групі іпілімумабу, а її частота була вищою у раніше не лікованих пацієнтів (46%) ніж у пацієнтів, які отримували другу лінію терапії. Всі пацієнти, у яких досягнута повна відповідь на лікування після 2-річного прийому пембролізумабу, залишались живими на момент 5-річного спостереження. Також варто зауважити, що повторне призначення пембролізумабу після прогресування захворювання дозволяє досягнути його контролю у 80% пацієнтів (G.V. Long, 2018).
Клінічний випадок
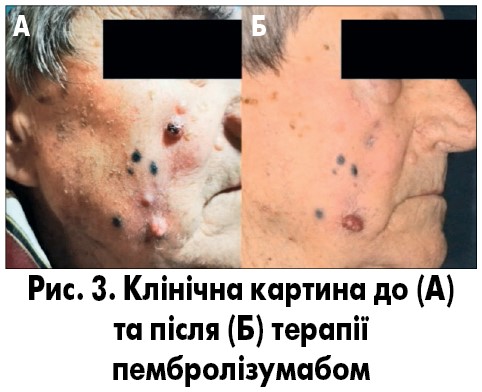 Пацієнт 90 років. В анамнезі – множинні епізоди базальноклітинного раку шкіри. У лютому 2020 р. було проведено ексцизійну біопсію та видалення пігментного утворення шкіри правої щоки і встановлено діагноз поверхнево-поширена меланома шкіри у фазі вертикального росту (pT4b). У вересні 2020 р. пацієнт помітив появу пігментації та вузлів у зоні хірургічного втручання та збільшення регіонарних лімфатичних вузлів. У жовтні 2020 р. пацієнт звернувся у клініку EuroDerm, де його було дообстежено та розпочато терапію пембролізумабом у дозі 200 мг. Станом на 10 березня 2021 р. отримав 6 інфузій препарату. Під час та після лікування побічних ефектів і змін лабораторних показників не відзначено. Клінічно спостерігали регресування двох верхніх вузлів, нижній вузол значно зменшився, а вузлик над ним зник. Окрім цього, відбувається регресування пігментних елементів (рис. 3).
Пацієнт 90 років. В анамнезі – множинні епізоди базальноклітинного раку шкіри. У лютому 2020 р. було проведено ексцизійну біопсію та видалення пігментного утворення шкіри правої щоки і встановлено діагноз поверхнево-поширена меланома шкіри у фазі вертикального росту (pT4b). У вересні 2020 р. пацієнт помітив появу пігментації та вузлів у зоні хірургічного втручання та збільшення регіонарних лімфатичних вузлів. У жовтні 2020 р. пацієнт звернувся у клініку EuroDerm, де його було дообстежено та розпочато терапію пембролізумабом у дозі 200 мг. Станом на 10 березня 2021 р. отримав 6 інфузій препарату. Під час та після лікування побічних ефектів і змін лабораторних показників не відзначено. Клінічно спостерігали регресування двох верхніх вузлів, нижній вузол значно зменшився, а вузлик над ним зник. Окрім цього, відбувається регресування пігментних елементів (рис. 3).
Значне зменшення уражених лімфатичних вузлів і стабілізація процесу були також підтверджені при проведенні комп’ютерної томографії після 4 інфузій пембролізумабу.
Таким чином, імунотерапія з використанням інгібітора імунних контрольних точок PD‑1 пембролізумабу продемонструвала високу протипухлинну активність, яка зберігалась навіть після її припинення та при повторному призначенні препарату.
 Принципи ад’ювантної імунотерапії (АІТ) при меланомі шкіри висвітлив онкохірург, співробітник науково-дослідного відділення онкоортопедії, пухлин шкіри та м’яких тканин Національного інституту раку (м. Київ), кандидат медичних наук Василь Васильович Остафійчук.
Принципи ад’ювантної імунотерапії (АІТ) при меланомі шкіри висвітлив онкохірург, співробітник науково-дослідного відділення онкоортопедії, пухлин шкіри та м’яких тканин Національного інституту раку (м. Київ), кандидат медичних наук Василь Васильович Остафійчук.
– Незважаючи на наявні можливості лікування, меланома залишається причиною понад 60 тис. випадків смерті щорічно. Однією із причин високої смертності є пізнє звернення пацієнтів у лікувальні заклади. Так, згідно з даними за 2016 р., із 140 850 уперше виявлених хворих із меланомою у США, Японії, Франції, Німеччині, Італії, Іспанії та Великобританії у 8,2% випадків діагноз було встановлено на ІІІ стадії, коли тільки хірургічного лікування вже не достатньо.
Згідно з 8-ю версією класифікації Американського об’єднаного комітету з раку (AJCC), сьогодні виділяють ІІІА, ІІІB, IIIC та IIID стадії меланоми, ЗВ при кожній із яких значно різниться. Так, якщо 5-річна ЗВ при ІІІА стадії сягає 93%, а 10-річна – 88%, то при ІІІD вона знижується до 32 та 24% відповідно. Рецидиви меланоми ІІІА, ІІІВ та ІІІС стадій через 5 років виявляють у 35; 75 та 90% випадків відповідно. Саме тому у пацієнтів із меланомою ІІІ стадії вагоме значення надається АІТ.
Історія розвитку АІТ бере початок у 1995 р., коли Управління з контролю якості харчових продуктів і лікарських препаратів США зареєструвало використання інтерферону альфа (ІНФ-α) в ад’ювантному режимі. Проте покращення ЗВ та ВБП при застосуванні ІНФ-α у низьких дозах доведено не було, тоді як високі дози ІНФ-α покращували лише ВБП та тільки у разі виразкових форм IIB-IIC стадій. Сьогодні ІФН-α не включений у стандарти надання допомоги хворим із меланомою шкіри.
Останнім часом спектр опцій лікування метастатичної меланоми значно розширився. Так, до основного хірургічного методу поступово додано променеву, хіміотерапію, а згодом і стереотаксичну радіохірургію, яка свого часу стала проривом у лікуванні хворих на меланому, зокрема із метастазами у головному мозку. Також з’явились клінічні дослідження, присвячені такому методу лікування меланоми, як використання онколітичних вірусів. Сьогодні включення пацієнтів у клінічні дослідження залишається пріоритетом, особливо у країнах із низьким рівнем економічного розвитку, та дозволяє отримувати лікування із використанням новітніх методів. Такими методами є імунотерапія, яка включає використання блокаторів PD‑1 (пембролізумаб та ніволумаб) та цитотоксичного Т-лімфоцитасоційованого антигену 4 (CTLA-4; іпілімумаб), а також таргетна терапія інгібіторами BRAF-кінази (вемурафеніб, дабрафеніб) як у монорежимі, так і в комбінації з інгібіторами МЕК-кінази (кобіметиніб, траметиніб).
Дія інгібіторів BRAF- та МЕК-кінази специфічно спрямована на блокування сигнального шляху мітогенактивованої протеїнкінази (MAPK), що виникає внаслідок мутації BRAF V600 та зумовлює неконтрольовану проліферацію клітин і блокування апоптозу. На відміну від таргетної, імунотерапія діє не на саму пухлину, а на клітини імунної системи. Зокрема, використання CTLA‑4 та PD‑1-інгібіторів контрольних точок, так зване блокування контрольних точок, шляхом збільшення кількості Т-клітин сприяє стимуляції протипухлинної імунної відповіді.
У 2015 р. анти‑CTLA‑4 препарати визнано проривом у АІТ меланоми. Їх застосування порівняно з плацебо знизило ризик смерті на 28%, прогресування захворювання – на 24%, сприяло збільшенню безрецидивної виживаності (БРВ) приблизно на 10% та ЗВ – на 11%. Проте застосування анти‑CTLA‑4 препаратів супроводжувалось вираженою токсичністю. Так, побічні прояви 3-4 ступеня виникали у 54,1% пацієнтів, при цьому у 46,1% вони були представлені реакціями з боку імунної системи. Загалом смертність, пов’язана з імуноопосередкованими побічними проявами анти-CTLA‑4 лікування, склала 1,1% (A.M.M. Eggermont et al., 2016), що зумовило необхідність продовжити пошук менш токсичних препаратів для АІТ.
Принципово новим підходом в АІТ меланоми стало використання анти-PD-1 препарату пембролізумабу. У вересні 2020 р. на онлайн-конгресі Європейського товариства медичної онкології (ESMO) було представлено результати дослідження ІІІ фази EORTC1325-MG/KEYNOTE‑054, які засвідчили ефективність використання пембролізумабу як АІТ. Критеріями включення у це дослідження слугували гістологічно підтверджена меланома шкіри ІІІА, ІІІВ, ІІІС стадії та метастази у лімфатичних вузлах (транзиторні метастази відсутні) після повної регіонарної лімфодисекції. Загалом було залучено 1019 пацієнтів, яких рандомізували на 2 групи. Хворі однієї групи отримували 200 мг пембролізумабу через кожні 3 тижні впродовж 1 року, а другої – плацебо у такому ж режимі. При медіані спостереження 3,5 року застосування пембролізумабу значно подовжувало БРВ у хворих із III стадією меланоми високого ризику. Так, у групі пембролізумабу БРВ склала 59,8 проти 41,4% у групі плацебо (відношення ризиків – ВР – 0,59; 95% довірчий інтервал – ДІ – 0,49-0,70; P<0,001; рис. 4). Результати виявились зіставними в усіх підгрупах хворих із ІІІА, ІІІВ, ІІІС стадіями за 7-ю та 8-ю версіями класифікації AJCC та не залежали від статусу PD‑L1 і наявності чи відсутності мутації BRAF (A. Eggermont et al., 2020).
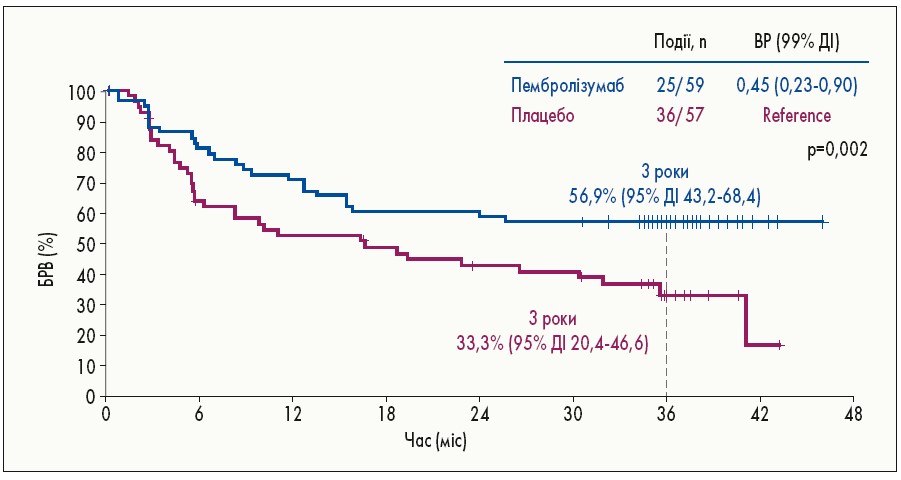 Рис. 4. БРВ у дослідженні KEYNOTE‑054
Рис. 4. БРВ у дослідженні KEYNOTE‑054
Примітно, що БРВ прямо пропорційно залежала від імуноопосередкованих побічних реакцій. Так, у групі пембролізумабу ризик рецидиву або смерті знижувався (p=0,03) після розвитку побічних проявів з боку імунної системи, наприклад ендокринних порушень, вітиліго (ВР 0,37; 95% ДІ 0,24-0,57), порівняно із таким до або без розвитку імунних побічних проявів (ВР 0,62; 95% ДІ 0,49-0,78).
За рекомендаціями NCCN (2021) та ESMO (2019), імуно- та таргетна терапія є основними методами лікування пацієнтів із неоперабельною формою меланоми. Необхідно пам’ятати, що за відсутності АІТ при меланомі ІІІ стадії ризик рецидиву становить понад 70%, а 5-річна ЗВ не перевищує 55%.
Отже, ІФН-α не довів своєї ефективності в АІТ меланоми шкіри, а анти-CTLA‑4 препарати хоча і стали проривом, підвищивши 5-річну ЗВ хворих до 65,4%, проте їх висока токсичність обмежила ефективне використання. На відміну від анти-CTLA‑4 препаратів, пембролізумаб продемонстрував менш виражену токсичність та активно використовується при меланомі III та IV стадії.
Таким чином, терапія інгібіторами PD-1 характеризується хорошою переносимістю та сприяє покращенню БРВ у хворих із III стадією меланоми високого ризику.
 Старший науковий співробітник науково-дослідного відділення пухлин шкіри і м’яких тканин Національного інституту раку (м. Київ), кандидат медичних наук Марія Миколаївна Кукушкіна розповіла про особливості ведення небажаних явищ, зумовлених імунотерапією з приводу меланоми.
Старший науковий співробітник науково-дослідного відділення пухлин шкіри і м’яких тканин Національного інституту раку (м. Київ), кандидат медичних наук Марія Миколаївна Кукушкіна розповіла про особливості ведення небажаних явищ, зумовлених імунотерапією з приводу меланоми.
– Імунотерапія міцно закріпила свої позиції у сучасних рекомендаціях щодо лікування різноманітних злоякісних новоутворень. Зокрема, сьогодні вкрай складно уявити лікування меланоми шкіри без використання CTLA‑4 та PD‑1-інгібіторів контрольних точок. Проте зворотним боком цього методу лікування є токсичність препаратів, яка проявляється імуноопосередкованим ураженням будь-яких органів і систем, а її корекція потребує мультидисциплінарного підходу. Варто зауважити, що профіль безпеки різних інгібіторів контрольних точок різниться. Зокрема, частота побічних проявів 3-4 ступеня залежно від препарату коливається від 11 до майже 60% (F.S. Hodi et al., 2010). При застосуванні іпілімумабу найчастіше спостерігали такі побічні реакції, як діарея (54%) та коліт (8-27%), а також прояви з боку шкіри (37-70%; J.R. Brahmer, 2018). Такі реакції розвиваються досить швидко, приблизно з 4-го тижня від початку лікування, а їх тривалість різна, зокрема, ендокринні ураження часто є незворотними (J.S. Weber, 2012). Що стосується пембролізумабу, то імунозалежні побічні ефекти при терапії цим препаратом виникають із частотою 86%, а побічні прояви 3-4 ступеня – 14,7% (O. Hamid et al., 2018). Серед побічних проявів найчастішими є діарея (≤19%), дисфункція щитоподібної залози (близько 10%) та ін. Гепатотоксичність, пневмоніт і нефрит при застосуванні пембролізумабу зустрічаються вкрай рідко.
Для оцінювання ступеня тяжкості побічних проявів прийнято використовувати шкалу CTCAE (Common Toxicity Criteria for Adverse Events, версія 5) Національного інституту раку США. За цією класифікацією виділяють 5 ступенів токсичності:
- 1 ступінь (легкий) – відсутність симптомів або невиражені симптоми; потребує клінічного та діагностичного спостереження; лікування не проводиться (за винятком ураження центральної нервової системи, деяких видів гематологічної та кардіотоксичності);
- 2 ступінь (помірний) – потребує проведення мінімального локального або неінвазивного втручання й обмеження фізичного навантаження. При цьому ступені лікування припиняють доти, доки побічні прояви стануть такими, що відповідають 1 ступеню тяжкості. При неможливості знизити інтенсивність токсичних проявів за допомогою симптоматичного лікування призначають кортикостероїди (КС) у дозі 0,5-1,0 мг/кг на добу;
- 3 ступінь (тяжкий або клінічно значущий, але не несе безпосередньої загрози життю пацієнта) – потребує госпіталізації або її пролонгації; характеризується обмеженням самообслуговування. При цьому ступені токсичності імунотерапію припиняють, окрім пацієнтів із шкірними й ендокринними проявами токсичності. Рекомендоване призначення КС у високих дозах (1-2 мг/кг на добу). Якщо на фоні терапії КС не спостерігається розрішення симптомів, призначають іншу імуносупресивну терапію, наприклад, із використанням химерних моноклональних антитіл;
- 4 ступінь (небезпечний для життя) – потребує негайного втручання. Імунотерапію повністю припиняють, окрім випадків ендокринної токсичності;
- 5 ступінь – зумовлює смерть пацієнта.
При виникненні у пацієнта того чи іншого прояву токсичності для швидкого визначення його ступеня та вибору подальшої тактики ведення можна використовувати спеціальні додатки для телефону. Зокрема, їх можна завантажити за посиланнями: https://ctep.cancer.gov/protocolDevelopment/electronic_applications/ctc.htm#ctc_50 та https://apps.apple.com/ru/app/ctcae-plus-v5-0-v4-03-v3-0/id1097838147?l.
Рекомендації ESMO щодо ведення небажаних явищ імунотерапії в українському перекладі сьогодні можна знайти у вільному доступі в інтернеті.
З метою запобігання виникненню небажаних явищ до лікування проводять збір анамнезу, звертаючи особливу увагу на наявність автоімунних захворювань, імуносупресії, вірусу імунодефіциту, ендокринопатії, нейропатії й інфекційних захворювань, а також належне фізикальне обстеження та лабораторні дослідження. Крім загального аналізу крові (ЗАК) та сечі, проводять біохімічний аналіз крові із визначенням так званих печінкових і ниркових проб, рівня електролітів та глюкози. Необхідно оцінити функцію щитоподібної залози, вивчаючи рівні тиреотропного гормону (ТТГ) та тироксину (Т4), провести електрокардіографію та виключити наявність вірусів імунодефіциту і гепатитів В та С. Збір анамнезу, фізикальне обстеження, ЗАК, біохімічний аналіз крові та оцінювання функції щитоподібної залози проводять перед кожним введенням препарату.
Особливостями симптоматичної терапії при шкірних проявах токсичності є призначення емолентів, антигістамінних препаратів і топічних КС. Розвиток гіпотиреозу передбачає призначення замісної гормональної терапії левотироксином у дозі 0,5-1,5 мкг/кг, а при клінічних проявах гіпертиреозу, таких як тахікардія, тремор, застосовують бета-блокатори (пропранолол, атенолол), карбімазол – у разі наявності антитіл до ТТГ і КС у дозі 0,5 мг/кг на добу при больовому синдромі на фоні тиреоїдиту. Необхідно пам’ятати, що у клінічній практиці гіпертиреоз часто змінюється гіпотиреозом, а нормальний або знижений рівень ТТГ разом зі зниженням Т4 може бути проявом порушення функції гіпофіза та потребує консультації ендокринолога.
Гепатотоксичність розвивається нечасто, на початковому етапі виявляється лише при лабораторному дослідженні, проте може мати вкрай негативні наслідки. Корекція гепатотоксичності здійснюється шляхом введення КС у дозі 1-2 мг/кг залежно від ступеня її вираженості. При неефективності лікування та токсичності 4 ступеня рекомендовано розглянути призначення мікофенолату мофетилу у дозі 500-1000 мг 2 рази на добу, а при подальшому погіршенні стану – такролімусу. Пневмоніт також виникає рідко, а його лікування передбачає призначення антибактеріальних препаратів і преднізолону при їх неефективності, за необхідності – штучної вентиляції легень.
Потрібно пам’ятати про необхідність поступової відміни КС, знижуючи дозу впродовж 2-4 тижнів після їх перорального застосування та впродовж 6-8 тижнів після внутрішньовенного введення. На фоні призначення КС рекомендується прийом препаратів кальцію, вітаміну D та профілактика пневмоцистної інфекції. Якщо дозу КС неможливо знизити до 10 мг/кг на добу – імунотерапію відміняють. Токсичність, пов’язана із лікуванням, яка не знижується до 0-1 ступеня впродовж 12 тижнів після останнього введення імунного препарату, також потребує відміни лікування.
Загалом імуноопосередковані побічні реакції, що виникають при застосуванні інгібіторів контрольних точок, є керованими і рідко потребують повного припинення терапії. Проте іноді навіть незначні на перший погляд прояви токсичності можуть мати несприятливі наслідки, а тому потребують своєчасної діагностики та мультидисциплінарного підходу до лікування.
Після виступів відбулася жвава дискусія з обговоренням низки питань клінічної практики та застосування імунотерапії у лікуванні меланоми шкіри.
Підготувала Ольга Нестеровська
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 2 (69) 2021 р.
СТАТТІ ЗА ТЕМОЮ Дерматологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




