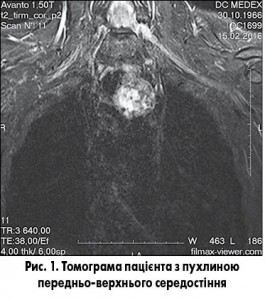
Можливості відеоторакоскопічного видалення новоутворень середостіння на прикладі клінічного випадку
Пухлини середостіння є одним із найбільш складних розділів у торакальній хірургії та онкології. Незважаючи на те що пухлини середостіння трапляються рідко (близько 3-7% у структурі пухлинних захворювань грудної клітки), вони продовжують залишатися цікавою діагностичною і терапевтичною проблемою для торакальних хірургів (О.М. Білий, 2004; Akshatha Rao Aroor, 2014). Актуальність проблеми зумовлена тим, що ембріо- та гістогенетична різноманітність пухлин середостіння, їх топографо-анатомічні особливості, своєрідність клінічної картини ускладнюють діагностику й уточнення нозологічної належності патологічних процесів цієї ділянки (З.О. Мачаладзе, 2008; S. Juanpere et al., 2013).
Дані щодо співвідношення добро- та злоякісних новоутворень неоднозначні. Так, за даними M. Vaziri та співавт. (2009), Akshatha Rao Aroor та співавт. (2014), злоякісні пухлини середостіння більш поширені, ніж доброякісні, і становлять 60 і 68,57% випадків відповідно, тоді як у більш ранніх повідомленнях ця частота фіксувалась на рівні 25-49% (K.S. Azarow et al., 1993; M. Wongsangiem et al., 1996). Щодо більшої поширеності доброякісних пухлин зазначалося у дослідженнях, проведених R.D. Davis і співавт. (1987) та V.O. Adegboye і співавт. (2003), – 58 і 57% відповідно.
За останні десятиліття спостерігається збільшення кількості пухлин середостіння майже вдвічі, переважно за рахунок зростання кількості лімфатичних пухлин (В.С. Шавлохов, 2009; N. Pearce та співавт., 2005).
У лікуванні пухлин середостіння тривалий час застосовували і застосовують дотепер стандартні методи оперативних втручань, які проводять через стернотомічний чи торакотомічний доступи. Вони вважаються досить травматичними й супроводжуються значною кількістю післяопераційних ускладнень, що пов’язано з топографо-анатомічними особливостями переднього середостіння. На сьогодні в лікуванні середостіння дедалі більшої популярності набуває мініінвазивний метод відеоторакоскопічної хірургії, який за підсумками численних досліджень був визнаний ефективною діагностичною і терапевтичною альтернативою (L.M. Cirino et al., 2000; R.D. Shah, T.A. D’Amico, 2014; Gonzalez-Rivas, 2016). Торакоскопія (особливо відеоторакоскопія) дає змогу детально візуалізувати медіастінальну пухлину, визначити її поширеність, зв’язок з оточуючими органами і тканинами, виконати прицільну біопсію її різних відділів і встановити морфологічний діагноз у понад 90,0% досліджень (Т.Н. Борисова и др., 2014).
Засновником торакоскопії як ендоскопії внутрішньої порожнини грудної клітки вважають H.C. Jacobaeus, який у 1910 році використав модифікований цитоскоп для зменшення спайок у плевральній порожнині та колапсу легені при туберкульозі. Два важливих наукових прориви наступних десятиліть дали змогу покращити хірургічну техніку. Перший – запровадження у 1960-ті роки окремої вентиляції легень, що дало змогу проводити процедури з невентильованою легенею, і другий – використання відеокамери до хірургічної оптики, що забезпечило передачу зображення на екран телевізора у збільшеному вигляді. Відтоді в торакальній хірургії за кордоном почали використовувати абревіатуру VATS (video-assisted thoracoscopic surgery) і ВТСХ (відеоторакоскопічна хірургія) – у нашій країні (J.B. Brodsky та співавт., 2000; J. Deslauriers та співавт., 2002).
Спершу, в період між 1992 і 2002 роками, показаннями до VATS були діагностичні процедури (плевроскопія, медіастеноскопія, біопсія легень, плевральна біопсія, медіастенальна біопсія) і малі торако-хірургічні процедури (симпатектомія, пневмоторакальна хірургія, Nuss-хірургія). З 2002 року техніку VATS широко використовують не лише для діагностики середостіння, легень і плевральних захворювань, а й для виконання великих торакальних хірургічних процедур, таких як резекція стравоходу або всієї легені (лобектомія, пневмонектомія, езофагектомія, тімектомія).
Розвиток мініінвазивної хірургії сприяв тому, що в країнах західної Європи та США почала зростати кількість мініінвазивних втручань: за даними різних авторів, кількість відеоторакоскопічних операцій сягнула 25-30% серед хворих, що потрапляють у торакальні відділення (D.M. Hansell et al., 2009; R.D. Shah et al., 2014).
Відеоторакоскопічні втручання дозволяють досягти майже 100% верифікації діагнозу в пацієнтів з пухлинами середостіння (L.M. Cirino et al., 2000), а кількість післяопераційних ускладнень під час використання відеоторакоскопії становить усього 2,7-4% (M.P. Lochowski, J. Kozak, 2014). Ускладнення після VATS можуть статися під час операції і, як правило, пов’язані з основним захворюванням, тоді як ускладнення в післяопераційному періоді найчастіше пов’язані із самим методом (J. LoCicero, 1993). Ускладнення процедур VATS можуть відбуватися зі змінною частотою при різних захворюваннях. Найбільш частим ускладненням є тривалий післяопераційний витік повітря. Іншими значними ускладненнями є кровотечі, інфекції, післяопераційні болі та рецидиви. Найбільш важливими факторами ризику тривалого витоку повітря є емфізема, пневмоторакс, вік старше 70 років, чоловіча стать і обсяг форсованого видиху за 1 с (ОФВ1) <70% (A. Brunelli et al., 2004). До факторів ризику інфекції після процедури VATS належать наявність пухлини, пригнічення імунітету, наявність інфекції до початку лікування VATS, тривале перебування в стаціонарі до операції, наявність центрального катетера (D.N. Nan et al., 2011), а також хронічні обструктивні захворювання легень і ОФВ1 <70% (A. Imperatori et al., 2008). Рецидив є ускладненням, що строго пов’язаний із хірургічною технікою. Ризик виникнення цього ускладнення збільшується при лікуванні мезотеліоми, метастазів саркоми або меланоми та злоякісного плеврального випоту у VATS. Використання коагуляції рани знижує ризик розвитку цього ускладнення (K. Parekh et al., 2001).
Відповідно до класифікації D. Dindo, N. Demartines, P.A. Clavien (2004) ускладнення поділяють на 5 категорій. Перші дві категорії включають незначні ускладнення: I – не становлять небезпеки для життя, не потребують лікування і не подовжують тривалість госпіталізації у середньому більш ніж удвічі, II – потенційно небезпечні для життя, потребують лікарської терапії, парентерального харчування або переливання. У III категорії – пацієнти з небезпечними для життя ускладненнями, потребують госпіталізації, діагностичних ендоскопічних процедур або повторної операції. До IV категорії належать серйозні загрозливі для життя ускладнення із залишковою або тривалою непрацездатністю. V категорія – смерть пацієнта.
Зазначимо, що, незважаючи на велику кількість типів ускладнень, вони зустрічаються рідко і їх можна уникнути за рахунок правильного підбору пацієнтів і володіння відповідною хірургічною технікою (M.P. Lochowski, J. Kozak, 2014).
Розвиток мініінвазивних хірургічних втручань сприяв застосуванню VATS при таких розладах, як грудні пухлини середостіння і рак стравоходу.
У разі патології середостіння VATS найчастіше застосовують до нейрогенних пухлин, лімфатичних вузлів і пухлин переднього середостіння. Діагностичні процедури зазвичай здійснюють, коли інші діагностичні методи є негативними. Ускладнення після цих процедур є рідкісними. Привертає увагу лімфорея, яка трапляється в 1% випадків після процедур VATS у середостінні. Близько 50% випадків лімфореї можуть бути припинені шляхом застосування консервативного лікування: дренування плевральної порожнини та використання дієти з низьким умістом тригліцеридів (A. Imperatori et al., 2008). Якщо таке лікування виявиться неефективним, тактикою вибору є перев’язка грудної протоки через праву плевру. Лікування можливе з використанням техніки VATS (A. Watanabe et al., 2007).
Як зазначають M.R. Asgary та співавт. (2014), серед пацієнтів з пухлиною середостіння незначно переважають чоловіки (56,4%), більшість із них перебувають між третьою і п’ятою декадами життя. Зазначені автори виявили неходжкінську лімфому у 30,7%, тімому – у 13,8% і лімфому Ходжкіна – у 12,9% випадків. 78,2% пухлин локалізувались у передньому середостінні, а далі в порядку зменшення частоти – в задньому і середньому середостінні. Дослідження показало, що лімфома і тімома були більш поширені в передньому середостінні, а нейрогенні пухлини – в задньому середостінні. Найбільш поширеними в порядку зменшення частоти симптомами були кашель, задишка і лихоманка (M.R. Asgary et al., 2014).
Вищенаведені дані свідчать про те, що застосування відеоторакоскопічних втручань є актуальним вирішенням питань більш ефективного та безпечного лікування, а також діагностики захворювань середостіння.
Клінічний випадок
Пацієнтка А., 1966 р.н., госпіталізована у НІХТ ім. О.О. Шалімова зі скаргами на дискомфорт за грудиною, відчуттям нестачі повітря. З анамнезу відомо, що в 2014 році пацієнтка скаржилася на болі в грудному та шийному відділі хребта, у зв’язку з чим їй було виконано МРТ-дослідження грудного та шийного відділу хребта, під час якого і було діагностовано новоутворення середостіння. В умовах клініки хворій проведено обстеження.
Загальний аналіз крові: еритроцити – 4,98×1012/л, гемоглобін – 135 г/л, кольоровий показник – 0,8, лейкоцити – 4,5×109/л, тромбоцити – 139×109/л, ШОЭ – 6 мм/год.
Біохімічний аналіз крові: загальний білок – 78,7 г/л, загальний білірубін – 8,1 мкмоль/л, прямий білірубін – 2,1 мкмоль/л, аланінамінотрансфераза – 19 мОд/л, аспартатамінотрансфераза – 23 мОд/л, a-амілаза – 49 мОд/л, сечовина – 4,0 ммоль/л, креатинін – 68,6 мкмоль/л, глюкоза – 6,7 ммоль/л.
Коагулограма: протромбіновий час – 11,0 с, протромбіновий індекс – 95%, міжнародне нормалізоване співвідношення – 1,0; фібриноген – 4,4 г/л.
МРТ: Загрудинно на рівні верхнього середостіння візуалізується об’ємний утвір гетерогенної структури, що неоднорідно накопичує гадолінієвий агент та має у своїй структурі включення гіперінтенсивного МР-сигналу на T1WI (кальцинати?), розміри 37,7×31,6×36,4 мм. Утвір розташований ліворуч від трахеї, дислокуючи її, і прилягає до дуги аорти (рис. 1).
Прийнято рішення про виконання відеоторакоскопічного видалення пухлини передньо-верхнього середостіння.
Хід операції. Виконано інтубацію трахеї двопросвітною інтубаційною трубкою 35F. Розпочато однолегеневу вентиляцію. У грудну клітку зліва введено 4 троакари: у VIII міжребер’я – 15 мм, у VII міжребер’я – 10 мм, у V міжребер’я – 5 мм, у IV міжребер’я – 5 мм. Під час ревізії явної органічної патології в лівій половині грудної клітки не виявлено. Після розтину медіастинальної плеври нижче рівня діафрагмального нерва, вище дуги аорти виявлено щільно-еластичне пухлиноподібне утворення до 4 см у діаметрі в капсулі, розташоване на судинах дуги аорти (лівої підключичної і лівої загальної сонної артерій). Тупим шляхом і за допомогою ультразвукового скальпеля Harmonic утворення мобілізовано і видалено в єдиному блоці з капсулою. Контроль гемостазу по ходу операції – сухо. Пухлина видалена з грудної порожнини в контейнері. Дренування плевральної порожнини зліва. Легеня розправилась. Пошарові шви ран. Асептичні пов’язки. Одразу після оперативного втручання оглянули препарат макроскопічно (рис. 2, А, Б).
Патогістологічний висновок: ектопія тканин щитоподібної залози з ознаками макро- та мікрофолікулярного колоїдного зобу.
Післяопераційний період протікав відповідно до обсягу оперативного втручання. На 4-ту добу після операції пацієнтку було виписано в задовільному стані.
Висновки та перспективи подальших розробок
Відеоторакоскопічне видалення новоутворень середостіння – безпечний та ефективний метод лікування хворих такого контингенту, що дає змогу скоротити перебування пацієнта в стаціонарі й зменшити кількість післяопераційних ускладнень після торакальних оперативних втручань.
Прагнення спеціалістів – науковців і практиків – розширити показання відеоторакоскопічного методу й обґрунтувати доцільність його застосування в різних розділах торакальної хірургії зумовлене зростанням популярності мініінвазивної хірургії у зв’язку зі значно меншою його травматичністю порівняно із загальноприйнятою торакотомією, яка нерідко перевищує сам етап видалення пухлини.
Література
- Білий О.М. Оптимізація діагностики та лікування пухлин середостіння, що зустрічаються найчастіше: автореф. дис. на здобуття наук. ступеня к.мед.н.: спец. 14.01.07 «Онкологія» / О.М. Білий. – Донецьк, 2004. – 20 с. 2.
- Клинические рекомендации по диагностике и лечению больных опухолями средостения и вилочковой железы [Электронный ресурс] / [Борисова Т.Н., Бредер В.В., Горбунова В.А. и др.]. – Москва, 2014. – 64 с. – Режим доступа: http://www.oncology.ru/association/clinical-guidelines/2014/48.pdf.
- Мачаладзе З.О. Опухоли средостения (дифференциальная диагностика и лечение): автореф. дис. на соискание уч. степени д-ра мед. наук: спец. 14.00.14 «Онкология» / З.О. Мачаладзе. – М., 2008. – 51 с. 4.
- Шавлохов В.С. Хирургические вмешательства в диагностике и терапии лимфатических опухолей средостения и легких: автореф. дис. на соискание уч. степени д-ра мед.наук: спец. 14.00.29 «Гематология и переливание крови», 14.00.27 «Хирургия» / В.С. Шавлохов. – Москва, 2009. – 40 с. 5.
- A diagnostic approach to the mediastinal masses / Sergi Juanpere, Noemі Canete, Pedro Ortuno [et al.] // Insights Imaging. – 2013. – Vol. 4 (1). – P. 29-52.
- A Study of Clinical Characteristicsof Mediastinal Mass / Akshatha Rao Aroor, Rama Prakasha S., Shubha Seshadri [et al.] // J. Clin. Diagn. Res. – 2014. – Vol. 8 (2). – P. 77-80.
- Brodsky J.B. Video-assisted thoracic surgery / J.B. Brodsky, E. Cohen // Curr. Opin. Anaesthesiol. – 2000. – Vol. 13. – P. 41-5.
- Davis R.D. Primary cysts and neoplasms of the mediastinum: recent changes in clinical presentation, methods of diagnosis, management, and results / R.D. Davis, H.N. Oldham, D.C. Sabiston // Ann. Thorac. Surg. – 1987. – Vol. 44. – P. 229-37.
- Deslauriers J. Thoracoscopy for diagnosis and staging. Pearson’s thoracic & esophageal surgery / J. Deslauriers, C. Sirois. – Philadelfia: Churchill Livingstone, 2002. – P. 103-15.
- Diagnosis and treatment of mediastinal tumors by thoracoscopy / L.M. Cirino, J.R. Milanez de Campos, A. Fernandez [et al.] // Chest. – 2000. – Vol. 117 (6). – P. 1787-92.
- Diagnosis and Treatment of Mediastinal Tumors by Thoracoscopy / Luіs Marcelo Inaco Cirino, Josе Ribas Milanez de Campos, Angelo Fernandez [et al.] // Chest. – 2000. – Vol. 117, Issue 6. – P. 1787-1792.
- Dindo D. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey / D. Dindo, N. Demartines, P.A. Clavien // Ann. Surg. – 2004. – Vol. 240. – P. 205-13.
- Epidemiology of Mediastinal Tumors during Six Years (2006-2012) in Rasht City / M.R. Asgary, M. Aghajanzadeh, H. Hemmati, M. Jafari // Emergencias. – 2014. – Vol. 2. – P. 88-94.
- Imaging of Diseases of the Chest / D.M. Hansell, D.A. Lynch, H. Page McAdams, A.A. Bankier [5th edition]. – 2009. – 1208 p.
- Lochowsk M.P. Video-assisted thoracic surgery complications / M.P. Lochowski, J. Kozak / Wideochir. Inne Tech. Maloinwazyjne. – 2014. – Vol. 9 (4). – P. 495-500.
- Lochowski M.P. Video-assisted thoracic surgery complications / M.P. Lochowski, J. Kozak // Wideochir. Inne Tech. Maloinwazyjne. – 2014. – Vol. 9 (4). – P. 495-500.
- LoCicero J. 3rd credentialing issues and complications of video-assisted thoracic surgery / J. LoCicero // Semin. Thorac. Cardiovasc. Surg. –1993. – Vol. 5. – P. 303-4.
- Nosocomial infection following video-assisted thoracoscopic surgery / D.N. Nan, M. Fernаndez-Ayala, C. Farinas-Alvarez [et al.] // Rev. Esp. Quimioter. – 2011. – Vol. 24. – P. 217-22.
- Pearce N. Agricultural exposures and non-Hodgkin’s lymphoma / N. Pearce, D. McLean // Scand. J. Work Environ. Health. – 2005. – Vol. 31 (Suppl 1). – P. 18-25.
- Peri-operative complications of video-assisted thoracoscopic surgery / A. Imperatori, N. Rotolo, M. Gatti [et al.] // Int. J. Surg. – 2008. – Vol. 6 (suppl 1). – S. 78-81.
- Predictors of prolonged air leak after pulmonary lobectomy / A. Brunelli, M. Monteverde, A. Borri [et al.] // Ann. Thorac. Surg. – 2004. – Vol. 77. – P. 1205-10.
- Presentation of primary mediastinal masses in Ibadan / V.O. Adegboye, A.O. Ogunseyinde, M.O. Obajimi [et al.] // East African Medical. Journal. – 2003. – Vol. 80. – P. 484-7.
- Primary mediastinal masses. A comparison of pediatric populations / Azarow K.S., Pearl R.H., Zurcher R. [et al.] // J. Thorac. Cardiovasc. Surg. – 1993. – Vol. 106. – P. 6772.
- Shah R.D. Modern impact of video assisted thoracic surgery / R.D. Shah, T.A. D’Amico / J. Thorac. Dis. – 2014. – Vol. 6 (Suppl 6). – S. 631-636.
- Shah R.D. Modern impact of video assisted thoracic surgery / R.D. Shah, T.A. D’Amico // J. Thorac. Dis. – 2014. – Vol. 6 (Suppl 6). – S. 631-6. doi: 10.3978/j.issn.2072-1439.2014.08.02.
- Supradiaphragmatic thoracic duct clipping for chylothorax through left-sided video-assisted thoracoscopic surgery / A. Watanabe, T. Koyanagi, S. Nakashima, T. Higami // Eur. J. Surg. – 2007. – Vol. 31. – P. 313-4.
- Uniportal thoracoscopic surgery: from medical thoracoscopy to non-intubated uniportal video-assisted major pulmonary resections / Diego Gonzalez-Rivas // Annals of Cardiothoracic Surgery. – 2016. – Vol. 5 (2). – P. 85-91.
- VATS port site recurrence: a technique dependent problem / K. Parekh, V. Rusch, M. Bains [et al.] // Ann. Surg. Oncol. – 2001. – Vol. 8. – P. 175-8. VATS port site recurrence: a technique dependent problem / K. Parekh, V. Rusch, M. Bains [et al.] // Ann. Surg. Oncol. – 2001. – Vol. 8. – P. 175-8.
- Vaziri M. Mediastinal masses: Review of 105 cases / M. Vaziri, A. Pazooki, L. Zahedi-Shoolami // Acta Medica Iranica. – 2009. – Vol. 47. – P. 297-300.
- Wongsangiem M. Primary tumours of the mediastinum: 190 cases analysis (1975-1995) / M. Wongsangiem, A. Tangthangtham // J. Med. Assoc. Thai. – 1996. – Vol. 79. – P. 689-97.
СТАТТІ ЗА ТЕМОЮ Хірургія, ортопедія та анестезіологія
Дисфагія є поширеним явищем у пацієнтів відділення інтенсивної терапії (ВІТ), але вона часто залишається недостатньо розпізнаною та неконтрольованою, незважаючи на те що пов’язана з небезпечними для життя ускладненнями, тривалим перебуванням у ВІТ та госпіталізацією. Запропонований у статті експертний висновок щодо діагностики й лікування дисфагії розроблений на основі доказових клінічних рекомендацій та думок лікарів-практиків. Автори рекомендують прийняти ці клінічні алгоритми для надання стандартизованої та високоякісної допомоги, яка передбачає своєчасний систематичний скринінг, оцінку та лікування дисфагії в екстубованих пацієнтів і пацієнтів із трахеостомою у ВІТ. ...
Больовий синдром при хронічних ранах є рутинним явищем хірургічної практики. Рана вважається такою, що тривало не загоюється, якщо, незважаючи на відповідну терапію та достатній термін лікування (4-6 міс), відсутні або практично відсутні ознаки загоєння. Неопіоїдні та опіоїдні анальгетики є основними препаратами, що застосовуються для лікування больового синдрому при ранах. На науково-практичній конференції «Міждисциплінарний підхід у лікуванні коморбідних хірургічних пацієнтів», що відбулася наприкінці 2023 року, тему менеджменту хронічної ранової хвороби представив у доповіді «Контроль болю в хірургії ран та трофічних дефектів м’яких тканин різної етіології» завідувач кафедри хірургії та судинної хірургії Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Сергій Іванович Саволюк. Ключові слова: ранова хвороба, трофічна виразка, ВАК-терапія, больовий синдром, нестероїдні протизапальні препарати, Дексалгін®....
Актуальність проблеми переломів на сьогодні не залишає сумнівів, зокрема в контексті старіння населення та поширеності остеопорозу. Кальцій та вітамін D, виконуючи ключову роль у формуванні та підтриманні щільності кісткової тканини, є необхідними елементами для успішної профілактики переломів, особливо у вразливих груп населення. Також важливим є достатній рівень кальцію та вітаміну D в організмі для оптимального зрощення переломів і посттравматичної зміни кісток. У цьому контексті велике значення має вибір конкретного комплексу Са + D із позицій ефективності, безпеки та високого комплаєнсу. Ключові слова: остеопороз, крихкість кісток, кальцій, вітамін D, профілактика переломів. ...
З установленням центральних венозних катетерів (ЦВК) пов’язані різноманітні ускладнення, включаючи ті, що зумовлені безпосередньо введенням і/або доступом, через який уводиться катетер, а також віддалені (>1 тижня) ускладнення, такі як дисфункція катетера, стеноз або тромбоз центральної вени та розвиток інфекції. Кількість і тяжкість ускладнень зростають зі збільшенням розміру катетера, кількості використовуваних катетерів та часу їх перебування в організмі. У статті наведено огляд сучасних даних щодо ускладнень, пов’язаних із ЦВК, а також стратегії їх профілактики та лікування. Ключові слова: центральний венозний катетер, ускладнення, пункція артерії, пневмоторакс, тромбоз центральної вени, інфекції кровотоку, дисфункція катетера. ...