Эффективность Флороспазмила при абдоминальном болевом синдроме
 Абдоминальный болевой синдром является одним из наиболее частых клинических проявлений при большинстве заболеваний органов пищеварения. Боль – это спонтанное субъективное ощущение, возникающее вследствие поступления в центральную нервную систему патологических импульсов с периферии (в отличие от болезненности, которая определяется при обследовании, например, при пальпации) [2, 3]. Абдоминальные боли подразделяют на острые, которые, как правило, имеют небольшую продолжительность (минуты, редко – несколько часов), а также хронические, которые сохраняются или рецидивируют на протяжении недель и месяцев.
Абдоминальный болевой синдром является одним из наиболее частых клинических проявлений при большинстве заболеваний органов пищеварения. Боль – это спонтанное субъективное ощущение, возникающее вследствие поступления в центральную нервную систему патологических импульсов с периферии (в отличие от болезненности, которая определяется при обследовании, например, при пальпации) [2, 3]. Абдоминальные боли подразделяют на острые, которые, как правило, имеют небольшую продолжительность (минуты, редко – несколько часов), а также хронические, которые сохраняются или рецидивируют на протяжении недель и месяцев.
Причины абдоминального болевого синдрома многообразны и могут быть связаны как с заболеваниями брюшной полости, так и с экстраабдоминальной патологией (например, почечная колика, заболевания малого таза), быть следствием как органической, так и функциональной патологии. По механизму возникновения боли в брюшной полости подразделяются на висцеральные, париетальные (соматические), отраженные (иррадиирующие) и психогенные. Соматическая боль обусловлена наличием патологических процессов в париетальной брюшине и тканях, имеющих окончания чувствительных спинномозговых нервов. Основными импульсами для ее возникновения являются повреждение брюшной стенки и брюшины. Подавляющему большинству больных с наличием соматических болей, как правило, необходимо хирургическое лечение. Висцеральная боль возникает при наличии патологических стимулов во внутренних органах и проводится симпатическими волокнами. Основными импульсами для ее возникновения являются внезапное повышение давления в полом органе и растяжение его стенки (наиболее частая причина), растяжение капсулы паренхиматозных органов, натяжение брыжейки, сосудистые нарушения. Наиболее часто висцеральные боли возникают вследствие синдрома раздраженного кишечника (СРК) и билиарной дисфункции. Висцеральные боли, возникающие у больных как с наличием органических поражений органов пищеварения, так и без них, являются следствием нарушения в первую очередь их дисмоторных функций. В результате в полых органах повышается давление и/или наблюдается растяжение их стенок, возникают условия для формирования восходящих ноцицептивных импульсов.
Моторная функция желудочно-кишечного тракта (ЖКТ) определяется активностью гладкомышечных клеток, находящейся в прямо пропорциональной зависимости от концентрации цитозольного Са2+. Ионы кальция, активируя внутриклеточные биоэнергетические процессы (фосфорилирование белков, превращение АТФ в цАМФ и др.), способствуют соединению нитей актина и миозина, что обеспечивает сокращение мышечного волокна. Одним из условий, необходимых для сокращения мышечного волокна, является высокая активность фосфодиэстеразы, которая участвует в расщеплении цАМФ и обеспечении энергией процессов соединения актина с миозином. В регуляции транспорта ионов кальция участвует ряд нейрогенных медиаторов: ацетилхолин, катехоламины (норадреналин), серотонин, холецистокинин, мотилин и др. Связывание ацетилхолина с М‑холинорецепторами способствует открытию натриевых каналов и вхождению ионов натрия в клетку. Последнее снижает электрический потенциал клеточной мембраны (фаза деполяризации) и приводит к открытию кальциевых каналов, через которые ионы кальция поступают в клетку, вызывая мышечное сокращение.
Основные направления купирования болевого абдоминального синдрома включают:
- этиологическое и патогенетическое лечение основного заболевания;
- нормализацию нарушений моторики;
- снижение висцеральной чувствительности;
- коррекцию механизмов восприятия болей.
Наиболее часто в купировании острых абдоминальных болей применяются спазмолитики, механизм действия которых реализуется через уменьшение сокращений гладкой мускулатуры. Кроме того, некоторые спазмолитики также могут воздействовать и на повышенную висцеральную чувствительность [9]. С фармакологической точки зрения спазмолитики можно разделить на 2 главные группы – антихолинергические препараты и прямые релаксанты гладкой мышечной ткани (миотропные спазмолитики). Каждый представитель этих групп обладает как преимуществами, так и определенными недостатками, ограничивающими их клиническое применение [3-5].
Эффективность антихолинергических препаратов, таких как скополамин (гиосцин), дицикломин или прифиния бромид, обусловлена блокадой мускариновых рецепторов, расположенных в стенке кишки, и возникающим вследствие этого быстрым и выраженным, хотя и непродолжительным, спазмолитическим эффектом. К сожалению, широкое применение этих препаратов ограничивается неселективностью их действия и блокадой М‑рецепторов гладкомышечной мускулатуры других органов, что приводит к атропиноподобным побочным эффектам и обуславливает неблагоприятный профиль безопасности и переносимости, поэтому в связи со своими атропиноподобными побочными эффектами эти препараты длительно не применяются (прием «по требованию», обычно в течение нескольких дней) [1].
Среди миотропных спазмолитиков выделяют 3 основные группы с разными механизмами действия. Первая группа – это неселективные спазмолитики, такие как папаверин и дротаверин, являющиеся блокаторами фосфодиэстеразы цАМФ и цГМФ. Вторая группа – селективные блокаторы кальциевых каналов – пинаверия бромид, отилония бромид и флороглюцинола дигидрат, которые избирательно воздействуют на гладкие мышцы ЖКТ. Третья группа – селективные блокаторы натриевых каналов гладких мышц ЖКТ, такие как мебеверин. Конечный этап действия любого из этих спазмолитиков – это уменьшение концентрации ионов кальция в миоците и гладкомышечная релаксация [1, 6, 10]. Они проявляют свою эффективность в отношении симптоматики в связи с тем, что снижают сократительную активность или спазмы пищеварительного тракта, которые ассоциируются с болью. Как правило, неселективные спазмолитики, оказывающие быстрый и выраженный, но краткосрочный эффект, также длительно не применяются и назначаются в основном для купирования выраженного болевого синдрома. Наоборот, селективные блокаторы кальциевых или натриевых каналов оказывают более длительный эффект, являются более безопасными и хорошо переносимыми, в связи с чем обычно применяются в виде курсового (недели, месяцы) лечения.
Одним из популярных в Европе спазмолитиков является флороглюцинола дигидрат – неатропиновый спазмолитик, селективный блокатор кальциевых каналов с элементами системного действия. В Украине этот препарат в инъекционной форме зарегистрирован под торговым названием Флороспазмил. Флороглюцинол селективно блокирует Ca2+-каналы и Ca2+-депо при переизбытке Ca2+, ограничивает выход K+ из клетки и препятствует развитию спазма гладкомышечной клетки, не вызывая атонии или гипотонии кишечника. Благодаря системному всасыванию и выведению, спазмолитический эффект реализуется не только в кишечнике, но и в желчевыводящих путях, а также в урогенитальном тракте. В отличие от неселективных спазмолитиков у флороглюцинола отсутствуют системные побочные явления. Не менее важным механизмом действия флороглюцинола является его ингибирующий эффект на циклооксигеназу‑1 и -2. Таким путем реализуется влияние препарата на каскад арахидоновой кислоты и биосинтез простагландинов, что уменьшает воспаление и улучшает работу различных звеньев иммунитета. Угнетение NO‑опосредованных механизмов облегчает передачу возбуждения вследствие растяжения ЖКТ и, как следствие, продвижение внутрикишечного содержимого вдоль тракта существенно снижает тонус гладкомышечных клеток. Защитное влияние флороглюцинола на клетки осуществляется в условиях оксидативного стресса, опосредованного активацией каталазы.
Таким образом, за счет сложного комбинированного механизма действия реализуется спазмолитический эффект флороглюцинола на уровне организма: ингибируются спазмы гладкой мускулатуры при сохраненной перистальтической активности. Изучение влияния флороглюцинола на желчный пузырь и желчные протоки показало, что данное соединение частично блокировало сокращения изолированного желчного пузыря, стимуляцию оттока желчи и потенцирование эффектов катехоламинов. Не менее эффективным было применение флороглюцинола в урологии. В частности, проводилось рандомизированное исследование эффективности тамсулозина, нифедипина и флороглюцинола в купировании почечной колики (камни в дистальном отделе мочеточников) [8]. В этих клинических исследованиях эффективность флороглюцинола была подтверждена по таким показателям, как продолжительность пребывания в стационаре, сроки выведения камней, обезболивающее действие, потребность в дальнейшей госпитализации и эндоскопическом лечении, а также число потерянных рабочих дней, уровень качества жизни и наличие побочных эффектов. Введение флороглюцинола значительно ослабляло почечную дисфункцию и гистологические повреждения, вызванные ишемией. Флороглюцинол также проявляет спазмолитическое действие на матку. В частности, проведенное клиническое исследование [7] подтвердило способность флороглюцинола эффективно улучшать раскрытие шейки матки во время родов и хорошую переносимость как организмом матери, так и новорожденного.
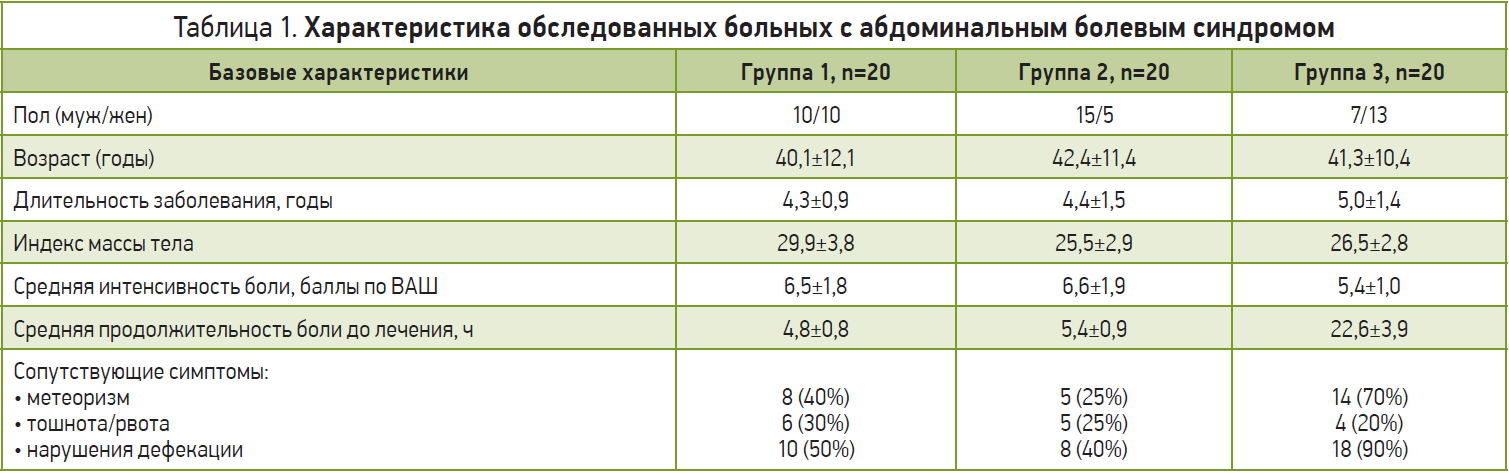
Нами проведено открытое клиническое исследование эффективности и безопасности Флороспазмила у 60 больных с абдоминальными болями, возникшими вследствие билиарной патологии (желчнокаменная болезнь, гипермоторная дисфункция желчного пузыря – группа 1), мочекаменной болезни (группа 2) и СРК (группа 3). Характеристика обследованных больных представлена в таблице 1.
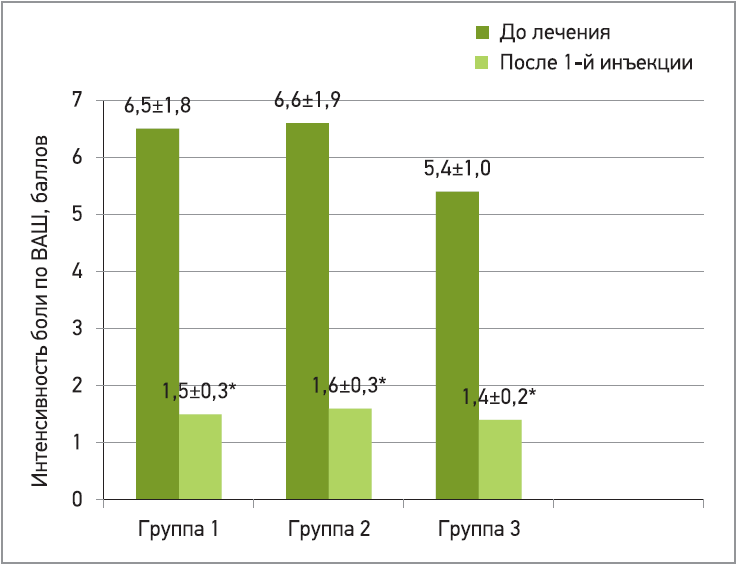
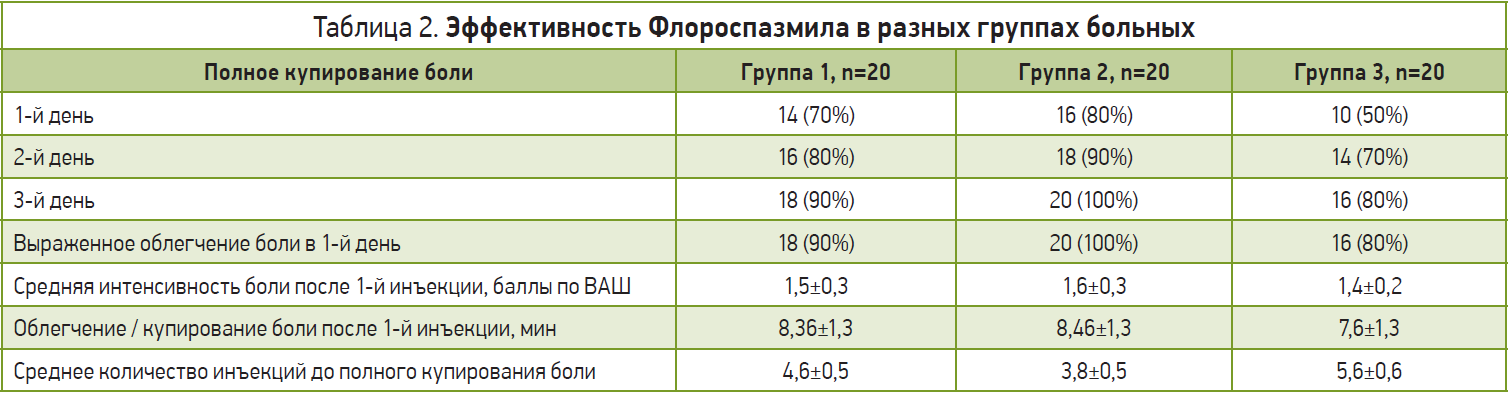
У всех больных после клинического обследования, включающего осмотр хирурга, общеклинические и биохимические анализы, УЗИ органов брюшной полости и ЭГДС (при болях в верхней части живота), была исключена острая хирургическая патология. Флороспазмил вводился в разные сроки после появления абдоминальной боли внутримышечно по 4,0 мл 2 р/день (в зависимости от купирования или облегчения болевого синдрома в течение 1-3 дней). В качестве критериев эффективности оценивали количество больных с полным или частичным купированием боли и сопутствующих симптомов, а также скорость и степень снижения интенсивности боли по 10-балльной визуально-аналоговой шкале (ВАШ). Выраженность абдоминальной боли в баллах оценивалась при помощи ответов на вопрос: «Как Вы оцениваете интенсивность боли в животе по шкале от 0 («полное отсутствие боли») до 10 баллов («сильная боль, какая только может быть»)?». Оценивали также переносимость лечения и частоту побочных эффектов. Полученные результаты представлены в таблице 2 и на рисунке. Проведенное исследование показало, что практически у всех больных применение Флороспазмила было эффективным и безопасным, причем абдоминальный болевой синдром (независимо от его природы) купировался или значительно уменьшался уже после 1-й инъекции через 8-10 мин. Средняя интенсивность болевого синдрома по шкале ВАШ после 1-й инъекции снижалась в 3-4 раза. Выраженное облегчение боли в течение 1-го дня отмечено в 1-й группе у 90%, во 2-й – у 100%, в 3-й – у 80% больных. Если в течение 1-го дня полного купирования болевого синдрома не отмечалось, сохраняющиеся боли низкой интенсивности мы трактовали как остаточные; практически во всех случаях они были связаны с динамическим парезом кишечника после приступа желчной или почечной колики. Полное купирование абдоминальной боли в течение 1-го дня в 1-й группе было отмечено у 70%, во 2-й – у 80%, в 3-й – у 50% больных. В течение 2-го дня болевой синдром полностью купирован соответственно у 80, 90 и 70% больных; в течение 3-го дня – соответственно у 90, 100 и 80% больных. Таким образом, эффективность Флороспазмила в купировании или выраженном облегчении болевого синдрома была более выражена у больных с билиарной патологией и мочекаменной болезнью.
Рис. Интенсивность боли по шкале ВАШ (0-10 баллов) после 1-й инъекции Флороспазмила
Примечание: * p≤0,01 по сравнению с исходным.
Каких-либо неблагоприятных побочных эффектов при применении Флороспазмила в указанной дозировке не было; все больные переносили лечение хорошо.
Таким образом, наше открытое исследование свидетельствует об эффективности и безопасности инъекционного введения Флороспазмила для купирования или выраженного уменьшения интенсивности абдоминальной боли у подавляющего числа больных с билиарными дисфункциями, почечной коликой на фоне мочекаменной болезни и СРК. Его несомненными преимуществами являются высокая эффективность в купировании болевого синдрома, высокая скорость достижения облегчения / устранения боли, сравнимая с плацебо безопасность и переносимость, благодаря чему он практически не имеет противопоказаний (за исключением идиосинкразии).
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 18 (511), 2021 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...