Білі плями в призначенні йодовмісних препаратів
У вересні 2021 року у форматі онлайн відбулося чергове засідання науково-освітнього проєкту «Школа ендокринолога». Із доповіддю про діагностику, лікування й профілактику йододефіцитних станів, а також про доцільність призначення йодовмісних препаратів виступила провідний науковий співробітник Інституту ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України (м. Київ), кандидат медичних наук Юлія Валеріївна Булдигіна.
Перші згадки про зоб, кретинізм і методи їх лікування і профілактики можна зустріти ще в трактатах Давнього Китаю. Доказом наявності йододефіциту впродовж усієї історії людства є також живопис IX-XI століть. Так, часто портрети людей із зобом можна побачити серед робіт майстрів альпійських країн. Потовщення шиї у святих в іконописі цієї епохи вважали ознакою божественного осяяння. У 1820 р. швейцарець Коіндет вперше представив науковій спільноті результати дослідження, яке продемонструвало позитивний вплив малих доз йоду на стан 150 пацієнтів із зобом. І лише наприкінці XIХ ст. недостатню забезпеченість організму людини йодом було визнано основною причиною захворювань щитоподібної залози (ЩЗ).
За оцінками ВООЗ приблизно третина світової популяції проживає в йододефіцитних регіонах. Україна, як і більшість країн Європи, є ендемічним за йододефіцитом регіоном. Йододефіцитні регіони визначають за середньою концентрацією йоду в сечі (медіаною). Якщо вона становить <100 мкг/л, регіон вважають йододефіцитним. Наступним важливим показником напруженості йододефіциту є частота виникнення зобу в популяції. Якщо вона перевищує 5%, регіон вважається ендемічним. У разі тяжкого йододефіциту (медіана йоду в сечі <20 мкг/л) і поширеності зобу більш як 30% в 1-10% населення виявляють ознаки кретинізму, а в більшої частини жителів – затримку інтелектуального розвитку і різні неврологічні порушення. У районах із помірним і легким дефіцитом йоду (медіана йодурії – 20-99 мкг/л) – 5-30% випадків кретинізму не спостерігають, але коефіцієнт інтелектуального розвитку (IQ) у більшої частини населення в середньому на 10-15 пунктів знижений проти такого в йодозабезпечених регіонах.
Йод є основною складовою для синтезу тиреоїдних гормонів. Він потрапляє у фолікули ЩЗ завдяки натрій-йодному симпортеру, надалі йод потрапляє в колоїд, де за допомогою тиреоїдної пероксидази і відбувається йодування тиреоглобуліну і синтез тиреоїдних гормонів (кон’югація, ендоцитоз, протеоліз). Далі синтезовані тироксин і частково трийодтиронін у разі потреби, під впливом тиреотропного гормону (ТТГ), виділяються у кров. Якщо в організмі йоду недостатньо, виділяється надлишкова кількість тиреоглобуліну і збільшується маса ЩЗ.
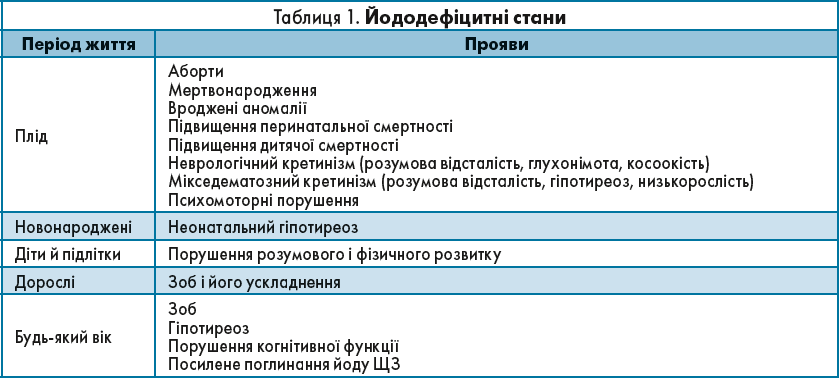
Спектр йододефіцитних станів був описаний Hetzel у 1983 р., він залишається актуальним і донині (табл. 1).
Дефіцит йоду призводить до зниження IQ на 15-20%. Це відбувається тому, що в умовах нестачі йоду діти швидко втомлюються, виснажуються. Їм важко зосереджувати увагу, аналізувати та запам’ятовувати інформацію, отримувати нові знання і навички. Загальна щорічна втрата IQ через йододефіцит у країні становить 462 700 одиниць – це можна порівняти із сумою показників IQ понад 3 тис геніїв. Отже, йододефіцит формує відстале суспільство. Спочатку дітям після закінчення школи важко отримати професію і достатній заробіток. У дорослих слабшає імунітет, погіршується пам’ять і працездатність. Щорічні економічні втрати, пов’язані зі зниженням продуктивності праці в Україні, становлять щонайменше 43,8 млн доларів США (понад 5 млн пропущених робочих днів). Як висновок, країна втрачає інтелектуальний, освітній, професійний і науковий потенціал.
Дифузний зоб є першою ознакою йододефіциту. найчастіше перебіг цієї патології відбувається безсимптомно. Можливі симптоми визначаються локалізацією зобу і динамікою його перебігу (механічна компресія трахеї – диспное, механічна компресія стравоходу – дисфагія). Зазвичай зоб стає помітним, коли об’єм ЩЗ збільшується до ≥40 мл.
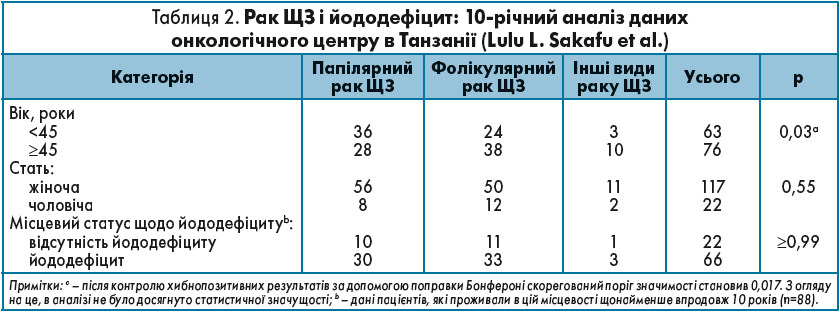
За умови дефіциту йоду збільшується кількість захворювань на папілярний і фолікулярний рак ЩЗ (табл. 2).
Важливим моментом у профілактиці йододефіциту є його діагностика. Варто зазначити, що визначення екскреції йоду із сечею не є інформативним для оцінки стану йододефіциту в конкретної особи, а використовується лише для скринінгових досліджень, оскільки йодурія залежить від харчування, яке передує збору сечі.
Методів індивідуальної йододіагностики немає, оскільки йододефіцит – це проблема конкретної географічної території, де встановлений дефіцит йоду. Індивідуально оцінити цей стан у конкретного пацієнта можна вже за клінічними наслідками, наприклад за розвитком зобу і збільшенням концентрації тиреоглобуліну.
Інформованість популяції щодо зазначеної проблеми залишається низькою. За даними лабораторії інституту, загалом 39% населення дізнається про йододефіцит завдяки радіо і телебаченню, у 15% випадків – із газет і журналів і в такому самому відсотку випадків – від друзів і родичів. У 30% випадків ця інформація надходила від медичних працівників, які, до речі, також не обізнані належним чином.
Йодопрофілактика буває двох видів. Масова («німа») полягає в постійному використанні населенням конкретної країни йодованої солі як універсального носія цього хімічного елементу. Групову та індивідуальну йодну профілактику проводять у країнах, де не здійснюється масова профілактика; вона направлена на захист найвразливіших верств населення – дітей, підлітків, вагітних, жінок у період лактації. Але і в країнах, де проводять масову профілактику, вагітним і жінкам-годувальницям додатково призначають індивідуальну йодну профілактику через підвищену потребу в надходженні йоду в ці періоди життя.
Стан профілактики дефіциту йоду в Україні залишається вкрай незадовільним. Аналіз анкет-опитувальників показав, що в окремих населених пунктах частота постійного споживання йодованої солі сягала 50%, в інших – 30%, загалом по Україні йодовану сіль споживає лише 26% населення. З огляду на світовий досвід, це дуже мало. За цим критерієм рівня профілактики йододефіциту Україна посідає передостаннє місце в Європі.
У нашому суспільстві тема йодопрофілактики оповита певними міфами, на яких варто зупинитись окремо.
Міф 1 – дефіцит йоду можна компенсувати харчуванням (правда: єдиний спосіб – щоденне споживання свіжої морської риби і морепродуктів).
Міф 2 – йодована сіль нестійка, зберігається недовго, випаровується за високої температури (правда: раніше використовували 23 мг йодиду калію на 1 кг солі, тепер – 40 мг йодату калію на 1 кг солі. Сполука є стійкою і майже не випаровується під час приготування їжі. За умови щоденного вживання 6 г солі до організму надходить 150 мкг йоду).
Міф 3 – йодовану сіль не можна використовувати для консервації (правда: вагомий контраргумент – це якість консервованих продуктів країн Західної Європи, в яких використовують лише йодовану сіль).
Міф 4 – алергія на йод (правда: йод – мікроелемент, а алергічні реакції виникають тільки на органічні речовини).
Міф 5 – морська сіль краща за йодовану (правда: на жаль, у процесі випаровування, очищення, сушіння йод із морської солі майже повністю зникає. Так, в 1 г морської солі міститься приблизно 1 мкг йоду, а в йодованій солі – 40 мкг).
Міф 6 – багатьом людям йод протипоказаний (правда: йод протипоказаний лише пацієнтам після хірургічного лікування раку ЩЗ під час підготовки до терапії радіоактивним йодом).
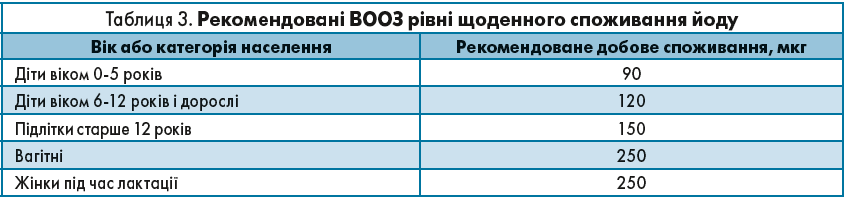
Рекомендовані ВООЗ рівні щоденного споживання йоду наведено в таблиці 3.
Індивідуальну профілактику йододефіциту проводять препаратами йодиду калію. На фармацевтичному ринку України представлений препарат Йодомарин у двох дозуваннях – 100 і 200 мкг. Щоденний прийом препарату Йодомарин 100 протягом 6 міс чинить позитивний вплив на зростання, розвиток, стан вищих психічних і розумових функцій, супроводжується зниженням частоти гострих респіраторних захворювань у дітей віком 3-6 місяців. Згідно з наказом № 254 МОЗ України індивідуальна йодна профілактика в період вагітності та під час годування груддю має проводитися препаратами, які містять йодид калію, у добовій дозі 200 мкг на добу. Дітям старше 12 років призначають по 1-2 таблетки (100-200 мкг) Йодомарин 100. Немовлятам і малюкам Йодомарин – у дозі 50-100 мкг. Зручністю застосування препарату є можливість індивідуального підбору дози відповідно до міжнародних рекомендацій із боротьби з йододефіцитом. Якщо вагітна чи мати-годувальниця використовує йодовану сіль, вона вже отримує 150 мкг йоду, що необхідно враховувати, призначаючи дозу препарату Йодомарин.
Харчові йодовмісні добавки вагітним і жінкам-годувальницям не рекомендуються, оскільки такі добавки не мають у своєму складі чітко визначеної і, головне, контрольованої кількості йоду. Також, згідно з висновком Наукового комітету з харчування Європейської комісії здоров’я та захисту споживача 2002 року, вживання збагачених йодом препаратів морських водоростей, особливо висушених продуктів, може спричинити небезпечне надмірне надходження йоду, із ризиком виникнення порушення функції ЩЗ. Необхідно пам’ятати, що передозування йоду так само небезпечне, як і його нестача. Жінкам-годувальницям треба уникати споживання високих доз йоду – 500-1100 мкг/добу, оскільки неадекватне проведення йодної профілактики може бути причиною виникнення аутоімунного тиреоїдиту, гіпотиреозу та йодіндукованого тиреотоксикозу.
За наявності певних факторів ризику рекомендовано проведення дослідження вмісту ТТГ гіпофіза. Такими ризиками є:
- проживання в місцевості з нестачею йоду (від помірної до тяжкої; майже по всій території України визначається помірна йодна недостатність);
- наявність в анамнезі: гіпотиреозу/гіпертиреозу або поточних симптомів / ознак дисфункції ЩЗ; опромінення голови/шиї або операцій на ЩЗ; викидня, передчасних пологів, безпліддя; аутоімунних захворювань ЩЗ або її дисфункції; ожиріння ІІІ ступеня ([індекс маси тіла] ІМТ >40 кг/м2);
- наявність антитіл до ЩЗ (антитіла до пероксидази/тиреоглобуліну) або зобу;
- вік понад 30 років;
- цукровий діабет 1 типу або інші аутоімунні захворювання;
- більш як 2 попередні вагітності;
- застосування препаратів аміодарону або літію, нещодавнє введення йодовмісних рентгеноконтрастних речовин.
Усім вагітним жінкам при будь-якій дисфункції ЩЗ необхідно призначати пероральне лікування від початку вагітності до пологів.
Проблема дефіциту йоду залишається актуальною донині і стосується країн із різним рівнем доходів. На щастя, її вирішення не потребує масштабних економічних витрат, а полягає в щоденному застосуванні йодованої солі і/або, за наявності показань, калію йодиду. Вартість терапії Йодомарином становить 1-2 грн/добу. Застосування цього препарату є основною складовою успішної профілактики йододефіцитних станів, оскільки Йодомарин містить фізіологічну дозу йоду.
Підготувала Катерина Рихальська
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (56) 2021 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....
Метформін – протидіабетичний препарат першої лінії, який пригнічує глюконеогенез у печінці і в такий спосіб знижує рівні глюкози в крові. Крім того, він знижує ризик кардіоваскулярних подій, чинить нефропротекторний ефект і здатен подовжувати тривалість життя. Завдяки цим властивостям метформін нині розглядають як мультифункціональний препарат і дедалі частіше застосовують для лікування та профілактики різноманітних захворювань....
Сучасне лікування хворих на цукровий діабет (ЦД) 2 типу включає зміну способу життя і медикаментозну терапію для контролю глікемії та профілактики ускладнень. Проте дослідження показують, що на практиці небагато хворих досягають контролю захворювання (частково через погану прихильність до лікування). Частка пацієнтів, які дотримуються протидіабетичної терапії, коливається від 33 до 93% (упродовж 6-24 міс) [1, 2]....