Ефективність амантадину в рамках терапії хвороби Паркінсона, леводопа‑індукованих дискінезій та COVID‑19
Порушення рухової функції, характерні для хвороби Паркінсона (ХП), зазвичай лікують леводопою. Однак тривале лікування може призводити до леводопа-індукованих дискінезій (ЛІД), зумовлюючи негативний вплив на якість життя пацієнта. Амантадин, як і леводопа, ефективний для збільшення вмісту дофаміну при ХП. Результати досліджень і метааналізів підтверджують, що амантадин є ефективним для лікування ранньої або стабільної ХП. Клінічну ефективність амантадину для лікування ЛІД доповнене результатами систематичних оглядів і метааналізів (Butterworth, 2020). Пропонуємо до вашої уваги аналіз сучасних досліджень ефективності амантадину в рамках терапії ХП, ЛІД та COVID‑19.
Лікування хвороби Паркінсона
ХП є тяжким нейродегенеративним захворюванням, для якого характерні брадикінезія, тремор спокою, ригідність, змінена постава та нестабільність ходи. Леводопа, попередник дофаміну, є найефективнішим препаратом для лікування ХП. Втім, після 5‑10 років замісного лікування леводопою більшість пацієнтів із ХП страждають від дискінезії, яка проявляється аномальними мимовільними рухами тулуба, голови та кінцівок, що має серйозний вплив на повсякденне життя пацієнтів та спричинює інвалідизацію (Bastide et al., 2015; Fabbrini et al., 2007).
Дискінезія, принаймні частково, пов’язана з аномальною глутаматергічною активністю смугастого тіла через патологічну взаємодію дофаміну та глутамату (DeLong et al., 2015; Picconi et al., 2012). Патогенез ХП та дискінезія пов’язані з гіперактивністю глутаматергічного рецептора N-метил-D-аспартату (NMDAR) у смугастому тілі. Нині амантадин є єдиним препаратом, у якого антидискінетична активність при ХП має переконливу доказову базу (Bezard et al., 2001; Crosby et al., 2003; Da Silva-Junior et al., 2005; Jankovic et al., 2005).
Механізми дії амантадину при лікуванні моторних симптомів хвороби Паркінсона
За даними дослідження in vitro та in vivo, амантадин має потенціал щодо збільшення синтезу, обміну, вивільнення дофаміну (Hesselink et al., 1999; Mizoguchi et al., 1994; Quack et al., 1995; Takahashi et al., 1996), а також прямого інгібування його зворотного захоплення (Heikkila et al., 1972; Mizoguchi et al., 1994). Додатково механізм пояснюється дією препарату як антагоніста NMDAR (Deepet et al., 1999). В експериментах на тваринах за допомогою техніки церебрального мікродіалізу in vivo продемонстровано, що перфузія амантадину (0,1‑1 мМ) через мікродіалізний зонд призводить до збільшення Ca2+-залежного вивільнення дофаміну. Внутрішньовенне (в/в) введення антагоніста NMDA рецепторів MK 801 значно послаблювало індуковане амантадином збільшення вивільнення дофаміну в смугастому тілі (Takahashi et al., 1996). Ці результати підтверджують концепцію взаємодії дофамінергічної та глутаматергічної передачі в регуляції вивільнення дофаміну в смугастому тілі.
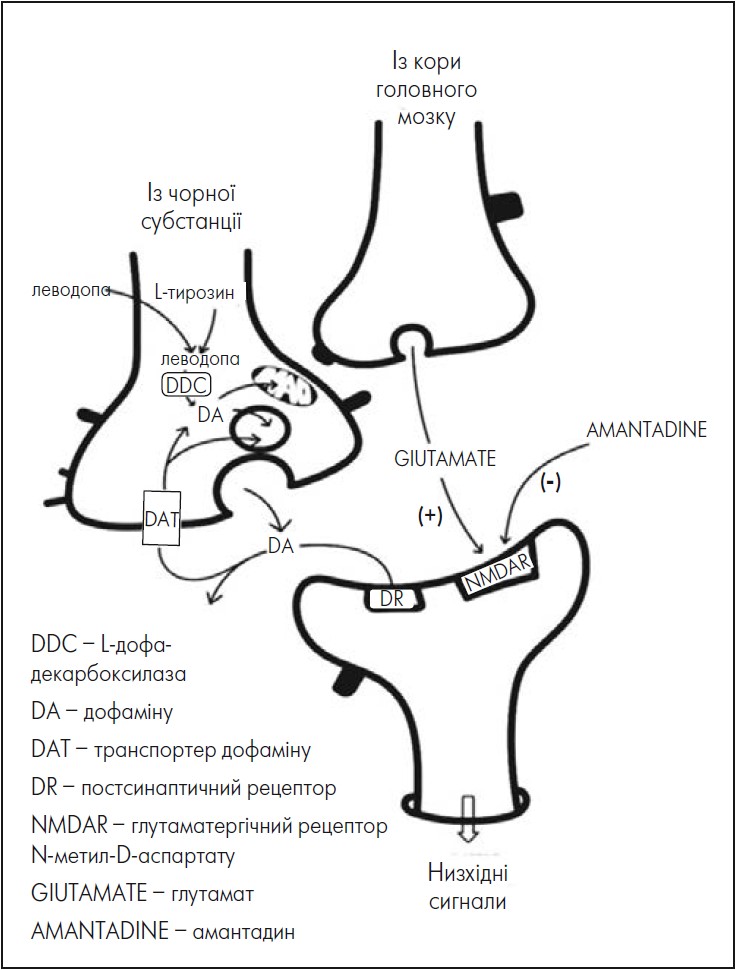
На рисунку зображено дофамінергічне нервове закінчення нігростріарного волокна з ключовими елементами, залученими до синтезу дофаміну: завдяки тирозингідроксилазі L-тирозин (L-TYR) перетворюється на леводопу, а також завдяки L-дофа-декарбоксилазі (DDC) на дофамін, який або зберігається в синаптичній везикулі до вивільнення в синаптичну щілину, або перетворюється на метаболіти за допомогою моноаміноксидази. Вивільнений дофамін активує постсинаптичний рецептор (DR) або повторно захоплюється через транспортер дофаміну (DAT). І леводопа, і амантадин мають потенціал для заповнення нігростріарного дефіциту дофаміну, характерного для ХП: леводопа – завдяки постачанню субстрату для DDC; амантадин – завдяки стимулюванню синтезу дофаміну в поєднанні з блокуванням його повторного захоплення. Користь амантадину для лікування ЛІД, як правило, пояснюється властивостями препарату як неконкурентного антагоніста NMDAR. Блокада цих рецепторів призводить до модуляції взаємодії кортикостріатального глутаматергічного та нігростріарного дофамінергічних входів, що сприяє зменшенню ознак леводопа-індукованих дискінезій (Oertel et al., 2017). Використання позитронно-емісійної томографії та ліганду 6-[18F]-Fluoro-L-Dopa допомогло встановити, що стимуляція активності DDC відбувається внаслідок взаємодії NMDA рецепторів та амантадину (Deepet et al., 1999). За даними досліджень дофамінергічних нейронів, мікроглії та астроглії, клінічно значущі концентрації амантадину можуть мати нейропротекторні властивості внаслідок подвійного механізму дії, зокрема зменшення вивільнення прозапальних чинників з активованої мікроглії разом зі збільшенням експресії гліального нейротрофічного фактора (GDNF) (Ossola et al., 2011).
Рисунок. Схематичне зображення клітинних взаємодій, пов’язаних зі сприятливими ефектами застосування леводопи та амантадину
Адаптовано за W. Oertel et al., 2017.
Корекція моторних симптомів ХП
У клінічному дослідженні, проведеному на замовлення Товариства рухових захворювань (MDS), амантадин був, імовірно, ефективний і клінічно корисний як засіб симптоматичної монотерапії, а також симптоматичної допоміжної терапії при ранній або стабільній ХП. Проте доказів щодо ефективності лікування моторних флуктуацій бракує (Fox et al., 2018). Пошук у Medline, PubMed, Cochrane Library та інших базах даних публікацій, здійснених до травня 2016 р., допоміг виявити дев’ять рандомізованих контрольованих плацебо досліджень (РКД) за участю 303 пацієнтів. Лікування амантадином сприяло значущому зменшенню моторних симптомів ХП, що було визначено за Уніфікованою шкалою оцінювання ХП III (UPDRS) навіть на пізніх стадіях ХП (p=0,01) (Kong et al., 2017).
Корекція моторних флуктуацій
У контрольованому плацебо дослідженні амантадин значно зменшував виразність моторних флуктуацій (n=9; p<0,01), тривалість періоду «вимкнення» (n=14; UPDRS IV пункт 39, 1 [0‑2] проти 1,5 [1‑3]; p<0,001), поліпшував повсякденну активність під час періоду «увімкнення» і «вимкнення» (UPDRS II) (Metman et al., 1999). Спостерігалося скорочення середньої тривалості періоду «вимкнення» на 38% на тлі інфузій амантадину та поліпшення стану на 53% (p<0,001) (Ruzicka et al., 2000). Застигання під час ходи (фризінг) є одним із найтривожніших симптомів прогресуючої ХП, а також деяких атипових синдромів паркінсонізму, яке часто рефрактерне до дофамінергічних препаратів (Giladi, 2008). У двох РКД отримано докази щодо терапевтичної користі амантадину для зменшення фризінгу (Kim et al., 2012; Lee et al., 2013). Акінетичні кризи (як-от гостра акінезія, злоякісний нейролептичний синдром та злоякісний синдром, подібний до нейролептичного; синдром паркінсонізму-гіперпірексії) є найтяжчими ускладненнями ХП і пов’язаних із нею розладів (Thomas et al., 2005). Ці небезпечні для життя стани, що характеризуються гострим наростанням паркінсонічних симптомів, порушенням свідомості, дисфагією, гіпертермією, нечутливістю до дофамінергічної терапії, виникають зі щорічною частотою три випадки на 1000 пацієнтів із паркінсонізмом (Capasso et al., 2015). Вони можуть бути успішно купірувані швидким введенням амантадину у формі в/в розчину (Rascol, 2021). Повідомлялося про користь амантадину для пацієнтів із прогресуючим супрануклеарним паралічем та з кортико-базальною дегенерацією (Kompoliti, Litvan et al., 1998; Kompoliti, Boeve et al., 1998). Звіти про застосування амантадину при мультисистемній атрофії свідчать про різну його ефективність (Wenning et al., 1994).
Лікування леводопа-індукованих дискінезій
Амантадин успішно застосовували для корекції ЛІД (Jenner, 2008). Вплив на дофамін загалом є результатом змін кортикостріатного шляху через NMDAR. Кортикостріарний (глутаматергічний) і нігростріарний (дофамінергічний) вхідні стимули сходяться в смугастому тілі, де вони чинять ключовий модулювальний вплив на активність нейронів і, отже, на руховий контроль. За допомогою методики позитронно-емісійної томографії та ліганду 11 C-N-метил‑3-(тіометилфеніл)-ціанаміду (маркера активованих каналів NMDAR) порівнювали глутаматергічну функцію у пацієнтів із ХП із/без ЛІД (Ahmed et al., 2011). Масштабний (11 досліджень із контролем плацебо, 253 пацієнти з ХП, ускладненою ЛІД) метааналіз даних щодо ефективності антагоністів NMDA-рецепторів засвідчив, що амантадин вірогідно знижує частоту дискінезії піку дози і зменшує загальну тяжкість симптомів (за III і IV частинами UPDRS) (Elahi et al., 2012). Переваги пероральних або в/в форм амантадину оцінювали у пацієнтів із ХП і ЛІД у декількох РКД:
- Лікування амантадином (300 мг/добу) пов’язане з поліпшенням на 64% за шкалою оцінювання дискінезії Раша порівняно з 16% у пацієнтів, які отримували плацебо (Sawada et al., 2010).
- Після 15 днів лікування амантадином загальна кількість балів при оцінюванні дискінезії зменшилася на 45%, спостерігалося зниження балів UPDRS IV за пунктами 32‑34 порівняно з початковим рівнем і групою плацебо (p<0,001) (Thomas et al., 2004).
- Показники чотирьох із восьми шкал демонстрували зменшення дискінезії після 8 тиж. лікування амантадином (до 300 мг/добу протягом 8 тиж.) порівняно з плацебо (Goetz et al., 2013).
- У 3-місячному багатоцентровому РКД AMANDYSK за участю 57 пацієнтів із дискінезією, які отримували амантадин (200 мг/добу) протягом ≥6 міс., скасування перорального застосування амантадину значно погіршувало ознаки ЛІД (Ory-Magne et al., 2014).
Антидискінетичний ефект амантадину підтверджено у низці контрольованих плацебо досліджень, де встановлено значне зниження виразності та тривалості дискінезій без зменшення періоду «увімкнення». Амантадин сприяв зниженню дискінезій піку дози в середньому в 40–60 % (Ahmed et al., 2011; Luginger et al., 2000). За даними багатоцентрового контрольованого плацебо перехресного дослідження з використанням амантадину (300 мг протягом місяця), встановлено зменшення виразності дискінезій за шкалою UPDRS-IV на 64,7% (Stocchi et al., 2013). Мультиваріаційний аналіз засвідчив, що ефект амантадину є найкращим у пацієнтів із пізнішим початком захворювання і тих, хто раніше застосовував агоністи дофамінових рецепторів (Kaplan et al., 2014; Sawada et al., 2010). Антидискінетичний ефект амантадину пов’язують із дією на рівні субталамічного ядра, оскільки препарат неефективний щодо дискінезій, які розвинулися після субталамотомії (Merello et аl., 2006). Результати Кокранівського огляду N.J. Crosby et al. (2003) підтверджують безпеку амантадину та ефективність щодо ЛІД. Нині амантадин включено до європейських та американських рекомендацій як засіб першої лінії лікування дискінезій (рекомендована добова доза – 200-400 мг).
Пізня дискінезія
У низці досліджень вивчали вплив амантадину на пацієнтів із пізньою дискінезією (Angus et al., 1997; Freudenreich and McEvoy, 1995; Pappa et al., 2010). Зокрема, у 18-тижневому подвійному сліпому перехресному РКД продемонстровано, що терапія амантадином (300 мг/добу протягом 7 тиж.) у комбінації з антипсихотиком сприяла редукції симптомів пізньої дискінезії на 15 % за шкалою аномальних мимовільних рухів (AIMS) (Angus et al., 1997). У подвійному сліпому РКД приймання амантадину (100 мг/добу) значуще знижувало загальну оцінку за AIMS (на ~ 22 %) і за окремими її підшкалами у пацієнтів із пізньою дискінезією та стабільним психіатричним станом (Pappa et al., 2010). Низка досліджень містить звіти про клінічні випадки, що демонструють сприятливий вплив амантадину (Allen, 1982; Freudenreich and McEvoy, 1995). За результатами клінічних досліджень Підкомітет із розроблення рекомендацій Американської академії неврології (AAN) підготував науково обґрунтовану настанову «Лікування пізніх синдромів», визначивши призначення амантадину (на короткий термін) разом з антипсихотиком як рекомендацію (рівень доказовості C): «може розглядатися як засіб лікування пізнього синдрому» (Bhidayasiri et al., 2013; 2018). Докази ефективності амантадину є лише для одночасного призначення з флупентиксолу деканоатом, хлорпромазином, галоперидолом, трифлуоперазином.
Амантадин у терапії пацієнтів із ХП та COVID‑19
ХП і COVID‑19 мають багато спільних рис, зокрема вікову залежність тяжкості захворювання та зв’язок із такими супутніми станами, як діабет, респіраторні проблеми та серцево-судинні патології. Відомо, що симптоми ХП погіршуються під час системних інфекцій, а симптоми COVID‑19, як-от лихоманка, втома та стрес, не тільки посилюють тремор, порушення ходи та дискінезії при ХП, але також можуть знижувати ефективність леводопи (Butterworth et al., 2020).
Імовірність взаємодії COVID‑19 і ХП, яка може призвести до клінічного погіршення за обох станів, можливо пом’якшити після початку лікування амантадином. Останні дослідження надають переконливі докази користі амантадину при лікуванні COVID‑19. Ідеться про два незалежні механізми: 1) зниження експресії протеаз у клітинах, результатом є порушення вивільнення вірусного геному в цитоплазмі клітини-хазяїна; 2) активація NMDA рецепторів, яка залучена до патогенезу гострої дихальної недостатності, характерної для COVID‑19 (Butterworth et al., 2020).
Висновки
Амантадин як ефективний неконкурентний антагоніст NMDA є потенційно дієвим засобом лікування ЛІД. Докази ефективності препарату для лікування ЛІД у пацієнтів із ХП ґрунтуються на результатах РКД, опублікованих за останні два десятиліття, у межах яких використовували діапазон дозування амантадину 200‑400 мг/добу.
Терапія амантадином може також стати вибором для пацієнтів із ХП під час лікування COVID‑19, зважаючи на зростаючу кількість доказів на користь того, що вказаний препарат, окрім доведеного впливу на моторику та дискінезії, може обмежувати розмноження вірусу SARS-CoV‑2.
UA-LEVC-PUB-022023-035
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 1 (64) 2023 р.
СТАТТІ ЗА ТЕМОЮ Неврологія
Проблема когнітивних розладів є однією з найважливіших у сучасній клінічній медицині. Це зумовлено не тільки збільшенням частки людей старшого віку серед населення, а й посиленням ролі стресу та інших патогенетичних чинників. У березні відбувся семінар «Академія сімейного лікаря. Біль в грудній клітині. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста», у якому прийняли участь провідні вітчизняні науковці і фахівці різних галузей. У рамках заходу професор кафедри військової терапії Української військово-медичної академії Міністерства оборони України, кандидат медичних наук Мар’яна Миколаївна Селюк представила доповідь «Війна та когнітивні порушення. Причина чи наслідок? Як вирішити проблему?». Подаємо огляд цієї доповіді у форматі «запитання – відповідь»....
Хоча нестероїдні протизапальні препарати (НПЗП) мають численні серйозні побічні ефекти, вони належать до найчастіше застосовуваних препаратів у всьому світі (McGettigan P., Henry D., 2013). Через часте застосування побічні дії НПЗП становлять значну загрозу для громадського здоров’я. Так, уже декілька декад тому було описано підвищення артеріального тиску та ризик загострень серцевої недостатності на тлі прийому цих препаратів (Staessen J. et al., 1983; Cannon P.J., 1986)....
У лютому відбувся медичний форум Ukraine Neuro Global 2024, організований ГО «Українська асоціація медичної освіти» (м. Київ). Під час заходу обговорювалися найактуальніші проблеми сучасної неврології. У рамках форуму відбувся сателітний симпозіум «Актуальні питання фармакотерапії в неврології». Слово мала в.о. завідувача кафедри неврології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Марина Анатоліївна Тріщинська з доповіддю «Краніоцервікалгії: особливості діагностики та лікування»....
Запаморочення є поширеним та іноді стійким симптомом після струсу мозку чи легкої черепно-мозкової травми (лЧМТ). Терміном «запаморочення» часто описують декілька симптомів, як-от головокружіння (вертиго; ілюзія руху), порушення рівноваги (нестійкість, нестабільність) і, власне, запаморочення (пресинкопальний стан). Запаморочення після струсу мозку є клінічним викликом, оскільки існує багато причин цього розладу, а його ведення залежить від етіології [1-3]. Однією з таких причин є пошкодження периферичної вестибулярної системи (внутрішнього вуха). У разі травм, отриманих під час війни, лЧМТ часто пов’язана з вибуховою дією, яка може пошкоджувати внутрішнє вухо. Лікарям важливо розуміти вестибулярні наслідки вибухової лЧМТ, оскільки ЧМТ є дуже характерною для сучасних війн [4]....