Эффективность и безопасность клотримазола в форме вагинальных таблеток по сравнению с пероральным флуконазолом в лечении тяжелого вульвовагинального кандидоз
Вульвовагинальный кандидоз (ВВК) – симптоматический вагинит, который по крайней мере один раз в жизни переносят 75% женщин детородного возраста. Заболевание может быть неосложненным и осложненным. Последняя категория включает рецидивирующий (РВВК) и тяжелый вульвовагинальный кандидоз (ТВВК). Центры по контролю и профилактике заболеваний (CDC, США) для лечения ТВВК предлагают использовать две дозы перорального флуконазола 150 мг. В ряде других руководств для лечения РВВК и ТВВК рекомендуется клотримазол в форме вагинальных таблеток 500 мг. Целью настоящего исследования было сравнить эффективность и безопасность этих двух подходов у пациенток с ТВВК.
Материалы и методы
В открытое проспективное рандомизированное исследование включали женщин в возрасте 18-50 лет с ТВВК и без сопутствующих заболеваний. В ходе лечения пациентки должны были воздерживаться от половых контактов либо использовать презервативы. Кроме того, не разрешалось применять другие вагинальные средства. Пациенток с неосложненным и рецидивирующим ВВК из исследования исключали. Критериями исключения также были: заболевания, передающиеся половым путем, или другие гинекологические нарушения, требующие терапии; заболевания, предрасполагающие к кандидозам (например, сахарный диабет), лечение антибиотиками или кортикостероидами; применение противогрибкового препарата в пределах 7 дней до включения; ожидаемая менструация в пределах 7 дней от начала лечения; инфицирование ≥1 штаммом Candida.
Пациенток, соответствовавших вышеуказанным критериям, рандомизировали для получения клотримазола в форме вагинальных таблеток 500 мг или перорального флуконазола 150 мг. Оба препарата применялись двукратно в 1-й и 4-й день.
Контрольные обследования проводили через 7-14 и 30-35 дней после второй дозы. В ходе обследований у пациенток оценивали симптоматику, расспрашивали их о наличии побочных эффектов и использовании сопутствующих препаратов. Клиническое излечение определяли как разрешение симптомов, присутствовавших до начала терапии, при этом общая тяжесть симптомов не должна была превышать 2 балла. Улучшение определяли как значительное (на ≥50%) уменьшение тяжести исходных симптомов. При отсутствии клинического излечения или улучшения лечение считали неэффективным. Микологическое излечение определяли по отрицательным результатам культурального исследования.
Результаты
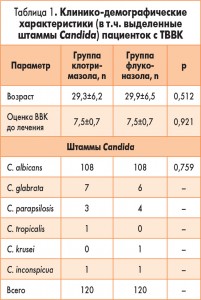
В исследование было включено 240 пациенток с ТВВК (средний возраст – 29 лет). По исходным клинико-демографическим характеристикам группы терапии статистически не различались (табл. 1). В 90% случаев заболевание было вызвано C. albicans. Кандиды non-albicans включали C. glabrata (5,4%), С. parapsilosis (2,9%), C. inconspicua (0,8%), C. tropicalis и C. krusei (по 0,4%).
Восемь пациенток (по 4 в каждой группе) завершили исследование досрочно из-за нежелания продолжать лечение. Три женщины (все из группы флуконазола) прекратили терапию вследствие побочных эффектов или наступившей беременности. Шесть пациенток (2 из группы клотримазола и 4 из группы флуконазола) не явились на контрольное обследование. В окончательном анализе безопасность оценивали у 115 пациенток группы клотримазола и у 113 участниц группы флуконазола, эффективность – у 114 и 109 женщин соответственно.
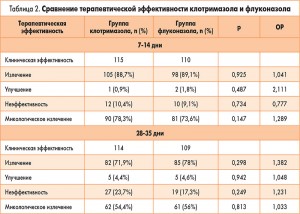
Частота клинического излечения при обследовании через 7-15 дней от начала терапии в группах клотримазола и флуконазола составила 88,7 и 89,1%, через 30-35 дней – 71,9 и 78% соответственно. Частота микологического излечения через 7-15 дней в двух группах терапии составила 78,3 и 73,6%, через 30-35 дней – 54,4 и 56% соответственно (р>0,05) (табл. 2).
Облегчение симптомов, таких как зуд, жжение, выделения и эритема, в группе клотримазола достигалось значительно быстрее по сравнению с группой флуконазола (рис. 1). Микологическая неэффективность наблюдалась во всех случаях инфицирования C. inconspicua, C. krusei и C. tropicalis, а также у 12 из 13 пациенток, у которых заболевание было вызвано C. glabrata.
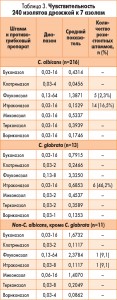
В таблице 3 представлены результаты определения in vitro чувствительности 240 изолятов дрожжей к 7 азолам. Значения МПК90 (минимальной концентрации, которая подавляет рост 90% штаммов) для C. albicans, C. glabrata и non-Candida albicans (кроме C. glabrata) составили 0,25-4, 0,25-4 и 0,13-4 мкг/мл соответственно, количество резистентных штаммов – 0-6,5, 0-46,2 и 0-9,1% соответственно.
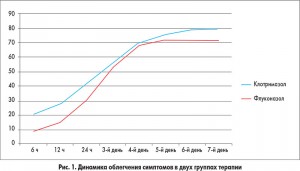
До начала лечения нормальная вагинальная микрофлора (оценивалась по шкале Nugent) присутствовала у 30,8% женщин группы клотримазола и у 28,3% пациенток группы флуконазола. На первом контрольном обследовании эти показатели составили 83,5 и 72,7%, на втором – 79,8 и 80% соответственно (р>0,05). По количеству лактобацилл группы терапии также не различались.
В группе клотримазола побочные эффекты имели преимущественно локальный и легкий характер. В то же время большинство побочных эффектов в группе флуконазола были системными (табл. 4).
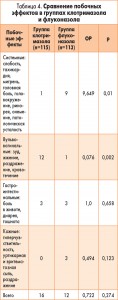
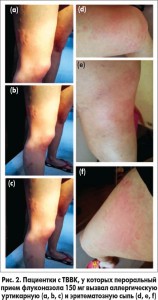
У двух пациенток, получавших флуконазол, наблюдались тяжелые кожные аллергические реакции; эти больные завершили исследование досрочно (рис. 2). В одном случае в группе флуконазола потребовалась внутривенная инфузия дексаметазона на протяжении 4 дней и дифенгидрамина в течение 7 дней. Две пациентки в группе флуконазола были беременны; у одной из них произошел спонтанный аборт, у другой было проведено искусственное прерывание беременности.
Обсуждение
Клотримазол – антимикотический препарат с широким спектром активности, применяющийся в лечении кандидоза и других грибковых инфекций. Главный механизм действия клотримазола в отношении дрожжей основан на подавлении энзиматического превращения ланостерола в эргостерол (последний является эссенциальным компонентом клеточной мембраны гриба). При лечении ВВК рекомендованные дозы клотримазола составляют 100, 200 или 500 мг 1 р/сут в течение 6-ти, 3-х или 1-го дня соответственно.
Ранее Richter и соавт. (2005) установили, что 3,6 и 16,2% вагинальных изолятов C. albicans были резистентными к флуконазолу и итраконазолу соответственно. В настоящем исследовании азолы демонстрировали сопоставимую активность против изолятов C. albicans, в частности, резистентность к флуконазолу наблюдалась в 2,3% случаев. В то же время показатель МПК90 для клотримазола для всех изолятов дрожжей у пациенток с ТВВК был самым низким из 7 исследованных препаратов, за исключением вориконазола, который в настоящее время не применяется в лечении ВВК. Высокая противогрибковая активность и высокие локальные концентрации, достигаемые при лечении клотримазолом в форме вагинальных таблеток, могут обеспечивать лучшую эффективность.
Ross и соавт. (1995) изучали влияние инфекции C. albicans и терапии клотримазолом на вагинальную микрофлору in vitro. Экспозиция C. albicans вызывала нарушения микрофлоры, тогда как клотримазол приводил к полному уничтожению инфекции в течение 48 ч.
Boag и соавт. оценивали влияние клотримазола в форме вагинальных пессариев 500 мг и перорального флуконазола 150 мг на вагинальную микрофлору. В течение 10 дней после лечения значимые различия показателей микрофлоры по сравнению с исходными и между группами терапии отсутствовали.
В настоящем исследовании микрофлору оценивали по шкале Nugent и количеству лактобацилл в вагинальных мазках. Процент нормальных мазков до начала лечения на первом и втором контрольном обследовании в группах клотримазола и флуконазола существенно не отличался. После лечения состав вагинальной микрофлоры в обеих группах значительно улучшился.
Ritter и соавт. (1982) установили, что фунгицидные концентрации клотримазола в вагинальной жидкости обнаруживаются в течение 3 дней после применения одной вагинальной таблетки 500 мг. При этом плазменные уровни клотримазола были ниже 0,1 мкг/мл, что обеспечивало высокую безопасность и хорошую переносимость лечения. Топические формы клотримазола являются безрецептурными препаратами и ассоциируются с низкой частотой побочных эффектов. При их использовании не повышается риск аномалий развития плода, и эти препараты могут назначаться в период грудного вскармливания. В настоящем исследовании побочные реакции в группе клотримазола были преимущественно локальными, и ни одна пациентка не прервала лечение вследствие тяжелых неблагоприятных эффектов.
Назначение пероральных азолов, включая флуконазол, не рекомендуется в I триместре беременности из-за риска врожденных дефектов плода. В частности, в датском исследовании прием флуконазола в этих сроках гестации ассоциировался более чем с трехкратным повышением риска рождения ребенка с тетрадой Фалло. Кроме того, частыми побочными эффектами пероральных азолов являются диарея, тошнота, головная боль, сыпь и аллергические реакции. В настоящем исследовании у двух пациенток из группы флуконазола наблюдалась тяжелая кожная аллергия, и они были вынуждены завершить лечение досрочно. У одной беременной пациентки, получавшей флуконазол, произошел спонтанный аборт, хотя точную причину последнего определить не представлялось возможным.
В целом эти данные свидетельствуют о большей безопасности применения клотримазола в форме вагинальных таблеток по сравнению с пероральным флуконазолом у женщин с ТВВК репродуктивного возраста.
Таким образом, результаты исследования показали, что у пациенток с ТВВК две дозы клотримазола в форме вагинальных таблеток 500 мг и перорального флуконазола 150 мг обеспечивают одинаковые показатели клинического и микологического излечения. Преимуществом клотримазола является более быстрое облегчение симптомов кандидоза и более высокий профиль безопасности.
Статья печатается в сокращении.
Список литературы находится в редакции.
Zhou X., Li T., Fan S. et al. The efficacy and safety of clotrimazole vaginal tablet vs. oral fluconazole in treating severe vulvovaginal candidiasis. Mycoses. 2016 Apr 13.
Перевел с англ. Алексей Терещенко
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Чи варто змінювати свої харчові звички під час вагітності? Довкола цієї теми є багато суперечностей і рекомендацій, у яких легко заплутатися. Команда платформи доказової інформації про здоров’я «Бережи себе» спільно з лікарем-дієтологом Тетяною Лакустою з’ясували, чим раціон жінки в цей період особливий та на що слід звернути увагу. ...
Хронічний тазовий біль (ХТБ) є поширеним патологічним станом, який відзначається у жінок будь-якого віку і супроводжується сексуальною дисфункцією, емоційною лабільністю, аномальними матковими кровотечами, порушенням сечовипускання, розладами з боку кишечника тощо. Пацієнтки, які страждають на ХТБ, часто скаржаться на симптоми тривоги та депресії, що негативно позначається на їхній повсякденній активності, включаючи зниження працездатності та погіршення якості життя [1]. Сьогодні проблема ХТБ є економічним тягарем, пов’язаним із прямими або непрямими медичними витратами, які в середньому в різних країнах світу оцінюються у 4,9 млрд доларів на рік [2]. Раціональна фармакотерапія,спрямована на полегшення та контроль симптомів болю, є ключовою стратегією боротьби із ХТБ...
Дефіцит заліза є найпоширенішим патологічним станом у світі та однією з п’яти основних причин інвалідності. У той час як низький показник феритину у сироватці крові є діагностичною ознакою залізодефіциту, підвищений його рівень визначається як гострофазовий маркер, що може реєструватися при запальних станах уже в І триместрі вагітності. Відповідно до сучасних настанов, проведення рутинного скринінгу на залізодефіцит у невагітних та вагітних жінок за відсутності ознак анемії не рекомендоване. З огляду на останні літературні дані ця рекомендація має бути переглянута...
Наказ Міністерства охорони здоров’я України від 25.08.2023 № 1533 ...