Экспертные рекомендации и реалии практики при выборе антикоагулянта для пациентов с острым коронарным синдромом
По материалам XVII Национального конгресса кардиологов Украины (21-23 сентября, г. Киев)
На клинические исходы у пациентов с нестабильной стенокардией и острым инфарктом миокарда (ОИМ) влияют многие факторы, одним из которых является характер антикоагулянтной терапии.

Доктор медицинских наук, профессор кафедры госпитальной терапии № 2 Днепропетровской медицинской академии МЗ Украины (ДМА) Елена Акиндиновна Коваль прокомментировала принципы выбора и назначения инъекционных антикоагулянтов при различных клинических сценариях острого коронарного синдрома (ОКС).
Клинический сценарий № 1
Мужчина 75 лет, с ОИМ, которому проводится тромболитическая терапия (ТЛТ) тенектеплазой на догоспитальном этапе.
Европейские стандарты антикоагулянтной терапии при ОКС (рекомендации ESC 2012 г.) отдают приоритет эноксапарину по сравнению с нефракционированным гепарином (НФГ) в качестве адъювантного антикоагулянта при проведении ТЛТ (класс рекомендации I, уровень доказательности А), а также при первичном чрескожном коронарном вмешательстве – ПЧКВ (класс рекомендации IIb, уровень доказательности B). Первую дозу эноксапарина при ТЛТ – 30 мг предписывается вводить внутривенно болюсно (пациентам моложе 75 лет), затем в дозе 1 мг/кг массы тела подкожно через каждые 12 ч для пациентов всех возрастов (длительность терапии – до 8 дней). Перед ПЧКВ эноксапарин вводится внутривенно болюсно в дозе 0,5 мг/кг массы тела. В этих же рекомендациях указано, что фондапаринукс противопоказан при догоспитальной ТЛТ, а также при ПЧКВ без использования НФГ, однако его можно применять при госпитальной ТЛТ стрептокиназой и при госпитальной терапии всех форм ОКС с учетом индивидуальных рисков.
Унифицированный клинический протокол медицинской помощи при ОКС с элевацией сегмента ST (2014 г.) МЗ Украины повторяет данные рекомендации для эноксапарина при проведении ТЛТ, однако допускает выбор из трех опций адъювантной антикоагулянтной терапии – НФГ, фондапаринукс и эноксапарин, что, по-видимому, продиктовано социальным аспектом оказания помощи. Первую дозу эноксапарина следует вводить в промежуток времени за 15 мин до или 30 мин после начала ТЛТ. У пациентов старше 75 лет и с проявлениями почечной недостаточности внутривенный болюс эноксапарина не вводится, терапия начинается с подкожных инъекций в дозе 0,75 мг/кг массы тела.
Возраст пациента – 75 лет в данном случае является пограничным, но для эффекта быстрого фибринолизиса под действием мощного тромболитика (тенектеплазы) введение первого болюса эноксапарина внутривенно является возможным.
Профессор Е.А. Коваль подчеркнула, что неправильное применение или игнорирование адъювантной антикоагулянтной терапии даже при успешной догоспитальной ТЛТ может обернуться повторным закрытием инфарктзависимой коронарной артерии, и проиллюстрировала это еще одним клиническим примером, когда пациенту после успешного тромболизиса тенектеплазой без сопутствующей антикоагуляции потребовалась ургентная ЧКВ по прибытию в стационар.
Комментируя медико-социальный аспект выбора антикоагулянта при ОКС, профессор Е.А. Коваль уделила внимание вопросам, связанным с появлением доступных по стоимости биосимиляров низкомолекулярных гепаринов (НМГ).
При обсуждении данной темы были представлены результаты небольшого слепого исследования, проведенного на клинической базе кафедры внутренней медицины ДМА для сравнения фармакокинетического профиля различных формуляций эноксапарина у пациентов с ОИМ по динамике активированного частичного тромбопластинового времени (АЧТВ) – для оценки фармакокинетики, не контроля за эффективностью. Дизайн исследования предусматривал независимый и ослепленный лабораторный контроль АЧТВ до и в течение 48 ч после введения Клексана или эноксапарина украинского производства. Решение о назначении того или иного препарата принимали лечащие врачи. У пациентов, получавших Клексан и биосимиляр, наблюдалась различная динамика АЧТВ в течение 48 ч от начала терапии особенно выраженная в первые 6-9 ч от начала терапии. Применение оригинального препарата Клексан приводило к более предсказуемому изменению АЧТВ в первые 9 ч, что особенно важно для догоспитального и раннего госпитального этапов лечения ОИМ, а также при планирующемся ЧКВ.
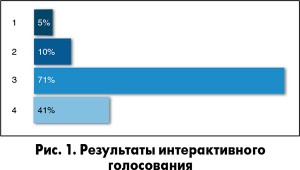
В ходе интерактивного голосования профессор Е.А. Коваль предложила аудитории ответить на следующий вопрос: может ли изменение отдельных лабораторных характеристик иметь клинические последствия при использовании разных антикоагулянтов?
1. Данный вопрос представляет только академический интерес.
2. Возможно, с ограниченными конечными точками.
3. Да, влияет на смертность, частоту ИМ и реваскуляризаций.
4. Подобное влияние не изучалось.
Большинство врачей выбрали правильный вариант.
Профессор Е.А. Коваль обосновала ответ результатами исследования французских ученых, которые изучали прогностическую ценность пяти биомаркеров воспаления и тромбообразования у пациентов с ОКС без элевации сегмента ST, а также влияние терапии НФГ и эноксапарином на эти маркеры. Многовариантный анализ показал, что повышение уровня фактора фон Виллебранда в первые 48 ч являлось независимым и достоверным предиктором неблагоприятного исхода (смерть, развитие ИМ, рефрактерная стенокардия) и потребности в реваскуляризации миокарда на 14-е и 30-е сутки наблюдения. Эноксапарин вызывал ингибирование высвобождения фактора фон Виллебранда, что ассоциировалось с достоверным снижением частоты неблагоприятных событий комбинированной конечной точки по сравнению с группой НФГ (G. Montalescot et al., 1998).
Таким образом, разница в динамике лабораторных показателей коагуляции действительно может определять различия исходов ОКС при терапии сравниваемыми антикоагулянтами. Для пациентов с ОИМ или нестабильной стенокардией это может иметь серьезные клинические последствия. Поэтому очевидно, что назрела необходимость проведения исследований с целью подтверждения терапевтической эффективности биосимиляров, используемых в лечении больных высокого кардиоваскулярного риска, тем более что это отвечает требованиям современного украинского законодательства.
Клинический сценарий № 2
Пациент 76 лет, с ОИМ, доставлен в клинику, где возможно выполнение ЧКВ.
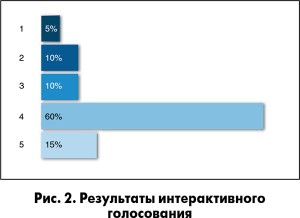
Вопрос к аудитории: будет ли решение о введении эноксапарина (Клексана) безопасным и эффективным при выполнении ПЧКВ у пациента такого возраста?
1. Небезопасно в связи с риском кровотечения.
2. Неэффективно в сравнении с НФГ.
3. Эффективность сопоставима с НФГ.
4. Эффективно и безопасно в отношении малых кровотечений.
5. НФГ имеет преимущества, особенно в пожилом возрасте.
Мнения врачей разошлись, но большинство уверены в эффективности и безопасности эноксапарина у пациентов старшей возрастной категории. Действительно, как показал недавно опубликованный субанализ результатов исследования ATOLL, эноксапарин у пациентов с ОКС в возрасте 75 лет и старше не уменьшал частоту конечных точек (смерть, повторный ОКС, экстренная реваскуляризация) в течение 30 дней после ПЧКВ по сравнению с НФГ, но частота малых кровотечений в группе эноксапарина была достоверно ниже: 5,9 против 22,8%. По результатам этого субанализа был сделан вывод о том, что внутривенное введение эноксапарина (Клексана) является безопасной альтернативой НФГ при выполнении ПЧКВ у пожилых пациентов с ОКС (Z. Liu et al., 2016).
В последних рекомендациях Европейского общества кардиологов и Европейской ассоциации кардиоторакальной хирургии по реваскуляризации миокарда (ESC/EACTS 2014 г.) внутривенная инфузия эноксапарина в дозе 0,5 мг/кг массы тела получила класс рекомендации IIa при проведении ПЧКВ у больных ОИМ с элевацией сегмента ST (НФГ – I класс рекомендации). Украинский клинический протокол по ОКС с элевацией сегмента ST (2014) аналогично допускает выбор из двух антикоагулянтов при проведении ПЧКВ – НФГ или эноксапарина. Однако докладчик напомнила, что нежелательно переходить с одного антикоагулянта на другой. Для пациентов, у которых терапия ОКС начиналась с эноксапарина, перед ПЧКВ оптимальным решением будет введение болюса эноксапарина 0,5 мг/кг, если после предыдущей инъекции прошло более 8 ч.
Клинический сценарий № 3
Женщина 67 лет, с повторным ОИМ без элевации сегмента ST (предыдущий перенесла 6 мес назад), в течение недели прогрессирует стенокардия. На ЭКГ – выраженная депрессия сегмента ST. Тропонин 2,3 нг/мл. Болеет сахарным диабетом (СД) 2 типа в течение двух лет, инсулинотерапию не получает. АГ, дислипидемия. Ожирение II степени (индекс массы тела 38,8). Фибромиома матки без кровотечений.
В данном клиническом примере докладчик снова отметила социальный аспект оказания помощи пациентам с ОКС в Украине, а именно: по ургентным показаниям ЧКВ выполняется в рамках бюджетной программы только пациентам с ОИМ с элевацией сегмента ST. Родственникам больной была предложена инвазивная реваскуляризация за собственные средства. В результате потребовалась неделя на сбор средств, и пациентке было успешно проведено ЧКВ на фоне плановой терапии Клексаном в дозе 1 мг/кг подкожно 2 р/сут.
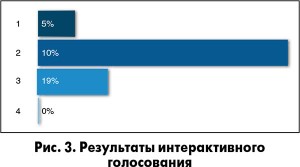
Возникает вопрос: противоречит ли данное решение современным рекомендациям по применению антикоагулянтов у больных ОКС без элевации сегмента ST?
1. Да, противоречит.
2. Не противоречит, так как больная исходно подлежит инвазивной тактике ведения.
3. Пациентка должна получать фондапаринукс с переходом на НФГ перед процедурой.
4. НФГ исходно имеет преимущества, особенно в пожилом возрасте.
Выбор стратегии инвазивного лечения в данном случае абсолютно оправдан, поскольку пациентка имеет сразу несколько значимых факторов тромботического риска: ОИМ в анамнезе, высокий уровень сердечного тропонина, стойкую депрессию сегмента ST и СД. Риск перехода в ОИМ с элевацией сегмента ST очень высокий. В то же время геморрагический риск у пациентки умеренный, его формируют только возраст старше 65 лет и женский пол.
Европейские рекомендации по ОКС без элевации сегмента ST (ESC 2015 г.) предписывают фондапаринукс (2,5 мг/сут подкожно) независимо от стратегии лечения. Эноксапарин (1 мг/кг 2 р/сут подкожно) или НФГ рекомендуются, если фондапаринукс не доступен. Вместе с тем не рекомендуется одновременное применение НФГ и НМГ, а такое переключение при решении вопроса о выполнении ЧКВ будет неизбежным. Поэтому в данном случае, с учетом того что вариант отсроченной ЧКВ был предусмотрен заранее, назначение эноксапарина с первых часов ОКС является вполне обоснованным и рациональным решением.
В пользу выбора эноксапарина также свидетельствуют результаты анализа Национального французского реестра FAST-MI, который ведется с 2010 г. и содержит данные 1734 пациентов с ОИМ без элевации сегмента ST. 240 пациентов получали антикоагулянтную терапию фондапаринуксом, 1027 – эноксапарином. Пациенты имели сопоставимые оценки риска по шкале GRACE. В обеих группах частота применения инвазивной стратегии составила 69%. Частота госпитальных кровотечений и годичная выживаемость достоверно не различались между группами эноксапарина и фондапаринукса. Многовариантный анализ Кокса, полностью скорректированный с учетом остальных влияющих факторов, показал, что применение фондапаринукса не ассоциировалось со снижением риска смерти. Анализ с подбором пар пациентов с одинаковой предрасположенностью к кровотечениям также показал сопоставимую годичную выживаемость в группах эноксапарина и фондапаринукса. Лучшая выживаемость отмечена в подгруппе пациентов, которым фондапаринукс вводили в комбинации с НФГ (E. Puymirat et al., 2014).
Выводы
Эноксапарин (оригинальный препарат Клексан) является оптимальным антикоагулянтом для использования при всех формах ОКС независимо от стратегии лечения.
Фондапаринукс при современной тактике терапии не обеспечивает достоверно лучшей выживаемости больных независимо от формы ОКС, но в целом характеризуется высокой безопасностью и может применяться у госпитализированных пациентов с низким и очень низким риском, у которых не планируется инвазивная реваскуляризация миокарда.
Для широкого применения биосимиляров Клексана необходимо изучение их терапевтической эквивалентности.
Подготовил Дмитрий Молчанов
Справка ЗУ
Согласно определению Европейского агентства лекарственных средств (EMA) биосимиляр – это лекарственный препарат, подобный по эффективности, безопасности и качеству зарегистрированному референтному биотехнологическому лекарственному препарату, срок действия патентной защиты которого истек. В отличие от генериков (копий низкомолекулярных синтетических лекарственных средств) биосимиляр никогда не может быть идентичным референтному препарату, а только подобным ему, поскольку производство биотехнологических лекарственных средств, действующим началом которых является белковая молекула, связано с участием биологических объектов, обладающих значительной индивидуальностью и изменчивостью.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....