Новые открытия в области регуляции ренин-ангиотензиновой системы

Представления о компонентах и функциях ренин-ангиотензиновой системы (РАС) в организме человека претерпели серьезные изменения на рубеже столетий. Изоформа ангиотензина 1-7, открытая Santos и соавт. в 1988 г., через двадцать лет была признана ключевым биологически активным звеном РАС. Ее эффекты противоположны неблагоприятным эффектам главного прессорного пептида РАС – ангиотензина II, которые так хорошо знакомы кардиологам и на блокировании которых основывается действие антагонистов рецепторов ангиотензина 1 типа – сартанов.
Следующим шагом стало открытие гомолога ангиотензинпревращающего фермента – АПФ2, активность которого не подавляется под действием ингибиторов АПФ. АПФ2 катализирует образование ангиотензина-(1-7) из ангиотензина II, а также менее эффективным путем гидролиза ангиотензина I до ангиотензина-(1-9) с последующим образованием ангиотензина-(1-7) под действием АПФ (M. Donoghue et al., 2000; S.R. Tipnis et al., 2000).
Также было установлено, что спаренный с G-протеином рецептор Mas на поверхности клеток является функциональным связывающим сайтом для ангиотензина-(1-7) (R. Santos et al., 2003). Вместе эти три новые звена РАС составляют контррегуляторный сигнальный путь АПФ2 / ангиотензин-(1-7) / Mas, который по своей физиологической роли является антиподом системы АПФ / ангиотензин II / АТ1-рецептор.
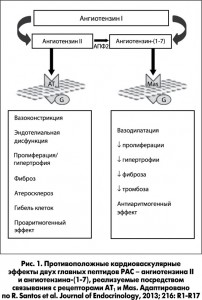
Таким образом, подтвердилась гипотеза о дуализме РАС, и теперь известно, что наряду с вазоконстрикторной и пролиферативной осью РАС существует антагонистическая ось, реализующая противоположные (а в контексте патогенеза сердечно-сосудистой патологии – благоприятные) эффекты в стенке сосудов, миокарде, почках и других органах (рис. 1).
Важнейшим связующим звеном между двумя осями РАС является АПФ2, так как этот фермент способен превращать вазоконстрикторный/пролиферативный пептид ангиотензин II в вазодилатирующий/антипролиферативный ангиотензин-(1-7).
АПФ2 и уникальность олмесартана среди ингибиторов РАС
АПФ2 в большом количестве синтезируется в почках, особенно в клетках эпителия проксимальных канальцев. В экспериментах на мышиной модели диабетической нефропатии повышение экспрессии АПФ2 сопровождалось угнетением АПФ, в связи с чем было высказано предположение о ренопротективном значении АПФ2 (M. Ye et al., 2004). АПФ2 определяется в моче и считается перспективным неинвазивным биомаркером заболеваний почек (J. Wysocki et al., 2013). Повышение концентрации АПФ2 наблюдалось у пациентов с диабетической нефропатией и перенесших трансплантацию почки (G. Wang et al., 2008; S. Mizuiri et al., 2011; F. Xiao et al., 2012).
До недавних пор не изучалось содержание АПФ2 у пациентов, принимающих сердечно-сосудистые препараты. Японские авторы первыми провели подобное исследование (M. Furuhashi et al. American Journal of Hypertension, 2015; 28 (1): 15-21), в котором изучали, как влияет на уровень АПФ2 терапия антагонистами РАС (ингибиторами АПФ и блокаторами рецепторов 1 типа к ангиотензину II– БРА) в сравнении с препаратами альтернативного механизма действия – блокаторами кальциевых каналов (БКК).
Обследовали 100 практически здоровых лиц (контрольная группа) и 100 пациентов с артериальной гипертензией (АГ), которые лечились в течение 1 года. Из них 22 принимали амлодипин, 7 – нифедипин длительного действия, 6 – эналаприл, 5 – лозартан, 19 – кандесартан, 15 – валсартан, 13 – телмисартан и 13 – олмесартан. Подгруппа БКК должна была служить дополнительным контролем по отношению к пациентам, принимавшим антагонисты РАС, поэтому в нее включали только при условии монотерапии амлодипином или нифедипином. Для подгрупп ингибиторов АПФ и БРА требования монотерапии не было, и некоторые из включенных пациентов принимали ингибиторы РАС в составе комбинированной антигипертензивной терапии.
Концентрацию АПФ2 в моче определяли с помощью коммерческого набора иммуносорбентного анализа (AdipoGen, Корея) с нормализацией по уровню креатинина (в мк на 1 г креатинина). Кроме АПФ2, определяли ряд биохимических параметров крови.
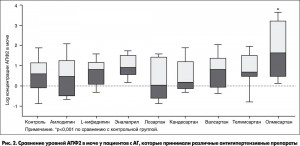
В результате контрольная группа и группы терапии АГ не различались по клиническим характеристикам, за исключением гликемии, гликированного гемоглобина (HbA1c), соотношения альбумин/креатинин в моче и содержания АПФ2. Пациенты, которые принимали эналаприл, телмисартан или олмесартан, имели достоверно более высокие уровни глюкозы и HbA1c, чем субъекты контрольной группы. Соотношение альбумин/креатинин в моче (индикатор альбуминурии) было достоверно выше у пациентов, которые принимали эналаприл, чем в контрольной группе: 67 против 9 соответственно (р<0,05). Уровень АПФ2 в моче был достоверно выше у пациентов, принимавших олмесартан: в среднем 5,8 мкг/г креатинина по сравнению с 1,9 в контрольной группе (р<0,001). Все остальные сравнения между контрольной группой и пациентами, которые принимали БКК или другие ингибиторы РАС, кроме олмесартана, были не достоверными (рис. 2). Многовариантный регрессионный анализ с поправками на возраст, пол и другие факторы показал, что применение олмесартана было независимым предиктором повышения уровня АПФ2 (коэффициент регрессии t=3,38; р<0,001) и полностью объясняло 32,6% вариативности этого параметра.
Практическое значение полученных результатов
Исследование Furuhashi и соавт. – первое в своем роде, продемонстрировавшее, что олмесартан обладает уникальным свойством повышать концентрацию АПФ2 в моче (а значит, и в канальцах почек), в то время как остальные антигипертензивные препараты, включая БКК и другие антагонисты РАС, такого эффекта не проявляли.
Ранее сообщалось о многочисленных функциональных различиях между представителями класса БРА (сартанами), которые не связаны с блокированием рецепторов к ангиотензину II (T.W. Kurtz, M. Pravenec, 2008). Клиническое значение влияния олмесартана на активность АПФ2 в почках заключается в дополнительном ренопротективном действии, выделяющем этот БРА в своем классе. Об этом свидетельствуют и результаты исследования H. Ikeda и соавт. (2009), в котором замена текущего БРА (валсартана, кандесартана, телмисартана или лозартана) на олмесартан при лечении гипертензивных пациентов с диабетической нефропатией приводила к достоверному дополнительному снижению у них уровня альбуминурии.
Еще одно исследование японских авторов было посвящено оценке влияния терапии олмесартаном в сравнении с кандесартаном на гипертрофию левого желудочка сердца у пациентов с АГ (T. Tsutamoto et al., 2010). Из 50 стабильных амбулаторных пациентов, которые принимали кандесартан более 1 года, 25 рандомизировали к приему олмесартана, а остальные продолжили терапию кандесартаном в прежней дозе. По истечении года в группе пациентов, которых перевели на олмесартан, отмечалось достоверное уменьшение индекса массы миокарда левого желудочка по данным эхокардиографии в сравнении с группой кандесартана, что сопровождалось снижением уровня ангиотензина II в плазме крови. При этом снижение артериального давления (АД) в обеих группах было сопоставимым. Эти результаты косвенно подтверждают, что, повышая активность АПФ2, олмесартан ингибирует синтез основного прессорного пептида РАС ангиотензина II в пользу образования его антипода – ангиотензина-(1-7). Для практики это означает, что при равном снижении АД олмесартан обеспечивает дополнительный кардиопротективный эффект у пациентов с АГ.
Выводы и перспективы
РАС оказалась намного сложнее, чем представлялось двадцать лет назад. В 2000-2007 гг. были описаны и изучены новые элементы этой системы, а в настоящее время можно утверждать о существовании двух осей РАС с противоположными ролями в сердечно-сосудистом континууме. Помимо хорошо известной оси АПФ / ангиотензин II / рецепторы AT1, реализующей неблагоприятные эффекты, существует антагонистическая ось АПФ2 / ангиотензин-(1-7) / рецепторы Mas. Результаты многочисленных экспериментальных исследований доказывают участие этих новых компонентов РАС в регуляции АД, метаболизма и в патогенезе сердечно-сосудистых заболеваний.
В соответствии с новой концепцией дуализма РАС представляется перспективной разработка новых препаратов, которые действовали бы как активаторы положительной оси РАС (A.J. Ferreira et al., 2012). Вместе с тем эта концепция подводит к переосмыслению фармакодинамических характеристик и клинической роли традиционных средств фармакотерапии, таких как БРА. В клинических исследованиях на эту тему показано, что олмесартан является уникальным представителем своего класса, способным повышать почечную экспрессию АПФ2 и обеспечивать таким образом дополнительную защиту органов-мишеней.
Подготовил Дмитрий Молчанов
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....